CuNPs/PAA/GR纳米新材料修饰玻碳电极检测猪肉中的莱克多巴胺
张翠忠,张贞发,连 欢,梁彩云,李 凯,彭金云*
(1.广西民族师范学院,广西 崇左 532200;2.广西高校桂西南特色植物资源化学重点实验室培育基地,广西 崇左 532200)
CuNPs/PAA/GR纳米新材料修饰玻碳电极检测猪肉中的莱克多巴胺
张翠忠1,2,张贞发1,2,连 欢1,2,梁彩云1,2,李 凯1,彭金云1,2*
(1.广西民族师范学院,广西 崇左 532200;2.广西高校桂西南特色植物资源化学重点实验室培育基地,广西 崇左 532200)
采用一种温和且简单的原位生长法将铜纳米粒子和石墨烯非共价键合,形成一种对莱克多巴胺催化活性高的复合纳米新材料CuNPs/PAA/GR。该材料用扫描电镜表征形貌,用阻抗表征修饰电极。不同扫速和pH值条件下,以其修饰玻碳电极构建的电化学体系受吸附控制,莱克多巴胺在该电极表面的反应机理属两电子转移过程。体系中电化学参数为:电子转移数(n)=1.7,修饰电极的有效面积为3.57 cm2,为裸电极的12.6倍,电极吸附量(Гs)为1.98×10-12mol/cm2。采用微分脉冲伏安法进行检测,莱克多巴胺的浓度在1~30 μmol/L范围内呈良好线性关系(r2=0.990 2),检出限(S/N=3)为18.3 nmol/L。该传感器经济易制备、灵敏性高、稳定性与重现性好。将该传感器用于猪肉中莱克多巴胺的检测,其回收率为97.0% ~102.5%,相对标准偏差为2.8%~3.2%。
还原石墨烯;莱克多巴胺;纳米铜;计时库仑;微分脉冲伏安法
β受体激动剂是一种在芳香环和末端氨基上具备不同取代基的苯乙醇胺类化合物,包括莱克多巴胺(RAC)、盐酸克伦特罗(CLB)、沙丁胺醇(SAL)和苯乙醇胺(PHL)等[1],临床上对治疗心肺疾病和哮喘病效果明显[2]。由于饲养家畜的纯正谷物饲料成本较高,经营者更愿意选择低成本的“肉骨粉(MBM)”饲料喂养牲畜,而这种饲料中含有副产物莱克多巴胺(RAC)[3]。RAC潜在的营养成分再分配可减少动物体内脂肪,增加肌肉量。某些经营者为了获取更多利益,将RAC添加于饲料和动物用水中[1]。因此,β受体激动剂不仅作为处方药出现在各大医疗机构,更多的存在动物和健康的人体组织中。由于β受体激动剂在动物体内具有积累特性,人类食用这种肉食动物后更容易富集在人体组织中,当富集在体内浓度达到一定程度,会出现心悸、震颤和呼吸急促等症状,对患高血压、青光眼、糖尿病、前列腺肥大等疾病患者的危害更大,甚至可能危及生命[4]。
石墨烯(Graphene)是一种具有二维平面结构的新型碳纳米材料,其特殊的结构在常温下表现出众多独特的性质,基于良好的导电性、大的比表面积以及广泛的生物兼容性[5],电分析化学家将其应用于各种类型的传感器中,检测效果明显[6]。最近,研究者将无机纳米金属引入官能化的石墨烯,这种改性后的材料相比氧化石墨烯表现出更高的稳定性和催化活性,一定程度上提高了检测的灵敏度[7-8]。基于此,本文提出一种温和且简单的原位生长法将铜纳米粒子和石墨烯非共价键合,制备出CuNPs/PAA/GR纳米新材料共同修饰玻碳电极,并将该修饰电极成功用于RAC的检测。
1 实验部分
1.1 仪器与试剂
CHI620E电化学分析仪(上海辰华仪器有限公司);PHS-3C型pH计(上海精科实业有限公司);移液枪(0.5~10,20~200,100~1 000 μL,上海沃珑仪器有限公司);玻碳电极(GCE,直径3 mm,天津英科联合科技有限公司),饱和甘汞电极(SCE,天津英科联合科技有限公司),铂丝电极(天津英科联合科技有限公司);TGL-16C离心机(常州朗越仪器制造有限公司);扫描电子显微镜(EVO MA 15/LS 15,德国卡尔蔡司公司)。
聚丙烯酸(PAA,天津市科密欧化学试剂公司);30%过氧化氢(H2O2,成都市科龙化工试剂厂);高锰酸钾(KMnO4)、硼氢化钠(NaBH4)、二水合氯化铜(CuCl2·2H2O),均购于国药集团化学试剂有限公司;莱克多巴胺(RAC,Aladdin公司);上述试剂均为分析纯。膨胀石墨(青岛福金石墨有限公司)。实验用水均为二次水。
1.2 氧化石墨烯及CuNPs/PAA/GR复合材料的制备
首先采用改进的Hummers法制备氧化石墨[9],再将45.00 mg氧化石墨烯(GO)超声分散在45 mL水中,加入20 mL 15%(wt)PAA,超声分散5 h,保持静置过夜。次日在磁力搅拌机协助下加入75 mL 0.2 mol/L CuCl2,室温下保持磁力搅拌2 h后,逐滴加入0.4 mol/L NaBH4直至溶液呈棕褐色,静置分层。将混合物进行抽虑,再分别用CH3OH和H2O各洗4次。产物在50 ℃真空中干燥。
1.3 GCE/CuNPs/PAA/GR修饰电极的制备
移取2 μL已制备的CuNPs/PAA/GR溶液滴涂于已处理好的裸玻碳电极(GCE),室温下晾干备用。
1.4 猪肉样品的制备
[3,10]对猪肉样品的制备加以改进:将猪肉样品剁成碎片,并存储在-20 ℃下。分析时,取出冷冻样品放在4 ℃环境中解冻后称取10.0 g样品,添加一定浓度的莱克多巴胺溶液,称重后转移至250 mL锥形烧瓶中。将40 mL乙酸乙酯和2 mL 4 mol/L K2CO3加至样品锥形烧瓶中,超声30 min。将此样品溶液转移至离心管,以3 000 r/min的转速离心10 min,收集乙酸乙酯层溶液至200 mL烧杯中。再加入40 mL乙酸乙酯至剩余的残余物中,充分混合后继续按上述方法离心,收集两次离心的乙酸乙酯层溶液,在温度接近但小于40 ℃的条件下蒸发至干,将固体残余物保存备用。按此方法制备空白样品,即未加入莱克多巴胺的猪肉样品。
2 结果与讨论
2.1 扫描电镜(SEM)及能谱(EDX)表征
图1A为超声分散后氧化石墨烯(GO)的扫描电镜图,可以看出石墨烯在玻碳电极表面形成一层均匀的单层膜。图1B为NaBH4参与还原铜离子后的纳米复合材料CuNPs/PAA/GR,由于PAA分子上存在大量的羧基,当其与氧化石墨烯的羟基键合后,会增加石墨烯表面的配位氧原子,配位氧原子遇到配体铜自然形成一种稳定的络合物,因此可以观察到CuNPs均匀且稳定地分散在石墨烯中,未出现团聚现象。图1C为能谱图,表明该材料含有元素C(1.70%)和Cu(1.08%),其中Au是测样喷金的缘故。

图1 GCE/GO(A)与GCE/CuNPs/PAA/GR(B)的扫描电镜图,以及GCE/CuNPs/PAA/GR(C)的能谱图Fig.1 SEM images of GCE/GO(A),GCE/CuNPs/PAA/GR(B),and EDX image of GCE/CuNPs/PAA/GR(C)
2.2 交流阻抗(EIS)对修饰电极的表征

图2 GCE(a),GCE/GO(b)及GCE/CuNPs/PAA/GR(c)的交流阻抗谱图Fig.2 Nyquist plots of 2 mmol/L [Fe(CN)6]3-/4- in 0.1 mol/L KCl at GCE(a),GCE/GO(b) and GCE/CuNPs/PAA/GR(c) frequency range:0.05-100 kHz;Ac amplitude:5 mV
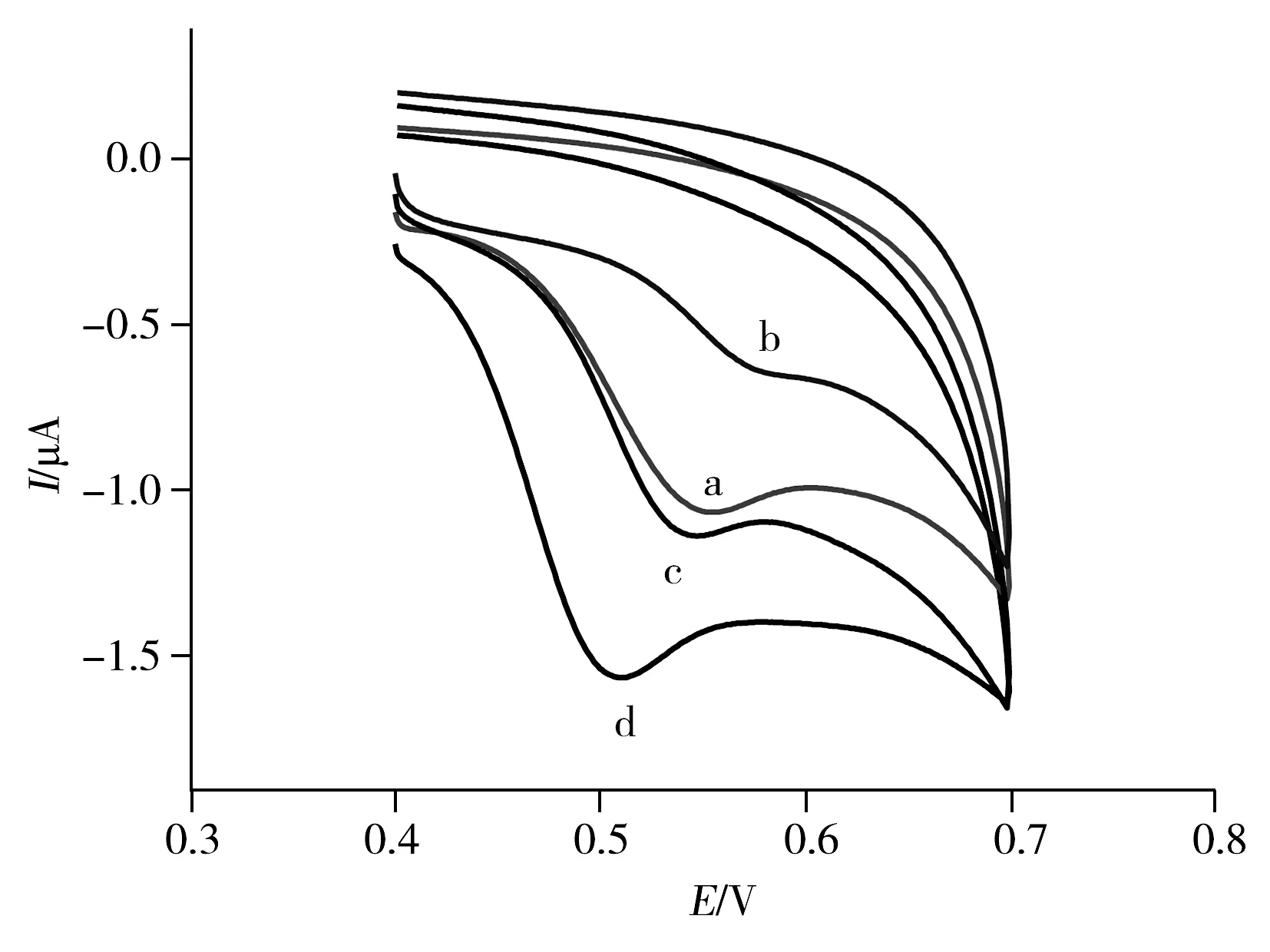
图3 RAC在不同修饰电极上的循环伏安图Fig.3 Cyclic voltammograms of RAC on different electrodes a.GCE,b.GCE/GO,c.GCE/GR,d.GCE/CuNPs/PAA/GR;scan rate:10 mV/s
EIS是表征电极表面修饰特征的有效手段[11],电子传递阻抗(Ret) 在数值上等于半圆的直径。本实验采用交流阻抗图(EIS)分别对GCE(a),GCE/GO(b)及GCE/CuNPs/PAA/GR(c) 3种电极进行表征(图2)。可以看出GCE在高频区有微弱的拐点,但整体上呈直线(曲线a),说明裸玻碳电极(GCE)在[Fe(CN)6]3-/4-溶液中的导电性能良好。GCE/GO电极在高频区半圆稍微增大,说明石墨烯顺利修饰在电极表面(曲线b)。而GCE/CuNPs/PAA/GR修饰电极的半圆弧度扩大更明显(曲线c),可能是导电性相对较弱的聚丙烯酸(PAA)被键合在石墨烯上且Cu离子的活泼性远小于Fe离子,所以修饰电极在[Fe(CN)6]3-/4-溶液中的阻抗值最大,即观察到半圆弧最大。
2.3 不同修饰电极在莱克多巴胺(RAC)中的电流响应
图3为不同修饰电极在RAC中的循环伏安图,从图中可以看出裸玻碳电极(GCE)检测到RAC的氧化峰电流比较明显,约1.07 μA(曲线a)。在氧化石墨烯(GO)修饰GCE中可观察到RAC的氧化峰电流大幅降低,仅为0.63 μA(曲线b),这是因为氧化所得石墨烯被引入大量含氧官能团(羧基、环氧基和羟基),其平面sp2共轭体系受到严重破坏,因此导电性降低[12]。在还原石墨烯(GR)修饰GCE中,可以看出RAC的氧化峰电流继续增至1.15 μA(曲线c),这是因为利用化学还原方法可以转移 GO 表面的含氧基团,所得GR电子共轭体系重新构建,导电能力恢复并增强[12]。而经CuNPs/PAA/GR 3种纳米复合物修饰的GCE,其峰电流与其他修饰电极相比增加程度更为明显(曲线d),其原因可能是:一方面,纳米尺寸的过渡金属Cu在某些方面比贵金属Au等具有更高的氧化电势,呈现出潜在的催化优势[13-14];另一方面,在聚丙烯酸(PAA)的协助下CuNPs被均匀而稳定地分散在还原后的石墨烯中,彼此的活性位点均裸露于材料表面,从而更好地发挥了协同催化效应[15]。
2.4 pH值的影响
考察了GCE/CuNPs/PAA/GR修饰电极在不同pH值(1.0,2.0,3.0,4.0,5.0,6.0,7.0,8.0,9.0,10.0,11.0)下RAC峰电流的响应信号。结果表明,随着pH值从1.0增至 7.0,GCE/CuNPs/PAA/GR修饰电极的峰电流呈上升趋势,此后,继续增大pH值则峰电流减小。因此,本文选择在pH 7.0的0.1 mol/L PBS缓冲溶液中进行后续实验。
2.5 扫速的影响
采用循环伏安法考察了不同扫速(30 ~130 mV/s)对30 μmol/L RAC氧化峰电流和电位的影响,扫描速率在30 ~130 mV/s范围内,当扫速以10 mV/s的规律不断递增时,RAC的氧化峰电流或峰电位呈线性递增关系。其中氧化峰电流与扫速的线性方程为:Ipa=-0.017v-0.497(r2=0.991 2),这说明RAC在GCE/CuNPs/PAA/GR电极表面受吸附控制。氧化峰电位与扫速对数的线性方程为Epa=0.03lnv+0.453(r2=0.995 9),根据Laviron[16]方程:Epa=E0′+(RT/αnF)ln(RTk0/αnF)+(RT/αnF)lnv,式中,Epa表示氧化峰电位,v为扫描速率,α为电荷转移系数(通常对于完全不可逆的电极过程,α取值0.5)[17],n为电子转移数,T为开尔文温度273.16 K,F为法拉第常数96 480 C/mol,R为摩尔气体常数8.314 J/(mol·K-1)。计算得到电子转移数n=1.7,属于两电子双质子的传递过程。
2.6 电化学有效面积及吸附量的计算
GCE/CuNPs/PAA/GR修饰电极的电化学有效面积采用以下公式进行计算[18]:Q(t)=2nFAcD1/2t1/2/π1/2+Qdl+Qads,其中浓度为0.1 mmol/L的K3[Fe(CN)6] 作标准物质,扩散系数D为7.6×10-6cm2/s[19],电子转移数n为1,法拉第常数F为96 480 C/mol,Qdl为双层电荷,Qads为Faradaic电荷。

图4 不同浓度RAC在GCE/CuNPs/PAA/GR上的微分脉冲伏安图Fig.4 DPV curves of different concentration of ractopamine on GCE/CuNPs/PAA/GR RAC concentrations(from a to g):1,5,10,15,20,25,30 μmol/L;0.1 mol/L PBS solution;insert:relationship between peak current and concentration of RAC
通过计时库仑实验,GCE和GCE/CuNPs/PAA/GR的Q~t1/2曲线方程分别为Q=5.34t1/2+1.28(r2=0.995 1)和Q=67.4t1/2-10.7(r2=0.993 1),其中Q的单位为μC,t的单位为s。计算得到GCE/CuNPs/PAA/GR的有效面积为3.57 cm2,为裸电极的12.6倍。修饰电极的有效面积明显增加,可有效地提高RAC在电极上的电流响应。由于修饰电极在空白PBS中的Qads为1.39×10-6C,在RAC溶液中的Qads为2.76×10-6C,扣除空白溶液的吸附影响,根据Qads=nFAГs,可计算得到吸附量Гs为1.98×10-12mol/cm2。
2.7 RAC的标准曲线
微分脉冲伏安法(DPV)是一种灵敏度高、分辨率强的电化学检测技术,特别在识别背景信号方面远高于循环伏安等技术。本文使用DPV技术对不同浓度的RAC进行研究。图4为不同浓度RAC 的DPV响应图,可以看出随着RAC浓度的增加,氧化峰电流随之增加,在1~30 μmol/L范围内呈良好的线性关系,其线性方程为:Ipa(μA)=-0.09c(μmol/L)-3.85(r2=0.990 2),检出限(S/N=3)为18.3 nmol/L,优于近期文献报道的26 μmol/L[20]和23.8 nmol/L[21]。
本文将制备的GCE/CuNPs/PAA/GR修饰电极避光保存于4 ℃冰箱,采用DPV法考察了该修饰电极的稳定性、重现性。规定观察时长30 d,观察频次为1次/5 d,每次做3组平行实验。实验结果表明,随着存放天数的增加,电流响应值不断降低,直至第30 d降为初始值的91%,说明该电极的寿命长、稳定性好;通过考察3组平行实验,测得相对标准偏差(RSD)不高于2.8%,说明该修饰电极的重现性好、精密度高。

2.8 分析应用
为了进一步研究该修饰电极的实用性,将“1.4”方法中得到的固体残余物用1.0 mL 50%甲醇溶解后转移至50 mL容量瓶中,再用0.1 mol/L PBS(pH 7.0)溶液稀释至刻度。以DPV法分别对猪肉样品中的3个浓度水平(30,35,40 μg/g)RAC进行加标回收实验。结果显示,所检测的相对标准偏差均不大于3.6%,回收率分别为97.0%,99.5%,102.5%。表明该修饰电极的准确度高,精密度好,用于实际样品中RAC含量的测定具有较大的可行性。
3 结 论
本文采用一种温和且简单的原位生长法将铜纳米粒子和石墨烯非共价键合在一起,形成一种催化活性高、分散性好、比表面积大的复合纳米新材料CuNPs/PAA/GR,将该材料用于修饰玻碳电极(GCE/CuNPs/PAA/GR),并用于RAC的测定。结果显示,RAC属于两电子的传递过程,修饰电极的有效面积为3.57 cm2,为裸电极的12.6倍,电极吸附量Гs为1.98×10-12mol/cm2。通过DPV法构建标准曲线发现RAC的浓度在1~30 μmol/L范围内呈良好线性,其检出限为18.3 nmol/L。该电极的稳定性和重现性良好,准确度高,精密度好,有望用于实际样品中RAC含量的测定。
参考文献:
[1] Lin X Y,Ni Y N,Kokot S.J.Hazard.Mater.,2013,260:508-517.
[2] Kuiper H A,Noordam M Y,van Dooren-Flipsen M M,Schilt R,Roos A H.J.AnimalSci.,1998,76(1):195-207.
[3] Gressler V,Franzen A R L,de Lima G J M M,Tavernari F C,Dalla Costa O A,Feddern V.J.Chromatogr.B,2016,1015:192-200.
[4] Wu Y P,Bi Y F,Bingga G,Li X W,Zhang S X,Li J C,Li H,Ding S Y,Xia X.J.Chromatogr.A,2015,1400:74-81.
[5] Zhu X,Li C L,Liu Q,Zhu X H,Zhang Y T,Xu M T.Chin.J.Anal.Chem.( 朱旭,李春兰,刘琴,朱效华,张银堂,徐茂田.分析化学),2011,39(12):1846-1851.
[6] Gan T,Hu S S.Microchim.Acta,2011,175(1/2):1-19.
[7] Bae S Y,Jeon I Y,Yang J,Park N,Shin H S,Park S,Ruoff R S,Dai L,Baek J B.ACSNano,2011,5(6):4974-4980.
[8] Kamat P V.J.Phys.Chem.Lett.,2009,1(2):520-527.
[9] Chen C M,Yang Q H,Yang Y G,Lv W,Wen Y F,Hou P X,Wang M Z,Cheng H M.Adv.Mater.,2009,21(29):3007-3011.
[10] Liu Z,Zhou Y K,Wang Y Y,Cheng Q,Wu K B.Electrochim.Acta,2012,74:139-144.
[11] Saby C,Ortiz B,Champagne G Y,Bélanger D.Langmuir,1997,13(25):6805-6813.
[12] Zhang J L,Yang H J,Shen G X,Cheng P,Zhang J Y,Guo S W.Chem.Commun.,2010,46(7):1112-1114.
[13] Guo X N,Hao C H,Jin G Q,Zhu H Y,Guo X Y.Angew.Chem.Int.Ed.,2014,53(7):1973-1977.
[14] Zhang C Z,Lian H,Huang H F,Zhang Z F,Liang C Y,Meng M X,Peng J Y.J.Instrum.Anal.(张翠忠,连欢,黄海峰,张贞发,梁彩云,蒙美香,彭金云.分析测试学报),2016,35(7):888-892.
[15] Yin H J,Tang H J,Wang D,Gao Y,Tang Z Y.ACSNano,2012,6(9):8288-8297.
[16] Laviron E.J.Electroanal.Chem.,1979,101(1):19-28.
[17] Bard A J,Faulkner L R,Leddy J,Zoski C G.ElectrochemicalMethods:FundamentalsandApplications.New York:Wiley,1980.
[18] Anson F C.Anal.Chem.,1964,36(4):932-934.
[19] Adams R N.ElectrochemistryatSolidElectrodes.NewYork:MarcelDekker,1969.
[20] Rajkumar M,Li Y S,Chen S M.ColloidsSurf.B,2013,110:242-247.
[21] Kong L J,Pan M F,Fang G Z,Qian K,Wang S.Anal.Bioanal.Chem.,2012,404(6/7):1653-1660.
Determination of Ractopamine in Pork Using CuNPs/PAA/GR Nanocomposites Modified Glassy Carbon Electrode
ZHANG Cui-zhong1,2,ZHANG Zhen-fa1,2,LIAN Huan1,2,LIANG Cai-yun1,2,LI Kai1,PENG Jin-yun1,2*
(1.Guangxi Normal University for Nationalities,Chongzuo 532200,China;2.Guangxi Colleges and Universities Key Laboratory Breeding Base of Chemistry of Guangxi Southwest Plant Resources,Chongzuo 532200,China)
A moderate and simple in-situ growth approach was adpoted to bond coppernanoparticles noncovalently to graphene for preparation of CuNPs/PAA/GR nanocomposites which were used for electrocatalysis of ractopamine(RAC).The morphology of the material was observed by scanning electron microscopy(SEM),and the state of the modified glassy carbon electrode was investigated by electrochemical impedance(EIS).Tests at various scan rates and pH conditions indicated that the modified electrode has an adsorption-controlled electrochemical system.The mechanism for the electrode reaction for ractopamine involves a two-electron transter process accompanied by a deprotonation step.Electrochemical parameters were calculated as follows:the electron transfer number(n) was 1.7,the effective area for the CuNPs/PAA/GR/GCE electrode was 3.57 cm2,12.6 times as large as bare electrode,and the adsorption capacity(Гs) value was 1.98×10-12mol/cm2.Under the optimal conditions by differential pulse voltammetric measurement,the calibration curve of RAC was linear in the range of 1-30 μmol/L(r2=0.990 2) with a detection limit(S/N=3) of 18.3 nmol/L.With advantages of facile fabrication,high sensitivity,good stability and high reproducibility,the sensor was applied in the detection of ractopamine in pork samples with recoveries of 97.0%-102.5% and relative standard deviations(RSD) of 2.8%-3.2%.
graphene(GR);ractopamine(RAC);copper nanoparticles(CuNPs);chronocoulometry;differential pulse voltammetry(DPV)
2016-08-01;
2016-09-30
国家自然科学基金资助项目(21465004);2017年广西中青年能力提升项目;校级资助一般项目(2016YB033)
10.3969/j.issn.1004-4957.2017.02.016
O657.1;TQ460.72
A
1004-4957(2017)02-0247-05
*通讯作者:彭金云,博士,教授,研究方向:电化学,Tel:0771-7870708,E-mail:pengjinyun@yeah.net

