应用基于LC—TOF—MS分析的质量亏损过滤方法筛选黄芪注射液中的皂苷类成分
宋慧婷+李长印+万瑶瑶+丁选胜+谭喜莹+戴国梁+刘史佳+居文政

[摘要] 采用液相色谱与四极杆飞行时间质谱(LC-TOF-MS)联用技术分析黄芪注射液(HI)样品,获取正负离子模式下HI中化学成分的LC-TOF-MS分析数据。根据前期相关文献报道,建立黄芪皂苷类化合物的质量亏损过滤(MDF)方法,用于系统筛选HI中所含有的皂苷类成分。每个筛选化合物的存在需由不少于2个准分子离子进行确认。最后依据其母离子和子离子信息对所筛选的化合物进行初步鉴定。最终共从HI中筛选并初步鉴定出62个皂苷类化合物,其中15个为新发现的皂苷类化合物。鉴定结果提示,乙酰化、氢化、去氢化、甲氧基化和水化可能为HI中皂苷所涉及的主要转化反应。该研究丰富了黄芪化学物质基础研究内容,同时也表明基于LC-TOF-MS分析的MDF方法,是一种可行且有效的中药成分系统筛选工具。
[关键词] 黄芪注射液; 黄芪皂苷; 质量亏损过滤; LC-TOF-MS; 转化反应
[Abstract] The samples of Huangqi injection (HI) were analyzed by liquid chromatography coupled with quadrupole time-of-flight mass spectrometry (LC-TOF-MS), and both positive and negative ion modes were employed to obtain the LC-TOF-MS analysis information of chemical compounds in HI. Then the mass defect filtering (MDF) approach, which was developed based on the previously published articles, was utilized to rapidly screen the astragalosides from the obtained LC-TOF-MS data. Each screened astragaloside was confirmed by the presence of no less than 2 quasi-molecular ions. All the screened astragalosides were then tentatively assigned according to the parent ion and daughter ion information. Finally, a total of 62 astragalosides were screened and characterized from the HI samples, including 15 new detected ones. The identification results indicated that acetylation, hydrogenation, dehydrogenation, methoxylation and hydration might be the major conversion reactions involved in the formation of the astragalosides. The LC-TOF-MS-based MDF approach was proved to be a feasible and efficient tool to screen the chemical constituents in complex matrices such as herbal medicines.
[Key words] Huangqi injections; astragalosides; mass defect filter; LC-TOF-MS; conversion reactions.
明確中药中所含有的化学成分信息,是阐明中药的药效物质基础,评价中药质量和安全性的前提和基础。高效液相-飞行时间质谱(LC-TOF-MS)联用技术非常适用于中药化学成分定性分析,特别是非目标性系统性定性分析[1-2]。然而,由于中药成分复杂,其LC-TOF-MS分析数据信息异常丰富,如何对其快速有效解析,以准确全面地提取中药成分信息一直是研究者的一大挑战。近年来,质量亏损过滤(mass defect filtering,MDF)方法作为一种TOF-MS等高分辨质谱数据的新型数据处理技术,已被一些研究证明可用于中药成分的系统分析,并具有一定的独特优势[3-4]。然而这些研究均具有一定的局限性,它们或者需要对照品比对[3],或者没有考虑到化合物可能的加合离子[4]。黄芪注射液(HI)为已上市的临床常用黄芪制剂,皂苷类为其主要药效成分和制剂质量控制指标[5-6]。然而目前还没有对HI中皂苷类成分系统分析的研究报道。基于此,本研究结合前期文献报道和预试验结果,充分考虑皂苷类化合物可能产生的各种加合离子,建立了改进的黄芪皂苷类化合物的质量亏损过滤(MDF)方法,对HI中的皂苷类成分进行系统筛选和鉴定。
1 材料
LC (Agilent)-(AB) Triple TOFTM 5600液质联用仪,含Pump Agilent 1200G1312A,Column Oven Agilent 1200G1316A,Auto Sampler Agilent 1260G1367B和Triple TOF 5600 Mass spectrometer,LC-MS/MS系统由Analyst 1.6 Software 控制;CPA225D电子天平(德国Sartorius公司);高速低温离心机(ThermoSorvall Legend Micro 17R);WH2微型旋涡混合仪(上海沪西分析仪器厂)。
甲醇、乙腈(HPLC级,德国Merck公司);甲酸、甲酸铵(质谱级,瑞士Fluka-Sigma-Aldrich公司);超纯水由Millipore Milli-Q Advantage A10超纯水机制备;其余试剂为分析纯。黄芪注射液为正大青春宝药业有限公司生产,批号1212053,规格10 mL/支。TOF-MS正负离子调谐液(美国AB Sciex公司,产品编号分别为4460131,4460134)。Oasis@固相萃取(SPE)小柱(HLB 3cc,美国Waters公司)。
2 方法
2.1 样品处理 黄芪注射液经SPE处理后方可进行LC-TOF-MS分析。HLB型SPE小柱使用前需首先用3 mL甲醇活化,而后用3 mL水洗预平衡。将黄芪注射液涡旋30 s混匀,精密吸取600 μL上SPE小柱,而后用2 mL水洗除杂,待水洗完毕后用1 mL甲醇进行洗脱。将甲醇洗脱液涡旋30 s混匀,12 000×g,4 ℃离心5 min,取上清液5 μL进样分析。
2.2 色谱条件 Agilent Poroshell 120 SB-C18色谱柱(3.0 mm×100 mm,2.7 μm),Agilent Poroshell 120 SB-C18预柱(3.0 mm×5.0 mm,2.7 μm);流动相A为含2 mmol·L-1甲酸铵和0.1%甲酸的水相,B为含2 mmol·L-1甲酸铵和0.1%甲酸的等比混合的甲醇-乙腈;梯度洗脱(0~0.5 min,5% B;0.5~12 min,5%~100% B;12~16 min,100% B;16~16.1 min,100%~5% B;16.1~22 min,5% B);流速300 μL·min-1;柱温35 ℃;进样体积5 μL;进样室温度8 ℃。
2.3 质谱条件 离子源为电喷雾离子化(ESI)源,正负离子模式均用于数据采集。TOF-MS扫描模式参数设置如下:扫描范围 m/z 100~1 000,累积时间 0.250 015 s,离子化温度(TEM) 550 ℃,雾化气(GS1) 60 psi(1 psi=6.895 kPa),辅助加热气(GS2) 60 psi,气帘气(CUR) 35 psi,去簇电压(DP) 80 V,碰撞能量(CE) 10 eV,正负离子模式下喷雾电压(ISVF)分别为5 500,4 500 V。采用IDA,DBS和高灵敏度的模式采集数据。主要的IDA转换标准如下:信号强度大于500 cps,4以内排除同位素,相对分子质量误差0.05,每个循环最多监测8个候选离子。子离子扫描模式的参数设置如下:扫描范围 m/z 50~1 000,累积时间0.100 006 s,CE(35±15) eV,其他主要参数同TOF-MS扫描模式。采用AB公司的调谐液传递系统(CDS)对相对分子质量准确度进行自动校准。通过AB公司的软件Analyst TF 1.6 software控制仪器操作和数据采集。
2.4 数据分析 采用AB公司的软件Peakview Software TM v. 1.2对获得LC-TOF-MS分析數据进行处理。数据处理过程会用到Peakview软件的4个功能Mass Defect Filtering (MDF),Formula Finder,XIC manager和IDA Explorer。
首先,采用MDF功能筛选黄芪皂苷相关特征离子,质量亏损和相对分子质量筛选范围见表1,正负离子模式下离子信号强度下限分别为12 000,7 000 cps。仅在IDA Explorer项下筛选能产生子离子的特征离子,以方便后续鉴定过程。接着,利用Formula Finder功能对筛选所得目标离子的元素组成进行预测,主要参数设置见表1,此外相对分子质量最大允许误差5,正离子模式下氮、钠和钾原子0~1个,负离子模式下氮、氯原子0~1个。采用XICManager功能提取筛选所得的目标离子,以检验其
峰形完整性,确认其准确保留时间;在0.03 min的 保留时间允许误差范围内,匹配、合并源自1个化合物的多个特征准分子离子(如正离子模式下的[M+H]+,[M+Na]+,[M+K]+,[M+NH4]+,及负离子模式下的[M-H]-,[M+Cl]-,[M+HCOOH-H]-,[M+NO3]-等),并对其他可能的上述特征离子进行XIC提取确认,进而综合各种加合离子信息锁定目标化合物。同时,对于同一时间点所筛选到的多个目标化合物,仔细考察相互间的分子式/相对分子质量关联,以去除源于源内裂解离子的假阳性筛选结果。最后,结合IDA Explorer提供的子离子信息对目标化合物进行初步鉴定。
3 结果与讨论
3.1 分析条件的选择 本研究中选择的Poroshell 120 SB-C18色谱柱为Agilent公司开发的一类新型UPLC色谱柱,与亚2 μm柱具有相似的高柱效,但压力减少40%~50%,因此适用于Agilent 1200等常压液相色谱[7]。为了能与后续HI药效相关非靶标代谢组学研究进行衔接,并证明本文中MDF筛选方法的筛选能力和效率,未对洗脱梯度等分析条件进行系统优化,选择了代谢组学研究中采用的通用的分析条件(详见后续研究报道);流动相中加入甲酸和甲酸铵是为了提高离子化效率、改善色谱峰峰形和产生特征加合离子。正负离子同时检测以产生丰富的加合离子确证目标化合物的存在,并提供丰富的碎片离子以利化合物的结构鉴定。
3.2 MDF筛选方法的确定 MDF技术最初是用于代谢产物鉴定研究的,用来移除生物样本中大量的背景干扰离子[8-9]。而中药成分虽然十分复杂,但常常可归属为一类或几类具有相同结构母核的一系列化合物,他们可以看做(实际上也应该是)极少数几个具有独特结构母核的化合物的次生代谢产物,这与药物及其体内代谢产物的关系是类似的,因此MDF技术理应适用于中药成分的系统定性分析。本研究中,MDF方法的质量亏损和相对分子质量筛选范围的设定依据为已有文献报道的黄芪皂苷类化合物。先前研究中,根据24个已有报道的黄芪中皂苷类成分的分子式,借助Peakview软件的Mass calculator功能计算获得其5种常见准分子离子包括正离子模式下的[M+H]+,[M+Na]+,[M+NH4]+及负离子模式下的[M-H]-,[M+HCOOH-H]-的精确分子质量;据此得到正负离子模式下质量亏损的最大值和最小值,以及相对分子质量的最大值和最小值,进而设定了MDF的相关参数[10]。然而,由筛选结果可知,[M+HNO3-H]-为此前未见报道的一种出现频率极高的黄芪皂苷准分子离子,其出现频率仅次于[M+HCOOH-H]-;此外,[M+K]+和[M+Cl]–也经常出现。更为重要的是,相比[M-H]-和[M+H]+离子,多数情况下,黄芪皂苷的[M+HCOOH-H]-,[M+Na]+和[M+HNO3-H]-等加合离子往往具有更强的离子响应强度。筛选方法设定时不考虑这些准分子离子的存在会影响筛选方法的灵敏度和筛选结果的全面性。因此,根据各个已有报道的皂苷的上述所有8种准分子离子的精确相对分子质量和分子式,对上述MDF方法进行了修正,从而大大提高了化合物筛选的灵敏度。由于CDS自动校准可以实现0.01以内的分子质量自动校准,因此将质量亏损的误差范围设定为±0.01;而分子质量误差范围则设定为10,以涵盖可能出现的不可预知的皂苷类化合物。最终MDF方法具体参数设置见表1。
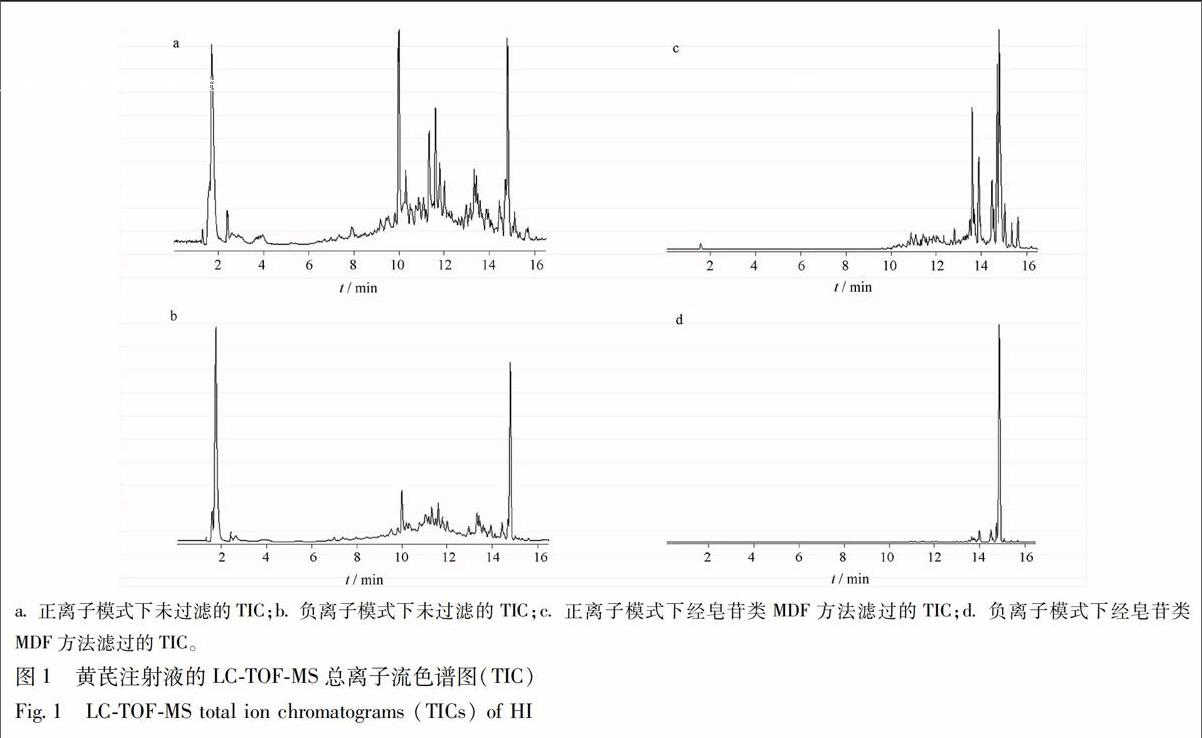
3.3 筛选结果 经MDF过滤后的LC-TOF-MS总离子流色谱图(TIC)的基线噪音水平显著降低,而黄芪皂苷类化合物对应的色谱峰也在TIC图谱中更加清晰明显,见图1。理论上来讲,凡是质量亏损落在设定范围内的信号离子均应作为皂苷相关离子被筛选出来进一步研究。而在本研究中,仅对能产生子离子且信号强度在12 000 cps(正离子模式)或7 000 cps(负离子模式)以上的皂苷相关离子进行筛选,以发现相对含量较高的黄芪皂苷类成分。最终根据1.2.4中所述方法,共从黄芪注射液中锁定62个皂苷类化合物。
a.正离子模式下未过滤的TIC;b.负离子模式下未过滤的TIC;c.正离子模式下经皂苷类MDF方法滤过的TIC;d.负离子模式下经皂苷类MDF方法滤过的TIC。
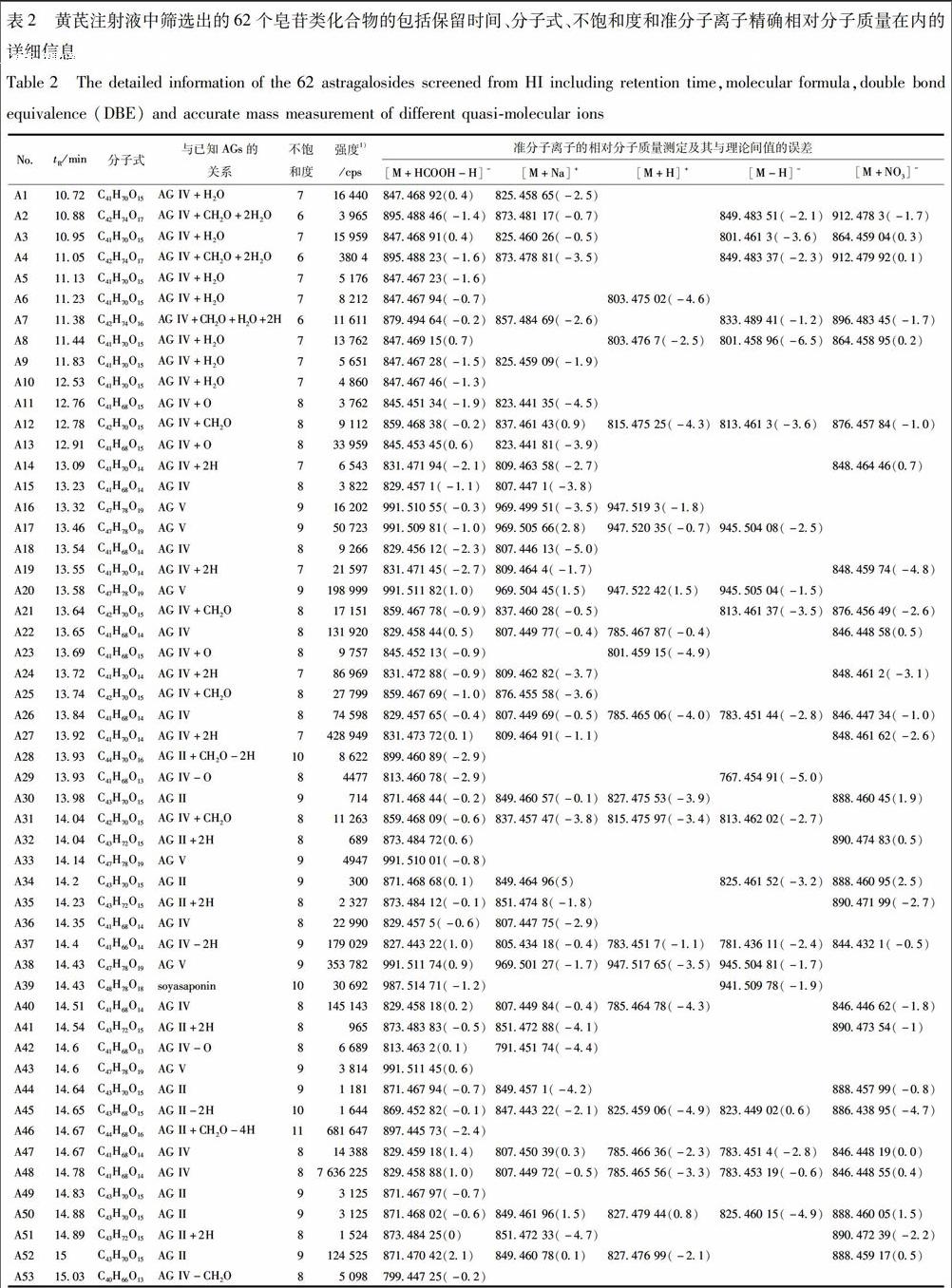
为了进一步确证62个皂苷类成分的存在,采用XIC manager重新提取了每个成分的8种准分子离子的XIC图谱,以确证各种准分子离子的存在。结果表明,大多数皂苷类成分均存在3个以上的准分子离子,进一步证明了筛选结果的可靠性。各种离子类型出现的频率从高到低依次为:[M+HCOOH-H]->[M+Na]+>[M+NO3]->[M-H]->[M+H]+>[M+Cl]->[M+K]+>[M+NH4]+。由此可见,在当前LC-MS条件下,[M+HCOOH-H]-是负离子模式下黄芪皂苷类化合物最常见的离子形式,而[M+Na]+则是正离子模式下黄芪皂苷的主要离子形式。此结果进一步证明了化合物筛选方法时考虑各种类型加合离子的重要性和必要性。总结62个化合物的详细信息,见表2,包括保留时间,分子式,不饱和度,5类主要准分子离子的分子质量测定值及其与理论值间的误差值,[M+HCOOH-H]-的信号强度,以及各化合物与已知黄芪皂苷的元素組成的关联性。
3.4 筛选化合物的鉴定 化合物的鉴定主要依据其元素组成与已报道的黄芪皂苷类化合物间的联系,子离子色谱图的特征诊断离子以及chemspider等已知化合物数据库。由前期研究[11]可知,在全扫描(TOF-MS scan type)模式下,皂苷类在正离子状态下极易产生苷元诊断碎片离子离子m/z 473.362 0 (C30H49O4),和一系列进一步脱水离子峰m/z 455.352 0 (C30H47O3),437.341 0 (C30H45O2),419.331 0 (C30H43O),以及C-17和C-20键裂解产生的25-hydroxy-20,24-epoxy残基离子m/z 143.106 0 (C8H15O2),这些离子的大量出现可为皂苷类化合物的存在提供依据,但是也会导致其相应准分子离子峰的信号大幅度减弱乃至缺失,从而无法获取针对某一离子的准确子离子信息。相反,在负离子状态下,黄芪皂苷类化合物在全扫描模式下往往仅产生丰度较强的[M-H]-或[M+HCOOH-H]-等准分子离子峰。这些准分子离子峰在子离子模式(product ion scan type)下则可产生源自此指定母离子的系列特征子离子,用于皂苷类化合物的结构鉴定。研究发现[10],黄芪甲苷(AGIV)在负离子TOF-MS模式下主要以m/z 829.459 8[M+HCOOH-H]-存在,此离子可在子离子模式产生m/z 783.456 4,651.410 4,621.398 1,489.357 0,179.056 1,161.045 6,149.045 8,143.034 1,131.034 1,119.035 6,113.024 7,101.024 9,89.0252,71.015 2,59.015 1等一系列特征离子,对应皂苷结构母核中的不同结构特征,见图2a。类似地,所有皂苷类化合物均可产生类似的特征碎片离子,见表3,据此可以初步描述化合物的化学结构,对其进行合理归属。以A13为例,见图2b,其[M+HCOOH-H]-可产生一系列特征碎片离子用于化学结构的解析。与黄芪甲苷一样,碎片离子179.06和149.05的出现表明A13结构中含有葡萄糖残基和木糖残基,而59.02和71.02的存在则表明A13结构中25-hydroxy-20,24-epoxy残基离子;离子505.4,637.4,667.4和黄芪甲苷的苷元特征离子489,621,651均相差1个氧原子的相对分子质量,提示羟基应存在于皂苷元母核上,而非其他3个环上。离子799的出现进一步证明845为A13的[M+HCOOH-H]-,且A13应为黄芪甲苷的羟基化产物。据此,给出A13的可能化学结构,见图2c。类似地,对所有62个化合物的结构进行了合理归属,见图3。其中共有47个已有报道的黄芪皂苷成分及其同分异构体,其中包含8个AGIV同分异构体(A15,A18,A22,A26,A37,A41,A48,A49),9个AGII同分异构体(A31,A35,A45,A50,A51,A53,A56,A57,A60),3个AGI同分异构体(A58,A61,A62),6个AGV同分异构体(A16,A17,A20,A34,A39,A44),乙酰AGI(A63),大豆皂苷(A40),以及19个先前黄芪口服液中首次发现的黄芪皂苷类化合物[10];包括A13在内的剩余15个化合物则为黄芪注射液中新发现的黄芪皂苷类化合物。归属所有62个新化合物的可能化学结构所需的子离子信息见表3。
a.负离子模式下黄芪甲苷(AGIV)的主要裂解途径及特征子离子;b.A13的母离子 [M+HCOOH-H]-m/z 845.5的子离子图谱;c.A13可能的化学结构。
3.5 筛选结果分析 根据筛选鉴定出的62个皂苷类化合物,可以对黄芪注射液中皂苷类成分的转化反应进行总结归纳。假设黄芪皂苷的转化始于AGIV,其他化合物则可看作是AGIV通过某些转化反应而生成的产物。事实上,已知的主要皂苷类成分AGII,AGI和AGV也可以分别看作是AGIV发生1,2,3次乙酰化后得到的系列转化产物。结果表明,共有乙酰化、(去)甲氧基化、(去)氢化、水合反应等9种转化反应参与黄芪皂苷类化合物的生成,见图3。结合各化合物[M+HCOOH-H]-的离子强度,可以初步认为,乙酰化、甲氧基化、氢化、去氢化和水合反应是黄芪注射液中黄芪皂苷类成分的主要转化途径。参考已知的主要皂苷类成分AGII,AGI和AGV的化学结构[11-13],以及ChemSpider数据库中结构类似的化合物,结合常规转化反应规律,初步推断可能的主要反应位点如下:AGIV结构中的A环被认为是乙酰化和甲氧基化的可能反应位点,而氢化反应可能发生于C9-C19位开环,去氢化则可能是C16位羟基羰基化,水合反应最有可能发生于C20-C24环氧基团。需要指出的是,并无确切证据证实AGIV为所有黄芪皂苷的母体化合物,因此上述转化反应在实际情况下有可能是逆向发生的。此外,本研究中未检测到丙二酸盐类皂苷成分,AGI的同分异构体及先前研究中未鉴定的1种皂苷成分,这些化合物的缺失可能与黄芪注射液的制备工艺有关。
1.乙酰化;2.去氢化;3.氢化;4.水合;5.甲氧基化;6.去羟基化;7.糖基化;8.羟基化;9.去甲氧基化。
4 结论
本研究在对HI进行LC-TOF-MS分析获取分析数据的基础上,采用MDF筛选方法共从HI中筛选出62个皂苷类化合物,其中15个为新发现化合物。
研究结果充分证明了基于LC-TOF-MS分析的MDF筛选方法应用于中药化学成分的系统定性分析的可行性和独特优势;同时,筛选出的62个皂苷类化合物间接阐明了HI中的黄芪皂苷次生代谢产物种类,丰富了对于黄芪皂苷类成分多样性的认识,对于科学评价黄芪制剂质量、促进制剂合理开发均具有一定的指导意义。
[参考文献]
[1] 张栋健, 李薇, 何庆文, 等. UHPLC-Q-TOF-MS分析枳壳炮制前后成分变化[J]. 中国中药杂志, 2016,41(11):2070.
[2] 吴金凤, 尹权微, 潘有智, 等. UPLC-Q-TOF-MS/MS快速分析苁蓉总苷胶囊化学成分[J]. 中国中药杂志, 2016,41(17):3244.
[3] Yan G, Sun H, Sun W, et al. Rapid and global detection and characterization of aconitum alkaloids in Yin Chen Si Ni Tang, a traditional Chinese medical formula, by ultra performance liquid chromatography-high resolution mass spectrometry and automated data analysis[J]. J Pharmaceut Biom Anal, 2010,53(3):421.
[4] Xie T, Liang Y, Hao H, et al. Rapid identification of ophiopogonins and ophiopogonones in Ophiopogon japonicus extract with a practical technique of mass defect filtering based on high resolution mass spectrometry[J]. J Chromatogr A, 2012,1227:234.
[5] 肖峰, 胡雅國, 吴石楠, 等. 黄芪皂苷提取物对糖尿病大鼠肾脏的保护作用[J]. 中国中药杂志, 2015,40(10):2014.
[6] 唐金海, 余东升, 潘立群. UV法测定黄芪注射液浓缩液微乳中黄芪总皂苷含量的实验研究[J]. 中华中医药学刊, 2007(10):2033.
[7] Chen F, Gong Z, Kelly B C. Rapid analysis of pharmaceuticals and personal care products in fish plasma micro-aliquots using liquid chromatography tandem mass spectrometry[J]. J Chromatogr A, 2015,1383:104.
[8] Zhang H, Zhang D, Ray K. A software filter to remove interference ions from drug metabolites in accurate mass liquid chromatography/mass spectrometric analyses[J]. J Mass Spectrom, 2003,38(10):1110.
[9] Zhu M, Ma L, Zhang D, et al. Detection and characterization of metabolites in biological matrices using mass defect filtering of liquid chromatography/high resolution mass spectrometry data[J]. Drug Metab Dispos, 2006,34(10):1722.
[10] Li C Y, Song H T, Liu S J, et al. Systematic screening and characterization of astragalosides in an oral solution of Radix Astragali by liquid chromatography with quadrupole time-of-flight mass spectrometry and Peakview software[J]. J Sep Sci, 2016,39(6):1099.
[11] Qi L W, Wen X D, Cao J, et al. Rapid and sensitive screening and characterization of phenolic acids, phthalides, saponins and isoflavonoids in DangguiBuxue Tang by rapid resolution liquid chromatography/diode-array detection coupled with time-of-flight mass spectrometry[J]. Rapid Commun Mass Spectrom, 2008,22(16):2493.
[12] Qi L W, Cao J, Li P, et al. Qualitative and quantitative analysis of Radix Astragali products by fast high-performance liquid chromatography-diode array detection coupled with time-of-flight mass spectrometry through dynamic adjustment of fragmentorvoltage[J]. J Chromatography A, 2008,1203(1):27.

