三维适形放疗放射野布局对治疗原发性肝癌患者放射性肝损伤的影响
王琴,张东成,董超,桂东,郝文胜
三维适形放疗放射野布局对治疗原发性肝癌患者放射性肝损伤的影响
王琴,张东成,董超,桂东,郝文胜
目的观察三维适形放疗(3-DCRT)治疗原发性肝癌患者不同布野对放射性肝损伤发生情况的影响。方法给予72例原发性肝癌患者3-DCRT治疗,其中36例采用多野,即≥5个共面/非共面照射野,另36例采用少野,即≤4个照射野治疗。处方剂量在35~60 Gy/8~30次,治疗后定期复查,根据肝功能情况记录急性和晚期放射性肝损伤发生情况。结果少野治疗患者急性放射性肝损伤发生率为36.1%,显著低于多野的97.2%(P<0.01);少野治疗患者3级和4级晚期放射性肝损伤发生率为5.6%,显著低于多野的33.4%(P<0.01)。结论少野3-DCRT治疗原发性肝癌患者可能减少放射性肝损伤发生率或减轻严重程度。
原发性肝癌;三维适形放疗;放射性肝损伤;照射野
肝脏最早被认为是放射线耐受性器官[1~3],近年来随着放射肿瘤学的发展,大量临床实践均显示肝脏是放射敏感器官[4~5]。放射治疗疗效确切,却因可能发生的并发症,如放射性肝损伤而造成不良后果[6]。降低放射性肝损伤的有效手段是减少正常肝脏组织照射剂量和照射体积[7]。近十年来,随着计算机技术的发展,以三维适形放疗(three-dimensional conformal radiotherapy,3-DCRT)为代表的精确放疗逐步运用于原发性肝癌患者的治疗,并达到了肿瘤放疗大剂量和重要脏器小剂量的目的,取得了良好的临床疗效。本研究观察了不同布野方案治疗原发性肝癌患者的疗效和放射性肝损伤发生情况,现报道如下。
1 资料与方法
1.1 临床资料2010年7月~2015年7月在我科就诊的无手术适应证或拒绝手术治疗的原发性肝癌患者72例,男性53例,女性19例;年龄为28~78岁,平均年龄为54±5岁。经B超或CT引导下行肝穿刺组织病理学检查证实为肝细胞癌。纳入标准:肝功能Child-Pugh A级,血小板计数>75× 109/L,无3-DCRT禁忌证,预期生存期超过6个月。将患者随机分为两组,一组为多野照射,射野数≥5个,另一组为少野照射,射野数≤4个。
1.2 3 -DCRT治疗方法使用Varian 600C直线加速器,6 MV X射线,使用Renderplan治疗计划系统。采用真空袋体模固定,双手置于头顶部,训练患者平静呼吸,行增强CT扫描定位,扫描层厚3 mm,扫描范围自膈顶上3 cm开始至右肾下极。将图像传入计划系统后,由固定的两名临床医生和一名影像科医生共同勾画病灶大体肿瘤靶区(gross tumor volume,GTV)。计划靶区(planning target volume,PTV)由GTV外放,外扩范围按下面的方法确定:对GTV<3 cm者,外扩1.5~2 cm;在3~5 cm者,外扩1~1.5 cm;对5~10 cm者,外扩0.5~1 cm;对>10 cm者,不外扩。需要勾画的危及器官(organs at risk,OARs)包括正常肝组织、十二指肠、结肠、胰腺、肾脏、胃和脊髓等。对OARs,不超过其耐受剂量。通过剂量体积直方图(dose volume histogram,DVH)进行评估并优化放射治疗方案。分别给予患者≥5个共面/非共面照射野(图1)或≤4个照射野(图2)。确定处方剂量原则如下:对肿瘤直径<5 cm者,给予4~6 Gy/F×8~15次,3~5次/w,总剂量为48~60 Gy;对5 cm以上者,给予2~3.5 Gy/F×10~30次,3~5次/w,总剂量为35~60 Gy。时间剂量因子(time dose factor,TDF)在100~150之间,以保障患者处方剂量相当于常规放疗剂量的60 Gy以上。均以90%以上剂量曲线包绕病灶。多野患者危及器官均不超过其耐受剂量,其中肝脏平均剂量小于25 Gy,接受≥30 Gy剂量照射的正常肝百分体积(V30)均<30%;少野患者在上述条件相同的情况下,保证30%以上的正常肝体积受照剂量≤10 Gy。当肿瘤体积≤10 cm时,保证30%以上正常肝脏体积无射野穿过。在放疗期间,给予护肝治疗。
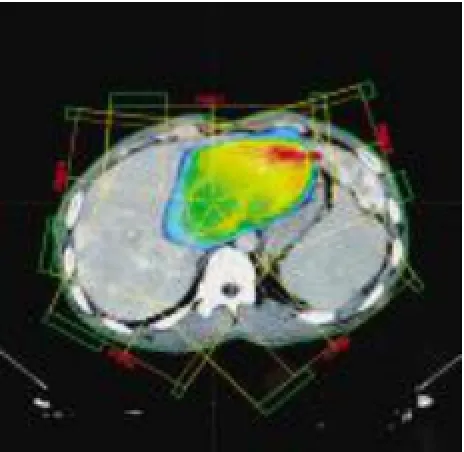
图1 多野照射的剂量分布图正常肝脏受照体积大
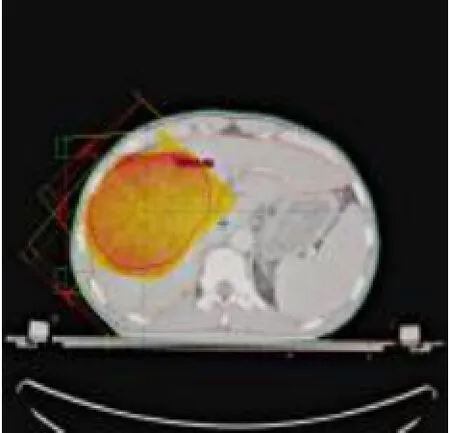
图2 少野照射的剂量分布图正常肝脏受照体积小
1.3 放射反应评价采用美国国家癌症研究院通用毒性标准2.0(national cancer institute common toxicity criteria 2.0,NCI-CTC)评估急性放射性肝损伤(0级:正常;1级:血清转氨酶1.26~2.5倍正常值上限;2级:血清转氨酶2.6~5倍正常值上限;3级:血清转氨酶5~10倍正常值上限)。采用美国和欧洲制定的正常组织晚反应系统(late effects normal tissue-subjective,objective,management,analytic,LENT/SOMA)评估晚期放射性肝损伤(1级:轻度疲倦,恶心、食欲不振,肝功能轻度异常;2级:中度症状,某些肝功能检查异常,血蛋白正常;3级:肝功能不全,肝功能检查大多异常,低蛋白血症,水肿或腹水;4级:肝性脑病)。
1.4 检测和检查使用德国西门子ADVIA2400自动生化分析仪检测肝功能指标(上海科华有限公司试剂);使用德国西门子Verio3.0T磁共振扫描仪行腹部检查。
1.5 统计学方法应用SPSS 19.0统计学软件行统计学分析,计数资料行卡方检验,P<0.05为具有统计学差异。
2 结果
2.1 两组急性放射性肝损伤发生率比较见表1。

表1 两组急性放射性肝损伤发生率(%)比较
2.2 两组晚期放射性肝损伤发生率比较见表2。
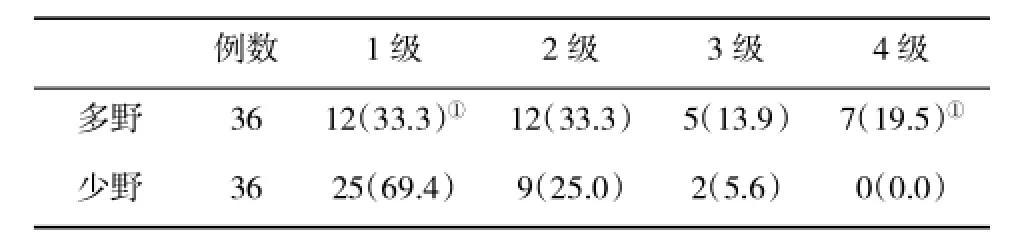
表2 两组晚期放射性肝损伤发生率(%)比较
3 讨论
临床上,制约放疗治疗肝癌的原因是放射性肝病(radiation-induced liver disease,RILD)的发生。一旦出现RILD,治疗便难于继续,临床治疗困难,多数患者最终发展为肝功能衰竭而死亡[8-10]。RILD典型病理学改变为肝组织出现中央静脉闭塞性病变[11],常表现为无黄疸性腹水、肝肿大、碱性磷酸酶升高≥2倍正常值,而转氨酶正常[12]。Child-Pugh B级患者在治疗后发生RILD远远高于Child-Pugh A级患者[13]。与RILD发生的相关因素很多,例如肿瘤分期、肿瘤体积、是否存在门静脉癌栓、肝硬化、Child-Pugh分级等[14],而RILD发生后行CT/MRI检查可见与射野形状一致的损伤区域,平均剂量(MHD)>35 Gy者发生率明显提高[6]。
本研究两组患者发生晚期放射性肝损伤的严重程度不同,少野患者发生晚期放射性肝损伤较轻微,差异有统计学意义(P<0.01)。
在随访期间,有7例多野治疗患者最终死于放射性肝坏死,而少野治疗者无死亡病例。在现今技术条件下,减少或尽量不让射野穿过正常肝脏也许能降低RILD的发生。患者在接受安全有效的放射治疗后,再结合介入治疗等其它有效的治疗手段,可以较长时间地控制肿瘤生长。
[1]赵增虎,刘俊堂,范青建.放射性肝损伤研究及防治进展.现代肿瘤医学,2011,19(10):2110-2113.
[2]Kennedy AS,Sangro B.Nonsurgical treatment for localized hepatocellular carcinoma.Curr Oncol Rep,2014,16(3):373-380.
[3]王华,魏伟.肝纤维化与细胞因子的关系.中国药理学通报,2002,18(2):132-136.
[4]Christiansen H,Sheikh N,Saile B,et al.X-irradiation in rat liver:consequent upregulation of hepcidin and downregulation of hemojuvelinandferroportin-1geneexpression.Radiology,2007,242(1):189-197.
[5]赵水喜,郑静晨,曹京旭,等.早期放射性肝损伤的CT影像和生化改变.肿瘤防治研究,2006,33(5):361-363.
[6]Dawson LA,Normolle D,Balter JM,et al.Analysis of radiation-induced liver disease using the Lyman NTCP model.Int J Radiat Oncol Biol Phys,2002,53(4):810-821.
[7]曾昭冲.原发性肝癌放射治疗的争论与共识.临床肿瘤学杂志,2008,13(2):97-104.
[8]陈万青,郑荣寿,张思维.2012年中国恶性肿瘤发病和死亡分析.中国肿瘤,2016,25(1):1-8.
[9]KondoY,KimuraO,ShimosegawaT.Radiationtherapyhas been shown to be adaptable for various stages of hepatocellular carcinoma.World J Gastroenterol,2015,21(1):94-101.
[10]Cheng JC,Liu HS,Wu JK,et al.Inclusion of biological factors inparallel-architecturenormal-tissuecomplicationprobability model for radiation-induced liver disease.Int J Radiat Oncol Biol Phys,2005,62(4):1150-1156.
[11]董天明,安宁豫.放射性肝损伤影像学研究现状.中国医学科学院学报,2013,35(6):694-697.
[12]Trotti A,Byhardt R,Stetz J,et al.Common toxicity criteria:version 2.0.An improved reference for grading the acute effects of cancer treatment:impact on radiotherapy.Int J Radiat Oncol Biol Phys,2000,47(1):13-47.
[13]Wu DH,Liu L,Chen LH.Therapeutic effects and prognostic factors inthree-dimensional conformal radiotherapy combined with transcatheter arterial chemoembolization for hepatocellular carcinoma.World J Gastroenterol,2004,10(15):2184-2189.
[14]梁世雄,蒋国梁,朱小东,等.原发性肝癌三维适形放疗后放射性肝病的影响因素.中华放射肿瘤学杂志,2005,14(4): 284-288.
(收稿:2016-11-25)
(本文编辑:陈宗炳)
Effect of radiation field layout on incidence of radiation-induced liver injury inpatients with primary liver cancer during three-dimensional conformal radiotherapy
Wang Qin,Zhang Dongcheng,Dong Chao,et al.Department of Oncology,105th Hospital of PLA,Hefei 230031,Anhui Province,China
Hepatoma;Three-dimensional conformal radiotherapy;Radiation-induced liver injury;Radiation field
10.3969/j.issn.1672-5069.2017.03.032
230031合肥市解放军第105医院肿瘤二科
王琴,女,25岁,皖南医学院硕士研究生。主要从事肿瘤综合治疗研究。E-mail:1196131703@qq.com
郝文胜,E-mail:hws69@sohu.com

