阵发性高血压合并肝门区占位一例
陆抑非 江建军 方崇峰 陆弋
阵发性高血压合并肝门区占位一例
陆抑非 江建军 方崇峰 陆弋
嗜铬细胞瘤(PCC)和副神经节瘤(PGL)合称为PPGL,是起源于肾上腺髓质和肾上腺外交感神经链的肿瘤,可合成大量儿茶酚胺类(CA)物质,如去甲肾上腺素(NE),肾上腺素(E)及多巴胺(DA),引起血压升高等一系列表现[1]。肝脏是恶性PPGL常见的转移部位之一[2],但是原发于肝脏的PGL却较罕见。现将本科室2016年4月20日收治的1例原发于肝脏的PGL患者报道如下。
1 临床资料
患者,女,59岁,因“血压增高7年余,胸闷气促1d”入院,发现高血压7年余,近期已行美托洛尔、缬沙坦氢氯噻嗪,硝苯地平等4联降压治疗,血压仍阵发性升高,可至240/150mmHg,伴头昏,1d前出现胸闷,外院CT示“肺水肿可能,肝门部占位”,后至本院治疗。无特殊既往史、个人史。入院体格检查:HR:93次/min,BP:152/84mmHg,双肺呼吸音粗,可及湿罗音,双下肢轻度浮肿。辅助检查:(BP:150/100mmHg时)血CA:DA:30.4ng/L(0.00~100ng/L),NE:1241.00ng/L(<600ng/L),E:72.90ng/L(0.00~100ng/L);(BP:240/150mmHg时)血CA:DA:30.4ng/L,NE:4074ng/L,E:25.70ng/L,4月29日突发畏寒寒战,最高体温38.8℃,急查降钙素原(PCT):0.93ng/ml,2d后复查PCT:41.13ng/L,MRI示上腹部增强:巨淋巴结增生症或异位嗜铬细胞瘤(图1~3),后停用美托洛尔,改特拉唑嗪控制血压,转北京大学第三医院治疗,行间碘苄胍(123I-MIBG)提示肝门区副神经节瘤,予酚苄明联合拜新同、美托洛尔控制血压,维持血压133~168/86~102mmHg,于2016年8月10日行“肝门部嗜铬细胞瘤切除术”,术后病理示(肝门区)副神经节瘤。术后拜新同、特拉唑嗪控制血压,血压趋平稳。为再评估于2016年11月23日再入本院,上腹部MR平扫+增强提示“异位嗜铬细胞瘤术后”,血、尿CA无殊。建议进一步MIBG显像或PET-CT排除术后复发,未接受出院。
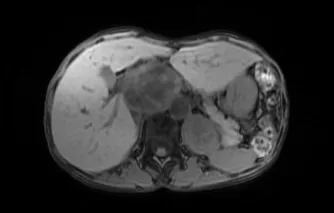
图1 MRI TIWI:瘤体呈低信号
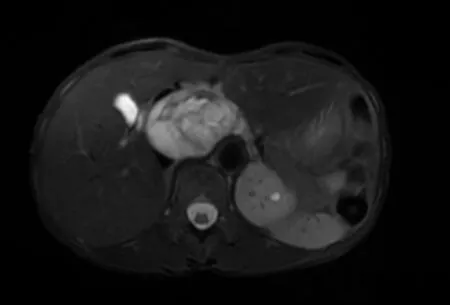
图2 MRI T2WI+FS呈混杂高信号

图3 增强后明显不均匀强化
2 讨论
PGL好发于颅底和颈部、胸腔、膀胱[3-6],而原发于肝门区罕见,本例原发于肝门区依据以下几点:(1)已完善胸部CT、腹部MR未发现他处有实质性肿瘤表现。(2)术后复查血、尿CA正常。(3)外院已完善MIBG显像,他处未发现有MIBG浓聚。因为对PGL的认知不够,其误诊率较高,且由于PGL与肝癌都是富血供肿瘤,CT和MRI难以鉴别,MIBG显像诊断价值高,但尚未普及。PGL被误诊及其危险,术中可由于挤压肿瘤导致大量CA入血引起PPGL危象,表现为严重的高血压、低血压反复交替发作,出现多脏器功能障碍,甚至休克、猝死等风险,切除肿瘤后可致明显低血压[1]。上述误诊病例术中均发生血压升高明显,部分预后不良。确诊PPGL需尽早手术切除肿瘤,但是围术期需要充分的准备:(1)术前需应用α-受体阻滞剂充分控制血压,如不理想,可加用CCB。β-受体阻滞剂适用于患者出现心动过速,且应用于α-受体阻滞剂之后,可能导致急性肺水肿和左心衰。(2)术中需严密监测和管理血压:若血压明显升高,可静脉滴注或泵入酚妥拉明或硝普钠;若心率增快或快速性心律失常时,可予艾司洛尔泵入治疗(选择性β1-受体阻滞剂且半衰期短)。(3)切除肿瘤后若血压下降明显,需尽快补充血容量,必要时使用血管活性药物[1]。
患者曾出现发热、血压升高,急查PCT 为0.93ng/ml,2d后PCT为41.13ng/L,但其无感染定位体征、血培养阴性、PCT高值时体温正常,未应用抗生素。PPGL合并PCT升高的相关报道较少,Schlumberger M等[2]在对20例发生远处转移恶性PPGL患者进行随访期间,发现PCT水平升高,但未阐述机制。某些研究发现一些神经内分泌肿瘤如“甲状腺髓样癌、部分类型肺癌、类癌综合征”可引起PCT水平升高[7-8]。PPGL属于神经内分泌肿瘤,亦可引起PCT升高。Trimboli P等[7]和Algeciras-Schimnich A等[8]发现可以通过监测PCT来判断甲状腺髓样癌有无复发,Avrillon V等[9]和Patout M等[10]发现肺癌可增加血清PCT水平,Patout M等[12]发现PCT升高提示肺癌的预后不良。目前鉴别良恶性PPGL主要是根据有无远处转移 ,是否也可以通过PCT来判断PPGL的远期预后和监测肿瘤复发,尚需要更多病例和长期随访。
[1] 中华医学会内分泌学分会肾上腺学组.嗜铬细胞瘤和副神经节瘤诊断治疗的专家共识.中华内分泌代谢杂志,2016,32(3):181-187.
[2] Schlumberger M,Gicquel C,Lumbroso J,et al.Malignant pheochromocytoma: clinical,biological,histologic and therapeuticdata in a series of 20 patients with distant metastases.J Endocrinol Invest,1992,15(9):631-642.
[3] Li ZJ,Lan XL,Hao FY,et al.Primary cerebellar paraganglioma:a pediatric case report and review of the literature.Pediatr Neurol,2014,50(4):303-306.
[4] Malec K,Cenda P,Brzewski P,et al.Paragangliomas of head and neck-A surgical challenge.J Craniomaxillofac Surg,2017,45(1):127-130.
[5] Muriana P,Bandiera A,Ciriaco P,et al.A case of endobronchial paraganglioma.Ann R Coll Surg Engl,2017,99(1):e28-e30.
[6] Katiyar R,Dwivedi S,Trivedi S,et al.Non-Functional Paraganglioma of the Urinary Bladder Treated by Transurethral Resection: Report of Two Cases.J Clin Diagn Res,2016,10(2):D1-D3.
[7] Trimboli P,Seregni E,Treglia G,et al.Procalcitonin for detecting medullary thyroid carcinoma: a systematic review.Endocr Relat Cancer,2015,22(3):R157-R164.
[8] Algeciras-Schimnich A, Preissner CM, Theobald JP, et al.Procalcitonin: a marker for the diagnosis and follow-up of patients with medullary thyroid carcinoma.J Clin Endocrinol Metab,2009,94(3):861-868.
[9] Avrillon V,Locatelli-Sanchez M,Folliet L,et al.Lung cancer may increase serum procalcitonin level.Infect Disord Drug Targets,2015,15(1):57-63.
[10] Patout M,Salaun M,Brunel V,et al.Diagnostic and prognostic value of serum procalcitonin concentrations in primary lung cancers.Clin Biochem,2014,47(18):263-267.
317000 浙江省台州医院心内科

