饮食干预对孤独症儿童相关症状改善的影响
崔永虹,戴晓红,徐新杰,尤 欣
孤独症谱系障碍(autism spectrum disorder,ASD)是一类儿童早期广泛性发育障碍类疾病,主要表现为社会交流和交往障碍,同时伴有局限兴趣和重复刻板行为[1],药物治疗疗效不佳,因此高额的康复费用和极差的预后给家庭和社会造成沉重负担。ASD的发病机制尚未完全阐明,目前认为可能与生命早期肠道菌群的失调、对某些特定种类的食物成分不耐受或变态反应等免疫状态异常有关[2-3]。ASD患者除神经系统功能异常之外,许多患儿常同时伴有胃肠道功能紊乱症状,如腹泻、便秘或胃肠胀气等[2]。近年来的研究提示,食物不耐受是某些特定种类的食物或营养物质引发的机体的异常反应,可导致腹痛、腹泻和腹胀等胃肠道症状的发生[4],其中一部分患者血液中存在大量的针对食物的IgG型抗体,可能与异常免疫反应有关。调查研究显示,普通人群中食物IgG抗体的检出率约为15%~20%[5],常见的不耐受食物主要包括牛奶、洋葱、豆类、甘蓝和小麦等[4];而ASD儿童中食物抗体的阳性率更高[6]。食物不耐受可增加ASD患儿的肠道通透性,进而可能会对神经系统的功能产生影响[7-8]。本研究主要探讨饮食干预3个月对ASD患儿孤独症主要症状、胃肠道症状、变态反应及挑食等方面的改善效果。
1 资料与方法
1.1 对象
采用前瞻性非随机对照研究方法,于2014年10月—2015年7月在北京市海淀区阳光友谊儿童康复训练中心招募儿童受试者,患者均在北京大学第六医院和北京市儿童医院确诊。纳入标准:(1)经专业儿童精神科医师确诊为ASD;(2)年龄2~8岁,男女不限;(3)不伴有其他神经系统疾病。
1.2 方法
1.2.1 受试者分组:所有受试儿童分为对照组和禁食组,其中对照组患儿仅接受常规行为康复训练;禁食组患儿在接受同等的常规行为康复训练的基础上接受3个月的不耐受食物禁食干预,不耐受食物主要包括麦麸、奶、蛋及检测出的其他不耐受食物。
1.2.2 症状评估:研究开始前和完成后采用儿童孤独症评定量表(Childhood Autism Rating Scale,CARS)和临床语言功能问卷(Clinical Language State Questionnaire,CLSQ)对儿童的孤独症行为和语言功能进行评分。此外为探讨饮食干预对ASD儿童其他相关症状的改善作用,通过问卷调查的形式对研究前后患儿胃肠道、睡眠障碍、兴奋、变态反应和挑食症状进行比较,其中胃肠道症状主要包括腹痛、腹泻、便秘、腹胀、打嗝等;睡眠症状主要包括入睡困难、早醒等;兴奋症状包括坐立不安或多动、不明原因的极度开心、情绪高昂、傻笑等;变态反应现象包括皮肤红肿、皮肤瘙痒、哮喘等。
1.3 统计学方法
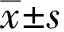
2 结果
2.1 受试者基线特征
本研究共招募符合入组标准的ASD儿童47例,其中对照组15例,饮食干预组 32例。两组儿童间性别构成比、年龄及干预前CARS和ABC评分差异均无统计学意义(表1)。
2.2 两组患儿干预前后ASD症状评分比较
2.2.1 干预前后CARS评分比较:干预前后对照组患儿CARS评分分别为34.5±6.6和31.6±5.7,差异无统计学意义(P>0.05);饮食干预后3个月禁食组患儿CARS评分为29.3±5.2,较干预前的34.4±6.3显著下降,差异有统计学意义(P<0.001)(图 1)。治疗后3个月对照组7例患儿CARS评分较干预前下降,约占46.7%;禁食组23例患儿CARS评分较干预前下降,约占71.9%(表 2)。
2.2.2 两组患儿干预前后CLSQ评分变化:干预前后对照组患儿CLSQ表达评分和认知评分差异无统计学意义(CLSQ表达评分: 4.2±3.3vs. 5.4±3.4,P>0.05;认知评分: 5.3±2.1vs. 6.1±1.8,P>0.05),禁食组患儿饮食干预3个月后CLSQ表达评分和认知评分较干预前均明显上升,其中CLSQ表达评分由干预前的4.2±3.0上升为干预后的6.8±2.9, CLSQ认知评分由干预前的5.7±2.4上升为干预后的7.4±1.9,差异均有统计学意义(均P<0.01)(图2)。干预后3个月对照组有8例患儿CLSQ表达评分较干预前上升,约占53.3%;禁食组24例患儿CLSQ表达评分较干预前上升,约占75.0%。对照组5例患儿CLSQ认知评分较3个月前上升,约占33.3%;禁食组17例儿童CLSQ认知评分较干预前上升,约占53.1%(表 2)。
2.3 两组患儿干预前后其他相关症状的改善情况
禁食组患儿在胃肠道症状、兴奋症状和挑食方面的改善例数明显高于对照组。干预前对照组患儿存在胃肠道症状者11例,干预后3个月仅有1例改善,占9.1%;干预前禁食组患儿存在胃肠道症状者27例,干预后3个月14例改善,占51.9%。

表1 受试者干预前基本信息Table 1 Demography of the subjects before food management
A:Fisher精确概率法;b:独立样本t样本;CARS:儿童孤独症评定量表;ABC:孤独症行为量表

图 1 对照组与禁食组ASD患儿干预前后CARS量表评分比较Fig 1 Comprison of CARS scores both in control group and food management before and after food control与各自组干预前比较,aP<0.001(配对t检验, 对照组:n=15;禁食组:n=32) CARS:儿童孤独症评定量表
干预前对照组存在兴奋症状者13例,干预后3个月5例患儿兴奋症状减轻,占38.5%;干预前禁食组存在兴奋症状者30例,干预后3个月24例兴奋症状减轻,占80.0%。对照组12例挑食患儿干预后症状均无改善,而禁食组26例存在挑食问题的患儿干预后3个月10例症状改善,占38.5%。在的改善率方面,禁食组患儿胃肠道症状、兴奋症状和挑食改善率均多于对照组,差异均有统计学意义(均P<0.05)。对照组和禁食组患儿睡眠障碍率分别为25%(3/12)和41.7%(10/24),变态反应症状改善率分别为33.3%(2/6)他33.3%(7/21),两组比较差异均无统计学意义(均P>0.05)。
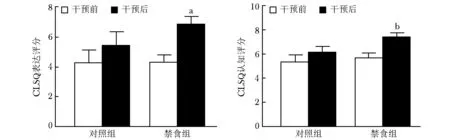
图2 对照组与禁食组ASD患儿干预前后CLSQ量表评分比较
Fig2 Comprison of CLSQ scores both in control group and dietery intervention group before and after food control
与干预前比较,aP<0.001; 与干预前比较,bP<0.05(配对t检验.对照组:n=15;禁食组:n=32); CLSQ:临床语言功能问卷

表2 两组患儿干预3个月后ASD相关症状缓解情况[n(%)]Table 2 Comprison of symptom improvement betweentwo groups before and after food control[n(%)]
CARS:儿童孤独症评定量表;CLSQ:临床语言功能问卷
3 讨论
本研究结果表明,与仅接受常规行为康复训练的对照组ASD儿童相比,在常规行为康复训练的基础上接受为期3个月的不耐受食物禁食可改善ASD儿童的相关症状,缓解胃肠道、兴奋和挑食症状。
对某些特定的食物或营养成分不耐受在ASD儿童中是一种较常见的现象。研究曾发现,部分ASD儿童体内可检测到针对谷蛋白和酪蛋白的抗体[9]。另有研究结果也表明,ASD儿童食物不耐受的检出率显著高于对照组,且食物不耐受患儿的症状较重[10]。食物不耐受可导致肠道黏膜炎症,并可引发包括腹胀、嗳气、腹泻和便秘等多种胃肠道症状[4]。
目前认为,ASD儿童对特定食物或营养成分的不耐受可能与其体内某些消化酶活性、免疫功能异常、肠道通透性增加及肠道菌群紊乱等多种因素有关[4,6]。ASD儿童肠道通透性的增加可使肠道内某些毒素和大分子异常代谢产物(如未被彻底消化的多肽片段)更易于透过肠黏膜屏障进入体内,影响机体免疫系统和其他神经递质的功能,可能引发ASD儿童的异常行为[8,11-12]。
目前国内外开展了多项通过饮食干预治疗ASD儿童相关症状的探索性研究,表明当去除食物中的谷蛋白或/和酪蛋白(gluten-free and casein-free diet,GFCF)后,部分ASD儿童的症状较未限制饮食的对照组改善更明显,主要为交流能力和注意力的改善[13-15]。我国研究者对37例伴有胃肠道功能紊乱的ASD儿童所做的小样本量研究发现,与未禁食患者相比,禁食敏感食物在短期内可改善儿童的孤独症症状,使ABC量表评分下降,但长期效果不显著[16]。然而,Harris 等[17]的研究则表明,对于接受GFCF饮食的儿童而言,尽管儿童父母反馈儿童的胃肠道症状和行为方式会有改善,但CARS和胃肠道症状评分则无明显变化。此外,值得注意的是,此种限制饮食疗法的具体效果存在个体差异,故并非所有儿童在接受此种疗法后都会获得同样的效果。这些研究结果提示,限制饮食疗法对某些ASD儿童可能会有一定的益处,但孤独症作为一类谱系障碍性疾病,不同患者之间在疾病的症状表现形式和具体发病机制上并不完全相同,限制饮食疗法的具体效果和适应人群尚需大规模随机对照双盲临床试验加以证实。
需要特别指出的是,长期禁食不耐受食物对儿童营养状况和生长发育的不良作用目前尚缺乏一致的结论。Johnson等[18]发现,禁食谷蛋白和酪蛋白3个月后ASD儿童的营养状况与接受常规饮食的ASD患儿相比无显著差异,也未观察到其他不良反应。Marí-Bauset 等[19]发现禁食谷蛋白和酪蛋白的ASD患儿体重指数及钙、磷和钠的摄入较低,建议对这些儿童同时补充维生素D。Hediger 等[20]对儿童骨皮质厚度进行测量,发现ASD患儿第二掌骨的骨皮质偏薄,接受谷蛋白和酪蛋白禁食疗法的患儿二掌骨骨皮质变薄更明显。上述研究提示在饮食干预的同时应及时监测儿童的营养状况,长期禁食不耐受食物对儿童生长发育的影响尚需进一步的大规模研究加以证实。
作为一项以儿童为研究对象的探索性实验,本研究主要存在以下几点不足:(1)本研究所涉及的胃肠道、兴奋及睡眠障碍症状主要通过问卷调查的方式获得,儿童父母在问卷填写的过程中不可避免地存在一定的主观性;(2)研究纳入的样本量较小,且受试儿童的分组为非随机双盲分组,研究可能存在一定的偏倚;(3)本研究尚未评估饮食干预对儿童相关症状改善的长期效果进行随访追踪。
尽管本研究尚存在以上不足,但作为一项探索性的临床研究,本研究的结果仍可说明禁食不耐受食物可在一定程度上缓解部分ASD患儿的相关症状,并改善患儿的胃肠道、兴奋、挑食症状,因此研究结果对孤独症患儿的康复治疗和发病机制研究可提供新的思路和视角。

