内毒素促进调节性T 细胞增殖预防哮喘炎症反应
牟密 胡超 王润生 胡鹏 徐丽娜 徐国纲
1解放军医学院,北京100853;2解放军总医院第八医学中心保健科,北京100091;3解放军总医院第二医学中心老年病研究中心,北京100853
支气管哮喘 (哮喘)是一种以Th2型细胞分化为主的炎症反应,临床表现为气道高反应性、炎细胞浸润、气道重塑[1-2]。内毒素是革兰阴性细菌细胞壁中的一种成分, 也叫做脂多糖(lipopolysaccharide,LPS),通过被抗原递呈细胞识别,诱导机体炎症反应,过去被认为是一种毒素,比如诱导急性肺损伤模型。但也有研究表明,生命早期阶段接触LPS可以降低哮喘发病率,在幼年期给予LPS刺激后,哮喘的发生率及严重程度会降低[3]。在欧洲奥地利、德国、瑞士农村地区,农场有奶牛的家庭,儿童过敏性疾病患病率较低,同样也提示细菌具有某些预防过敏性疾病的作用[4]。LPS结构非常复杂,主要由O 抗原、核心区域、脂质A 三部分构成,功能、机制多样[5],既有细胞毒性作用,也可以减轻过敏性疾病,具体功能、机制目前存在争议,仍需进一步探讨。我们推测给予LPS可能会抑制哮喘炎症反应,且不同给药方式会对机体产生不同免疫反应,本实验用卵清蛋白(ovalbumin,OVA)诱导哮喘模型,实验组提前给予LPS滴鼻,从肺组织病理、炎细胞浸润、细胞因子及分化趋向、蛋白水平等多维度,采用病理染色、酶联免疫吸附试验 (enzyme-linked immunosorbent assay,ELISA)、免疫印迹、流式细胞分析等多种方法,论证LPS不同时间节点和剂量预处理方式对哮喘的预防作用及机制,以期对哮喘的防治提供理论支撑。
1 材料与方法
1.1构建动物模型 采用6~8周龄BALB/c雌性小鼠,动物饲养许可证号:SYXK (京)2018-0002,体质量20~22 g,购于北京维通利华实验动物有限责任公司,饲养于首都医科大学动物实验中心SPF级屏障动物部,喂养不含OVA 的小鼠饲料和水,每笼5只,环境温度25 ℃,湿度为45%~55%,每日光照12 h。LPS 给药1 次组 (LPS1组)小鼠在第3天给予30μg LPS溶于50μl无菌生理盐水滴鼻;LPS给药2次组 (LPS2组)在第0天给予0.1μg LPS溶于无菌生理盐水滴鼻,第3天滴鼻30μg LPS溶于50μl无菌生理盐水。OVA和氢氧化铝佐剂按体积1∶1混匀,第6、13天腹腔注射200μl致敏 [OVA,500 mg/L,阴性对照组(NS 组)用无菌生理盐水代替OVA]。第17天至第22天用OVA 滴鼻激发 (溶于无菌生理盐水,50μl,1 g/L),用OVA 致敏和激发的OVA组作为阳性对照组(OVA 组),图1。
1.2肺功能及取材 在最后一次OVA 滴鼻24 h后,腹腔注射2%戊巴比妥钠,待小鼠麻醉后,将小鼠置于解剖台上,用眼科剪剪开气管做T 型切口,插入气管插管针,将小鼠以仰卧位方式通过气管插管与小动物肺功能测量仪相连接后,进行压力-容积曲线测定,用生理盐水和不同梯度的乙酰胆碱溶液(顺序:0、6、12、24、48 g/L)雾化激发10 s,1 min后测定肺组织力学参数。得到总气道阻力与乙酰甲胆碱剂量反应曲线。各组小鼠采集完肺功能数据后,将小鼠置于解剖台上,分2次通过金属插管向气管注入1 ml无菌PBS灌洗液,反复抽吸后回收约1.5 ml肺泡灌洗液,取50μl涂在载玻片上,静置30 min 后滴4%多聚甲醛溶液固定。剩余肺泡灌洗液离心,上清-80 ℃冻存。剪开胸腔,使用20 ml注射器于右心室注入预冷PBS冲洗肺部血液,待肺变白后,获取小鼠肺组织标本。
1.3炎细胞分类计数 将收集的肺泡灌洗液离心后,收集上清,-80 ℃冻存,然后在细胞沉淀中加红细胞裂解液并室温孵育4 min,加PBS终止反应,稀释后取10μl放入自动计数仪计数,计数完细胞总数后,取50μl细胞悬液制片,待快干燥后用50μl 4%多聚甲醛固定。干燥后用刚果红染色,至少计数300个细胞并进行细胞分类,分别计算巨噬细胞、嗜酸粒细胞、中性粒细胞和淋巴细胞数量。
1.4病理染色
1.4.1HE 染色 用切片机将肺石蜡包块切成厚度4μm 切片,依次浸入二甲苯脱去石蜡,浸入降梯度乙醇、蒸馏水2 min水化。苏木精染色5 min,流水冲洗。1%盐酸酒精脱水后伊红染色10 s,依次浸入升梯度乙醇脱水,浸入二甲苯透明。最后中性树胶封片,普通光学显微镜观察拍片。
1.4.2过碘酸-希夫 (periodicacid-schiff,PAS)染色 石蜡切片放置在60 ℃恒温箱中烘烤,浸入二甲苯Ⅰ脱去石蜡,依次浸入降梯度乙醇水化,用高碘酸溶液染色,切片充分蒸馏水洗10 min,Schiff避光染色,苏木素浅染细胞核,升梯度酒精脱水,最后二甲苯透明,中性树胶封片。
1.4.3刚果红染色 石蜡切片放置在60℃恒温箱中烘烤,浸入二甲苯Ⅰ脱去石蜡,依次浸入降梯度乙醇水化,刚果红染色,流水冲洗后苏木精染色3 min,1%盐酸酒精脱水,升梯度酒精脱水,最后二甲苯透明,中性树胶封片。
1.5ELISA 方法检测细胞因子 采用ELISA 试剂盒,按试剂盒说明书操作,包被后放入冰箱,隔日加入样品和配置标准品孵育,加入检测抗体孵育,加入Avidin-HRP 结合检测抗体,孵育30~60 min后加入TMB显色,最后用稀释的硫酸终止后放入酶标仪检测底物吸光度值。
1.6流式细胞术 将制备的单细胞悬液置于冰上待用,采用PE Anti-Mouse Foxp3(3G3)、FITC Anti-Mouse CD4 (RM4-5)、Ghost DyeTMViolet 510,购于美国Tonbo 公司。数据采集采用FACSAriaII(BD Biosciences),数据分析采用Flow Jo 10.0。
1.7统计学分析 采用SPSS 19.0、Graph Pad Prism 7等软件进行统计分析,所有实验数据符合正态分布,采用t 检验、Two-way ANOVA 方法分析,P <0.05为差异有统计学意义。
2 结果
2.1LPS组小鼠的气道高反应性低 为了探索哮喘机制,我们分2种方式用LPS预处理随机分组的BALB/c小鼠,然后用OVA 联合铝佐剂诱导动物哮喘模型 (图1),实验随机分为4 组:LPS1组、LPS2 组、NS 组、OVA 组。在 最 后1 次OVA 滴鼻激发24 h后,连接动物呼吸机检测总气道阻力,不同乙酰甲胆碱浓度激发时组间比较。总气道阻力OVA 组最高,LPS1组和LPS2组较低,NS组最低 (图2),统计方法采用多因素方差分析,乙酰甲胆碱为24 g/L、48 g/L时,LPS1组和LPS2 组的总气道阻力较OVA 组低,P <0.05。由此推断OVA 腹腔致敏前给予LPS 可以改善总气道阻力。

图1 脂多糖预处理节点及卵清蛋白哮喘模型构建方法
2.2各组炎细胞浸润和肺组织病理评分 为了探寻各组肺组织炎细胞浸润和黏液分泌情况,石蜡包埋肺组织切片后进行HE染色和PAS染色并评分。LPS1组、LPS2 组比NS 组炎细胞浸润多,但较OVA 组炎症减轻 (图3),HE 染色炎症评分也低于OVA 组(图4)。OVA 组支气管、血管周围大量炎细胞浸润,而LPS1组和LPS2组炎细胞浸润数量较少,LPS2组减少更加明显。PAS染色提示LPS组黏液糖原分泌也较OVA 组有明显减少 (图5),PAS染色评分同样证实这一点 (图6)。我们将收集的支气管肺泡灌洗液涂片染色,2人独立分别显微镜下计数至少300个细胞,炎细胞浸润绝对数提示OVA 组中性粒细胞和嗜酸粒细胞最高,LPS组炎细胞绝对数较少,哮喘密切相关的嗜酸粒细胞组间较OVA 组降低非常明显,LPS2组嗜酸粒细胞减少更为显著 (图7)。可见LPS可以抑制OVA 诱导哮喘黏液的分泌和炎细胞募集,具有显著的病理学差异。

图2 各组不同乙酰甲胆碱浓度激发下的气道高反应性差异
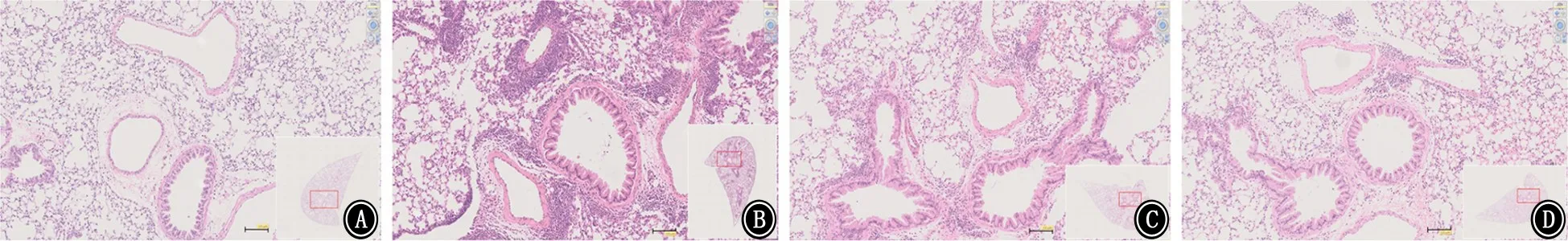
图3 肺组织HE染色 HE ×100 A:生理盐水阴性对照组;B:卵清蛋白组;C:LPS给药1次组;D:LPS给药2次组
2.3LPS预处理调节细胞因子和调节性T 细胞(regulatory T cells,Treg) 为了比较各组之间细胞因子水平的炎症变化,我们采用ELISA 的方法检测肺组织匀浆上清中细胞因子变化。IL-6 是非常重要的炎症上游因子,与很多炎症相关[6],IL-5、IL-13 是重要的哮喘代表性Th2 细胞因子[7],而IL-10家族细胞因子通过抑制炎症反应过度,上调先天免疫功能,促进组织修复机制,在感染和炎症过程中发挥维持组织稳态的重要作用[8]。LPS1、LPS2组与OVA 组比较,IL-6、IL-5、IL-13明显降低,而抑炎因子IL-10在LPS组中呈升高趋势(图8~11)。Treg具有免疫保护的功能,能分泌转化生长因子β 和IL-10 调节炎症平衡,Foxp3是Treg细胞最重要的标志,其表达决定了CD4+T 细胞向Treg细胞分化。为了进一步探索这种保护机制,我们用CD4+Foxp3+标记肺组织单细胞悬液,通过比较CD4+Foxp3+T 细胞比例,可以看到LPS2组的Treg细胞较OVA 组有所增加(图12),LPS2 组与OVA 差异有统计学意义(P <0.05),由此我们推断,早期给予低剂量LPS联合中等剂量LPS刺激后,可以促进Treg细胞增殖。

图4 肺组织HE染色炎症评分
3 讨论
细菌是与人类共生的微生物,在每一个人的身体中大概有500~1 000种不同种类的细菌,这些细菌大多与其宿主建立有益的共生关系,对宿主的新陈代谢和消化效率做出重要贡献[9]。LPS 是革兰阴性菌细胞壁的主要成分,在免疫系统识别细菌的过程中起到重要作用,但是具体机制仍然不清楚。在先天性免疫系统中,模式识别受体可以通过十多种Toll样受体识别LPS、脂蛋白、鞭毛来识别细菌,让有限的配体受体结合方式识别数百种细菌成为可能,LPS、脂蛋白等细菌的表面一定存在共同的结构模式[10]。通过识别细菌表面LPS,机体产生预警机制,提高适应性免疫能力。

图5 肺组织过碘酸-希夫染色 过碘酸-希夫 ×100 A:生理盐水阴性对照组;B:卵清蛋白组;C:LPS给药1次组;D:LPS给药2次组

图6 肺组织过碘酸-希夫染色评分
支气管嗜酸粒细胞浸润是过敏性哮喘重要特征之一,我们通过支气管肺泡灌洗液刚果红染色及电镜下分类细胞计数证明了LPS1组、LPS2组的嗜酸粒细胞数量较OVA 组明显减少。已经有研究证明,生命早期接触LPS能通过JAK 激酶2-信号转导及转录激活因子6 (janus kinase 2-signal transducersand activators of transcription 6,JAK2-STAT6)通路抑制Muc5ac黏蛋白,抑制气道黏液分泌[3],在本实验中肺组织HE 染色、PAS染色中也证实了LPS减轻炎症和黏液分泌。
过敏性哮喘Th2 型细胞因子分泌增多,IL-4和IL-13可以促进杯状细胞化生并分泌黏液,IL-5主要作用是促进嗜酸粒细胞募集并导致气道炎症、气流受限、气道高反应性,无论是儿童早发型哮喘还是成人迟发型哮喘都伴随着嗜酸粒细胞的增高,IL-5抗体有效并已经在临床上运用[11]。本研究检测了IL-5和IL-13,发现LPS能阻碍OVA 诱导小鼠产生Th2型细胞因子IL-5和IL-13,但LPS1组和LPS-2组的Th2型细胞因子2组之间差异无统计学意义。

图7 肺泡灌洗液中各组间中性粒细胞、嗜酸粒细胞、巨噬细胞、淋巴细胞比较
IL-6 是早期的炎症因子,通过与IL-6 受体gp130结合,调控JAK/STAT 信号通路参与众多炎症反应,调控T 细胞的增殖、存活和分泌并调节其效应细胞因子的产生,影响Th1型和Th2型细胞增殖和活性[12]。IL-10是重要的抑炎因子,属于IL-10家族,通过JAK/STAT 信号通路调控免疫,虽然几乎所有的T 细胞亚群都能够分泌IL-10,但对于调节性T 细胞来说尤为重要,来源于胸腺的Foxp3+Treg细胞能够分泌IL-10抑制免疫应答[13]。有研究表明金黄色葡萄球菌特异的Th17细胞产生大量的IL-17,但不产生IL-10,但当在激活状态(刺激后3~5 d)测试时,相同的细胞产生高水平的IL-10,同时瞬时降低IL-17的产生,推断IL-10产生的延迟动力学可能是由于需要重塑IL-10位点以允许转录[14-15]。
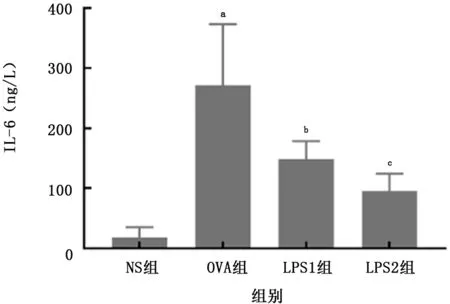
图8 肺组织匀浆用酶联免疫吸附试验检测IL-6

图9 肺组织匀浆用酶联免疫吸附试验检测IL-5
因此在时间节点的选择上,我们选择了提前3 d或6 d这个节点,在实验中我们发现,提前给予小剂量1μg LPS 的LPS2 组能够促进CD4+Foxp3+细胞增殖。我们还发现与致敏滴鼻1次相比,提前给予小剂量联合中等剂量LPS滴鼻的小鼠比单纯致敏前滴鼻1次的小鼠嗜酸粒细胞数量更低,Treg细胞数量也较多。但是LPS1组和LPS2组为何存在差异的具体机制仍然不清楚,可能与LPS给药时间和剂量有关。LPS 结构和作用非常复杂,LPS被机体识别可能涉及的细胞信号通路包括核因子激活的B细胞的κ-轻链增强途径、干扰素调节因子3途径、JAK/STAT 途径、丝裂原活化蛋白激酶途径等[16-19],我们将继续探索LPS干预免疫调控的相关机制,为哮喘的防治提供新的思路。
利益冲突所有作者均声明不存在利益冲突

图10 肺组织匀浆用酶联免疫吸附试验检测IL-13

图11 肺组织匀浆用酶联免疫吸附试验检测IL-10

图12 各组肺组织单细胞悬液调节性T细胞比例 A:生理盐水阴性对照组;B:卵清蛋白组;C:脂多糖给药1次组;D:脂多糖给药2次组
[4] Illi S,Depner M,Genuneit J,et al.Protection from childhood asthma and allergy in alpine farm environments-the GABRIEL advanced studies[J].J Allergy Clin Immunol,2012,129(6):1470-1477.e6.DOI:10.1016/j.jaci.2012.03.013.
[5] Beutler B,Rietschel ET.Innate immune sensing and its roots:the story of endotoxin[J].Nat Rev Immunol,2003,3(2):169-176.DOI:10.1038/nri1004
[6] Hunter CA,Jones SA.IL-6 as a keystone cytokine in health and disease[J].Nat Immunol,2015,16(5):448-457.DOI:10.1038/ni.3153.
[7] Nakayama T,Hirahara K,Onodera A,et al.Th2 cells in health and disease[J].Annu Rev Immunol,2017,35:53-84.DOI:10.1146/annurev-immunol-051116-052350.
[8] Ouyang W,O'Garra A.IL-10 family cytokines IL-10 and IL-22:from basic science to clinical translation[J].Immunity,2019,50(4):871-891.DOI:10.1016/j.immuni.2019.03.020.
[9] Hooper LV.Do symbiotic bacteria subvert host immunity[J]?Nat Rev Microbiol,2009,7(5):367-374.DOI:10.1038/nrmicro2114.
[10] Rathinam VAK,Zhao Y,Shao F.Innate immunity to intracellular LPS[J].Nat Immunol,2019,20(5):527-533.DOI:10.1038/s41590-019-0368-3.
[11] Leckie MJ,ten Brinke A,Khan J,et al.Effects of an interleukin-5 blocking monoclonal antibody on eosinophils,airway hyper-responsiveness,and the late asthmatic response[J].Lancet,2000,356(9248):2144-2148.DOI:10.1016/s0140-6736(00)03496-6.
[12] Rincón M,Anguita J,Nakamura T,et al.Interleukin(IL)-6 directs the differentiation of IL-4-producing CD4+T cells[J].J Exp Med,1997,185(3):461-469.DOI:10.1084/jem.185.3.461.
[13] Shouval DS,Biswas A,Goettel JA,et al.Interleukin-10 receptor signaling in innate immune cells regulates mucosal immune tolerance and anti-inflammatory macrophage function[J].Immunity,2014,40(5):706-719.DOI:10.1016/j.immuni.2014.03.011.
[14] Dong J,Ivascu C,Chang HD,et al.IL-10 is excluded from the functional cytokine memory of human CD4+memory T lymphocytes[J].J Immunol,2007,179(4):2389-2396.DOI:10.4049/jimmunol.179.4.2389.
[15] Zielinski CE,Mele F,Aschenbrenner D,et al.Pathogeninduced human TH17 cells produce IFN-γor IL-10 and are regulated by IL-1β[J].Nature,2012,484(7395):514-518.DOI:10.1038/nature10957.
[16] Shakhov AN,Collart MA,Vassalli P,et al.Kappa B-type enhancers are involved in lipopolysaccharide-mediated transcriptional activation of the tumor necrosis factor alpha gene in primary macrophages[J].J Exp Med,1990,171(1):35-47.DOI:10.1084/jem.171.1.35.
[17] Han J,Lee JD,Bibbs L,et al.A MAP kinase targeted by endotoxin and hyperosmolarity in mammalian cells[J].Science,1994,265(5173):808-811.DOI:10.1126/science.7914033.
[18] Hambleton J,Weinstein SL,Lem L,et al.Activation of c-Jun N-terminal kinase in bacterial lipopolysaccharide-stimulated macrophages[J].Proc Natl Acad Sci U S A,1996,93(7):2774-2778.DOI:10.1073/pnas.93.7.2774.
[19] Herrera-Velit P, Knutson KL, Reiner NE.Phosphatidylinositol 3-kinase-dependent activation of protein kinase C-zeta in bacterial lipopolysaccharide-treated human monocytes[J].J Biol Chem,1997,272(26):16445-16452.DOI:10.1074/jbc.272.26.16445.

