骨标志物水平与2型糖尿病患者心血管疾病风险研究
刘 艳,曾高峰
(南华大学附属第二医院内科,湖南 衡阳 421000)
糖尿病病情具有迁延性特征,易患心血管疾病(cardiovascular disease,CVD),其出现CVD的风险是正常人的2~4倍[1]。研究表明[2],血管壁中钙磷物质的大量沉积,会引起血管钙化。近期研究发现,血管钙化与骨形成机制具有相似性,主要表现为血管的平滑肌细胞(vascular smooth muscle cell,VSMC)出现成骨样分化征。临床研究发现[3],高血糖可诱导VSMC增殖及表达骨标志物。在这些骨标志物中,骨钙蛋白、骨桥蛋白和骨粘连蛋白通过阻断羟基磷灰石形成来抑制VSMC的钙化[4-6]。骨保护素可以抑制骨和血管组织中的破骨细胞分化,被认为是血管钙化和CVD风险的保护因素[7]。碱性磷酸酶能导致血管内稳态受损并增加骨代谢,较高水平的碱性磷酸酶与CVD风险增加有关[8]。骨硬化蛋白是一种有效的骨形成抑制剂,在肾功能受损的患者,骨硬化蛋白水平随着肾功能的恶化而增加[9]。然而,目前缺乏前瞻性证据来研究这些骨标志物与CVD事件之间的关系。因此,本研究旨在评估6种骨标志物(骨钙蛋白、骨硬化蛋白、骨桥蛋白、碱性磷酸酶、骨粘连蛋白以及骨保护素)是否与2型糖尿病患者的CVD风险相关。
1 资料与方法
1.1 一般资料
选择2014年1月至2017年1月间进入本院的2型糖尿病患者(40~60岁)作为研究对象,随访3年,随机选取无CVD患者(n=100)和CVD患者(n=100)进行对比分析。纳入标准:与《中国2型糖尿病防治指南(2017年版)》内2型糖尿病的相关诊断标准相符[10];排除标准:(1)入组研究前已出现CVD;(2)并发继发性、原发性的骨代谢紊乱性病症;(3)入组前90天内曾接受会对骨代谢产生影响的药物治疗;(4)并发全身性严重性病症;(5)合并严重性感染或创伤;(6)合并恶性肿瘤。
1.2 检测方法
1.2.1 资料收集方法 于基线时,对所有患者一般资料进行收集,包括性别、年龄、收缩压、抽烟史、体重指数(BMI)及糖尿病病程等。同时,对患者空腹静脉血样进行采集,以全自动生化分析仪对其血清指标进行测定,具体包括糖基化血红蛋白检测(HbA1c)、总胆固醇检测(TC)、高敏C反应蛋白检测(Hs-CRP)、甘油三酯检测(TG)、高密度脂蛋白胆固醇检测(HDL-C)以及低密度脂蛋白胆固醇检测(LDL-C),并以CKD-EPI公式对肾小球滤过率(eGFR)进行计算。
1.2.2 骨标志物的检测 在基线时,于4 ℃环境下,按3 000 r/min离心15 min,常规分离血浆后,存储于-80 ℃冰箱内待测。以酶联免疫吸附试验对骨钙蛋白、骨硬化蛋白、骨桥蛋白、碱性磷酸酶、骨粘连蛋白以及骨保护素进行测定,测试所用试剂盒由上海钦诚生物科技有限公司所提供,测定流程参考设备及试剂说明书。
1.2.3 临床终点 给予患者展开3年随访,有27例患者失访,完成随访的患者中,随机选取出现CVD的糖尿病患者100例(CVD组)和未出现CVD的糖尿病患者100例(无CVD组)作为研究对象。CVD组包括:心脏血管性疾病(因心血管疾病死亡、因急性心衰事件而住院、心肌梗死、不稳定型心绞痛、行冠状动脉支架治疗及支架内血栓形成者等)、脑血管疾病(经MRI或CT检查诊断为缺血性脑卒中)、外周血管疾病(根据2014年ACC/AHA发布的降低成人动脉粥样硬化性心血管疾病风险胆固醇管理指南:踝臂指数小于0.9诊断为PDA)。
1.3 统计学方法
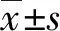
2 结 果
2.1 心血管病相关指标检测分析
两组患者的临床基线及实验室检查比较如表1所示,两组患者的性别、吸烟率、收缩压、总胆固醇、高密度脂蛋白胆固醇、HbA1c、eGFR以及Hs-CRP比较差异无统计学意义(P>0.05),而CVD组患者的年龄、BMI、糖尿病病程、LDL-C、骨钙素、骨硬化蛋白、骨桥蛋白、碱性磷酸酶、骨粘连蛋白以及骨保护素水平显著高于无CVD组(P<0.05)。

表1 心血管病指标检测
2.2 Cox回归风险分析
2型糖尿病出现CVD的Cox回归风险:以2型糖尿病患者出现CVD作为因变量,以6种骨标志物为自变量,其变量赋值为实测值,校正了年龄、BMI、eGFR水平、糖尿病病程、LDL-C水平、吸烟率及HbA1c水平后,分析各指标发现骨桥蛋白是2型糖尿病CVD发生的重要因素(P<0.001),骨钙素、骨硬化蛋白、碱性磷酸酶、骨粘连蛋白和骨保护素等与2型糖尿病CVD发生的关系无统计学意义(P>0.05)(见表2)。
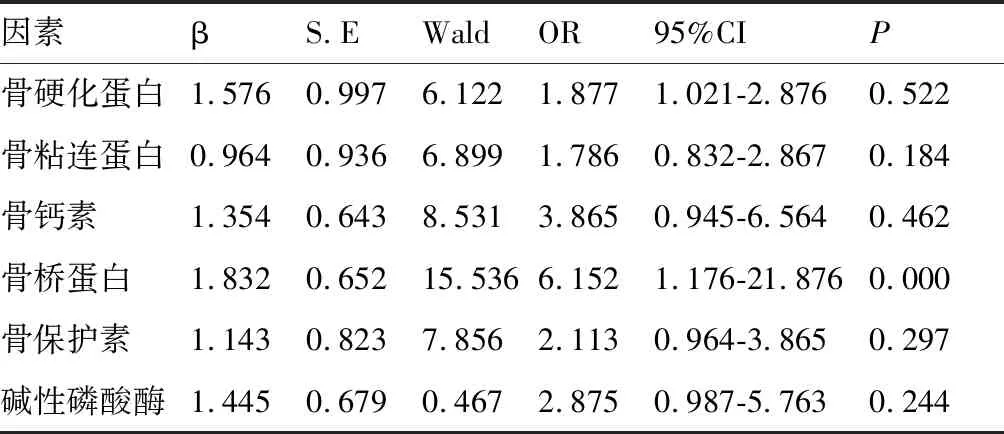
表2 2型糖尿病出现CVD的Cox回归风险
3 讨 论
近年来,糖尿病患病率逐年增加,且研究发现,血脂水平异常、高血压、抽烟及肥胖等CVD危险因素与糖尿病存在一致性,且CVD还会对2型糖尿病患者的长期预后水平产生影响。可见,找到糖尿病反映CVD风险的可靠的指标对减少糖尿病死亡率至关重要。最近研究显示,血管钙化在糖尿病患者并发CVD中起重要作用[13]。鉴于此,本研究评估了6种与血管钙化密切相关的骨标志物与2型糖尿病患者CVD风险之间的关系。Cox回归分析结果显示,高水平的骨桥蛋白能增加CVD发病的风险。
研究发现,血管钙化是CVD发病率和死亡率的重要预测因子,而血管钙化的发生发展取决于血管微环境中多种骨标记物的失衡,表现为促成骨因子的增加或/和抑制成骨因子的减少[10]。本研究首次探讨了6种重要的骨标志物与2型糖尿病患者CVD风险之间的联系。结果提示,在校正传统的危险因素下,骨桥蛋白与CVD风险存在显著的正相关性。骨桥蛋白是一种多功能蛋白质,在一些如粥样硬化等慢性炎症性疾病中高度表达,参与炎症因子的释放与趋化作用。研究提示[11],通过中和抗体抑制骨桥蛋白的活性能改善2型糖尿病胰岛素抵抗的程度。此外,在血管钙化区域,骨桥蛋白丰度明显升高,参与羟基磷灰石形成。因此,血浆骨桥蛋白水平的增高,可能会使血管钙化现象的发生风险增加,也可能加大2型糖尿病患者出现CVD的风险。
尽管本研究中未发现骨钙蛋白、骨粘连蛋白、骨保护素、碱性磷酸酶和骨硬化蛋白与糖尿病CVD风险之间存在关联性,但它们作为CVD风险预测的因子的潜在作用仍不可忽视。有趣的是,在老年男性(>70岁)中,较高的血浆骨钙蛋白水平与CVD风险的降低有关[12-13],而在老年女性这一关系却恰恰相反。在维持性血液透析的患者中,骨钙蛋白是心血管事件独立而可靠的预测因素。动脉粥样硬化斑块中检测到骨粘连蛋白,但缺乏针对骨粘连蛋白和CVD风险的队列研究。关于碱性磷酸酶水平与既往的前瞻性研究提示,碱性磷酸酶水平与老年男性CVD风险与卒中发生率增加相关[14]。然而,另外两项大规模前瞻性研究[15]没有发现碱性磷酸酶水平与卒中发病率或CVD死亡率的存在任何关联。骨硬化蛋白是骨形成的有效抑制剂,因此减少血管钙化。然而,本研究在2型糖尿病患者中,未发现骨钙蛋白、骨粘连蛋白、骨保护素、碱性磷酸酶和骨硬化蛋白与CVD发病率之间存在关联,考虑与下面两个因素有关:其一,入选的患者样本量较少,且eGFR基本在正常范围内,与既往文献的基础疾病状态不同;其二,入选的患者年龄在60岁左右,但骨质疏松及骨折发生率较低,部分骨标志物水平相对较低,导致其与CVD缺乏关联。因此,这一阴性的结果需要进一步的研究证实。
综上所述,高血浆骨桥蛋白水平是2型糖尿病患者并发CVD的危险因素。而骨钙蛋白、骨粘连蛋白、骨保护素、碱性磷酸酶和骨硬化蛋白与CVD风险并无显著的关联性。今后尚需要大样本、多中心以及前瞻性的研究进一步证实。

