机器人辅助腹腔镜根治性前列腺切除术中移行带前列腺癌切缘阳性的危险因素
李友健,杨 阳,李伟健,邱雪峰,郭宏骞,李笑弓
(南京大学医学院附属鼓楼医院泌尿外科,江苏南京 210008)
前列腺癌是发达国家男性最常见的恶性肿瘤。近年来,由于中国开始广泛地应用血清前列腺特异性抗原(prostate-specific antigen,PSA)进行前列腺癌筛查,前列腺癌的发病率正在逐渐增加。机器人辅助腹腔镜根治性前列腺切除术(robot-assisted radical prostatectomy,RARP)是治疗临床局限性前列腺癌最常用的手术方式[3]。2010年,GALFANO等[4]首次介绍了保留Retzius间隙的机器人辅助腹腔镜根治性前列腺切除术(retzius-sparing robot-assisted radical prostatectomy,RS-RARP)的手术途径,避免了经过Rezius间隙的手术操作,保留了Retzius间隙内与尿控相关的结构,从而使尿失禁和勃起功能得到了更好的恢复。与传统的机器人辅助腹腔镜根治性前列腺切除术(conventional robot-assisted radical prostatectomy,CON-RARP)相比,尽管这种新术式在术后尿控方面有了很大的改善,但对于RS-RARP术后切缘阳性率的增加,一直是人们非常关注的问题[5]。目前,对于两种手术途径术后切缘阳性率的相关研究甚多,但考虑到前列腺癌的起源区域与切缘阳性关系的却少之又少。由于移行带的位置偏前列腺前部,考虑到Retzius间隙的前部空间的保留,我们猜测RS-RARP是移行带前列腺癌术后切缘阳性的独立危险因素。因此,本研究回顾性分析了2015年7月至2019年7月南京大学医学院附属鼓楼医院泌尿外科收治的150例临床局限性移行带前列腺癌患者的病例资料,探讨其术后切缘阳性的影响因素。
1 资料与方法
1.1 临床资料收集2015年7月至2019年7月我院泌尿外科收治的150例临床局限性移行带前列腺癌患者的病例资料。年龄(68.65±7.49)岁。行CON-RARP 53例,行RS-RARP 97例。术后病理分期pT2期102例,pT3期48例,切缘阳性46例,阴性104例。临床和病理分期均根据美国癌症联合委员会的TNM分期标准判断。病理采用大组织切片技术[7],手术切缘阳性定义为肿瘤侵犯至切除标本墨迹表面。移行带前列腺癌定义[8]:移行带肿瘤体积占肿瘤总体积70%以上(图1)。所有患者术前均行多参数前列腺磁共振和骨扫描明确没有局部进展和骨转移,且均未服用5α-还原酶抑制剂或内分泌治疗药物,既往均无前列腺手术史。行机器人辅助腹腔镜根治性前列腺切除术,术后病理明确诊断为移行带前列腺癌。

T:移行带肿瘤;U:尿道;AS:前列腺尖部;TZ:前列腺移行带;PZ:前列腺外周带。
1.2 手术方式手术均由我院1名高年资泌尿外科医生进行,在全身麻醉下,采用经腹腔途径。CON-RARP主要步骤:切开脐尿管,打开Retzius间隙,游离、横向切开盆内筋膜,离断耻骨前列腺韧带,游离前列腺尖部,结扎静脉丛并离断尿道,切开狄氏筋膜,向上游离前列腺背侧,离断膀胱颈,切断双侧输精管及精囊,膀胱颈重建并吻合膀胱尿道。RS-RARP主要步骤:于直肠膀胱陷凹上方打开盆腹膜,暴露并离断双侧精囊及输精管,游离狄氏筋膜及前列腺后方层面至前列腺尖部,离断前列腺侧蒂后可显露前列腺包膜及前列腺侧筋膜,此层面可延伸至前列腺尖部,从膀胱后方识别前列腺与膀胱颈交界处,打开膀胱颈,离断膀胱颈前方,寻着前列腺前表面游离至前列腺尖部,充分游离前列腺尖部后,可离断尿道前列腺部远端,吻合膀胱尿道。所有高危患者均行扩大淋巴结清扫术。

2 结 果
2.1 切缘阳性和切缘阴性两组患者的各指标比较结果见表1、表2。临床指标中,术前PSA、穿刺Gleason评分、临床分期、危险分级、手术方式与术后切缘阳性相关(P<0.05),年龄和体质指数与术后切缘阳性不相关(P>0.05)。术后病理指标中,肿瘤体积、前列腺体积、肿瘤体积/前列腺体积、pGleason评分、神经侵犯、累及双叶、包膜侵犯与术后切缘阳性相关(P<0.05),脉管癌栓、精囊侵犯与术后切缘阳性不相关(P>0.05)。
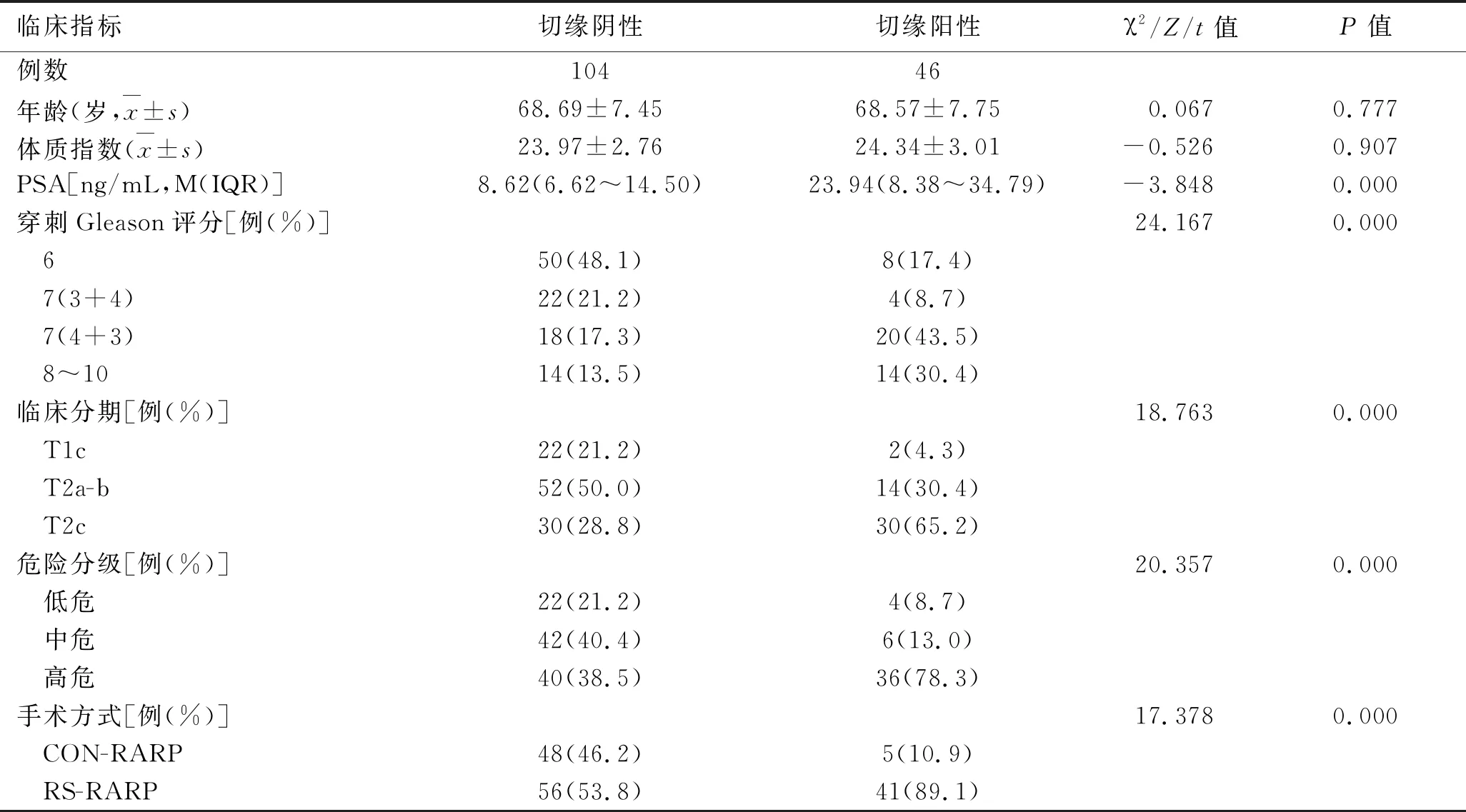
表1 RARP在处理移行带前列腺癌时切缘阳性和切缘阴性的临床指标比较
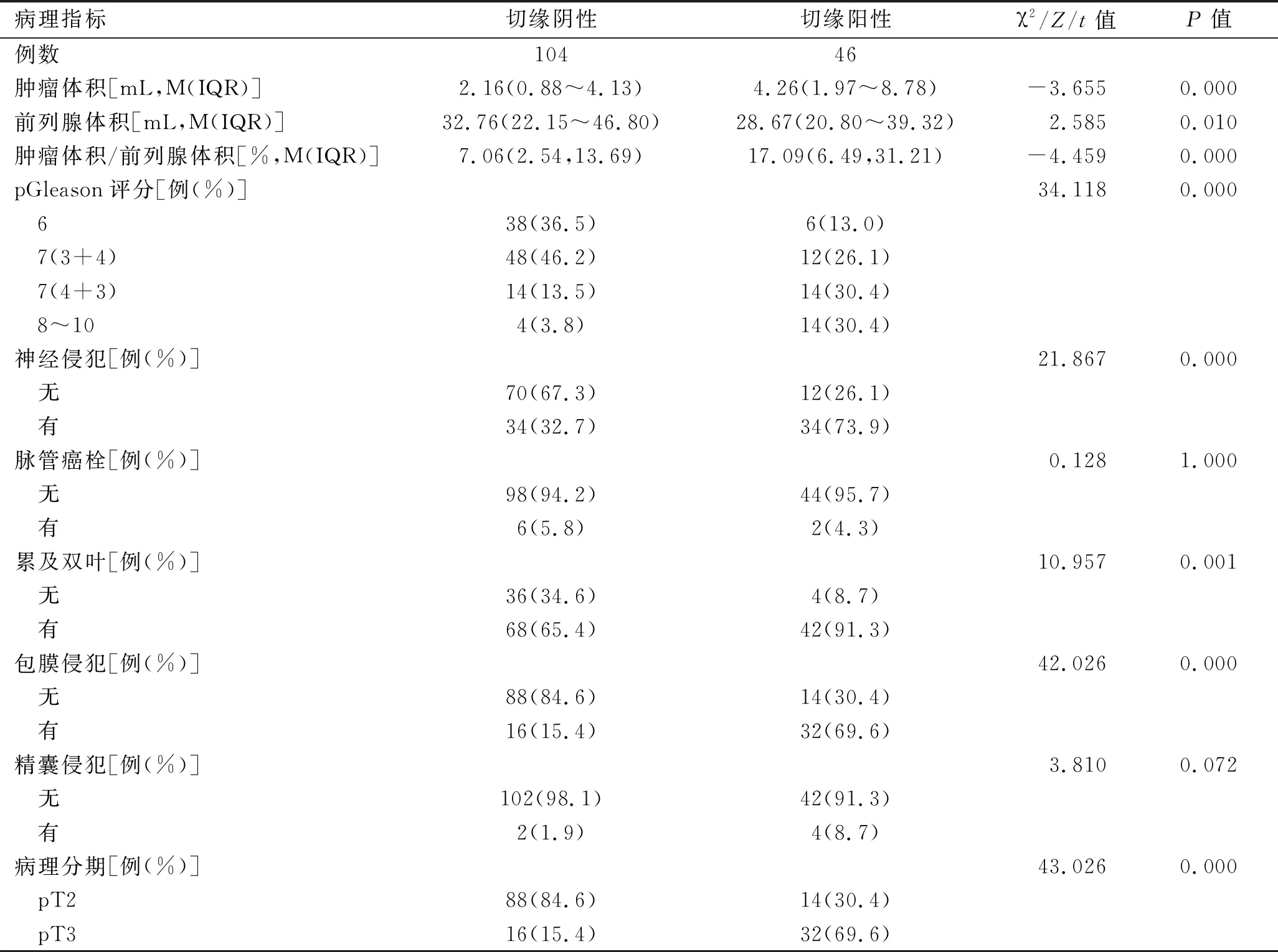
表2 RARP在处理移行带前列腺癌时切缘阳性和切缘阴性的病理指标比较
2.2 影响切缘阳性的多因素分析经过单因素分析,PSA、手术方式、前列腺体积、肿瘤体积、pGleason评分、神经侵犯、累及双叶和包膜侵犯等变量与切缘阳性相关(表中未显示),以上指标进入多因素分析,结果见表3。手术方式、前列腺体积、累及双叶和包膜侵犯与术后切缘阳性相关(P<0.05)。RS-RARP术式、累及双叶和包膜侵犯是RARP处理移行带前列腺癌时发生切缘阳性的独立危险因素,而前列腺体积(OR=0.957,95%CI:0.919~0.996,P=0.033)对切缘具有保护作用。
2.3 不同病理分期的亚组分析比较结果见表4。RS-RARP在处理病理分期为T2期的前列腺癌时,切缘阳性率与CON-RARP比较无统计学差异(P>0.05);而在处理病理分期为T3期的前列腺癌时,切缘阳性率显著高于CON-RARP(P<0.001)。最常见的切缘阳性位置为环周切缘前侧,而最少出现的位置为环周切缘后侧。
2.4 RARP在处理移行带前列腺癌时切缘阳性的位置分布80例切缘阳性者(每个手术标本切缘阳性位置可能不止1个)位置分布于尖端者18例(22.5%)、基底部者18例(22.5%)、环周前侧者40例(50.0%)、环周后侧者4例(5.0%)。
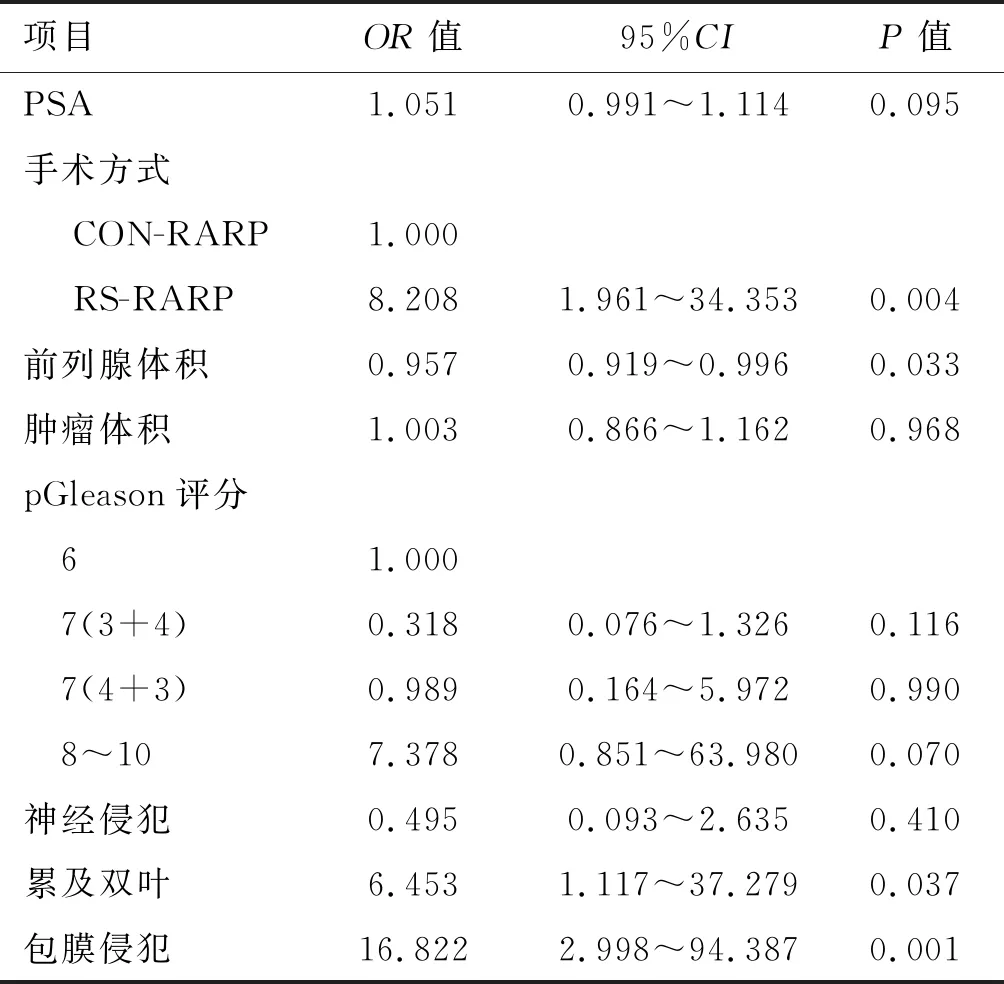
表3 RARP在处理移行带前列腺癌时切缘阳性的各指标的多因素分析

表4 CON-RARP和RS-RARP两种术式在处理不同病理分期的移行带前列腺癌的切缘阳性情况的亚组分析结果 [例(%)]
3 讨 论
本研究主要针对移行带这一特殊区域的前列腺癌,探讨RARP处理移行带前列腺癌时切缘阳性的相关危险因素。既往报道中,一些因素与RARP术后切缘阳性相关,特别是术前PSA、临床分期、活检Gleason评分和病理分期等与肿瘤恶性程度相关的特征。这些因素在理论上可作为RARP处理移行带前列腺癌时术后发生切缘阳性的危险因素。在本研究中,术后病理分期被证明是其切缘阳性的危险因素(表3),与已发表的研究结果一致。尽管RS-RARP改善了患者术后尿控,但是高切缘阳性率却成为了一个无法逃避的问题[13]。在本中心既往研究中发现,RS-RARP在处理移行带前列腺癌时术后的切缘阳性率明显高于外周带前列腺癌(42.6%vs.19.5%,P=0.01)[14]。在此次研究中,比较两种术式处理移行带前列腺癌时,发现RS-RARP术后的切缘阳性率远比CON-RARP高(43.3%vs.9.4%,P<0.001),这充分说明RS-RARP在处理移行带前列腺癌时,切缘阳性风险大大增加。亚组分析中,病理分期pT3分组中,RS-RARP术后切缘阳性率显著高于CON-RARP(87.9%vs.20.0%,P<0.001)。虽然pT2分组中,两种术式切缘阳性率无统计学差异,但RS-RARP术后的切缘阳性率也高于CON-RARP(18.8%vs.5.3%,P=0.075)。保留Retzius与常规入路的本质区别在于保留Retzius间隙的前部结构[4]。因此,推测RS-RARP可能是前部肿瘤术后切缘阳性的一个特殊危险因素。LIM等[15]之前的研究中也发现,与常规术式相比,保留Retzius间隙术式在前部区域观察到更高的切缘阳性率(8%vs.0%,P=0.018)。观察前列腺的解剖结构就可以发现,与后侧和左右两侧平面不同,从侧边延伸至前列腺前侧的前列腺筋膜融合到纤维肌层基质和逼尿肌裙中,且与前列腺包膜没有明确的界限[16]。因此,对于移行带前列腺癌患者,尤其是局部晚期的患者中,行RS-RARP术式治疗时,切缘阳性的风险会增加,且出现阳性的位置于环周切缘前侧多见,如术前通过多参数磁共振或者PSMA/PETCT对肿瘤病灶进行定位,则有助于手术方式的选择。目前,多参数磁共振成像已经成为了前列腺癌的术前常规影像学检查。已有研究表明,多参数磁共振对于临床有意义的前列腺癌的检测和定位具有很高的敏感性。本研究结果还发现,前列腺体积对切缘具有保护作用,这与既往文献报道相一致。可能因为前列腺体积较大时,正常腺体组织较多,肿瘤暴露的可能性会小些。
本研究的不足:首先,本研究为回顾性研究,因前列腺癌位于移行带的比例较少,病例数量偏少,且缺乏长期随访情况;其次,肿瘤的区域性是通过术后病理评估的,这样分析出来的结果更准确,但不能在术前提供相关信息,而术前通过磁共振对肿瘤进行定位有待进一步研究。
综上所述,肿瘤分期和保留Retzius间隙术式是RARP在处理移行带前列腺癌时发生切缘阳性的独立危险因素,肿瘤的分期我们无法改变,但是泌尿科医生在发现移行带肿瘤时应考虑避免保留Retzius间隙入路,尤其是局部分期较晚的患者,这样可以减少切缘阳性的发生。