可见光催化炔烃的含氟双官能团化的研究进展
袁 鑫,邱江凯,郭 凯
(南京工业大学 生物与制药工程学院,江苏 南京 211800)
炔烃为一类含有不饱和碳—碳三键的化合物,通过碳原子sp杂化,其独特的结构使分子具有较高的反应活性[1]。如何利用炔烃构建有价值的分子骨架一直广受人们的关注。其中,炔烃的双官能化是一种合成简单功能化化合物的有效方法,可以将炔烃转化为多种有机骨架。
太阳光是清洁的可再生能源,是大自然赠予人们的宝贵财富。1984年,Canoy等[2]首次报道了以[Ru(bpy)3](BF4)2作为光催化剂,在蓝光LED灯的照射下,以较高收率实现了Pschorr反应。然而在可见光区域内,可见光的能量不能直接引发常见的有机小分子化合物,必须依靠可见光的光敏剂引发,促使电子转移,从而实现光反应。因此,在之后的20年内,光催化反应并没有得到有机化学家们的关注,直至金属多吡啶络合物和有机染料可以在很温和的条件下,作为光敏剂参与反应被广泛报道。2008年,Ischay等[3]报道了以[Ru(bpy)3]Cl2作为光敏剂,在可见光光催化条件下,实现了分子内[2+2]环的加成反应。同年,Nicewicz等[4]报道了以[Ru(bpy)3]Cl2为光催化剂,首次将可见光催化剂和有机小分子催化结合,从而实现了α-位不对称烷基化的反应。这些具有重要意义的工作使光催化重新进入有机化学家们的视野,并得到了长远的发展。近十年来,可见光催化在反应方法学上有了突飞猛进的发展。
在光催化循环中,光敏剂吸收可见光产生活性中间体,这些激发态中间体具有较强的氧化和还原能力,通过电子转移的方式将光能转化为化学能。光循环机制分为两类,分别是氧化淬灭和还原淬灭循环。在有机化合物氧化剂和还原剂的存在下,激发态中间体被电子供体还原淬灭,而电子受体淬灭则为氧化淬灭。相比不稳定的自由基引发剂,光敏剂并不直接作为金属氧化还原剂参与反应,而是在温和的条件下,传递来自有机化合物氧化剂和还原剂的电子,其安全高效的特点符合绿色化学的理念。而光氧化还原催化和金属双循环催化的机制途径一般分为氧化还原途径或能量转移途径[5]。
在还原性淬灭途径中,激发态光催化剂可以被电子给体还原,从而得到作为强还原剂的物种。相应的,激发态光催化剂可以被电子受体氧化以提供PCox物种。除了光诱导分子内电荷转移,通过非共价相互作用组装的给体和受体之间的光诱导的分子间电荷转移,也是光化学界中众所周知的反应过程。
近十年来,在现代光致氧化还原催化领域中,经过国内外学者的引领,光催化反应历经了光致氧化还原-小分子双重催化[6]、光致氧化剂-过渡金属双重催化[7]、光致氧化剂-有机小分子-有机小分子三重催化[8]、光致氧化剂-有机小分子-过渡金属三重催化[9]、光致氧化剂-酶催化[10]和三苯基膦-碘化钠体系催化[11]的发展历程,且每一次新的发现都预示着一个全新的研究方向。
近年来,可见光催化炔烃的氟烷基化、氧化偶联、烯烃和炔烃的双官能团化领域均取得了重要进展。含氟类化合物由于其溶解度和亲酯性的变化,比非含氟类似化合物具有更好的膜渗透性和更高的生物利用度。炔烃氟化最直接有效的手段通常为自由基试剂、亲核试剂或者亲电试剂对炔烃进行的氟化双官能团化。笔者将基于近年来不同类型的氟化试剂对可见光催化炔烃的含氟双官能团化的研究进展进行总结。
1 自由基三氟甲基试剂
1.1 全氟碘代烷烃作为氟源
全氟碘代烷烃(通式CF3(CF2)nI)在合成药物分子、农药和材料等分子结构中一直占据着重要地位,在过去的几十年里受到了人们广泛的关注[12]。传统的方法是在短波紫外线(10~400 nm)辐射下,使用全氟烷基卤代物(Rf-X)对烯烃进行自由基全氟烷基化,但该方法通常存在选择性差、收率低以及反应条件苛刻等问题[13]。Haszeldine[14]早在1949年就报道了在光照或者加热的情况下,三氟甲基碘甲烷(CF3I)会激发产生三氟甲基自由基,在乙烯存在的情况下,三氟甲基自由基会加成到烯烃末端,以生成相应的自由基中间体,该自由基中间体从三氟甲基碘甲烷中捕获一个碘原子,进而产生3-碘-1,1,1-三氟丙烷和三氟甲基自由基(图1)。
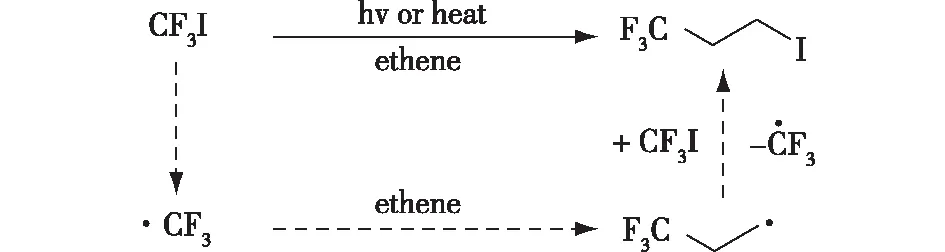
图1 CF3I生成·CF3的历程[14]Fig.1 The generation of ·CF3 radical from CF3I[14]
该工作被报道后,三氟甲基碘甲烷作为碳自由基前体的这种分子间电子转移/自由基加成(ATRA)已经成功被应用于各种炔烃。Me3Al[15],Et3B/O2[16],Na2S2O4[17],ET2ZN[18],FeSO4/H2O2/DMSO[19]等体系已经被广泛应用于引发三氟甲基自由基对炔烃的加成。近年来,由于可见光(400~760 nm)照射下光氧化还原催化体系的发展,自由基全氟烷烃化都得到了长远的发展[20-21]。
2012年,Wallentin等[22]提出了一种非常有效的碘代氟代烷基化的方法,利用钌或者铱的在蓝光(375~450 nm)照射下的联吡啶配体络合物的光氧化还原催化剂,将全氟碘代烷烃引入烯烃和炔烃中进行氟化反应,该方法条件温和,可以在0.5 h反应得到最高可达99%产率的目标产物。在此研究中,作者提出原子转移自由基加成ATRA的反应机制,实验结果表明,[Ir{(CF3)ppy}2(dtbbpy)]PF6的氧化淬灭可以有效应用于ATRA。另外,反应条件Ru(bpy)3Cl2的还原淬灭循环和抗坏血酸钠在可见光照射下作为牺牲电子供体,全氟烷基碘通过原子转移自由基加成ATRA的途径对炔烃可进行有效的加成反应。这些结果表明:光催化剂的氧化和还原淬灭途径可以相互互补,通过修改反应条件可以控制反应构型(图2)。该方案虽然可以有效介导末端炔烃与活化的烷基溴化物和碘化物之间的ATRA,但是反应条件不适合活化的烷基氯,1,2-二取代的烯烃或苯乙炔衍生物。

图2 原子转移自由基加成的机制路径[22]Fig.2 The mechanism of ATRA [22]
2014年,Iqbal等[23]发表了类似的工作,即采用同样的原始底物,利用Ru(phen)2+催化剂作为引发剂,通过控制催化剂、溶剂以及碱等细微的差异,经过ATRA的机制过程,获得炔烃的不同产物,如:碘三氟甲基化,氢三氟甲基化和三氟甲基化 (图3),但是该部分工作并不能很好地控制加成产物的构型。2016年,该课题组又成功地将Ru(phen)3+应用到该催化体系中[24]。值得注意的是,Choi等[25]采用无机电子盐[Ca2N]+·e-作为电子源的自由基介导反应,对未活化的炔烃进行氢氟甲基化,在转化过程中,阴离子从[Ca2N]+·e-的电子转移到三氟甲基化试剂全氟碘代烷烃,以引发自由基介导的三氟甲基化,反应中使用的乙腈同时充当了溶剂和电子释放促进剂以及氢原子源。

图3 不同的反应路径[23]Fig.3 Different reaction conditions[23]
尽管钌和铱与联吡啶配体络合的光氧化还原催化剂具备高效的反应性能,但成本十分昂贵。因此,近年来,人们开始研究光稳定、无毒性以及廉价的有机染料,如:曙红或者亚甲基蓝等在可见光辐射下作为有机光氧化还原催化剂的反应[26]。2017年,Matsuzaki等[27]探索了有机染料曙红Y作为光催化剂催化炔烃的ATRA反应[26]。除常规有机染料外,人工有机染料也备受关注,Kohei等[28]一直致力于对人工蓝色有机染料酞菁的结构进行设计和改造,使溶解性极差的酞菁可以高度溶解于各种有机溶剂中,并将其应用于光催化反应中,比较有代表性的工作为三氟乙氧基涂覆的硼亚酞菁可以在能量较低的红光(600~700 nm)辐照下催化烯烃和炔烃自由基烷基化,该方法高效温和,但是随着反应时间的增长,催化剂的催化活性会随之消失[27]。随后,该课题组又发表了在可见光照射下,由三氟乙氧基涂覆的锌酞菁锌催化的,包括炔烃在内的烯烃自由基全氟烷基化,成功解决了催化剂体系不稳定的缺点,该反应同样是经过一个ATRA的机制过程[28]。
为了降低成本,除了发展廉价的有机染料外,另外一种有效的策略也被人们发现,即采用廉价的金属铜等代替昂贵的铱、钌等金属与联吡啶进行配位后,作为光催化剂参与反应。2018年,Rawner等[29]使用菲咯啉铜催化剂代替传统的多吡啶络合物金属有机催化剂,进行光氧化还原催化苯乙烯和苯基乙炔的碘全氟烷基化反应。与常用的[Ru(bpy)3]Cl2,[Ru(phen)3]Cl2或fac-Ir(ppy)3相比,[Cu(dap)2]Cl能够更加有效地将苯乙炔转化为相应的全氟烷基,同位素标记的乙苯指出铜催化剂除了光致电子转移外,还具有其他作用。在此工作中,还首次提出了涉及Cu(III)中间体或[CuI]+中间体的配体的分子内催化循环。
随后,人们将注意力转向对炔烃底物的结构改造,即将烯烃与炔烃相连,形成1,n-烯炔,并对其进行氟化反应。Wang等[30]已开发出一种温和有效的可见光诱导的原子转移自由基加成物1,n-炔烃(n=6,7),与全氟烷基卤化物发生加成环化,最终生成全氟卤代N-杂环的方法(图4)。该方案提供了一种温和的、完全符合原子经济学的策略,可以将各种全氟化基团例如CF3I,n-C3F7等对1,6-烯炔,1,7-烯炔进行自由基加成环化。此外,使用带有叔丁基连接的炔基的1,7-烯炔(n=6,7)进行的反应亦可实现氢原子转移(HAT)过程的环化,从而产生新的α-卤代氟代2,4-二氢喹啉化合物。

图4 可见光催化合成全氟卤代N-杂环策略[30]Fig.4 The strategy for halogenated perfluoro-N- heterocyclic by blue LEDs[30]
1.2 三氟甲基磺酰氯(CF3SO2Cl)作为三氟甲基试剂
光催化循环的启动依赖于富电子芳烃的氧化作用,全氟碘代烷烃作为氟化试剂参与反应往往会受到竞争性芳基碘化,从而降低反应效率。因此人们开始寻求新的氟化试剂。2011年,Nagib等[31]发表了将三氟甲基磺酰氯在光照的情况下产生三氟甲基的自由基,并可对未活化的芳烃和杂芳烃进行直接三氟甲基化的工作。在全氟碘代烷烃内部采用缺电子体系(SO2)可以更轻松地还原,与其他氟化试剂相比,三氟甲基磺酰氯相对成本比较低,反应后处理简单(图5)。

图5 可见光催化的杂芳烃的三氟甲基化[31]Fig.5 Trifluoromethylation of heteroarenes by means of photoredox catalysis[31]
随后利用光催化全氟卤代烷烃以引发氟烷基自由基的策略被应用到炔烃的含氟双官能团化的研究中。2017年,Han等[32]开发了一种新的在温和条件下,利用光氧化还原催化芳基炔烃氯三氟甲基化的反应。该反应利用可以直接购买的CF3SO2Cl作为CF3和Cl源,以高区域选择性和立体选择性进行反应。在此机制的反应过程中,CF3自由基和氯离子的产生是通过fac-Ir(ppy)3光催化的CF3SO2Cl还原分解而产生的,通过Suzuki偶联,可以很容易地将三氟甲磺酰氯转化为四取代烯烃(图6)。

图6 四取代烯烃合成策略及可能的反应机制[32]Fig.6 The strategy of the synthesis of 1,1-bis-arylated olefin and its possible mechanism[32]
香豆素及其衍生物广泛存在于天然产物以及药物活性分子骨架中,因其重要的生物学和药理学特性得到了人们极大的重视[33]。近些年来,科研人员们就香豆素的合成策略已经开发出了形式多样的方法。2014年,Li等[34]利用Togni试剂制备含氟香豆素,但该方法底物适用性不广,缺电子底物的产率往往比较低[35]。2018年,Yuan等[36]报道了一种高效的方法,可将CF3SO2Cl作三氟甲基自由基源,与3-芳基丙酸酯反应构建3-三氟甲基香豆素。该反应采用级联环化/脱芳香化/酯迁移/氧化/再芳香化工艺,在蓝光LED灯(16 W)照射下,合成了产物1,为3-三氟甲基香豆素(图7),产率可高达85%。

图7 可见光催化合成3-三氟甲基香豆素策略[36]Fig.7 The strategy for the synthesis of 3-trifluoro- methylcoumarin by visible light[36]
笔者课题组一直致力于以绿色化学为主要研究方向。基于前人的可见光催化炔烃的含氟双官能团化的研究工作基础,课题组开发出在温和的条件下,有效地利用光氧化还原催化1,7-烯炔的卤代三氟甲基化反应方法[36]。该光催化方案提供了一种有效的功能性策略,分别可通过两种不同的自由基途径,从产物2,即1,7-烯炔中生成CF3-和含卤素的喹啉类化合物(图8)。其中一种自由基途径是利用有机催化剂9-均三甲苯基-10-甲基吖啶四氟硼酸盐作为光敏剂,以三氟甲基亚磺酸钠提供三氟甲基自由基,N-卤代酞酰亚胺C提供卤原子,合成喹啉类化合物。另外一种自由基途径是以fac-Ir(ppy)3作为光敏剂,以三氟甲基磺酰氯作为自由基供体,同时提供三氟甲基自由基和氯自由基。基于机制实验以及文献[32],推测该光催化卤代三氟甲基化反应的初步合理机制可能为:最初,可见光将Mes-Acr+诱导为激发态Mes-Acr+*,从而还原了Langlois试剂。通过单电子转移(SET)生成CF3自由基A。随后,CF3自由基被1,7-烯炔的碳碳双键捕获,得到季碳自由基B,然后进行六元环环化反应,以形成自由基中间体D。随后,自由基D可以与来自NCP的卤原子偶合,得到卤代三氟甲基化产物3。方法2的反应机制与方法1相似,该方法使用具有相同的自由基中间体B和D进行IrIII/IrIV催化。生成的碳正离子被Cl-捕获,形成目标产物3。

图8 可见光催化合成喹啉类化合物策略[36]Fig.8 The strategy for the synthesis of quinoline compound by visible light[36]
2 亲核性三氟甲基试剂
2.1 Langlois试剂
三氟甲基亚磺酸钠(Langlois试剂)为固体,反应过程中操作简单且具有良好的反应性能。2011年,Ji等[37]报道了利用三氟甲基磺酸钠作为三氟甲基试剂,参与了三氟甲基化反应的工作,该工作为后续的反应研究提供了新的思路。
2017年,Jana等[38]使用光氧化还原催化剂,三氟甲基亚磺酸钠为氟源,在无金属条件下,实现1,6-烯炔的加成环化反应(图9)。该反应通过光诱导三氟甲基磺酸钠产生三氟甲基自由基,然后进一步与烯烃进行加成、环化,提供乙烯基自由基,该自由基发生电子转移生成乙烯基阳离子或者被三氟甲基加成的烯烃部分发生电子转移,形成碳正离子,进行阳离子环化生成乙烯基碳正离子,随后H2O加成到乙烯基阳离子中,消除H2后生成三氟甲基化的C3-芳酰基/酰化杂环。该工作中一共拓展了43个底物,最高产率可达76%。Jana等[38]还将该方法运用到合成含有三氟甲基基团的药物分子中,成功得到两个目标产物。
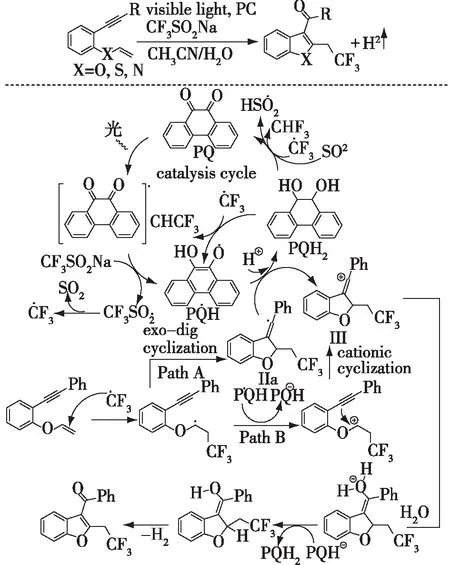
图9 蓝光催化1,6-烯炔的三氟甲基化和氧化[38]Fig.9 The strategy for the trifluoromethylation and oxidation of 1,6-enynes by blue LEDs[38]
2.2 溴二氟乙酸乙酯试剂
溴二氟乙酸乙酯试剂(CF2CO2Et)由于其独特的结构而受到人们的重视,因为该部分可以进一步修饰成各种含CF2的官能团。近年来,对过渡金属介导或过渡金属催化的芳基卤化物和芳基硼酸的二氟乙酰化,以构建Csp2-CF2CO2Et键的方法得到了深入研究。Ma等[39]等和Caillot等[40]还报道了一种将酰胺,呋喃直接二氟乙酰化的方法。另一种常用策略是利用CF2CO2Et自由基的高反应性。利用可见光催化将该结构加成到杂芳烃[41],烯烃[42],或者异氰酸酯[43]等结构上,这些方法已经被多个研究小组发现并报道。但是,这种光催化策略在炔烃的区域特异性二氟乙酰化中的应用仍然非常有限。
2015年,Fu等[44]开发了一种温和有效的方法,该方法通过可见光促进炔基与溴代二氟代乙酸乙酯的芳基二氟代乙酰化反应来合成3-二氟代乙酰化香豆素(图10)。该反应通过串联自由基环化过程直接形成Csp2-CF2CO2Et和碳碳键,实现了通过使用fac-Ir(ppy)3作为催化剂,碳酸钾作为碱在蓝色LED的照射下,2-溴-2,2-二氟乙酸酯和炔酸苯酯反应合成3-二氟乙酰化香豆素的方法。Fu等[44]认为催化循环可能为:首先,将光催化剂[fac-Ir(III)(ppy)3]辐照到激发态[fac-Ir(III)(ppy)3*],将其用BrCF2CO2Et氧化淬灭,生成[fac- Ir(IV)(ppy)3]+配合物和一个·CF2CO2Et自由基物种K。自由基K加成到炔酸酯4中生成自由基中间体H,该中间体进行分子内取代,得到自由基中间体I。中间体I然后被[fac-Ir(IV)(ppy)3]+氧化形成环己二烯基阳离子J并再生[fac-Ir(III)(ppy)3]。最终,通过碱辅助的去质子化得到产物5。

图10 蓝光催化的3-二氟乙酰化香豆素的合成[44]Fig.10 Blue-LEDs-mediated synthesis of 3-difluoroacethlated coumarins[44]
2017年,Li等[45]利用了类似的催化机制,在光催化下,利用9-均三甲苯基-10-甲基吖啶高氯酸盐代替昂贵的铱催化剂,实现了炔烃的光诱导邻二氟烷基化和氨基磺酰化。9-均三甲苯基-10-甲基吖啶高氯酸盐在可见光下催化2-溴-2,2-二氟乙酸乙酯,炔烃和DABCO·(SO2)2与肼的结合,通过自由基加成,并插入SO2进行4个组分反应,得到(E)-乙基 2,2-二氟-4芳基-4-氨磺酰基丁-3-烯酸酯,产率最高可达98%。2018年,该课题组又做出了一部分很有意思的工作,工作内容为采用DABSO作为催化剂在可见光催化下催化合成3-芳基-2-二氟乙酰茚(图11)[45]。

图11 光诱导溴二氟乙酸乙酯与1,3-二芳基丙-2-炔-1-酮的反应 [45]Fig.11 A photoinduced reaction of perfluoroalkyl halides with 1,3-diarylprop-2-yn-1-ones[45]
2018年,Deng等[46]同样利用fac-Ir(ppy)3作为光敏剂,在光催化作用下合成出3-二氟乙酰化喹啉(图12)。

图12 N-炔丙基芳胺的光氧化还原催化级联加成/环化[46]Fig.12 Photoredox-catalyzed cascade addition/cyclization of N-propargyl aromatic amines[46]
3 亲电性三氟甲基试剂
3.1 Umemoto试剂
2015年,Tomita等[47]发表了从简单的炔烃立体选择性合成四取代的三氟甲基化的烯烃的工作(图13)。在可见光照射下,[Ir(ppy)2(dtbbpy)](PF6)作为光氧化还原催化剂,用亲电的三氟甲基试剂,即YagupolÏskii-Umemoto试剂的三氟甲磺酸盐,对内部不对称炔烃进行磺酰氧基三氟甲基化,得到三氟甲基烯基三氟甲磺酸酯,该反应可以很好地控制立体选择性(以E/Z标记为99∶ 1)。根据一系列的机制实验,推测出光催化磺酰氧基三氟甲基化的可能反应机制。7与8区域特异性生成α-苯乙烯基型三氟甲基烯基基团6*,该基团通过离域至苯环的p轨道而稳定,关键中间体6*可以被高度可氧化的Ir光催化剂(IrIV)氧化为+1e⊖,氧化为烯烃,从而发生机制类似于先前报道的光氧化还原催化烯烃三氟甲基化的反应,以产生三氟甲基烯基阳离子6+。三氟甲基烯基三氟甲磺酸酯9的高度立体选择性形成可以用CF3基团的强负电子性来解释:由于静电排斥,三氟甲磺酸根阴离子的亲核攻击有利于CF3基团的反式加成。推测可能有另外一种机制,即通过将三氟甲磺酸根阴离子直接添加到6*上,然后进行1e⊖氧化。

图13 光氧化还原催化的炔烃立体选择性转化为四取代的三氟甲基化烯烃[47]Fig.13 Photoredox-catalyzed stereoselective conversion of alkynes into tetrasubstituted trifluoromethylated alkenes[47]
2018年,Malpani等[48]发表了采用Umemoto试剂提供CF3和H2O直接氧化成炔烃的工作,主要内容是利用光氧化还原催化反应,通过快速的烯醇-酮互变异构反应,获得α-三氟甲基酮(图14)。该反应表现出高的官能团耐受性和区域选择性。该方案获得的α-CF3取代的二酮合成了各种含CF3的杂环结构,从而证明了该方法广泛的适用范围。该策略同样被应用在一种光氧化还原催化的分子内环化反应,以用于合成三氟甲基化的杂环化合物[49]。该反应在温和的光催化条件下,官能团耐受性强,可以制备不同的含氧、硫或氮的杂环,底物广泛的适用范围证明了该策略在提高底物复杂性方面的潜力。

图14 光氧化还原催化的三氟甲基化分子内环化[49]Fig.14 Photoredox-catalyzed trifluoromethylative intramolecular cyclization[49]
3.2 Togni试剂
Xiang等[50]也应用过类似的策略,在可见光照射下,2-乙炔基苯磺酰胺在光催化剂存在下与Togni试剂反应,以良好的收率生成3-(2,2,2-三氟亚乙基)-2,3-二氢苯并[d]异噻唑1,1-二氧化物,随后的C—N键形成会产生相应的产物(图15)。

图15 在可见光下通过2-乙基苯磺酰胺的三氟甲基化 反应生成苯并磺酰胺[50]Fig.15 Generation of benzosultams via trifluoro- methylation of 2-ethynylbenzensulfonamide under visible light[50]
4 结语
综上所述,从对可见光催化炔烃的含氟双官能团化的研究进展总结中可以看出,目前常用的光催化剂主要为贵金属配合物(Ir、Ru等)和有机染料,金属配合物或者含有大π离域结构的有机分子在吸收低能量的可见光后,激发发生分子内电荷转移(CT),从而引发光反应。这些贵金属配合物和有机染料光催化剂大多结构复杂、不易合成、成本高昂,难以实现大规模的产业化应用。因此,追求更加廉价实用的光催化反应体系势必会对扩展其应用带来变革。该方向的发展总趋势是催化剂由多吡啶配体钌催化剂、多吡啶配体铱催化剂向廉价的有机染料或者锌、铜等价格廉价易得的金属催化剂转化,同时氟源的来源逐渐简化,合成的目标产物更倾向于直接合成药物分子并逐步趋向于工业化。

