结合逐步敲入策略与制剂工艺过程的肾宝片复杂成分辨识
陆 萌,贾晓斌,郭舒臣,易 欢,段龙强,耿 炤*,封 亮*
1.中国药科大学中药学院,江苏 南京 211198
2.江西汇仁药业股份有限公司 技术中心,江西 南昌 330052
肾宝片由淫羊藿、红参、肉苁蓉等22味中药组成,具有调和阴阳、温阳补肾、扶正固本的功效,可用于治疗腰腿酸痛、精神不振、夜尿频多、畏寒怕冷等症[1]。肾宝片的原剂型肾宝合剂在治疗遗尿方面具有很好的疗效[2],并具有助阳的功效与改善性功能的药理作用[3]。肾宝片是内科常用补益中成药[4],但其药效物质基础仍不明确,现有研究大多是针对肾宝片中某一单味中药中的化学成分进行测定[5-7],缺乏系统的物质基础研究。肾宝片与肾宝合剂制剂工艺不同,部分化学成分可能会发生变化。已有研究中主要测定了肾宝合剂中的淫羊藿苷、补骨脂素、异补骨脂素及蛇床子素[8],本研究拟通过对肾宝片化学成分进行进一步辨识,对可能的新产生成分进行解析,有助于对肾宝片制剂工艺过程的理解、认识和进一步的质量控制。
中药复方药效物质基础研究一直是中药现代化研究的重点内容之一,而对复方中药进行系统的化学成分表征研究是阐明其药效物质基础的前提。中药复方具有多组分、多靶点、整体性的特点,其药味众多、成分复杂,是大复方物质基础解析的主要难点[9]。近年来对于中药复方物质基础的研究,发展出了诸如中药血清药物化学研究[10]、谱效相关的药效物质基础研究[11]、中药整体药代动力学研究[12]等方法,这些方法在阐释中药物质基础方面起到了一定的积极作用。本研究为系统表征肾宝片制剂工艺过程中得到的各提取物的化学成分,采用逐步敲入策略,利用超高效液相色谱(UPLC)与超高效液相色谱-四极杆-飞行时间质谱(UPLC-Q-TOF-MS)解析各浸膏的化学成分,实现化学成分定性与分类,为肾宝片质量控制提供依据。
按照肾宝片制剂工艺分别得到肾宝片浸膏1、2与全浸膏,采用UPLC重点分析表征浸膏1、2与全浸膏,并按照逐步敲入浸膏1、2的方法,验证全浸膏中的成分。在初步归属全浸膏谱中21个成分后,采用UPLC-Q-TOF-MS技术对肾宝片各提取物(浸膏)化学成分进行定性分析,建立化学成分快速鉴定方法,结合对照品与各单味中药的相关文献,快速鉴定未知成分。整体技术路线图见图1。该方法较为全面系统地表征了肾宝片提取物的化学成分,为肾宝片的药效物质基础研究及质量控制方法的建立提供了实验依据,对药味组成复杂的中药大复方物质基础解析具有广泛的应用价值。
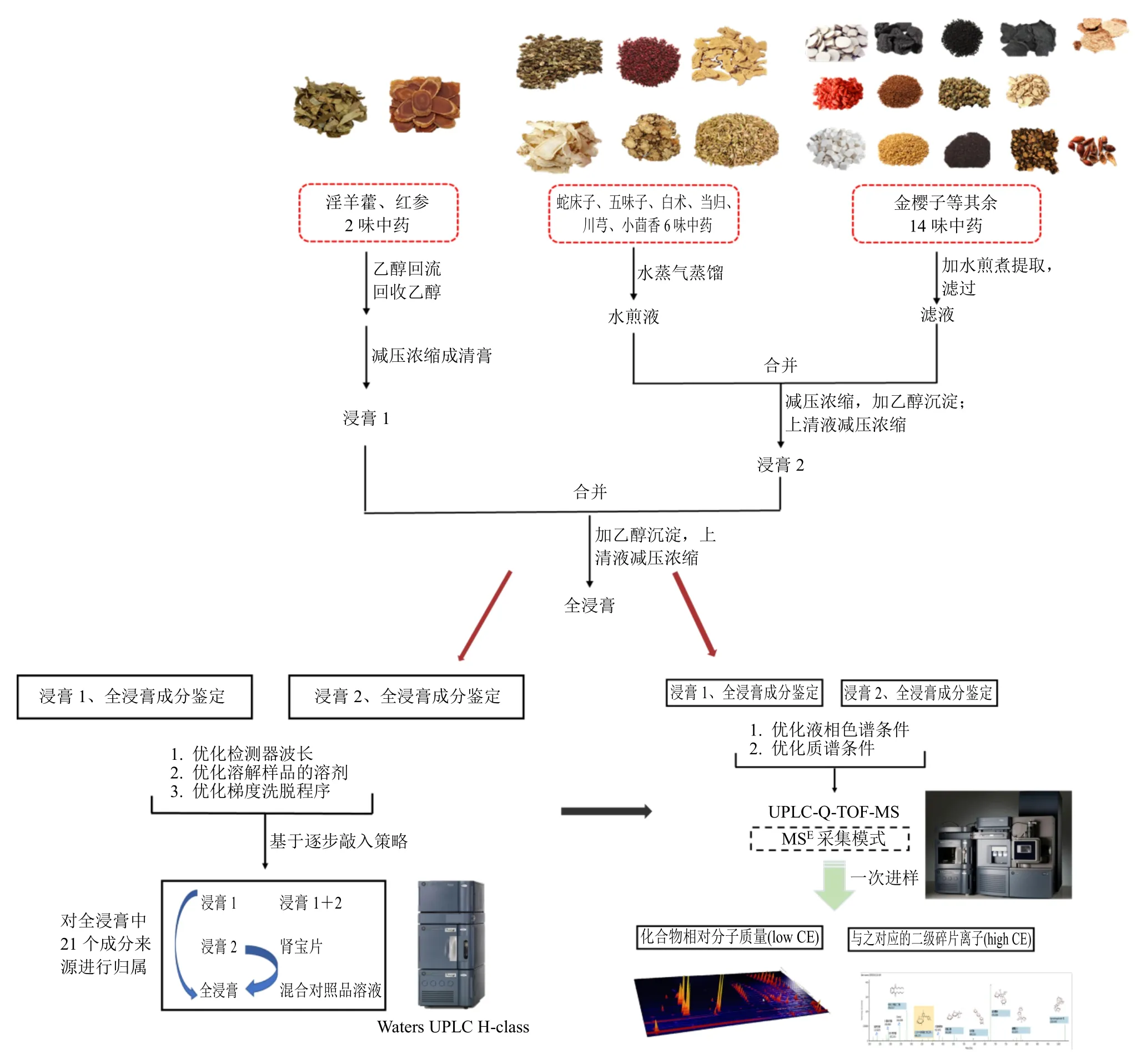
图1 结合逐步敲入策略与制剂工艺过程的肾宝片复杂成分辨识技术路线图Fig.1 Diagram of identification of complex components of Shenbao Pian based on stepwise knock-in strategy and preparation process
1 仪器与材料
1.1 仪器
Acquity UPLC H-Class超高效液相色谱仪、Waters Xevo G2-XS QTof质谱仪[配有电喷雾电离源(ESI)]、数据处理软件MassLynx V 4.2和UNIFI,美国Waters公司;KH-300TDB型高频数控超声波清洗器,昆山禾创超声仪器有限公司;Metter-Toledo GmbH XPR2电子分析天平,梅特勒-托利多仪器有限公司;Milli-Q纯水系统,美国Millipore公司。
1.2 试药与试剂
对照品人参皂苷Rg1(批号G16S10Y97436)、人参皂苷Re(批号B04D9S76499)、人参皂苷Rb1(批号 Z20S9X70603)、金丝桃苷(批号Y08N9X74602)、槲皮素(批号C09S8Y43412)、蛇床子素(批号T08M8B30733)、类叶升麻苷(批号Y21A9H59554)、补骨脂素(批号C22A9Q68562)、异补骨脂素(批号C05M10Q82078)、大黄素(批号C18F8Q29652)、大黄素甲醚(批号T26A8F34784)、阿魏酸(批号L03A9D57744)、松果菊苷(批号Y29M10H84490)、五味子醇甲(批号Y30N10H104712)均购于上海源叶生物科技有限公司;对照品朝藿定A(批号19072204)、朝藿定B(批号18011604)、朝藿定C(批号19072404)、淫羊藿苷(批号18012906)、宝藿苷I(批号19083008)均购于成都普菲德生物技术有限公司;对照品人参皂苷Ro(批号19012811)、四羟基二苯乙烯葡萄糖苷(批号19012803)均购于维克奇生物科技有限公司;各对照品质量分数均≥98%。
肾宝片及其中间品浸膏1、浸膏2与全浸膏,批号均为T1909156,江西汇仁股份有限公司。乙腈、甲醇为质谱纯,德国Merck公司;其余试剂均为色谱级。
2 方法
2.1 对照品溶液的制备
取金丝桃苷、槲皮素、朝藿定A、朝藿定B、朝藿定C、淫羊藿苷、宝藿苷I、人参皂苷Rg1、人参皂苷Ro、人参皂苷Rb1、人参皂苷Re对照品适量,精密称定,加50%乙腈分别制成质量浓度为116.5、219.7、199.2、201.6、164.6、215.4、204.2、217.2、199.0、196.0、165.6 μg/mL的混合对照品溶液,标记为混合对照品溶液1。
取蛇床子素、毛蕊花糖苷、补骨脂素、2,3,5,4-四羟基二苯乙烯葡萄糖苷、异补骨脂素、大黄素、大黄素甲醚、阿魏酸、松果菊苷、五味子醇甲对照品适量,精密称定,加50%乙腈分别制成质量浓度为105.5、196.4、208.3、116.2、207.4、209.0、251.2、190.5、219.7、217.3 μg/mL的混合对照品溶液,标记为混合对照品溶液2,混合对照品溶液1、2用于UPLC分析。
分别取朝藿定A、朝藿定B、朝藿定C、淫羊藿苷、宝藿苷I对照品适量,精密称定,加甲醇分别制成含各成分5~15 μg/mL的混合对照品溶液,标记为混合对照品溶液3。
分别取人参皂苷Rg1、人参皂苷Ro、人参皂苷Rb1、人参皂苷Re对照品适量,精密称定,加甲醇分别制成含各成分5~15 μg/mL的混合对照品溶液,标记为混合对照品溶液4。
分别取松果菊苷、毛蕊花糖苷、异毛蕊花糖苷、2,3,5,4-四羟基二苯乙烯葡萄糖苷、补骨脂素、异补骨脂素对照品适量,精密称定,加50%乙腈分别制成含各成分1~5 μg/mL的混合对照品溶液,标记为混合对照品溶液5。
分别取没食子酸、槲皮素、山柰酚、大黄素、大黄素甲醚、甘草苷、异甘草素对照品适量,精密称定,加50%乙腈分别制成含各成分1~5 μg/mL的混合对照品溶液,标记为混合对照品溶液6,混合对照品溶液3~6用于UPLC-Q-TOF-MS分析。
2.2 供试品溶液的制备
分别取浸膏1、2和全浸膏各1 g,精密称定,置于25 mL量瓶中,加适量50%乙腈超声溶解,冷却至室温,加50%乙腈定容至刻度,用0.22 μm微孔滤膜滤过,取续滤液作为浸膏1、2和全浸膏供试品溶液;分别吸取浸膏1、2供试品溶液各1 mL,等体积混合,0.22 μm微孔滤膜滤过,即得浸膏1+浸膏2供试品溶液;取肾宝片3片,除去包衣,研细,取2 g,精密称定,置于25 mL量瓶中,加适量50%乙腈超声溶解,冷却至室温,加50%乙腈定容至刻度,0.22 μm微孔滤膜滤过,取续滤液作为肾宝片供试品溶液;50%乙腈作为空白供试品溶液。
2.3 液相色谱条件1
Waters H-class液相色谱仪;色谱柱为Acquity UPLC BEH C18柱(100 mm×2.1 mm,1.7 μm);流动相为0.1%磷酸水溶液-乙腈;梯度洗脱:0~20 min,10%~20%乙腈;20~20.1 min,20%~24%乙腈;20.1~32 min,24%乙腈;32~32.1 min,24%~30%乙腈;32.1~38 min,30%~38%乙腈;38~42 min,38%~50%乙腈;42~50 min,50%~95%乙腈;50~57 min,95%乙腈;57~65 min,95%~10%乙腈;体积流量0.2 mL/min;柱温30 ℃;检测波长203、270 nm;进样量1 μL。
2.4 液相色谱条件2
Waters H-class液相色谱仪;色谱柱为Acquity UPLC BEH C18柱(100 mm×2.1 mm,1.7 μm);流动相为0.1%磷酸水溶液-乙腈;梯度洗脱:0~10 min,5%~15%乙腈;10~15 min,15%~24%乙腈;15~25 min,24%乙腈;25~40 min,24%~60%乙腈;40~45 min,60%~73%乙腈;45~52 min,73%~95%乙腈;52~60 min,95%~5%乙腈;体积流量0.2 mL/min;柱温30 ℃;检测波长254 nm;进样量1 μL。
2.5 液相色谱条件3
Waters I-class液相色谱仪;色谱柱为Acquity UPLC HSS T3柱(100 mm×2.1 mm,1.8 μm);流动相为0.1%甲酸水溶液-乙腈;梯度洗脱:0~0.5 min,22%乙腈;0.5~10 min,22%~95%乙腈;10~12 min,95%乙腈;12~12.5 min,95%~22%乙腈;12.5~14 min,22%乙腈;体积流量0.4 mL/min;柱温40 ℃;进样量为2 μL;2D检测波长203、270 nm;用于UPLC-Q-TOF-MS分析浸膏1和全浸膏。
2.6 液相色谱条件4
Waters I-class液相色谱仪;色谱柱为Acquity UPLC HSS T3柱(100 mm×2.1 mm,1.8 μm);流动相为0.1%甲酸水溶液-乙腈;梯度洗脱:0~0.5 min,5%乙腈;0.5~10 min,5%~50%乙腈;10~10.5 min,50%~95%乙腈;10.5~12 min,95%乙腈;12~12.5 min,95%~5%乙腈;12.5~14 min,5%乙腈;体积流量0.4 mL/min;柱温40 ℃;进样量2 μL;2D检测波长260、300 nm;用于UPLC-Q-TOFMS分析浸膏2和全浸膏。
2.7 质谱条件
电喷雾离子源(ESI)正、负离子模式分别进行MSE扫描;低碰撞电压6 V;高碰撞电压30~70 V;采集质量范围m/z50~1200;毛细管电压3 kV(ESI+)和2.5 kV(ESI-);锥孔电压40 V;脱溶剂气温度500 ℃;脱溶剂气体积流量1000 L/h;扫描时间14 min;亮氨酸脑啡肽(LE)实时校准质量数,正离子为m/z556.277 1,负离子为m/z554.261 5。
2.8 质谱数据分析
使用Masslynx V4.2和以中药数据库为基础的UNIFI软件进行数据采集与分析。利用Waters Traditional Medicine Library成分库搜索各单味中药的化学成分,基于UNIFI在线软件进行化学成分鉴定与匹配,具体参数设置如下:在查找3D峰模块勾选采用Lockmass进行校正,高能通道强度阈值设为50 counts,低能通道强度阈值设为200 counts,勾选“Target by Retention time”,Target match tolerance设为5×10-3;Lockmass校正质量数:正离子为m/z556.276 6,负离子为m/z554.262 0。通过人工校验与核实各化合物的精确相对分子质量以及碎片离子,确定浸膏1、2与全浸膏的化学成分。
3 结果与分析
3.1 逐步敲入浸膏1、2验证全浸膏中的成分
肾宝片成分复杂,根据不同成分的特点,分别采用液相色谱条件1和2对浸膏1、浸膏2、浸膏1+2、全浸膏以及混合对照品溶液1、2与肾宝片进行分析,按照逐步敲入浸膏1、2的方法,对全浸膏中的成分及来源进行验证。
在液相色谱条件1下重点分析了浸膏1中淫羊藿黄酮组分与人参皂苷组分,利用PDA检测器设置双波长,分别在270 nm下分析黄酮成分,在203 nm下分析皂苷成分,色谱图见图2、3。由图2可推测肾宝片全浸膏中含有朝藿定A、B、C、淫羊藿苷及宝藿苷I、槲皮素与金丝桃苷,其中朝藿定A、B、C、淫羊藿苷及宝藿苷I来自浸膏1,槲皮素与金丝桃苷可能来自浸膏2。由图3可知,仅通过保留时间较难推测全浸膏中是否含有人参皂苷Rg1、Re、Ro与Rb1,为进一步验证浸膏1、2和全浸膏中是否含有上述成分,将利用LC-MS对各浸膏成分进行鉴定。
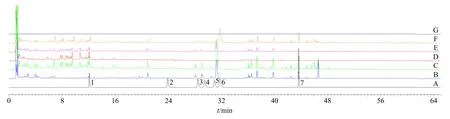
图2 验证全浸膏中成分色谱图 (液相色谱条件1, PDA: 270 nm)Fig.2 Validation of chromatogram of components in total extractum (liquid chromatography conditions1, PDA: 270 nm)
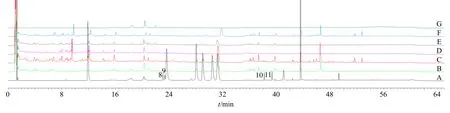
图3 验证全浸膏中成分色谱图 (液相色谱条件1, PDA: 203 nm)Fig.3 Validation of chromatogram of components in total extractum (liquid chromatography conditions1, PDA: 203 nm)
通过对色谱条件的摸索,在液相色谱条件2下重点分析了浸膏2中的成分,色谱图见图4。由于主要成分在前40 min出峰,因此,选取前40 min的色谱图进行对比,由图4可推测全浸膏中含有阿魏酸、松果菊苷、二苯乙烯苷、毛蕊花糖苷、补骨脂素、异补骨脂素、五味子醇甲、大黄素、蛇床子素9个成分,其中阿魏酸、松果菊苷、二苯乙烯苷、毛蕊花糖苷、补骨脂素、异补骨脂素、大黄素来自于浸膏2,且浸膏1对其无干扰,五味子醇甲、蛇床子素在浸膏2中的响应很低,需进一步通过液质分析进行验证。
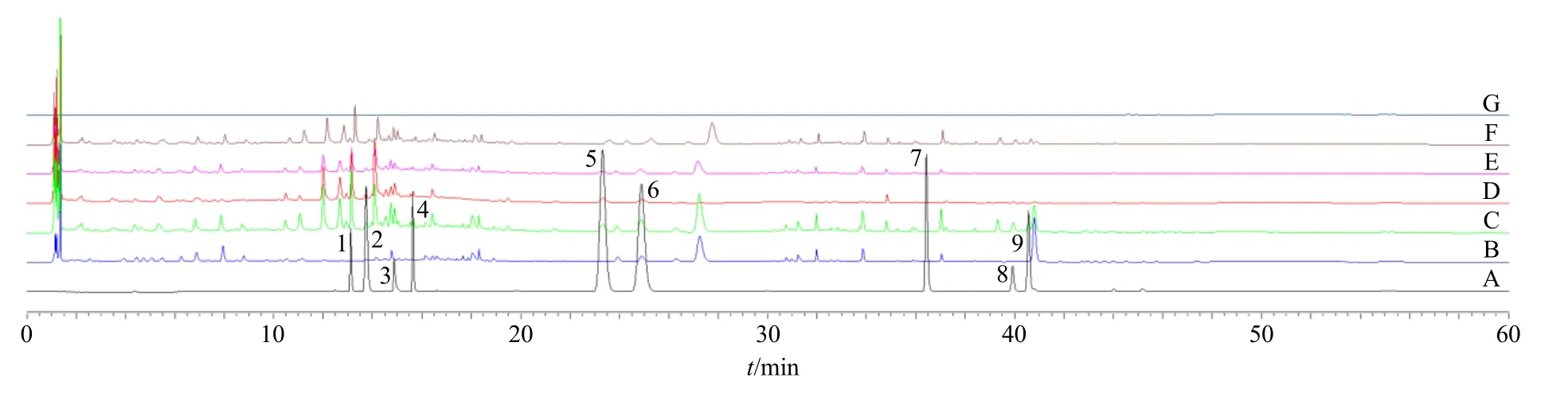
图4 验证全浸膏中成分色谱图 (液相色谱条件2)Fig.4 Validation of chromatogram of components in the whole infusion (liquid chromatography conditions 2)
3.2 UPLC-Q-TOF-MS分析浸膏1、2与全浸膏中的成分
为进一步验证全浸膏中是否含有上述21个成分,实现浸膏1、2与全浸膏的化学成分表征,利用UPLC-Q-TOF-MS对各浸膏进行分析。由于浸膏1与浸膏2成分差别较大,因此,分别针对浸膏1与浸膏2建立2个色谱条件,以进行浸膏1与浸膏2的成分特征性分析,浸膏1、2和全浸膏与混合对照品溶液正、负离子模式下基峰离子流图见图5、6。由于混合对照品溶液3中主要是淫羊藿黄酮类成分,在正离子模式下响应较好,因此,仅在正离子模式下对其进行分析,混合对照品溶液4中主要是红参皂苷类成分,在负离子模式下响应较好,因此,仅在负离子模式下对其进行分析。
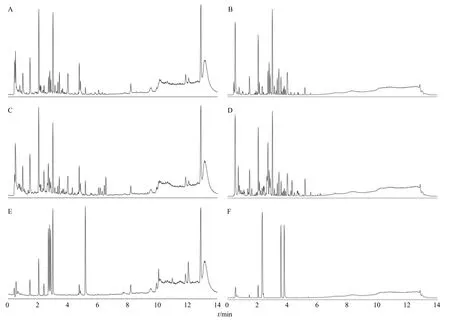
图5 浸膏1、全浸膏基峰离子流图Fig.5 Base peak intensity (BPI) of extractum 1 and total extractum
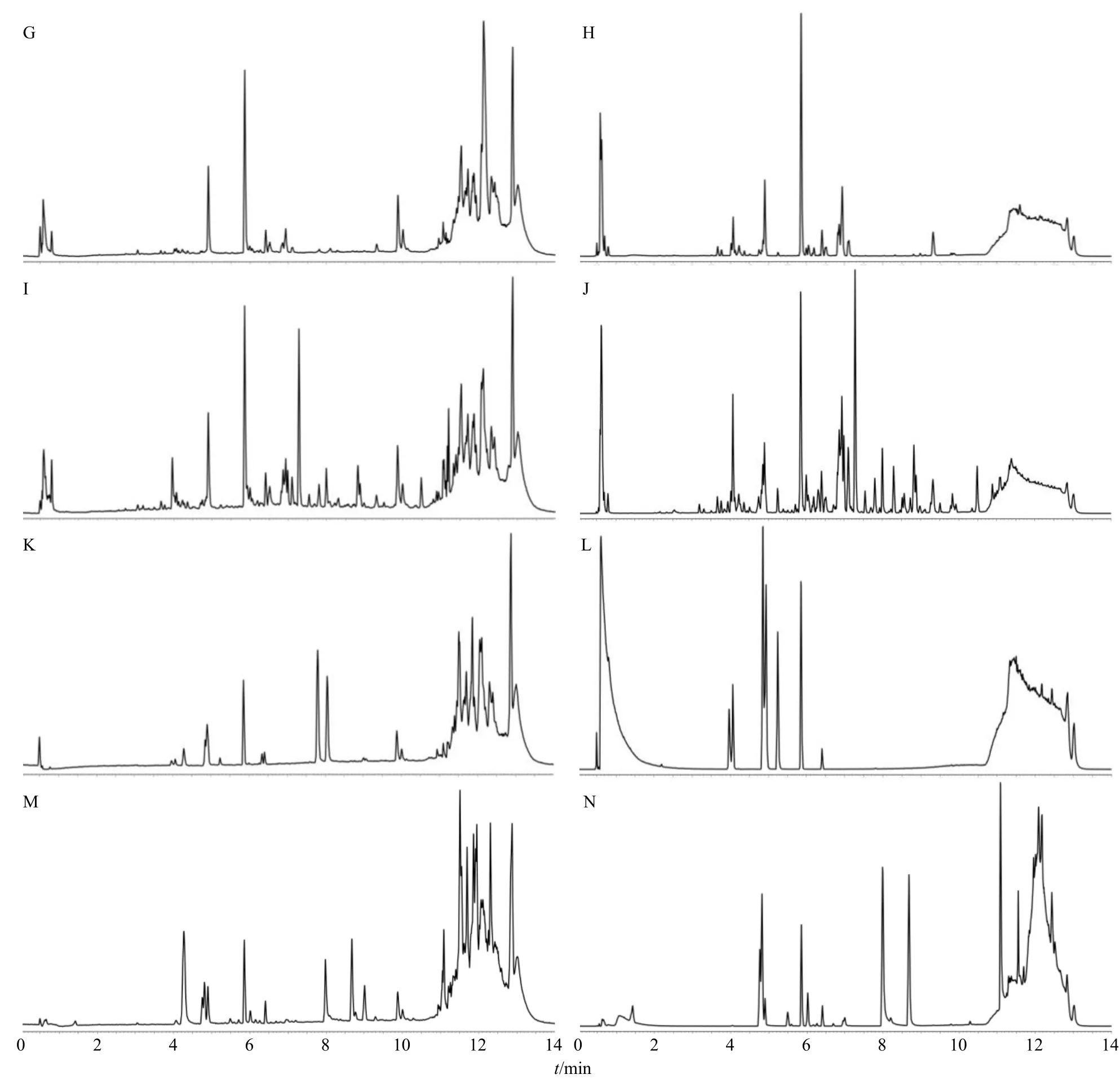
图6 浸膏2、全浸膏基峰离子流图Fig.6 Base peak intensity (BPI) of extractum 2 and total extractum
由图5、6可知,各浸膏在对应的色谱及质谱条件下均较好的分离,将该原始数据导入UNIFI软件中,对比参考文献与对照品,对成分进行鉴定,鉴定结果见表1~4。最终在浸膏1中检测到17个成分,浸膏2中检测到58个成分,在全浸膏中检测到82个成分,实现了各浸膏的复杂成分表征。
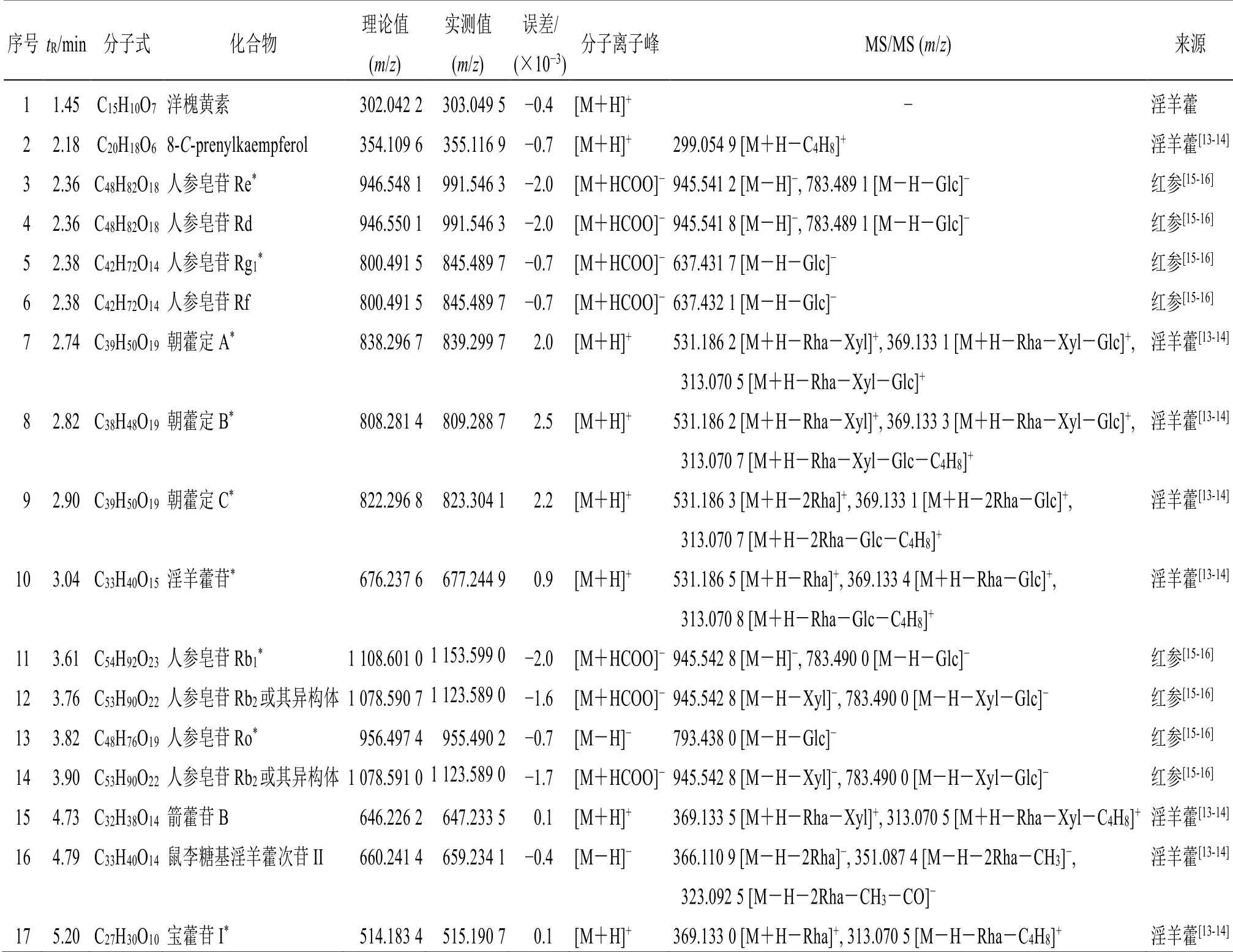
表1 浸膏1中化学成分的鉴定 (液相色谱条件3)Table 1 Components identification of extractum 1 (liquid chromatography conditions 3)
4 讨论
肾宝片由22味中药组成,化学成分复杂,分析时各成分之间容易产生干扰,因此,在建立UPLC针对各浸膏建立指纹图谱时对色谱条件以及溶解样品的溶剂进行了优化。
考察了流动相中的有机相,乙腈与甲醇相比,肾宝片全浸膏的信噪比有明显改善,因此,选择乙腈作为有机相。并采用PDA全波长扫描,选择最优波长,针对浸膏1中的皂苷及黄酮成分,最终将检测波长定为270 nm与203 nm,针对浸膏2中松果菊苷、补骨脂素等成分,检测波长设为254 nm,混合对照品溶液2及浸膏中各成分的响应均较好。由于浸膏中各成分溶解度差异较大,因此,分别考察了水、50%乙腈、75%乙腈以及乙腈作为溶解样品的溶剂,50%乙腈对各成分的溶解性较好。并对梯度洗脱程序进行了优化,建立了在同一色谱条件下对浸膏中多个成分分析的色谱条件。
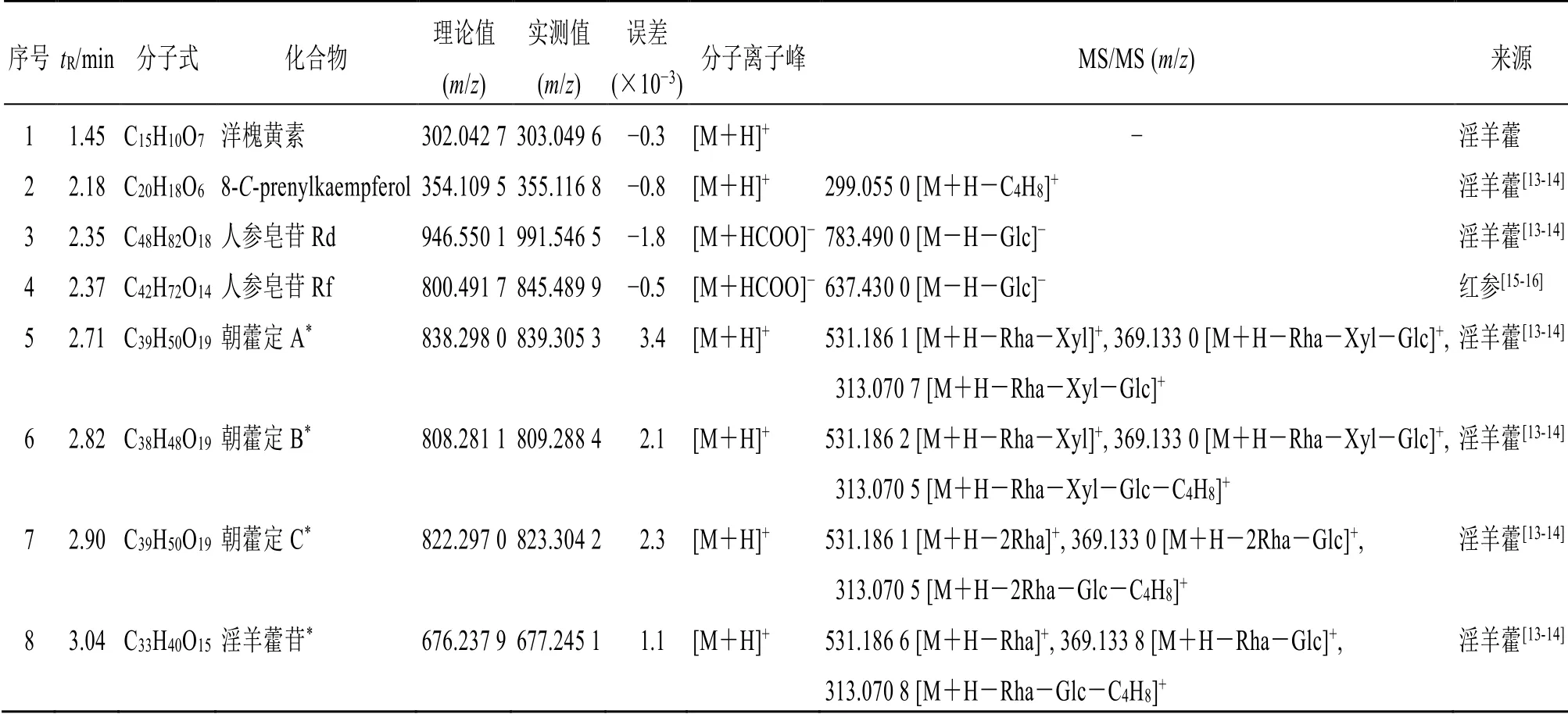
表2 全浸膏化学成分的鉴定 (液相色谱条件3)Table 2 Components identification of total extractum (liquid chromatography conditions 3)
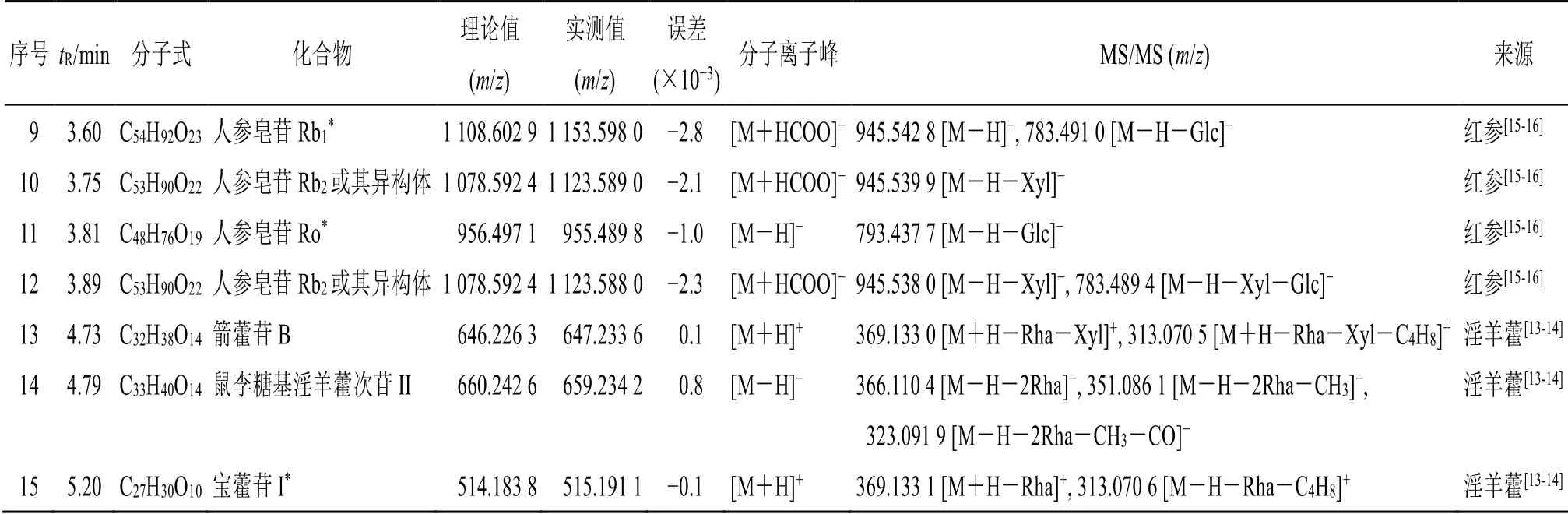
续表2
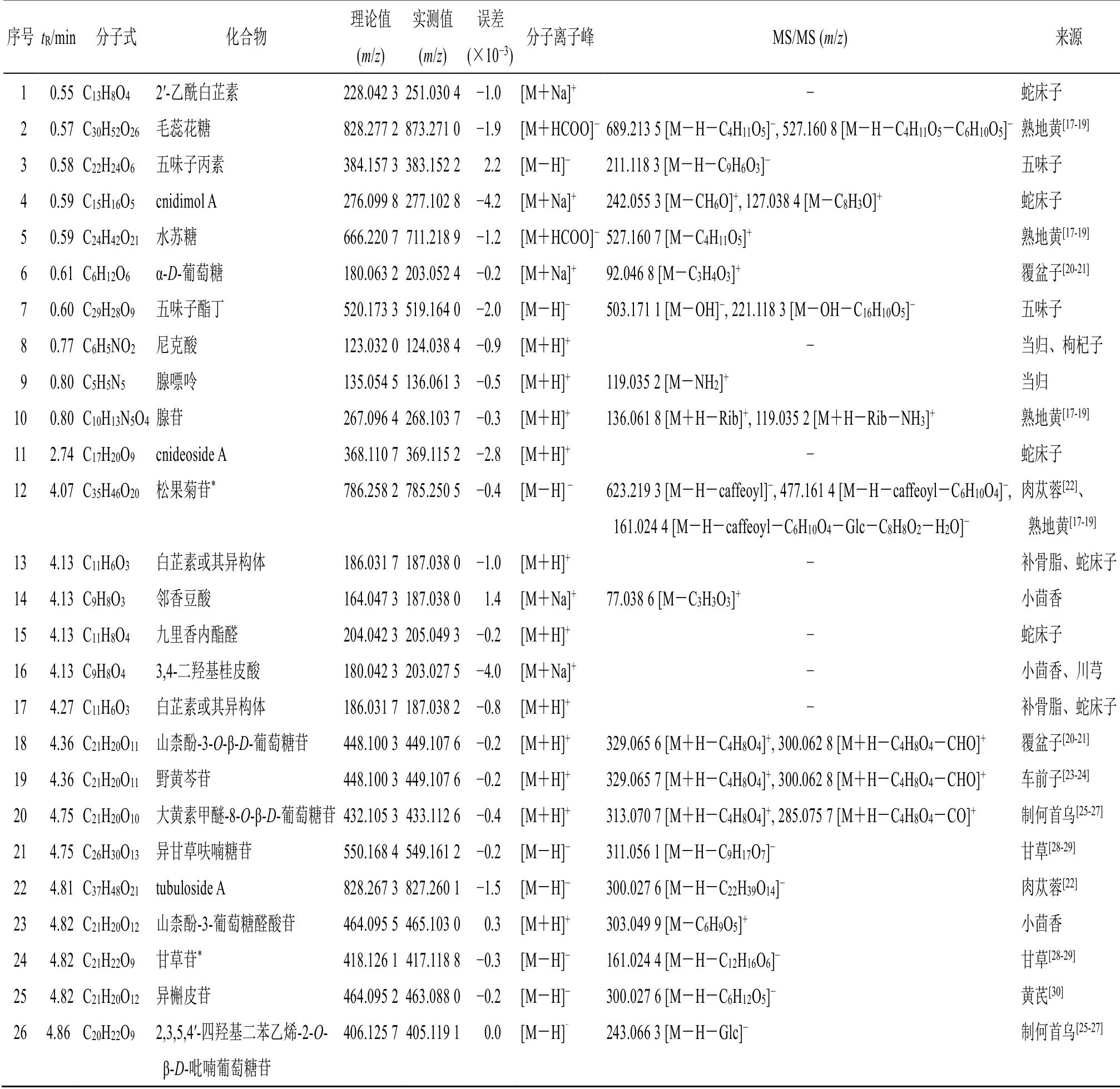
表3 浸膏2化学成分的鉴定 (液相色谱条件4)Table 3 Components identification of extractum 2 (liquid chromatography conditions 4)
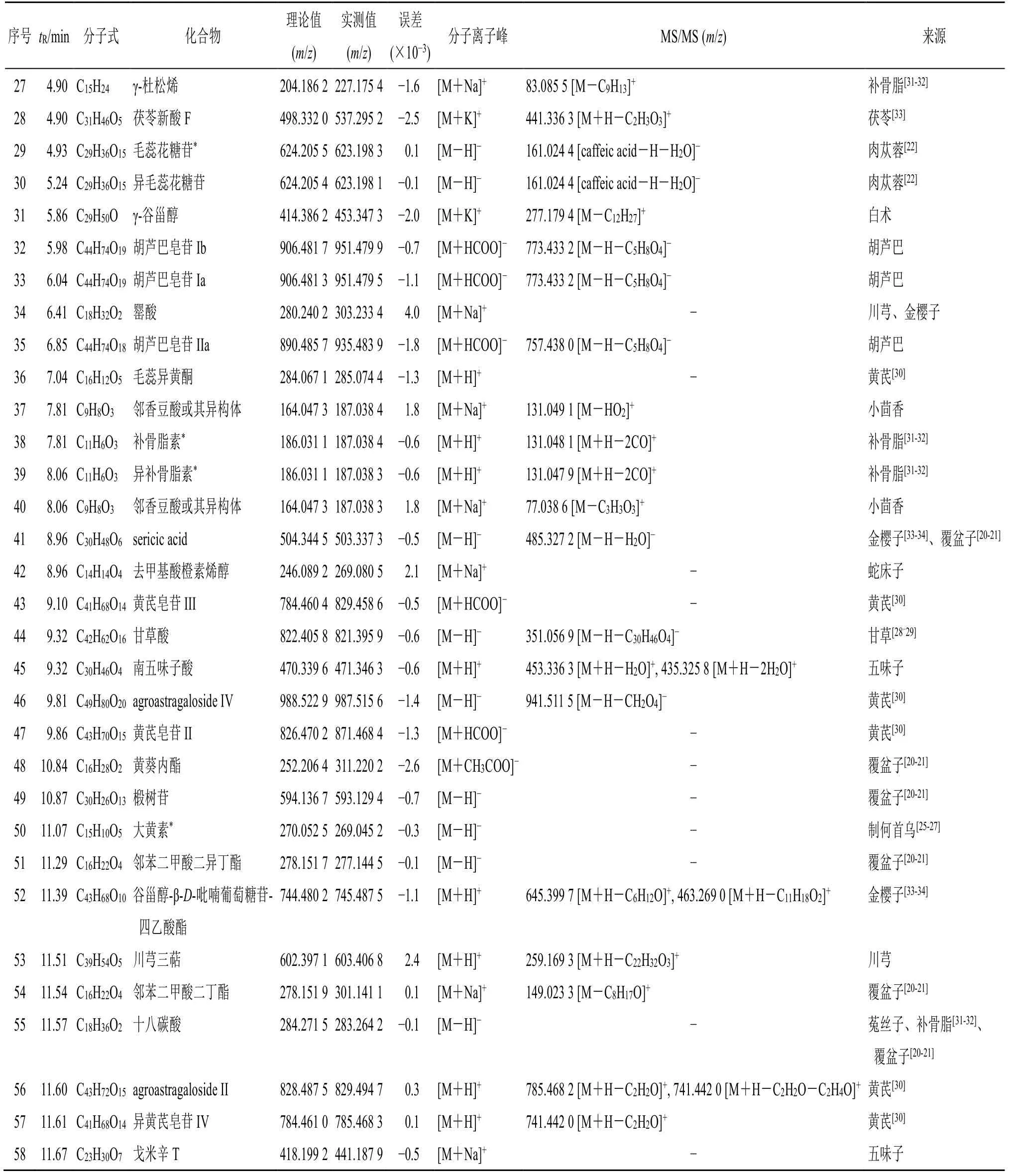
续表3
结合肾宝片制剂处方中各单味药的用量,最终选择21个成分对浸膏1、2以及全浸膏进行分析,按照浸膏1、2逐步敲入的方式,验证全浸膏中的成分。在UPLC分析的基础上,利用UPLC-Q-TOFMS对各浸膏中的成分进行鉴定,由于前期基于多成分分析时建立的UPLC色谱条件分析时间较长,因此,以缩短分析时间、保证分离度为目标,对梯度洗脱程序进行进一步优化。

表4 全浸膏化学成分的鉴定 (液相色谱条件4)Table 4 Components identification of total extractum (liquid chromatography conditions 4)
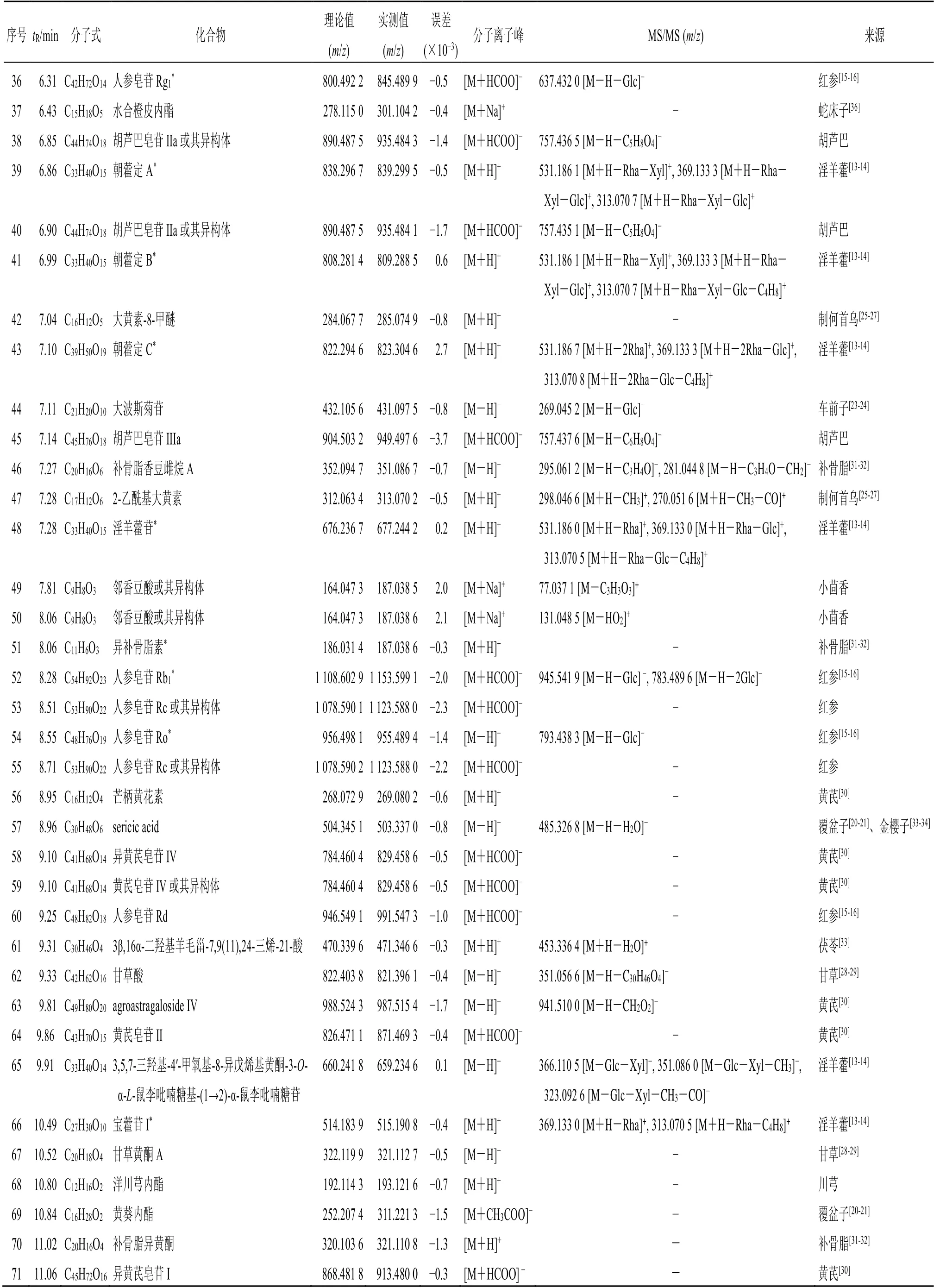
续表4
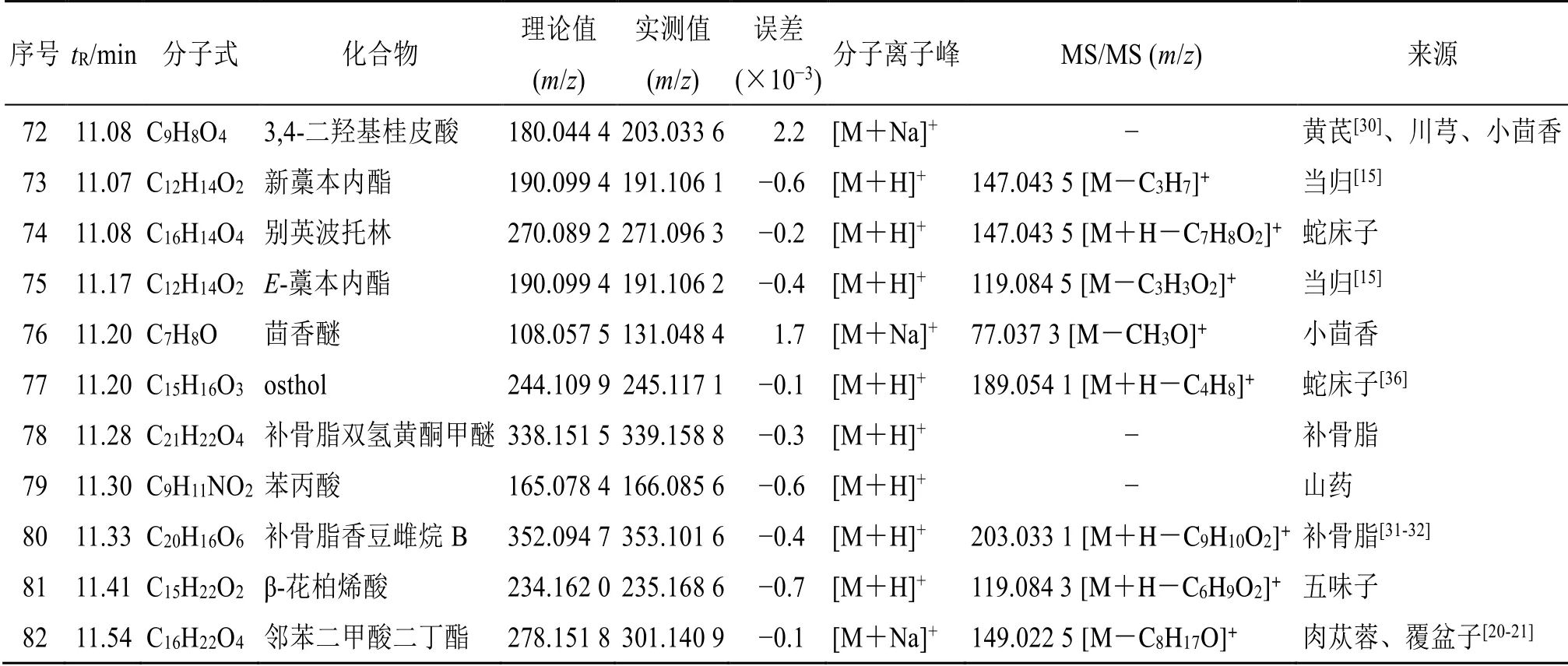
续表4
通过对浸膏1色谱条件的优化,将浸膏1的色谱条件优化至14 min。最终,在浸膏1中检测到17个化合物,所测成分中有9个化合物经与对照品比对得到鉴定;在相同条件下对全浸膏进行分析,在全浸膏中检测到15个化合物,其中7个化合物经与对照品比对得到鉴定,将此结果与浸膏1成分鉴定结果进行比较,全浸膏中15个成分均在浸膏1中检测到,即此15个成分均来自浸膏1。
在浸膏2中检测到58个化合物,其中6个化合物经与对照品比对确认。浸膏2中检测到的成分主要包括:(1)肉苁蓉苯乙醇苷组分:松果菊苷、毛蕊花糖苷、异毛蕊花糖苷;(2)黄芪皂苷组分:黄芪皂苷II、黄芪皂苷III、异黄芪皂苷IV、agroastragaloside II、agroastragaloside IV;(3)补骨脂香豆素组分:补骨脂素、异补骨脂素;(4)制何首乌中蒽醌组分:大黄素、大黄素甲醚-8-O-β-D-葡萄糖苷;(5)甘草黄酮组分:异甘草呋喃糖苷、甘草苷;(6)胡芦巴皂苷组分:胡芦巴皂苷Ib、胡芦巴皂苷Ia、胡芦巴皂苷Ⅱa;(7)黄芪黄酮组分:异槲皮苷、毛蕊异黄酮等。
在相同色谱及质谱条件下对全浸膏进行分析,并对22味中药的化学成分进行搜索,通过对正、负离子模式下全浸膏成分鉴定结果进行整理,共定性了82个化学成分,涵盖了肾宝片中22味中药,其中12个化学成分来自浸膏1,其余70个成分来自浸膏2,主要包括制何首乌中二苯乙烯苷组分和蒽醌组分、黄芪皂苷组分、补骨脂香豆素组分、胡芦巴皂苷组分以及甘草黄酮组分等。
本研究利用UPLC建立了各浸膏的指纹图谱,基于逐步敲入策略以验证全浸膏中的成分,并利用UPLC-Q-TOF-MS快速、方便、有效地对肾宝片全浸膏化学成分进行定性分析,结合UNIFI中药数据库、二级碎片离子信息以及对照品比对,实现了肾宝片各浸膏中复杂成分的快速辨识与归属,为肾宝片制剂工艺过程的质量控制提供了实验基础。
利益冲突所有作者均声明不存在利益冲突