红豆属植物化学成分及其药理活性研究进展
张琳婧,周文娟,倪 林,黄鸣清,张小琴,徐会有*
1.福建农林大学植物保护学院,福建 福州 350002
2.福建中医药大学药学院,福建 福州 350122
红豆属植物OrmosiaJacks.隶属于豆科(Leguminosae)蝶形花亚科(Papilionoideae),《中国植物志》记载该属植物共有135种,中国有35种,主要分布于广东、广西、云南、海南等地,国外美洲热带地区、东南亚、澳大利亚西北部约有100种[1,2]。红豆属植物的种子为红豆,又名“相思子”,其属名Ormosia来自希腊文“ormos”,意为项链,可作项链等装饰品[3]。古有“玲珑骰子安红豆,入骨相思知不知”的美誉[4],将红豆作为情爱相思的象征之物。其木材坚硬细致,纹理美丽,为珍贵家具的上等用材,具有极高的经济价值。多数树种均可药用,其种子与根、茎、皮和叶中含有丰富的化学成分,均可入药,具有通经活血的功效,古人用于治疗跌打损伤、风湿关节炎及无名肿痛等[5-6],但具有一定的毒性。
课题组一直致力于红豆树的资源开发与利用研究。据笔者统计,国内外学者已从红豆属植物中分离鉴定266种化合物,包括生物碱类(65种)、黄酮类(52种)、其他类化合物(27种)以及挥发油成分(122种)。近年来,红豆属树种栽培面积扩大,随着种子无菌萌发和人工扦插繁殖的研究,育种育苗技术突破,且作为推广树种,在广东、广西、福建等地经多年培育[7-10],人工林面积不断扩大,这已为扩大红豆属植物资源的开发与利用研究奠定基础。本文总结多年来国内外学者关于红豆属化学成分及其药理活性的研究,以期为红豆属药用价值的开发与利用提供参考。
1 红豆属化学成分
红豆属植物中已发现的化学成分主要有生物碱类、黄酮类、异黄酮类、挥发油及其他类化合物。
1.1 生物碱类化合物
红豆属植物富含生物碱类成分。目前,从中分离得到65个生物碱[11-19]。主要有金雀花碱(三环)型(1~15)、臭豆碱(四环)型(16~19)、鹰爪豆碱(四环)和羽扇豆碱(四环)型(20~40)、红豆(五环/六环)型(41~54)、类金雀花碱型(55~61)、其他型(62~65)生物碱。具体数据见表1和图1。
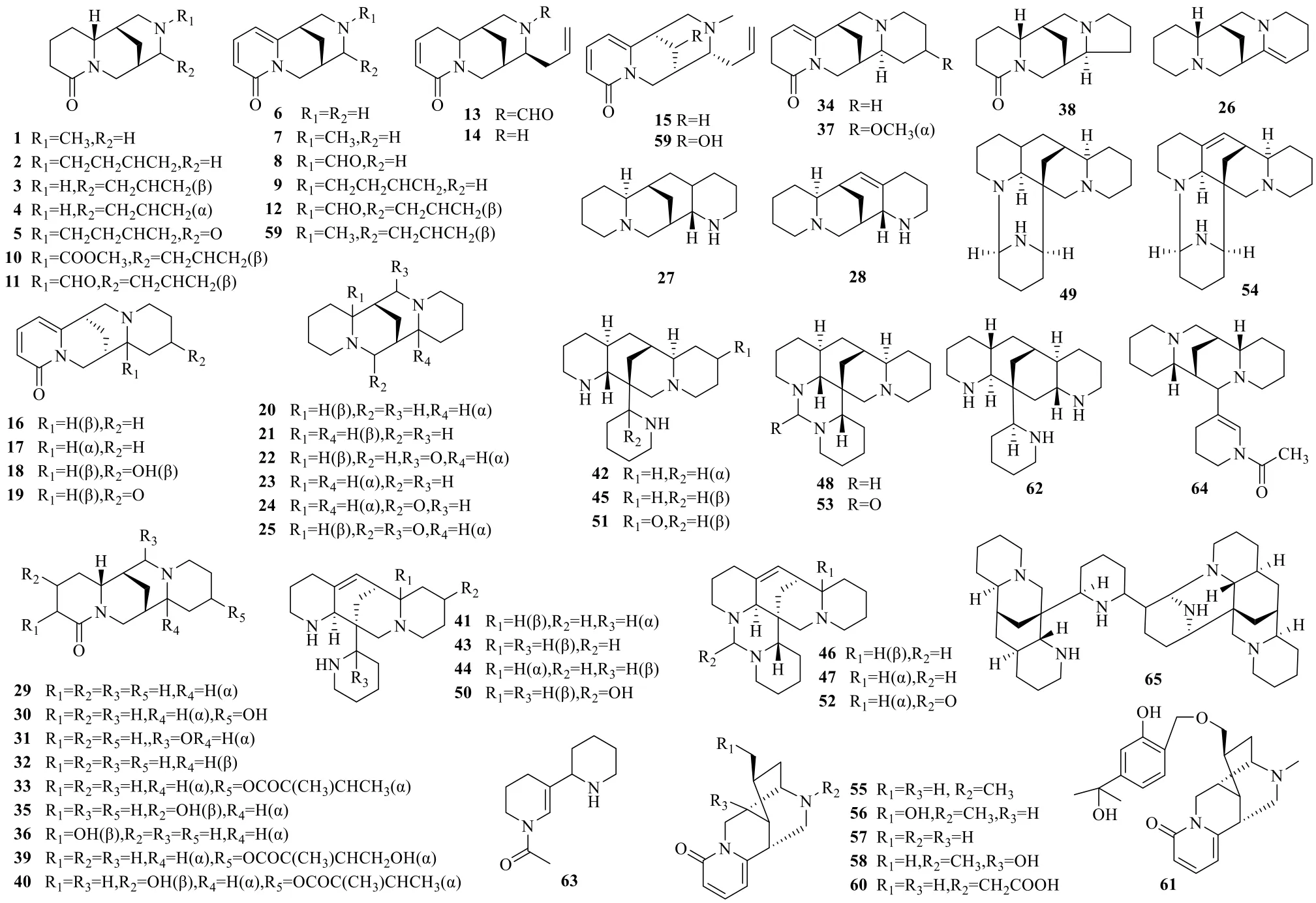
图1 红豆属植物中生物碱类化合物结构Fig.1 Chemical structures of alkaloids in Ormosia
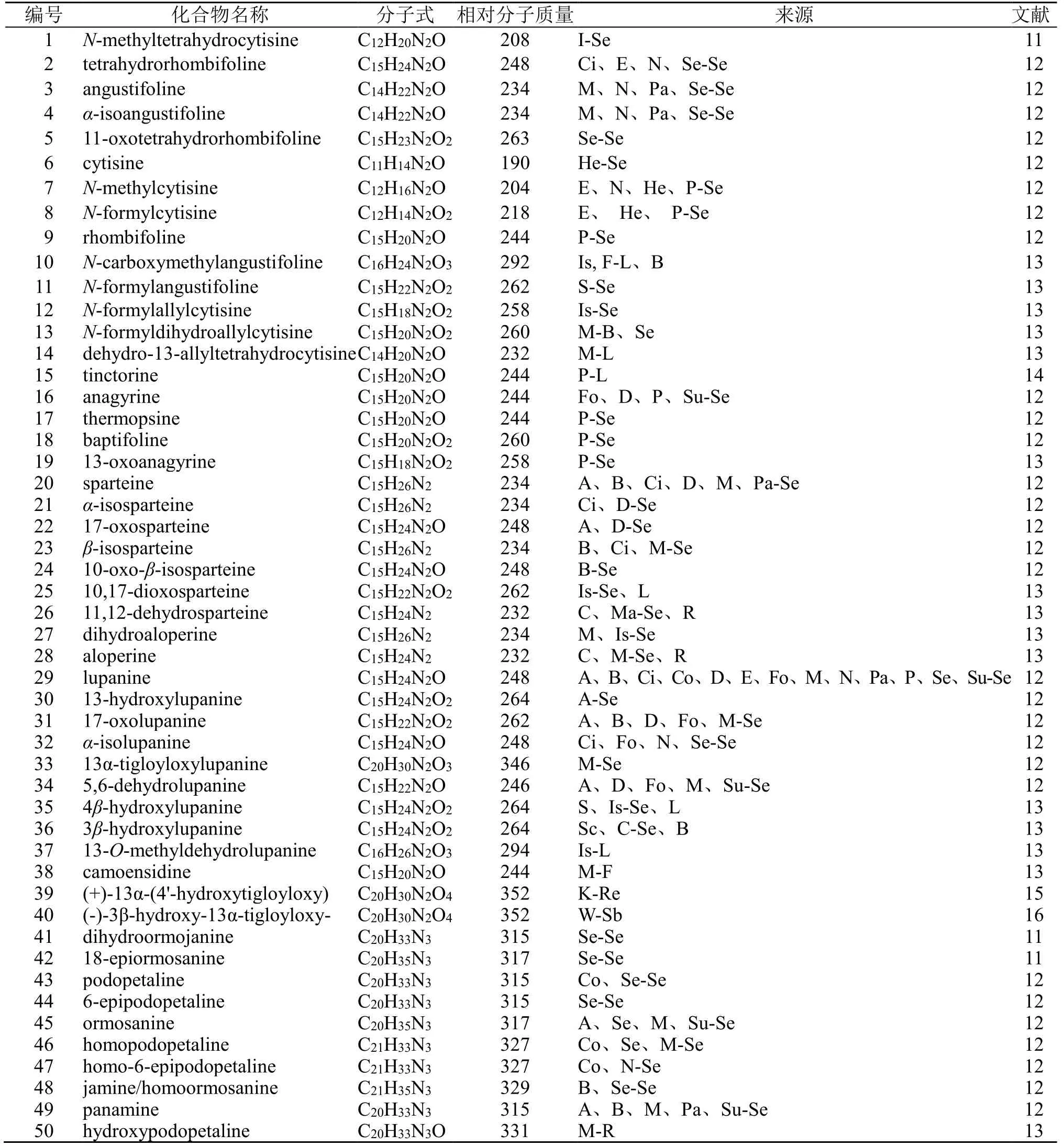
表1 红豆属植物中生物碱类化合物Table 1 Alkaloids in plants of Ormosia
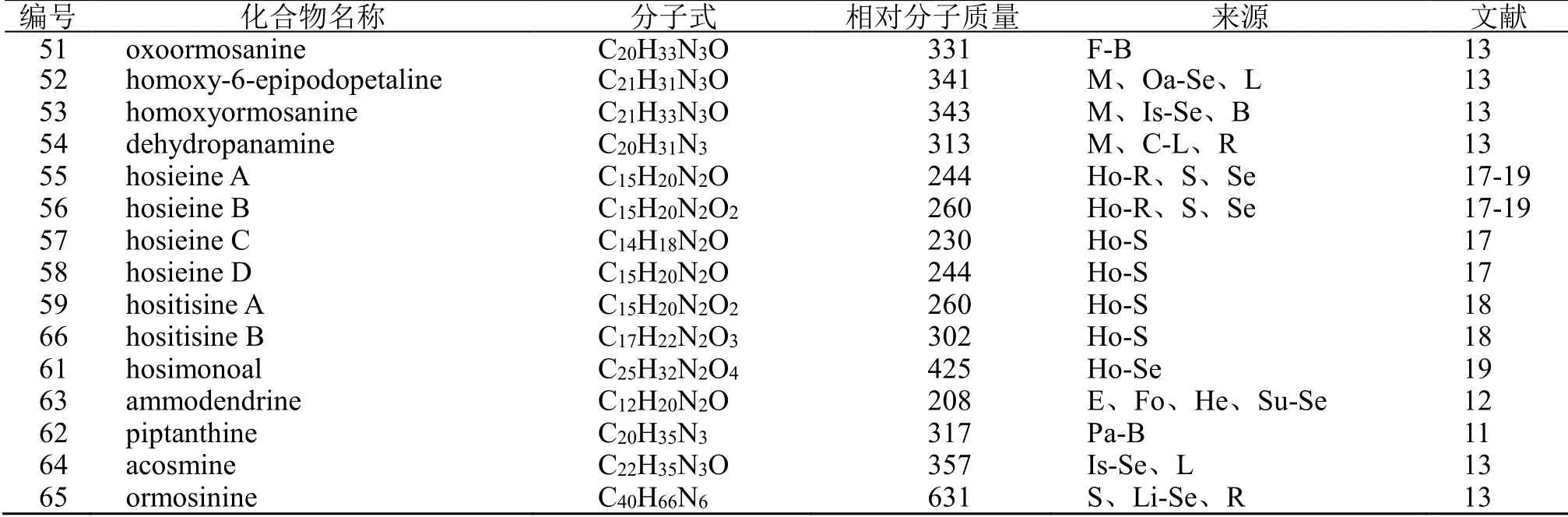
续表1
红豆属生物碱的文献报道始于1971年,加拿大学者McLean等[11]于从3种中国韧荚红豆、软荚红豆、茸荚红豆的种子和树皮提取物中分离鉴定了4个生物碱(1、41、42和62);1988年,美国学者Kinghorn等[12]从15种红豆属植物种子中提取并利用毛细管气相色谱法和质谱法等鉴定了30种生物碱(2~9、16~18、20~24、29~34、43~49和63);1999年,Ricker等[13]从9种红豆属植物的叶、果实等多个部位中提取分离得到共21种生物碱(10~14、19、25~28、35~38、50~54、64和65),并通过气相色谱-质谱联用技术鉴定了其结构。上述早年研究分析鉴定了这些生物碱的结构,但未曾报道其详细的理化性质,因此其准确性有待进一步考证。
从结构来看,化合物1~15属于金雀花碱型(三环型)生物碱,是喹诺里西啶和哌啶环骈合而成的衍生物,其常见结构特征:N-17取代不同基团、C-3和C-4或C-5和C-6的双键被氢化以及C-11连有烯丙基等。化合物16~19属于臭豆碱型(四环型)生物碱,是2个喹诺里西啶骈合而成的衍生物,其中1个喹诺里西啶含有酰胺结构,C-13位易引入羟基,也容易被羰基化。化合物20~40属于鹰爪豆碱或羽扇豆碱型(四环型)生物碱,是2个喹诺里西啶骈合而成的衍生物,常见的类型结构特征:C-2/C-10/C-17位易羰基化,少数C-3/C-4位含有羟基,C-13位羟基容易与巴豆酰基形成酯,少数羟甲基化;C-5与C-6或C-11与C-12氢化形成双键。其中化合物27、28含一个喹诺里西啶和一个哌啶环,化合物38为喹诺里西啶和吲哚里西啶骈合而成。化合物41~54属于红豆型(五环/六环型)生物碱,一类以苦豆碱为母核,C-9位连接1个哌啶环的衍生物,常见的类型结构特征:N-23位易与N-12位通过亚甲基环合;N-12位与C-22位连接闭合成环,构成六环型生物碱;C-16与C-17位双键容易被氢化还原。
在生物碱的研究中,Pouny等[17]的研究备受关注。从中国红豆树的根和枝条提取物中首次分离得到4种类似金雀花碱的新型生物碱,其C环和D环形成2-氮杂双环[3.2.1]辛烷,命名为hosieine A~D(55~58)。由于55结构独特,且在治疗精神分裂症和阿尔茨海默病中具有潜在的应用价值,2015年,Ouyang等[20]发现亚硝基-烯环化反应能够构建氮杂[3.2.1]辛烷体系,经过21步反应,完成了(-)-Hosieine A的首次不对称全合成;2018年,美国贝勒大学Huang等[21]以6-甲基-2-吡啶酮为起始原料,经过7步反应,完成了外消旋体 (±)-hosieine A的合成。随后,本课题组从红豆树O.hosieiPrain嫩枝和种子70%乙醇部位同样分离得到了hosieines A和B,以及3个新的类金雀花碱的生物碱hositisines A、B和hosimonoal(59~61),化合物61则是首次分离得到的类金雀花碱与单萜类成分以醚键相连形成的生物碱[18-19]。
1.2 黄酮类化合物
红豆属植物同其他豆科植物一样含有大量的黄酮类成分。目前,文献已报道52个黄酮类化合物[22-28],主要从花榈木、红豆树、O.monosperma、O.robusta以及O.sumatrana中分离得到。包括黄酮类(66~77)、黄酮醇类(78~81)、二氢黄酮类(82)、二氢黄酮醇类(83、84)、异黄酮类(85~110)、二氢异黄酮类(111~115)、紫檀素类(116)和花青素类(117),具体成分见表2及图2。异黄酮类化合物是红豆属植物中分离得到最多的一类黄酮,且能与不同的糖苷或异戊烯基相连或进一步成环,其结构变化多端。从花榈木和O.monosperma根皮及O.robusta树皮部位分离得到多个特殊的异黄酮(醇)异戊烯基取代物,化合物106~108、110、115的C-6连接异戊烯基,并与C-7羟基形成一个吡喃环,而化合物109则与C-5羟基氧化形成类似结构。化合物117为黄烷酮的二聚体且有桂皮酰基取代,首次从O.sumatrana叶部提取物分离鉴定。
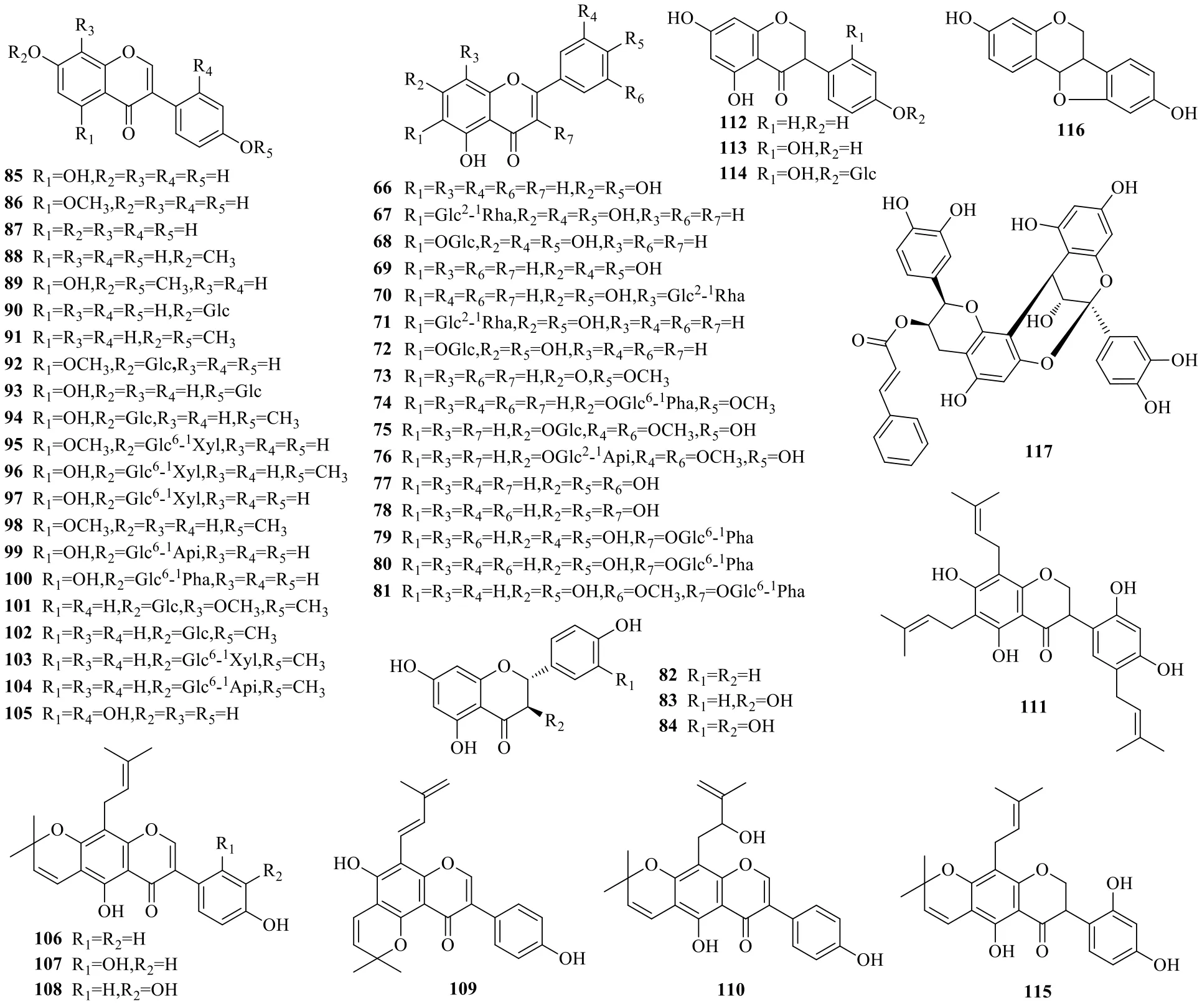
图2 红豆属植物中黄酮类化合物结构Fig.2 Chemical structures of flavonoids in Ormosia

表2 红豆属植物中黄酮类化合物Table 2 Flavonoids in plants of Ormosia
1.3 其他类化合物
主要包括萜类、苯丙酸类、木脂素类化合物等[16,19,22,24,27-29],共27种,具体化合物及结构见表3及图3。
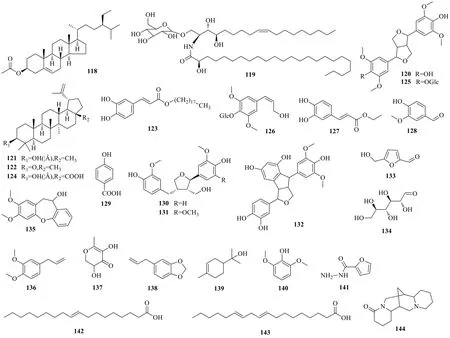
图3 红豆属植物中其他类化合物结构Fig.3 The chemical structures of other compounds in Ormosia

表3 红豆属植物中其他类化合物Table 3 Other compounds in plants of Ormosia
挥发油成分主要包括醛酮类、醇类、酯类、烯烃类、胺类、环烃类、羧酸类以及酰胺类等。据统计,目前对于红豆属挥发油成分的分离只涉及花榈木及红豆树2种,得到122种挥发油化学成分[30-33],具体成分见表4。其中,从花榈木中提取分离得到共89种(O1~89),从红豆树叶中提取分离得到36种(O35、O40、O52、O90~122),两者差异较大,共有的挥发油成分仅有O35、O40和O52,其他树种挥发油成分未见报道,差异性未知,值得进一步研究。
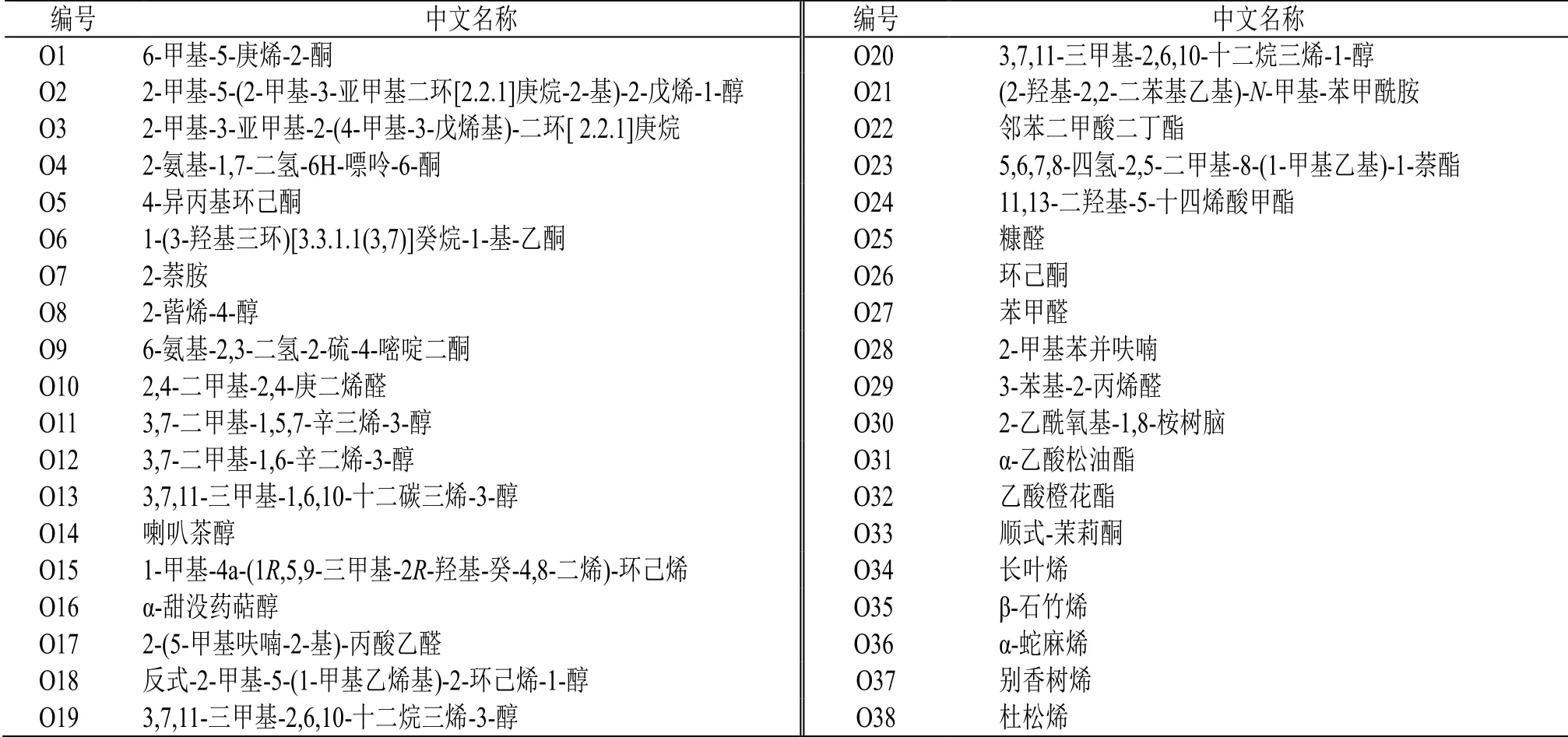
表4 红豆属植物中挥发油化学成分Table 4 The chemical constituents of the volatile oil from plants of Ormosia

续表4
2 生物活性
2.1 抗氧化活性
Ahmed等[27]对O.robusta树皮部甲醇提取物萃取部位进行总酚含量测定,发现酚类成分含量越高,对1,1-二苯基-2-三硝基苯肼(DPPH)自由基清除能力更强,其中醋酸乙酯部位清除能力最好,半数致死浓度(LC50)值为1.21 μg/mL,优于阳性对照二丁基羟基甲苯(BHT,IC50:21.45 μg/mL)。翟大才等[29]通过测定红豆树种子正丁醇、醋酸乙酯和石油醚等萃取物对DPPH自由基的清除作用,测得红豆树种子正丁醇、醋酸乙酯和石油醚萃取物及维生素C(Vc)对DPPH自由基清除作用的半数有效量(ED50)值分别为0.149 6、0.021 2、0.040 2和0.002 7 mg/mL;测定红豆树种子正丁醇、醋酸乙酯、石油醚萃取物和Vc对2,2’-连氮基-双-(3-乙基苯并二氢噻唑啉-6-磺酸)(ABTS)自由基的清除率,ED50值分别为0.027 2、0.122 8、0.023 0和0.002 3 mg/mL。Feng等[22]对异黄酮(111)进行了抗氧化活性评价,结果显示具有显著的清除DPPH自由基能力,IC50值为28.5 μmol/L,与阳性对照L-抗坏血酸(IC50:25.6 μmol/L)相当。
2.2 对中枢神经系统的作用
Lu等[23]第一次提出O.henryi叶部提取物具有初步的抗抑郁作用,小鼠在经过提取物治疗后观察到的变化包括:蔗糖偏好指数升高、进食潜伏期缩短、尾悬吊时间延长以及脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)表达上调,表明富含黄酮化合物的O.henryi叶部提取物是一种具有调节抑郁功能的营养保健品(或功能性添加剂)领域的新资源。Pouny等[17]发现从O.hosiei分离得到的生物碱55~57对神经元烟碱型乙酰胆碱α4β2受体具有显著的亲和力,其IC50值分别为0.96、3.9和4.8 μmol/L,优于阳性对照烟碱(IC50:4.9 μmol/L),表明红豆生物碱可能具有与中枢神经系统相关的潜在应用,如戒烟、抑制焦虑、增强认知等。
2.3 细胞毒活性
特异性蛋白酶抑制剂的研发是抗癌药物研发的热点,Su等[28]从O.sumatrana叶提取物氯仿溶解部位中发现化合物119对人白血病细胞HL-60具有抑制活性,其IC50值为30 μmol/L。Feng等[22]通过细胞存活率(MTT)分析方法对异黄酮(111)进行了细胞毒性评价,结果显示对人肺癌细胞(A549)、人肺腺癌细胞(LAC)、人肝癌细胞(HepG2)具有较强的抑制活性,IC50值分别为4.25、5.22和7.09 μmol/L,优于阳性对照阿霉素(IC50值分别为15.15、20.48和79.5 μmol/L)。Xu等[19]研究发现,化合物55、59~61和132对A549、HepG2、人卵巢癌细胞(A2780)和人乳腺癌细胞(MCF7)具有较好的抑制活性,IC50值在5.7~36.5 μmol/L。
2.4 抗炎活性
Ni等[18]研究表明,生物碱59和60在50 μmol/L浓度下可显著降低乳酸脱氢酶(lactate dehydrogenase,LDH)的释放,对氧糖剥夺/复氧(oxygen-glucose deprivation/reoxygenation,OGD/R)损伤的PC12细胞具有较强的保护作用。
2.5 抑菌活性
翟大才等[29]通过检测红豆树种子正丁醇、醋酸乙酯和石油醚等萃取物对金黄色葡萄球菌、苏云金芽孢杆菌和绿脓杆菌等菌株的抑菌活性,发现红豆树种子正丁醇萃取物对上述革兰阴性菌的抑制效果强于革兰阳性菌;而石油醚萃取物恰巧与此相反,其对上述革兰阳性菌的抑制效果强于革兰阴性菌。此外,翟大才等[33]还检测了红豆树叶挥发油对金黄色葡萄球菌、枯草芽孢杆菌、大肠杆菌及绿脓杆菌的抑菌活性,结果显示红豆树叶挥发油对革兰阳性和革兰阴性菌均具有一定的抑制效果,且在相同浓度下抑制强度为:金黄色葡萄球菌>绿脓杆菌>大肠杆菌>枯草芽孢杆菌。Linuma等[26]发现从O.monosperma的根皮部中分离得到的异黄酮(115)对口腔微生物(变形链球菌、牙龈卟啉菌和伴放线放线杆菌)具有中等抑制活性,其最小抑制浓度(MIC)均为6.3 μg/mL,化合物85对牙龈卟啉菌也具有抑制活性,MIC为12.5 μg/mL。邱亚铁等[25]对红豆树中分离的黄酮类化合物进行了抑制植物病原真菌的活性评价,结果表明,黄酮82、92和94在150 mg/L下对禾谷镰刀菌、西瓜尖镰孢菌和茄病镰刀菌的菌丝生长显示中等强度的抑制作用,且抑制率在25.65%~39.81%。
2.6 杀虫活性
Ahmed等[27]对O.robusta树皮部甲醇提取物用正己烷、四氯化碳、氯仿和醋酸乙酯进行萃取,并将这5个部位对盐水丰年虫进行致死性生物测定,结果发现均有较好的毒杀活性,其中正己烷部位毒杀作用最强,(LC50值为1.49 μg/mL,与阳性对照硫酸长春新碱相当。
3 结语
红豆属植物资源种类丰富,但其化学成分及生物活性的研究还有待更深入的研究。我国红豆属植物资源日渐丰富,而化学成分及活性研究中仅涉及花榈木、红豆树及海南红豆,极大限制了红豆属植物资源药用价值的开发与利用。已发现有一些新颖的生物碱类活性显著,但更深入的活性机制研究尚未见报道,有待进一步深入研究。本课题组致力于红豆属植物资源开发与利用,已经取得部分成果,后续将进行更系统的化学成分和生物活性的研究,为红豆属的药用资源开发与药效物质基础研究提供更多参考。
利益冲突所有作者均声明不存在利益冲突