二氯甲烷和甲苯对咪唑离子液体结构和性质及铝电沉积的影响
田国才,袁青香
1) 昆明理工大学省部共建复杂有色金属资源清洁利用国家重点实验室,昆明 650093 2) 昆明理工大学冶金与能源工程学院,昆明 650093
铝是国民经济和国防建设、战略新兴产业、航空航天等的基础和战略材料[1-2]. 当前工业铝生产常用的方法是霍尔-埃鲁特法,此法存在能耗高、腐蚀设备严重、污染环境等问题[3-4]. 寻找一种可在低温下绿色产铝的方法是科研者努力的方向. 近年来,我国在低温铝电解方面取得了不小成绩,主要的工作集中在传统熔盐体系的改进上,虽然体系的电解温度有一定的下降,但下降程度有限[2-4]. 离子液体的出现为开发低温铝电解技术提供了一种可能.
离子液体是由有机阳离子和一些有机或者无机的阴离子构成的接近室温或室温下呈液态的一类离子体系[5-8],其具有不易挥发、电化学窗口宽、液态温度范围宽、热稳定性良好和导电性及性质组合多变等优点而广泛应用于电化学(电沉积、电池)、催化、有机合成、提取分离等各领域并分别取得相关进展[5-17]. 近年来,离子液体作为一种新型绿色电解质,已被用于在室温或者接近室温的条件下电沉积铝,并取得了一定进展[9-15]. 但是还存在体系的黏度较大,沉积层枝晶严重和厚度较薄等问题亟待解决[11-15]. 添加剂的加入是解决这些问题的常用方法之一[12-14]. 近年来,研究者开展了氯化物、乙腈、芳香族化合物、羰基类小分子、卤代烷、烟酸及其衍生物等不同添加剂对离子液体电沉积铝的影响的研究,取得了一定进展[18-27].然而,实验中究竟什么样的添加剂有效无规律可循,添加剂对离子液体的微观结构及物化性质有何影响,以及添加剂在离子液体电沉积铝中的作用机制及其对铝沉积层质量影响等仍不清楚.
近年来,芳香烃如甲苯C7H8等常被用做离子液体电沉积铝中的有效添加剂. C7H8上甲基的存在使其更稳定,但由于甲基和苯环上碳原子杂化方式不同,导致C-C单键上的电子云偏向苯环一边,使苯环活化. Abbott和 McKenzie[28]、Robinson和 Osteryoung[29]、Pulletikurthi等[30]、Uehara等[31]研究了C7H8作为添加剂对离子液体电沉积铝的影响. 发现加入一定量的C7H8能够提高体系电导率和沉积层耐腐蚀性,并得到致密且附着力好的铝沉积层. 研究发现加入二氯甲烷可大幅提升离子液体体系的电导率,能获得较好的铝沉积层.Kang等[32]研究了卤代烷烃、芳香烃和酯类对氯化-1-丁基-3-甲基咪唑三氯化铝[BMIM]Cl/AlCl3离子液体体系电化学性质和电活性离子的影响. 发现加入卤代烷烃和芳香族化合物均可提高体系电解效率,降低黏度增加电导率,且电活性离子依旧是铝复合离子. 当添加剂摩尔分数约66.7%~75%时,以二氯甲烷(DCM)为添加剂可获得镜面亮泽的铝沉积层,以芳香烃C7H8为添加剂在体系中电沉积可获得白色扁平的铝沉积层. 然而卤代烷烃、芳香烃等添加剂如何影响离子液体体系中离子微观结构和存在形式、离子的迁移扩散及体系的物化性质(黏度、电导率)等,进而影响离子液体中铝电沉积的微观机理尚不清晰. 因此系统研究卤代烷烃与芳香烃对咪唑类离子液体结构与物化性质,及其对电沉积铝的影响机制,对设计筛选新型添加剂具有重要意义. 随着计算机性能的发展,以及量子化学计算和分子动力学模拟方法的进步,为从微观结构上分析添加剂对离子液体电沉积铝体系的影响提供了强有力的保障.
本文采用密度泛函理论与分子动力学模拟相结合的方法研究DCM和C7H8的加入对[BMIM]Cl/AlCl3(摩尔比为1∶2)体系结构、物化性质和铝电沉积的影响. 系统考查添加剂及离子液体的结构、反应活性及其之间的相互作用机制,揭示添加剂对离子液体体系中离子间的相互作用、径向分布函数、配位数和空间分布函数等结构特性,及对密度、黏度、电导率、扩散系数等物化性质的影响规律和机制,进一步阐明添加剂对离子液体体系电沉积铝的影响机制,为进一步在离子液体[BMIM]Cl/AlCl3中电沉积铝选择、开发高效稳定、环境友好的新型添加剂提供理论依据.
1 计算方法
[BMIM]Cl/AlCl3、DCM和C7H8的稳定构型、活性位点及其相互作用等采用密度泛函理论中常用的B3LYP方法在Guassian 09软件包[33]计算得到. 在6-311++G(d,p)基组水平下对结构进行全优化,得到的几何结构经过振动频率分析没有虚频确定为最稳定构型,之后以此稳定构型计算相关的物理量. 分子动力学模拟中,各离子及分子的构型与原子类型如图1所示. [BMIM]+、Cl-和AlCl3的力场参数取自de Andrade等开发的Amber型力场[34],DCM的力场参数取自Prampolini等[35]的力场,C7H8的力场参数取自Kim和Lee[36]的力场,力场中的原子类型与图1中原子类型一致. 分子动力学模拟采用MDynaMix[37]程序,模拟体系中离子液体与三氯化铝的摩尔比1∶2,为与实验浓度一致,添加剂的摩尔分数取为0.7,对应的[BMIM]Cl、AlCl3和添加剂的数目分别为30、61和212,将其随机放入模拟盒子中作为模拟体系的初始构型,初始速度从303.14 K下的Maxwel分布给出,采用三维周期性边界条件. 静电相互作用采用Ewald求和技术处理[38],运动方程采用Tuckerman-Berne双时间步长算法[39-41]求解,长时间和短时间步长分别取2 fs和0.2 fs. 模拟体系的温度和压力保持在303.14 K和0.1 MPa不变,温度和压强耦合常数分别为30 fs和700 fs. 体系先在NPT系综下平衡运行400 ps,得到体系的平衡构型及密度,然后将NPT系综模拟得到的平衡构型作为初始构型采用NVT系综进行模拟运行2 ns,每10步存储一次轨迹文件,用于径向分布函数、空间分布函数、扩散系数、黏度、电导率等物理量的进一步分析和计算.
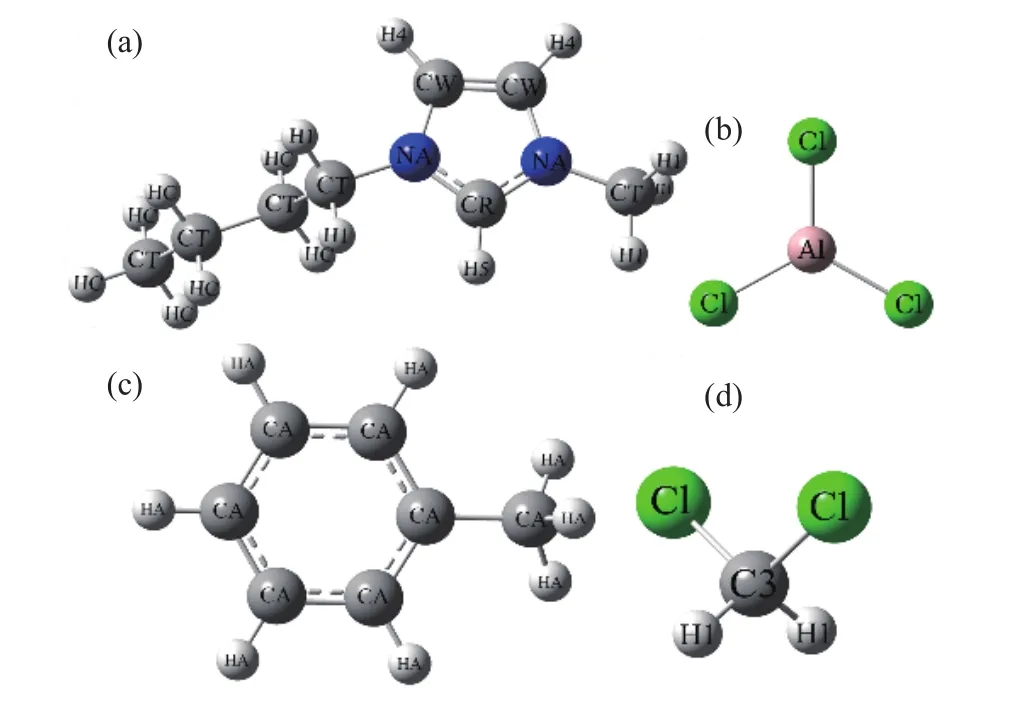
图1 模拟用到的阳离子和分子的结构以及相应原子的类型.(a)[BMIM]+;(b)AlCl3;(c)C7H8;(d)DCMFig.1 Structure of the molecules and cation, and the corresponding atom types: (a) [BMIM]+; (b) AlCl3; (c) C7H8; (d) DCM
2 结果和讨论
2.1 结构与反应活性的量子化学
图2给出了采用 B3LYP/6-311++G(d,p)方法计算得到的[BMIM]Al2Cl7/DCM和[BMIM]Al2Cl7/C7H8体系的稳定构型图. 表1给出了计算得到的[BMIM]Al2Cl7/M(M = DCM、C7H8)体系相关粒子的相互作用能Eint,其中阴阳离子间相互作用能Eint由Eint= EA-B-EA-EB计算,其中EA-B为A和B形成的离子对AB经零点能校正的构型能,EA为A经零点能校正的构型能,EB为B经零点能校正的构型能. 纯离子液体中[BMIM]+与的相互作用能 为 -275.02 kJ·mol-1. 纯离子液体中 [BMIM]+与能形成两组 C-H···Cl弱氢键 (C3-H10···Cl31,r=0.265 nm,θ=150.03°和 C6-H13···Cl27,r=0.283 nm,θ=153.12°). 氢键通常定义为 X-H···Y,其中氢键参数定义:H-Y的键长为r,X-H-Y之间的夹角为θ. 根据氢键参数可分为弱氢键(r=0.22~0.32 nm,θ=90°~150°),中强氢键 (r=0.15~0.22 nm, θ=130°~180°)和强氢键 (r=0.12~0.15 nm,θ=175°~180°).由图2(a)可知,加入DCM后阴离子与阳离子间的 C-H···Cl弱氢键 C3-H10···Cl31参 数 变 成 了 r =0.271 nm,θ=145.31°, C6-H13···Cl27变为了r = 0.299 nm,θ=144.0°. 因而,DCM加入使得体系中阴阳离子间氢键键长增加,键角减小,表明DCM的加入削弱了体系中阴阳离子间的相互作用. DCM与阴离子形成的 C-H···Cl弱氢键 (C35-H36···Cl28, r =0.288 nm,θ =165.54°),比 DCM 与阳离子 [BMIM]+形成的 C-H···Cl弱氢键 (C1-H9···Cl38,r = 0.319 nm,θ =159.77°)稍强一些. 这表明体系中DCM与[BMIM]+和的相互作用相差不大. 这与表1中计算得到的DCM与阴和阳离子的相互作用能差别不大的情况相一致. 从表1中可以看到,DCM加入后使体系阴阳离子间的相互作用能由-275.02 kJ·mol-1变为了-267.99 kJ·mol-1,表明加入DCM明显减弱了阴阳离子之间的相互作用,使得体系中阴、阳离子扩散更为容易,从而降低了体系的黏度,增加了体系的电导率,与实验结果一致[32]. 由图2(b)知,加 入 C7H8后 使 C3-H10···Cl31弱 氢 键 的 参 数 变 成了 r = 0.269 nm,θ=146.22°,键长增加键角减小,但对 C6-H13···Cl27弱氢键的参数变化较小,结合表 1中体系离子间的相互作用能可知,C7H8与[BMIM]+的相互作用能大于其与阴离子的相互作用能,这反映在图2(b)中C7H8分布在距离阳离子近的一侧. 当C7H8与阳离子结合时,阴阳离子间相互作用能由-275.02 kJ·mol-1变为-260.76 kJ·mol-1.同时从表1中可以看出,DCM比C7H8更容易与电活性离子作用形成更为稳定的配位离子,使得解离出电活性离子比较难,同时高浓度的添加剂的加入也会稀释电活性离子,活性离子的减少在电化学过程中会导致体系的过电位较大,电极反应速率下降,因而DCM的加入可以获得镜面亮泽的铝沉积层[32].
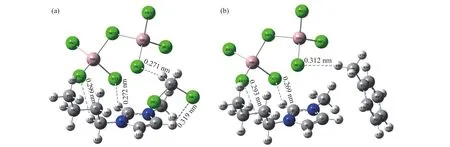
图2 B3LYP/6-311++G(d,p)方法得到的离子液体与添加剂作用的稳定构型. (a)[BMIM]Al2Cl7/DCM;(b)[BMIM]Al2Cl7/C7H8Fig.2 Stable structures of [BMIM]Al2Cl7 with additives and with B3LYP/6-311++G(d,p) method: (a) [BMIM]Al2Cl7/DCM; (b) [BMIM]Al2Cl7/C7H8

表1 B3LYP/6-311++G(d,p)方法得到的体系中各粒子间的相互作用能Table 1 Interaction energy in the system with B3LYP/6-311++G(d,p)method
为进一步考查体系的活性位点,在B3LYP/6-311++G(d,p)下计算了 DCM、C7H8、[BMIM]Al2Cl7、[BMIM]Al2Cl7/M(M=DCM、C7H8)体系的最高占有轨道(Highest occupied molecular orbital, HOMO)的能量EHOMO和最低空轨道(Lowest unoccupied molecular orbital, LUMO)的能量ELUMO,及其能隙差 (ΔE=EHOMO-ELUMO)、偶极矩 (μ)、电负性 (χ)等,结果在表2中给出. 从表2可看出,加入DCM后形成的稳定构型能量最低,DCM导致[BMIM]Al2Cl7体系μ明显减小ΔE增大,反应活性降低,与图2中DCM与阴、阳离子的相互作用能大小相当,容易与其形成弱氢键,进而更易分布在阴阳离子之间使阴阳离子间的相互作用减弱一致. 从表2中可以看出,加入C7H8导致体系偶极矩μ和ΔE减小,电负性χ增大,这表明C7H8的加入使[BMIM]Al2Cl7体系的反应活性增大且得电子能力增加. 这是由于甲苯中甲基的存在使C-C单键上的电子云更偏向苯环一边,导致苯环活化. 结合表2可知,C7H8的ΔE比DCM小,与实验中C7H8和阳离子存在溶剂化效应相一致性[32],因此可以发现体系量化参数的变化与添加剂的性质有很大的关系.

表2 B3LYP/6-311++G(d,p)方法得到的体系的相关量化参数Table 2 Quantitative parameters of the system from B3LYP/6-311++G(d,p) method
为进一步研究DCM和C7H8对体系反应活性位点等的影响,我们利用前线轨道来预测体系中可能发生相互作用的活性区. 图3中给出了[BMIM]Al2Cl7, C7H8, DCM, [BMIM]Al2Cl7/DCM,[BMIM]Al2Cl7/C7H8体系的前线轨道分布图. 对于分子的全局反应活性,从图3(a)中可以看出[BMIM]Al2Cl7的HOMO都分布在阴离子上,这是因为氯原子具有高的电负性,其被亲电攻击时容易失去电子. LUMO主要分布在阳离子的咪唑环上,这是因为咪唑环带正电,其被亲核攻击时容易接受电子,与芳香环两侧的π轨道周围存在循环的电子电流一致. 从图3(b)和(c)中DCM和C7H8的HOMO、LUMO分布可看出它们较活泼. 对比体系中阴阳离子的前线轨道分布知,在铝电沉积体系中它们容易吸附到电极表面,与非惰性电极界面的p轨道或者d轨道形成成键或者反键轨道[42].从图 3(d)和 3(e)中可看出加入 DCM 后,并没有明显改变体系分子前线轨道的分布,LUMO仍集中在咪唑环上,而HOMO集中在DCM和上,体系中优先还原的物质不变. 加入C7H8后改变了体系容易得失电子的位点,体系的HOMO完全集中到了C7H8上,咪唑环上不再有分布. 这说明在混合体系中C7H8比较活泼具有较强的供电子能力,同时由于其活性位点均在环上,所以在电化学过程中C7H8容易以平铺的方式吸附在电极表面的凸出部分,从而改变双电层的结构,抑制电活性铝配离子在该处的沉积,在电沉积过程起到整平的作用,因而实验中可以得到白色扁平的镀层[32]. 由图2和表1的量化计算结果可知,加入C7H8后,它只与阳离子有较强的相互作用,与阴离子相互作用较弱,体系中阴阳离子间的氢键作用也并未明显改变,这与实验中C7H8与[BMIM]+存在溶剂化效应一致[32]. DCM对体系结构的影响大于C7H8,DCM对体系中阴阳离子间相互作用的减弱效果更明显,DCM比C7H8更容易与电活性离子作用,使得解离出电活性离子比较难. 随着添加剂浓度的增加,电活性离子浓度逐渐降低,从而导致电化学过程中过电位较大,电极反应速率下降,进而细化晶粒. 同时DCM和阳离子的相互作用也较强,电化学过程中它们能平铺吸附在电极表面凸出部分起到一定的整平作用. 因而加入DCM可以获得镜面光亮的镀层[32].

图3 B3LYP/6-311++G(d,p)方法得到的前线轨道图. (a)[BMIM]Al2Cl7;(b)C7H8;(c)DCM;(d)[BMIM]Al2Cl7/DCM;(e)[BMIM]Al2Cl7/C7H8Fig.3 Frontier orbital distribution from B3LYP/6-311++G(d,p) method: (a) [BMIM]Al2Cl7; (b) C7H8; (c) DCM; (d) [BMIM]Al2Cl7/DCM; (e) [BMIM]Al2Cl7/DCM
2.2 微观结构和物化性质变化
通过模拟得到[BMIM]Cl的密度为1.101 g·cm-3,实验密度为1.08 g·cm-3[43]. 酸性离子液体[BMIM]Cl/AlCl3(AlCl3摩尔分数为 0.6667),DCM 以及纯 C7H8在298.15 K,0.1 MPa条件下的密度分别为1.3307,1.309 和 0.878 g·m-3,相同条件下的实验值(1.312[44],1.325 和 0.865 g·cm-3[45])符合较好. 表明所采用的[BMIM]Cl/AlCl3体系、DCM以及C7H8的力场可较好的描述各组分间的相互作用,并且能够较准确的预测体系性质.
2.2.1 C7H8和DCM对径向分布函数与配位数的影响
径向分布函数gA-B(r)是表征粒子聚集特征的物理量,它表示在中心原子A附近距离为r的球壳内B原子的分布情况. 图4给出了DCM和C7H8的摩尔分数为0.7时,体系[BMIM]+与与Cl-、[BMIM]+与M(M 为DCM、C7H8)及与M之间的径向分布函数图,其中gA-B(r)中分别采用CR代表[BMIM]+,Al代表代表DCM以及与烷基链接的CA代表C7H8(CR,Al,C3和CA与图1中分子力场定义的原子类型一致). 从图 4(a)和(b)可看出,DCM 和 C7H8均使的径向分布函数的峰值增加,表明两种添加剂均使其相互作用减弱. 其中加入C7H8使体系中与Cl-之间的径向分布函数峰值增加量均比DCM加入后增加的明显,这是由于尺寸效应,C7H8体积较大,加入摩尔分数为0.7的C7H8对体系稀释作用要比DCM更强的原因. 从图4(c)可以看出,[BMIM]+与C7H8的峰值比其与DCM的径向分布函数的第一高峰的出峰位置靠前,表明[BMIM]+与C7H8的相互作用大于其与DCM的相互作用. 由图4(d)可以看出与DCM的径向分布函数出峰位置靠前、峰值较大,而与C7H8径向分布函数的峰肩较宽、峰尖不明显,与表1中粒子间的相互作用能的顺序一致,即DCM与阴阳离子的相互作用能相当,C7H8只与阳离子有较强的相互作用.

图4 MD模拟计算得到体系中离子间的径向分布函数gA-B(r). (a)[BMIM]+与 ;(b)与Cl-;(c)[BMIM]+与M(M=DCM、C7H8);(d)与 M(M=DCM、C7H8)Fig.4 Calculated radial distribution functions gA-B(r) for particle A and B from MD simulation: (a) [BMIM]+-; (b)-Cl-; (c) [BMIM]+-M(M = DCM, C7H8); (d)-M(M = DCM、C7H8)
表3给出了DCM和C7H8的摩尔分数为0.7时,计算得到的与Cl-以及[BMIM]+与的配位数. 从表3 中可看出两种添加剂的加入都减小了阴阳离子间的配位数DCM加入阳离子周围的铝离子数降低最多. 从表3可看出添加剂加入均降低了周围Cl-的配位数,而且DCM引起的降低明显大于C7H8,其数值 0.68与由 AlCl3与Cl-形成电活性离子的理论比值0.5非常接近. 这表明加入DCM比加入C7H8更有利于减弱阴阳离子间的相互作用,体系中铝配离子更倾向于生成,这与实验[31]观测到的随着[BMIM]Cl/DCM体系中AlCl3的摩尔分数增加到0.667时,体系中大幅降低而大幅增加一致. 同时相互作用的减弱,降低了体系的黏度,也使得阴阳离子的移动更为容易,从而导致电导率增加,提升了体系的电化学性质,有利于铝的沉积,与实验结果一致[32].

表3 计算所得体系中主要粒子的配位数Table 3 Calculated coordination number of the main particles in the system
2.2.2 C7H8和DCM对体系空间分布函数的影响

图5 计算得到的三维空间分布图. (a)[BMIM]+周围 Cl-(绿色)、C7H8(黄色)、DCM(红色)、(蓝色)的三维空间分布;(b)周围 Cl-(绿色)、DCM(红色)、C7H8(黄色)空间分布Fig.5 Spatial distribution from simulation: (a) Cl- (green),(blue), DCM (red), and C7H8 (yellow) around the [BMIM]+; (b) Cl-(green), DCM (red), C7H8 (yellow) around
2.2.3 C7H8和DCM对体系离子自扩散系数的影响图6为DCM和C7H8的摩尔分数为0.7时,体系中各粒子的均方根位移(MSD)和自扩散系数的变化. 从图 6(a)~(c)中可看出,在 400~1800 ps内体系中各粒子的均方位移与时间呈线性关系,表明体系各粒子都已达到自由扩散的状态,因此在此段时间内计算得到的体系物理化学性质可靠. 虽然表1中显示的是C7H8与阳离子的相互作用较大,且在图4中也显示出径向分布函数峰值更高,但C7H8使体系密度大幅下降,由表4可知C7H8对体系中与Cl-和[BMIM]+与的配位数影响也较小,即C7H8对体系离子的存在形式影响较小,证实了在体系中C7H8减弱离子间相互作用的方式,与图6中加入C7H8小幅度提高了阴阳离子的扩散系数一致. 当添加剂为DCM时,更倾向分布在阴阳离子之间,明显减弱了阴阳离子间的相互作用,体系中与Cl-以及[BMIM]+与的配位数都有明显的减小,此时体系中铝配离子的存在形式主要为. 从图6也可看出DCM使体系中阴阳离子的扩散能力大幅增加,这有利于提高体系的电化学性质,进而促进铝电沉积,同时DCM扩散较快,易于到达并能平铺吸附在电极表面的凸出部分起到一定的整平作用,从而可得到光亮的铝沉积层[32].

表4 计算得到的303.14 K和0.1 MPa下体系的黏度(η)与电导率(κ)Table 4 Viscosity (η) and conductivity (κ) of the system from MD simulation at 303.14 K and 0.1 MPa
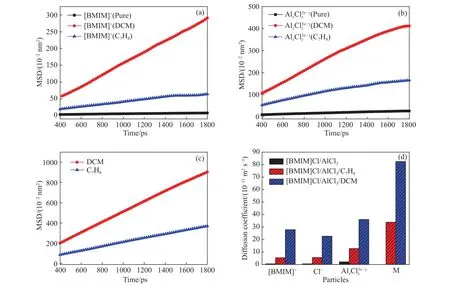
图6 DCM和 C7H8对体系中各粒子均方根位移(MSD)和扩散系数的影响. (a)[BMIM]+的 MSD;(b)的 MSD;(c)DCM和 C7H8的MSD; (d) 各粒子的扩散系数Fig.6 Effects of DCM and C7H8 on the root-mean-square displacement MSD and diffusion coefficient of particles: (a) MSD of [BMIM]+; (b) MSD of; (c) MSD of DCM and C7H8; (d) diffusion coefficient
2.2.4 C7H8和DCM对体系黏度和电导率的影响
表4给出了摩尔分数为0.7的DCM和C7H8对[BMIM]Cl/AlCl3体系黏度和电导率的影响. 模拟得到[BMIM]Cl/AlCl3纯体系在303.14 K,0.1 MPa下的黏度为 115.08 mPa·s,电导率为 2.71 mS·cm-1.从表4可看出加入C7H8和DCM均能引起黏度的大幅降低和电导率的大幅升高,而DCM使体系的黏度下降最大,电导率升高最多. 由前面相互作用能及配位数的分析可知,这是由于DCM比C7H8更有利于减弱阴阳离子间的相互作用,体系中阴、阳离子的扩散增大,从而导致体系黏度降低、电导率增加,同时能使铝配离子更能与周围的氯离子结合形成电活性铝配离子. 结合图6与表4,可以看出在303.14 K下加入摩尔分数为0.7的DCM对[BMIM]Cl/AlCl3体系黏度的降低以及电导率的提高有显著的作用,与实验得到的DCM对体系的电化学性质有显著的促进作用,有利于电沉积[32]的结论一致.
3 结论
(1)卤代烷烃DCM容易与阴、阳离子形成氢键,且相互作用能相当,DCM更倾向于分布在阴阳离子间,使阴阳离子间相互作用变弱、间距增加,而芳香烃C7H8只与阳离子相互作用较强,因此DCM更有利于使体系中自由移动粒子数目增加,对体系的电化学性质有显著的促进作用.
(2)DCM倾向分布于阴阳离子之间,随着DCM的增加不断升高,[BMIM]+与与Cl-间相互作用减弱,进而使离子扩散能力增加、明显降低了体系的黏度、增加了电导率. C7H8主要分布在阳离子周围,减弱阴阳离子间相互作用的能力有限,进而导致对体系电化学性质的促进不如加入DCM好. 分子动力学模拟得到的黏度和电导率与实验测得值符合较好.
(3)C7H8仅仅与阳离子有较大的相互作用,电化学过程中以平铺的方式吸附在电极表面凸出部分起到整平作用,得到白色扁平的镀层. 而DCM与阳离子和铝配离子的相互作用相当,一方面它容易与电活性离子作用使得电活性离子还原较难,同时添加剂浓度较大使得电活性离子浓度降低,导致电化学过程中过电位较大,从而电极反应速率下降,可以起到细化晶粒的作用.同时DCM和阳离子的相互作用也较强,电化学过程中它们能平铺吸附在电极表面凸出部分起到一定的整平作用. 因而DCM的加入可以获得镜面光亮的镀层.

