基于谱效关系的醋延胡索炮制前后特征成分研究
杜伟锋 ,孙海英,洪 浩,朱伟豪,洪智慧,葛卫红*,李昌煜 ,张光霁
1.浙江中医药大学药学院,浙江 杭州 311402
2.浙江中医药大学中药炮制技术研究中心,浙江 杭州 311401
3.浙江省台州医院,浙江 台州 317000
4.浙江中医药大学中医药科学院,浙江 杭州 310053
5.浙江中医药大学基础医学院,浙江 杭州 310053
延胡索为罂粟科紫堇属植物延胡索Corydalis yanhusuoW.T.Wang的干燥块茎,具有活血、行气、止痛功效。临床常用于治疗脘腹疼痛、胸痹心痛、经闭痛经、产后瘀阻等症[1]。现代研究表明,延胡索止痛作用与体内前列腺素、雌二醇等激素分泌水平有关[2-3],其主要有效成分为季胺类和叔胺类生物碱,包括延胡索乙素、去氢紫堇碱、紫堇碱、巴马汀、小檗碱等[4-8]。生延胡索经醋炙后,醋酸与生物碱形成可溶性醋酸盐,有利于煎煮时溶出,疗效增强。目前《中国药典》2020年版规定只有延胡索乙素单一成分含量测定,且延胡索生品和醋延胡索的限度要求一致,难以体现出炮制特色,难以完全满足延胡索饮片的质量控制和评价[9]。因此,开展醋延胡索化学成分与镇痛谱效关系研究,寻找炮制特征成分,建立炮制特色质量标准尤为关键[10-11]。
本实验采用HPLC建立不同批次生延胡索与醋延胡索饮片指纹图谱,确定生醋延胡索共有峰模式;通过建立大鼠扭体法疼痛模型,ig来源于同一批药材的生延胡索与醋延胡索药液,探讨生延胡索与醋延胡索饮片药效;在数据分析的基础上,结合灰色关联度分析法与熵权法研究醋延胡索炮制前后谱效关系[12-13],确定炮制特征成分,为醋延胡索炮制质量控制提供一定依据。
1 仪器与材料
1.1 仪器
U3000高效液相色谱仪,配置包括四元梯度泵、在线真空脱气机、自动进样器、柱温箱、变色龙谱数据工作站,美国Thermo Fisher公司;BIOBASEEL10A博科酶标仪,济南鑫贝西生物技术有限公司;NT-xs105电子分析天平,0.01 mg,瑞士Mettler Toledo公司;华兴HX-T电子秤,杭州三里亭电子秤行;DFD-700电热恒温水浴锅,天津市泰斯特仪器有限公司;TG16-WS台式高速离心机,上海卢湘仪离心机仪器有限公司;MIL-SYN型超纯水仪,美国Milipore公司。
1.2 材料
己烯雌酚(批号100033-201308,质量分数99.5%)、缩宫素(批号150529-200902,质量分数21 IU/支)、戊巴比妥(批号20190517,质量分数3%)、大鼠雌二醇试剂盒、大鼠孕酮试剂盒、大鼠前列腺素F2a(prostaglandin F2a,PGF2a)试剂盒、超氧化物歧化酶(superoxide dismutase,SOD)试剂盒、大鼠前列腺素E2(prostaglandin E2,PGE2)试剂盒、大鼠丙二醛试剂盒均购自上海酶联生物科技有限公司;罗通定片(批号190501)购自广西河丰药业有限责任公司。对照品原阿片碱(质量分数99.6%,批号110853-201805)、盐酸巴马汀(质量分数85.7%,批号110732-201913)、盐酸小檗碱(质量分数86.7%,批号110713-201814)、延胡索乙素(质量分数99.9%,批号110726-201819)均购自中国食品药品检定研究院;对照品四氢小檗碱,质量分数98%,批号190144-201907,购自上海鸿永生物科技有限公司;对照品延胡索甲素(质量分数95%,批号518-69-4)、去氢紫堇碱(质量分数95%,批号30045-16-0)购自上海标准科技有限公司。
生延胡索、醋延胡索均购自中药饮片公司,经浙江中医药大学葛卫红教授鉴定,分别为罂粟科紫堇属植物延胡索C.yanhusuoW.T.Wang的干燥块茎的生品和炮制加工后的醋制品。具体编号及来源见表1。

表1 延胡索样品来源信息Table 1 Information of origin of Corydalis Rhizoma samples
1.3 动物
清洁级SD大鼠,雌性,70只,体质量(200±20)g,来源于浙江中医药大学动物实验研究中心,动物许可证号SYXK(浙)2018-0012。饲养环境:湿度40%~60%、温度20~25 ℃,12 h光亮与12 h黑暗交替。所有动物实验遵循浙江中医药大学动物实验研究中心有关实验动物管理和使用的规定,均符合3R原则。
2 方法与结果
2.1 醋延胡索饮片的制备
生延胡索饮片,淋入米醋(100 kg饮片用米醋20 kg)搅拌均匀,按醋炙法炒制(温度180 ℃,25 kg为1锅,炒15 min),取出晾凉,即得醋延胡索饮片,批号见表1。
2.2 色谱条件
色谱柱为安捷伦Zorbax-Extend-C18(250 mm×4.6 mm,5 um);流动相为0.6%乙酸水溶液(三乙胺调pH值至5.0)-乙腈,梯度洗脱:0~22 min,17%~22%乙腈;22~30 min,22%~30%乙腈;30~50 min,30%~50%乙腈;50~75 min,50%~80%乙腈;体积流量1.0 mL/min;柱温25 ℃;检测波长280 nm。
2.3 溶液的制备
2.3.1 对照品储备液 取原阿片碱、盐酸小檗碱、四氢小檗碱、延胡索乙素、盐酸巴马汀、延胡索甲素、去氢紫堇碱对照品适量,精密称定,分别置于10 mL量瓶中,加甲醇配置成质量浓度分别为1.049、1.179、1.240、1.076、1.158、1.172、1.091 mg/mL的对照品母液,备用。
2.3.2 供试品溶液 取生延胡索、醋延胡索粉末(过三号筛)约0.5 g,精密称定,置平底烧瓶中,精密加入浓氨试液-甲醇(1∶20)混合溶液50 mL,称定质量,冷浸1 h后加热回流1 h,放冷,再称定质量,用浓氨试液-甲醇(1∶20)混合溶液补足减失的质量,摇匀,滤过。精密量取续滤液25 mL,蒸干,残渣加甲醇溶解,转移至5 mL量瓶中,并稀释至刻度,摇匀,用0.45 um微孔滤膜滤过,取续滤液,即得。
2.4 方法学考察
2.4.1 精密度试验 取生延胡索供试品溶液,连续进样6次测定,各色谱峰相对保留时间及相对峰面积RSD≤2%,指纹图谱相似度大于0.998,表明仪器精密度良好,符合实验要求。
2.4.2 重复性试验 取生延胡索粉末,按“2.3.2”项下方法平行制备6份供试品溶液,精密吸取10uL,注入液相色谱仪,各色谱峰相对保留时间及相对峰面积RSD≤2%,相似度≥0.996,重复性良好,符合实验要求。
2.4.3 稳定性试验 取生延胡索供试品溶液,按“2.2”项色谱条件,分别于制备后0、5、10、15、20、25 h进样测定,各色谱峰相对保留时间及相对峰面积RSD≤2%,相似度≥0.997,表明供试品溶液在25 h内稳定,符合实验要求。
2.5 醋延胡索炮制前后比较研究
2.5.1 HPLC指纹图谱的建立 将制备的生延胡索及醋延胡索样品各5批,按“2.3.2”项下方法制备供试品,进液相色谱仪检测,将得到的色谱数据导入“中药色谱指纹图谱相似度评价系统(2012版)”分析[14],以S1为参照图谱,时间窗宽度0.1 min,中位数法进行匹配,记录共有峰色谱峰面积,结果见图1。由图1可知,确定了31个共有峰;结合指纹图相似度评价可知,5批生延胡索HPLC指纹图谱相似度>0.95,5批醋延胡索HPLC指纹图谱相似度>0.96,同时得到了10批样品中31个共有峰的峰面积,见表2。结果表明,生延胡索与醋延胡索总体差异不大,但在常见成分含量上存在差异,通过比较生延胡索与醋延胡索的指纹图谱特征峰,可以有效地比较两者的化学成分变化,控制生延胡索与醋延胡索的质量。
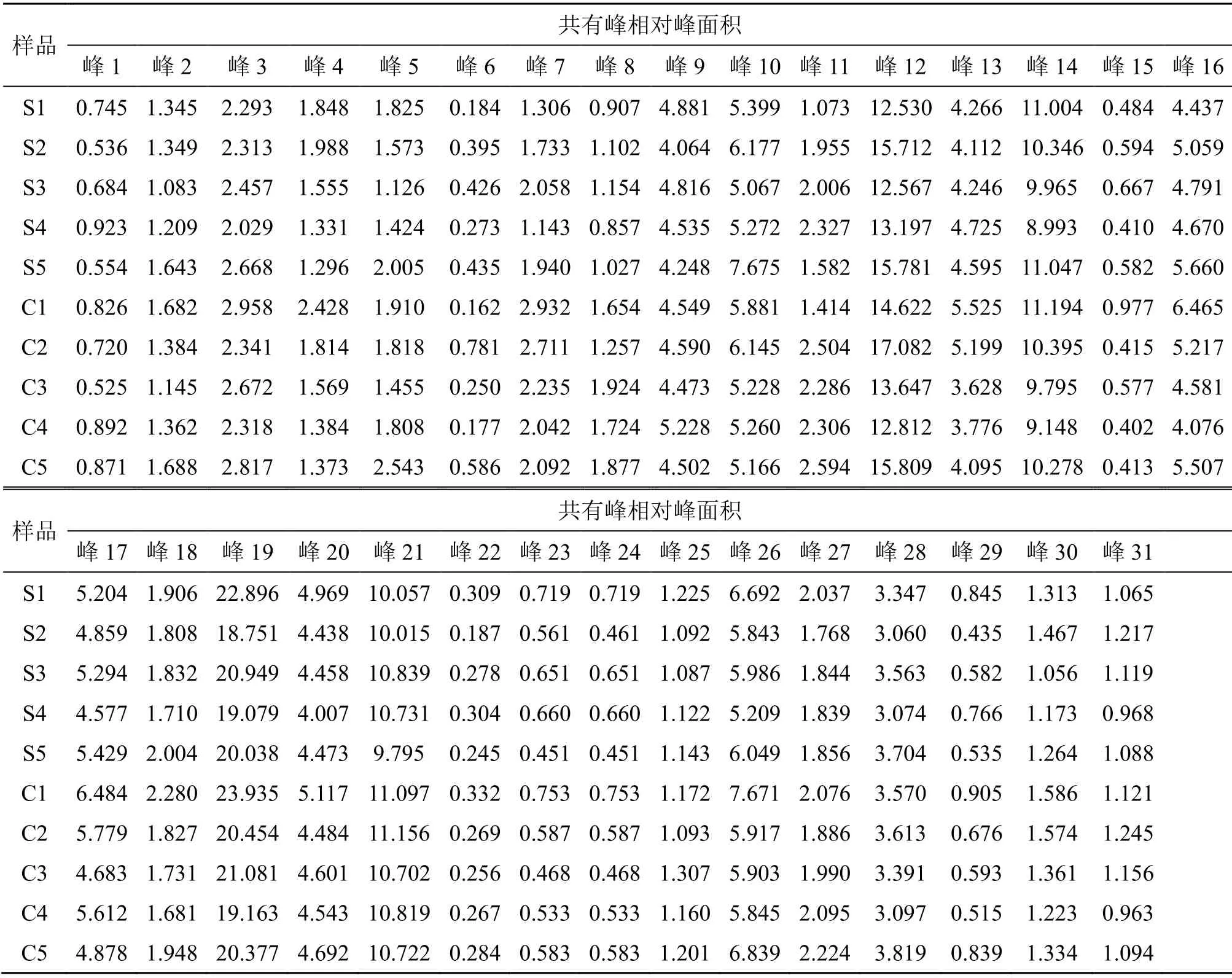
表2 延胡索样品共有峰相对峰面积Table 2 Peak area of common peaks of Corydalis Rhizoma samples

图1 生延胡索 (A)、醋延胡索 (B) HPLC共有指纹图谱 (I) 及其对照指纹图谱 (II)Fig.1 HPLC common fingerprint (I) and its contrast fingerprint (II) of crude Corydalis Rhizoma (A) and vinegar-processed Corydalis Rhizoma (B)
2.5.2 分层聚类分析(hierarchical cluster analysis,HCA) 对10批样品进行HCA,HCA结果如图2所示。生延胡索样品S1~S5明确划分为一个聚类,醋延胡索样品C1~C5明确划分为另一个聚类,证明了HCA是一种快速、简单、准确划分生延胡索与醋延胡索样品的方法,在接下来的药效学实验中,选择的样品来自于生延胡索(S1~S5)与醋延胡索样品(C1~C5)。

图2 10批样品HCAFig.2 HCA of 10 batches of samples
2.5.3 主成分分析(principal component analysis,PCA) PCA结果如图3所示,其中正方形为生延胡索样品,三角形为醋延胡索样品,将31个共有峰的峰面积标准化导入SIMCA14.1进行PCA,模型参数R2X(模型主成分对X变量的解释程度)为0.982,模型预测率(Q2)为0.863。在无监督PCA识别模式下,将延胡索样本自动分为2类。第1类(S1~S5)为生延胡索,分布在I、IV象限;第2类(C1~C5)为醋延胡索,分布在II、III象限。
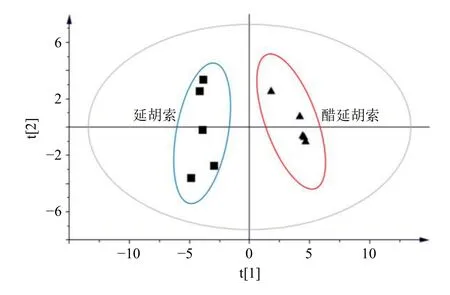
图3 10批样品PCA图Fig.3 PCA diagram of 10 batches of samples
2.5.4 正交偏最小二乘-判别分析(orthogonal least squares-discriminant analysis,OPLS-DA) OPLSDA结果如图4所示,将31个共有峰的峰面积标准化导入SIMCA 14.1进行OPLS-DA,模型预测能力参数Q2为0.988、累积解释能力参数(R2X、R2Y)分别为0.878、0.935,且3者的数值越接近于1,则表示模型拟合效果越好。以变量投影重要性(variable importance projection,VIP)值≥1为筛选指标,得到峰9、18~21、25、26共7个峰对差异贡献度最为显著,因此认为峰9、18~21、25、26为差异贡献量。

图4 10批样品OPLS-DA模型中共有成分的VIP值Fig.4 VIP values of components of OPLS-DA model of 10 batches of samples
2.6 醋延胡索炮制前后镇痛药效比较
2.6.1 药液制备 取己烯雌酚适量,加纯净水溶解,制成0.5 mg/mL的己烯雌酚溶液,备用。
将罗通定片适量,粉碎后用纯净水溶解,制成3 mg/mL的罗通定片溶液,作为阳性药,备用。
称取醋延胡索与生延胡索饮片各600 g,各加入10倍量纯净水浸泡30 min后,煎煮1 h滤过,滤渣再煎煮1 h,合并过滤煎煮液,浓缩至300 mL,得到2 g/mL的延胡索水煎液,备用。
2.6.2 造模、分组及给药 取65只健康雌性SD大鼠按照体重随机分为5组,即空白组(5只)、模型组(5只)、阳性药组(5只)、生延胡索组(25只)和醋延胡索组(25只)。除空白组外,剩余4组大鼠每日ig己烯雌酚2.00 mg/kg 1次,连续12 d;在造模第6天,生延胡索组和醋延胡索组ig相应药液10 g/kg;阳性药组大鼠ig罗通定混悬液30 mg/kg;空白组与模型组ig等体积生理盐水;在造模第12天,末次给药1 h后,给药组大鼠ip缩宫素40 U/kg,空白组ip等体积生理盐水,记录注射缩宫素后30 min内各组大鼠发生扭体反应的数量及扭体次数[15],结果见表3,空白组大鼠未出现扭体反应,模型组大鼠在ip缩宫素后30 min内的扭体发生率为90%,提示动物模型成功建立。与模型组相比,给药组大鼠扭体反应发生率都有所降低,扭体次数减少;其中醋延胡索组与阳性药组扭体次数显著减少;醋延胡索组扭体次数少于生延胡索组,无显著差异。
表3 醋延胡索炮制前后对痛经大鼠扭体反应的影响( )Table 3 Effects of crude and vinegar-processed Corydalis Rhizoma on writhing response of dysmenorrhea rats ( )

表3 醋延胡索炮制前后对痛经大鼠扭体反应的影响( )Table 3 Effects of crude and vinegar-processed Corydalis Rhizoma on writhing response of dysmenorrhea rats ( )
与模型组比较:*P<0.05*P < 0.05 vs model group
组别 n/只 给药剂量/(g·kg-1)扭体发生率/%30 min扭体次数空白 5 / 0 0模型 5 / 90 5.11±1.67阳性药 5 0.03 50 2.01±0.71*生延胡索 25 6 60 2.91±1.21醋延胡索 25 6 50 2.20±0.86*
2.6.3 指标检测 缩宫素注射1 h后,各组大鼠ip戊巴比妥麻醉,使用肝素抗凝管采集腹主动脉血后,在低温离心机中4 ℃、3000 r/min离心5 min,取上清液备用。采用酶联免疫(enzyme-linked immunesorbnent assay,ELISA)法测定大鼠血浆中雌二醇、孕酮、丙二醛水平及SOD活性。
在腹主动脉取血完成后,取出子宫组织,加入生理盐水,于冰浴下制成0.10 g/mL的组织匀浆,在低温离心机中设置4 ℃、3000 r/min离心5 min,取上清液备用。采用ELISA法测定大鼠子宫组织匀浆中PGF2a、PGE2水平。
2.6.4 药效结果比较 将6种药效指标数据导入SPSS统计软件进行分析,组间差异比较用t检验,P<0.05为差异有统计学意义。结果见表4,与空白组大鼠相比,缩宫素诱导的痛经大鼠SOD活性及孕酮、PGE2水平显著降低(P<0.05、0.01),丙二醛、雌二醇、PGF2α含量显著升高(P<0.01),给药后6种指标均有回调,其中醋延胡索组回调效果优于生延胡索组。
表4 醋延胡索炮制前后镇痛实验结果 ( , n = 5)Table 4 Analgesic experiment of crude and vinegar-processed Corydalis Rhizoma ( , n = 5)
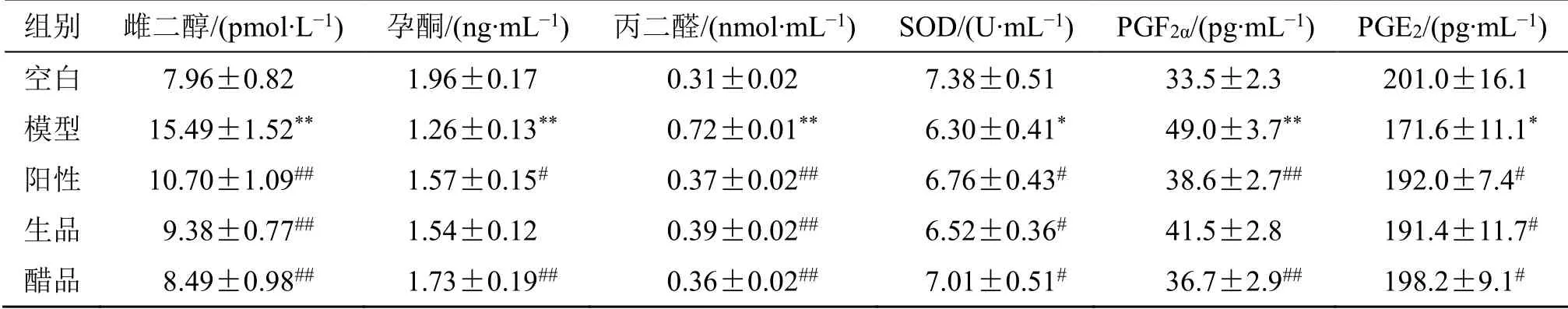
表4 醋延胡索炮制前后镇痛实验结果 ( , n = 5)Table 4 Analgesic experiment of crude and vinegar-processed Corydalis Rhizoma ( , n = 5)
与空白组比较:*P<0.05 **P<0.01;与模型组比较:#P<0.05 ##P<0.01*P < 0.05 **P < 0.01 vs blank group; #P < 0.05 ##P < 0.01 vs model group
组别 雌二醇/(pmol·L-1) 孕酮/(ng·mL-1) 丙二醛/(nmol·mL-1) SOD/(U·mL-1) PGF2α/(pg·mL-1) PGE2/(pg·mL-1)空白 7.96±0.82 1.96±0.17 0.31±0.02 7.38±0.51 33.5±2.3 201.0±16.1模型 15.49±1.52** 1.26±0.13** 0.72±0.01** 6.30±0.41* 49.0±3.7** 171.6±11.1*阳性 10.70±1.09## 1.57±0.15# 0.37±0.02## 6.76±0.43# 38.6±2.7## 192.0±7.4#生品 9.38±0.77## 1.54±0.12 0.39±0.02## 6.52±0.36# 41.5±2.8 191.4±11.7#醋品 8.49±0.98## 1.73±0.19## 0.36±0.02## 7.01±0.51# 36.7±2.9## 198.2±9.1#
2.7 基于灰色关联度法的谱效关系分析
2.7.1 原始数据的无量纲化处理 采用均值法对原数据进行变换。变换的母序列记为{Ym(k)},子序列记为{Yz(k)}。将生、醋延胡索的药效指标作为母序列,生、醋延胡索的共有峰峰面积作为子序列。
2.7.2 关联系数的计算 当t=k时(k为批次编号),母序列记为{Ym(k)},子序列记为{Yz(k)}。按下列公式,计算在t=k时母序列与子序列的关联系数p(k)。
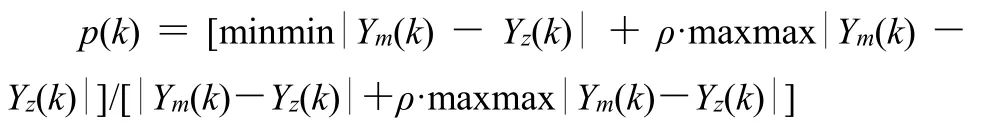
Ym(k)为生、醋延胡索止痛药效指标,Yz(k)为生、醋延胡索的共有峰峰面积归一化后的数值;z为峰号,k为不同批次的编号;ρ为分辨系数,取值范围为0<ρ<1,关系系数之间的差异及区分能力随着ρ的减小而上升,即ρ的取值越小,关系系数之间的差异越大,区分能力越强,通常情况下ρ取0.5;|Ym(k)-Yz(k)|为母序列与子序列差的绝对值,minmin|Ym(k)-Yz(k)|为第 2级最小差,记为 Δmin;maxmax|Ym(k)-Yz(k)|为第2级最大差,记为Δmax
2.7.3 关联度(R)的计算R实质上是对时间序列几何关系的比较,是母序列与子序列各个时刻的关联系数的平均值。

n为子序列的数据个数(即批次)
以指纹图谱中31个共有峰峰面积为子序列,痛经大鼠雌二醇、孕酮、丙二醛、SOD、PGF2α、PGE2含量为母序列,按照“2.7.2”项下的方法进行灰色关联度计算,得到生、醋延胡索各成分与7种药效指标灰色关联度,结果见表5、6。
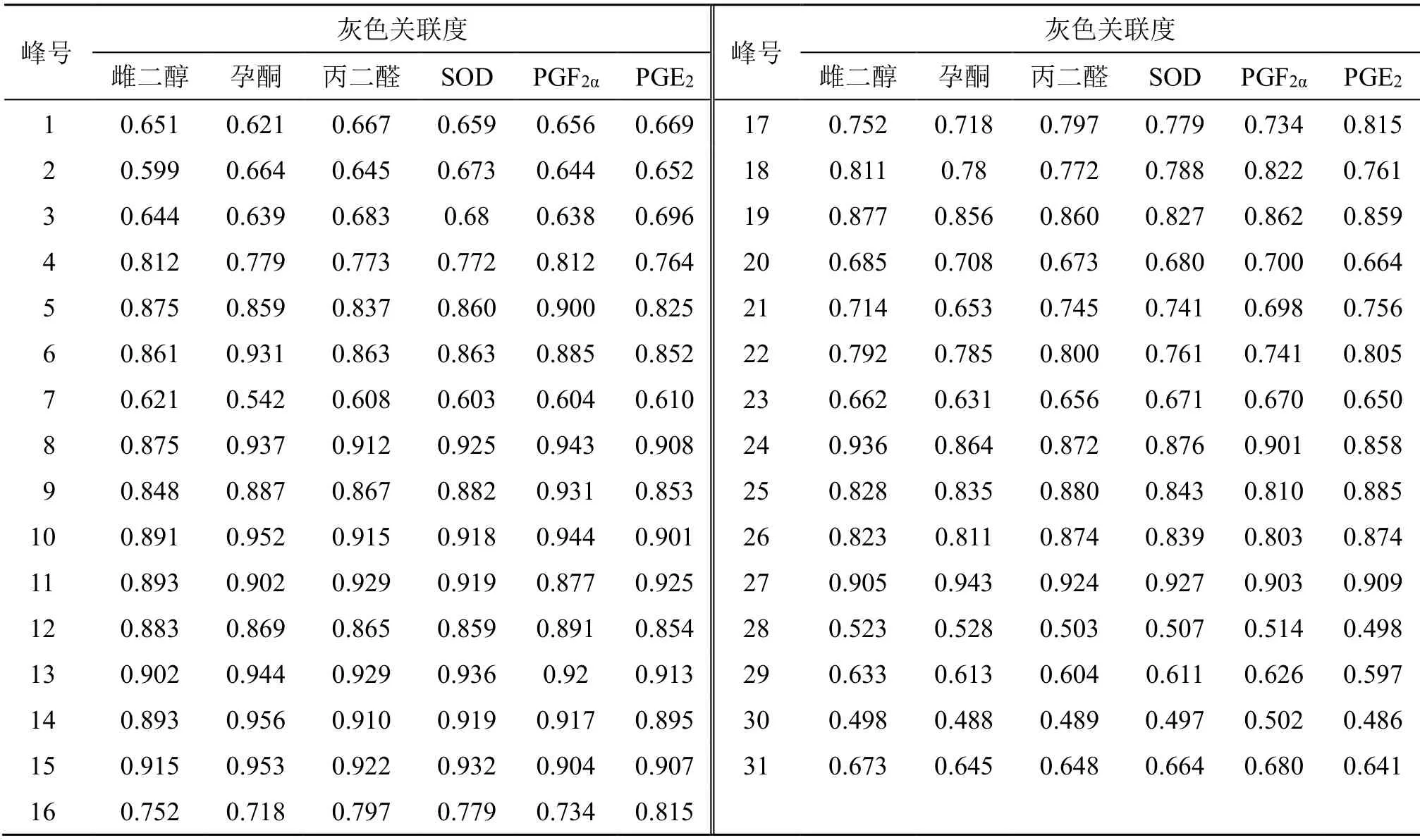
表5 生延胡索成分 (峰号) 与各药效指标灰色关联度Table 5 Grey correlation degree between components (peak numbers) of crude Corydalis Rhizoma and pharmacodynamic indexes
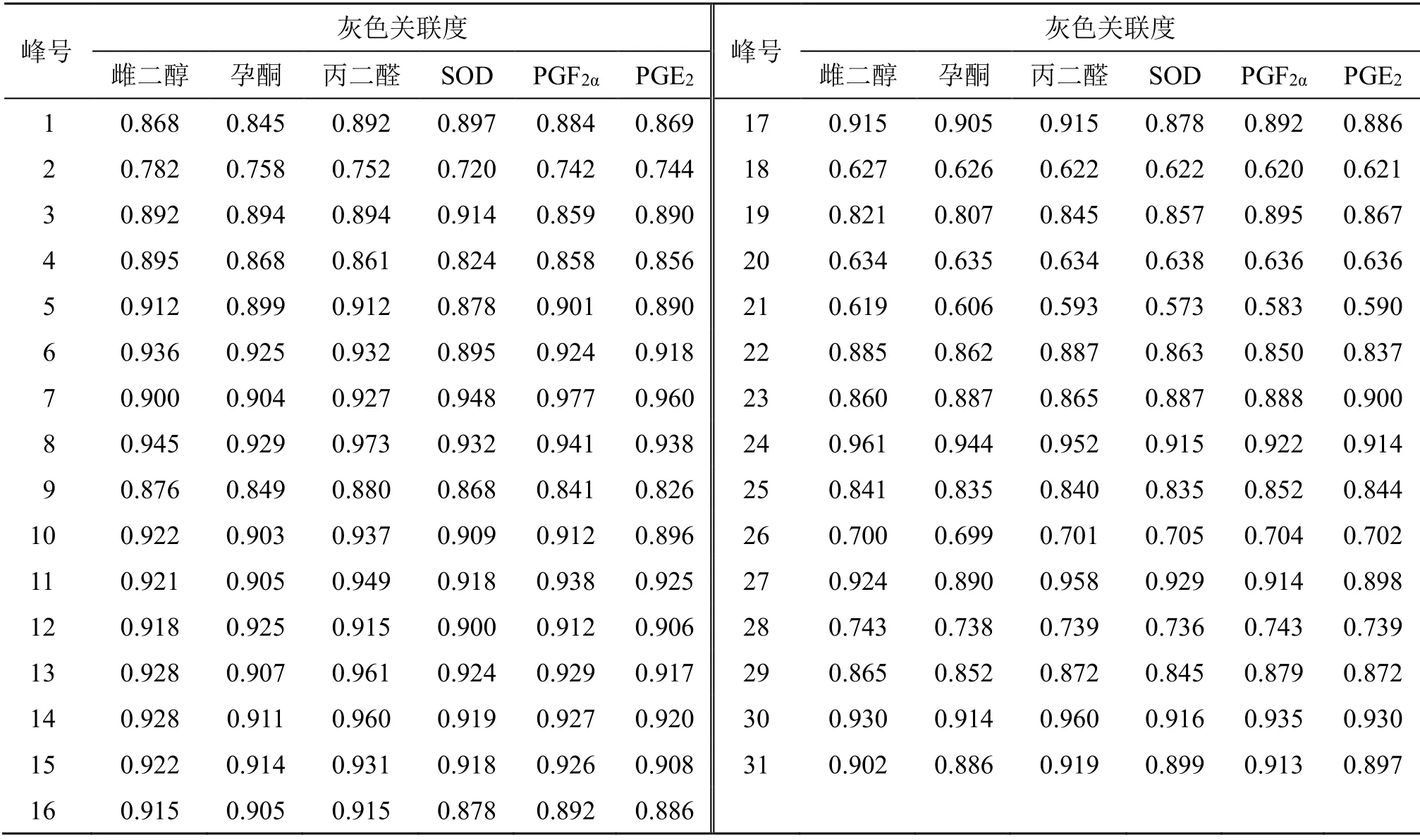
表6 醋延胡索成分 (峰号) 与各药效指标灰色关联度Table 6 Grey correlation degree between components (peak numbers) of vinegar-processed Corydalis Rhizoma and pharmacodynamic indexes
2.8 熵权法计算关联度综合得分
2.8.1 采用极差法按下列公式对关联度数据进行标准化处理。其中正向指标为与药效成正相关的药效指标,负向指标为与药效成负相关的药效指标。i为各色谱峰峰号,j为各药效评价指标的数值。min{Xj}与max{Xj}分别为所有色谱峰中第j项药效指标的最小值和最大值。
2.8.2 计算药效关联度综合得分 首先按下列公式对标准化后的数据计算各色谱峰的各药效指标值的比重(Tij)。
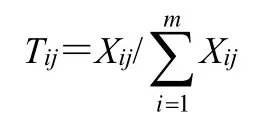
随后计算各指标的信息熵(ej)。
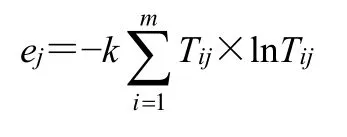
再计算信息熵冗余度(aj)。
aj=1-ej
其次计算各指标权重(Wi)。
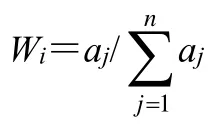
最后得到药效关联度综合得分(Fij)。
Fij=Wi×Xij
m为色谱峰数量,n为药效指标数量
以表5、6灰色关联度为基础,按照熵权法[16]计算,得到各色谱峰与药效指标的关联度得分,并进行排序,结果见表7。结果显示,醋制后,峰9排名上升11位,关联度得分排名第11;峰18排名上升14位、关联度得分排名第2;峰19排名上升12位,关联度得分排8;峰20排名上升7位,关联度排名第3;峰21排名上升10位,关联度排名第1;峰25排名上升11位,关联度得分排第7;峰26排名上升13位,关联度得分排第4。表明醋炙后,该7种成分对醋延胡索药效提升有较大影响,故确定这7种峰为炮制特征成分。经对照品确认,峰9、18~21、25、26分别为原阿片碱、盐酸巴马汀、盐酸小檗碱、去氢紫堇碱、延胡索乙素、四氢小檗碱、延胡索甲素。
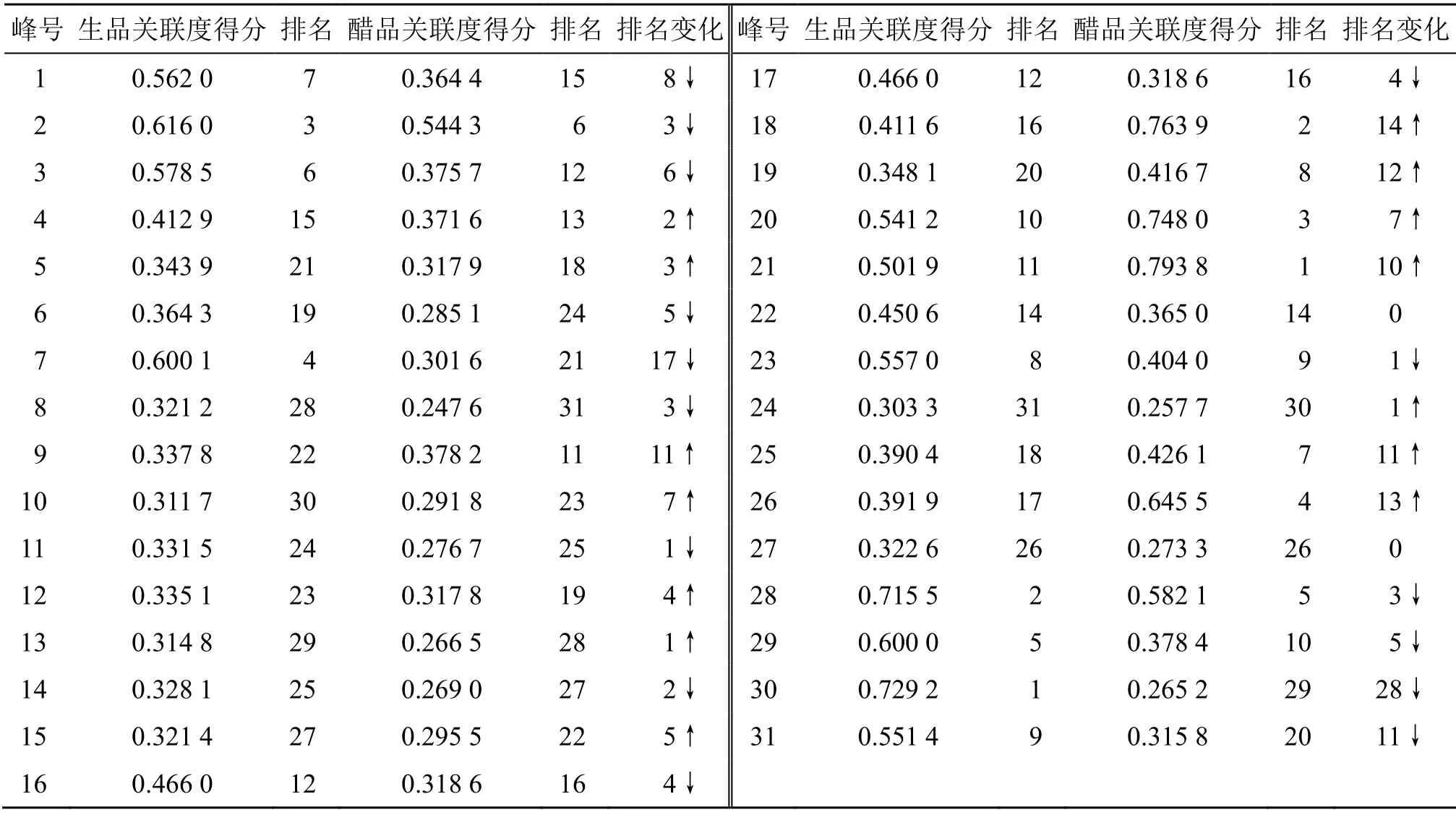
表7 生延胡索与醋延胡索特征成分与药效指标灰色关联度综合得分Table 7 Comprehensive score of grey correlation degree between characteristic components and pharmacodynamic indexes of crude and vinegar-processed Corydalis Rhizoma
3 讨论
延胡索止痛效果显著,中医常常将其作为治疗妇女经闭痛经的首选药物,故动物实验选择痛经模型大鼠作为实验对象开展谱效研究。经文献调研发现动物的痛经模型主要是通过注射缩宫素,刺激子宫平滑肌收缩,以达到模拟原发性痛经的效果[17],因此,在本研究中,通过ig己烯雌酚改善大鼠子宫敏感性后,注射缩宫素诱发子宫痉挛性收缩,结果发现造模成功,与空白组大鼠相比,模型组大鼠出现扭体反应明显,反应发生率高达90%。
而在给药后,大鼠扭体反应次数则显著下降,表明延胡索水提液镇痛效果显著,能极大地缓解大鼠疼痛,醋延胡索组扭体次数低于生延胡索组,提示醋延胡索镇痛作用优于生延胡索。并以SOD、丙二醛、PGE2、PGF2α、雌二醇、孕酮为药效学评价指标[18-20],与空白组大鼠相比,缩宫素诱导的痛经大鼠SOD活性、孕酮水平、PGE2显著降低,丙二醛、雌二醇、PGF2α含量显著升高,给药后6种指标均有显著回调,其中醋延胡索组回调效果优于生延胡索组。从药效指标上可以看出,醋延胡索水煎液止痛效果强于生延胡索,表明醋炙后,某些止痛成分的含量发生了变化,导致药效出现提升。为了更好地探明成分含量变化与药效变化之间的联系,本实验选择谱效关系作为研究方法,结合灰色关联分析手段展开研究。建立了10批延胡索的HPLC指纹图谱,共确定31个共有峰,相似度>0.9,表明各批次饮片质量基本稳定。
通过灰色关联度法对7种药效数据和生、醋延胡索指纹图谱共有峰进行分析,得到各色谱峰关联度,随后采用熵权法计算得到各色谱峰关联度得分,并比较生延胡索与醋延胡索共有峰关联度得分变化情况。结果表明,峰9、18~21、25、26醋炙后关联度得分有了显著的提升,与醋炙后镇痛疗效增加呈正相关。结合对照品比对结果,得出结论:原阿片碱、盐酸巴马汀、盐酸小檗碱、去氢紫堇碱、延胡索乙素、四氢小檗碱、延胡索甲素为醋延胡索炮制特征成分,这为醋延胡索炮制质量控制提供一定依据。
综上所述,本实验通过谱效关系,探究了醋延胡索炮制前后化学成分变化规律,初步明确了7种炮制特征成分,为醋延胡索炮制机制及饮片品质评价标准研究提供参考。
利益冲突所有作者均声明不存在利益冲突

