TiO2/Ni3[Ge2O5](OH)4复合材料的制备及光催化性能
闵 涛,马国华,刘桂君,郑玉婷
(西南科技大学分析测试中心,绵阳 621010)
0 引 言
水资源是人类赖以生存和发展的物质基础,一切人类活动都离不开水,但是随着人口的迅速增长、工农业城市的快速发展,大量的生活垃圾和工业废料直接排入水中,造成水体的严重污染,尤其是染料工业排放的染料废水已经成为重中之重的问题。亚甲基蓝染料是一种重要的噻嗪类阳离子染料,在棉、丝、毛的染色中应用广泛[1-3]。进入眼睛里时,可能对人类和动物的眼睛造成长期损伤[4];在吸入的情况下,会造成短时间的快速心跳[1]。因此,其染料废水的处理都是非常重要的。目前,用于降解染料废水的传统性方法如物理吸附[5]、生物降解[6]等都很难实现对亚甲基蓝的高效率降解。近年来,由于光催化技术方法安全、流程简单、费用低廉且无二次污染产生等特点,运用光催化技术降解染料废水引起了广大学者的关注[7-10]。在利用光催化降解有机污染物中,使用最广泛的光催化材料为TiO2。虽然目前已经合成了许多具有光催化性能的材料如氧化锌、氧化铁、硫化镉等,但因TiO2具有高效率、无毒、低成本等特点,一直没能被取代[11-12]。TiO2的禁带宽度比较大(Eg=3.2 eV), 只能吸收能量较高的紫外线,并且光生电子和空穴复合效率很高,导致光量子的效率低,从而限制了TiO2在实际生产中的应用。然而,近几年越来越多的学者通过选择稳定性好,表面积大,活性高的材料作为基底来负载TiO2制备出具有高催化效率的复合材料从而提高TiO2的响应程度以及光催化效果[13-16]。就目前为止,科研人员普遍通过比较复杂的工艺来制备TiO2复合材料,研究内容主要是将多种光催化材料进行结合或者掺杂其他离子对其进行改性,而对其本身利用效率的提高涉及较少。
在本文实验中,Ni3[Ge2O5](OH)4为六边形纳米盘结构,具有较大的表面积并且带有活性羟基[17],所以通过水热辅助液相沉积法将TiO2分散并结合在Ni3[Ge2O5](OH)4纳米盘上,从而得到TiO2/Ni3[Ge2O5](OH)4纳米复合材料,以亚甲基蓝作为目标污染物,探究TiO2/Ni3[Ge2O5](OH)4纳米复合材料的光催化性能。
1 实 验
1.1 TiO2的制备
水热辅助液相沉积TiO2的合成:量取0.197 9 g氟钛酸铵(≥98%)和0.185 5 g硼酸(≥99.5%)于烧杯中,加入30 mL去离子水超声溶解,将所得溶液倒入45 mL的水热釜中,在烘箱中170 ℃保温3 h,反应得到的产物先用去离子水清洗一遍接着用无水乙醇(≥99.7%)清洗两遍,最后再用去离子水清洗两遍,并在105 ℃的条件下烘干2 h,即可得到纯的TiO2粉末。
1.2 TiO2/Ni3[Ge2O5](OH)4纳米复合材料的制备
分别称取5份0.234 7 g Ni3[Ge2O5](OH)4材料于烧杯中,加入20 mL去离子水进行超声分散,所得悬浊液记为溶液1。分别称取不同量的氟钛酸铵(≥98%)和硼酸(≥99.5%)于烧杯中,其中氟钛酸铵与硼酸的摩尔比为1∶3[18],加入10 mL去离子水超声分散得到溶液2。将溶液1倒入溶液2中,并在磁力搅拌器下搅拌30 min,将混合均匀的溶液倒入45 mL的水热釜中反应。反应条件与合成TiO2粉末一致。最终得到不同包覆量的TiO2/Ni3[Ge2O5](OH)4纳米复合材料,分别记为TN1、TN2、TN3、TN4、TN5,实验条件如表1所示。
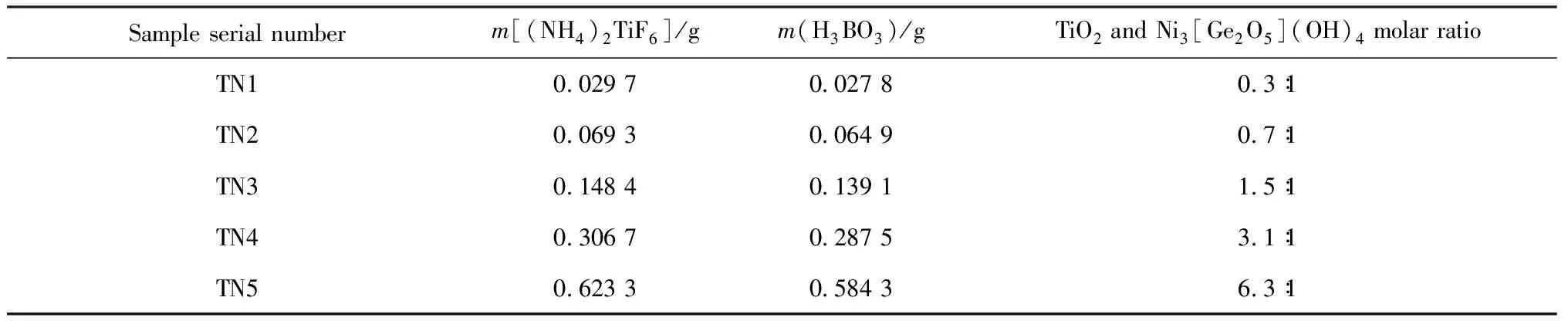
表1 不同量氟钛酸铵制备TiO2/Ni3[Ge2O5](OH)4的实验方案Table 1 Experimental scheme of preparing TiO2/Ni3[Ge2O5](OH)4 with different amounts of ammonium fluorotitanate
1.3 光催化降解性能测试
在室温下,称取TN1、TN2、TN3、TN4、TN5、TiO2各0.1 g,置于200 mL浓度为10 mg/L亚甲基蓝(≥98.5%)溶液中,在避光条件下磁力搅拌30 min以达到吸附平衡,间隔10 min取一次样液,每次取8~9 mL进行高速离心,吸附完成后,接着在光功率为50 W的氙灯照射下,间隔20 min取一次样液,每次取8~9 mL样液进行高速离心。取上清液用UV-3150型紫外-可见-近红外分光光度计在λ=664 nm处测量亚甲基蓝的吸光度A,并根据拟合方程(A=0.189 9C+0.007 8)计算其浓度C,用染料的脱色率D评价催化剂的活性。
(1)
式中:C0为亚甲基蓝的初始浓度,mg/L;Ct为t时刻亚甲基蓝的浓度,mg/L。
2 结果与讨论
2.1 TiO2/Ni3[Ge2O5](OH)4的XRD分析
图1是TiO2、Ni3[Ge2O5](OH)4和TiO2/Ni3[Ge2O5](OH)4的XRD图谱。从TiO2/Ni3[Ge2O5](OH)4衍射图样可以看出在2θ=25.2°、37.8°、47.8°、53.8°、54.8°、62.4°等位置出现锐钛矿型TiO2的特征衍射峰,与标准卡片(JCPDS#21-1272)匹配良好,表明TiO2/Ni3[Ge2O5](OH)4复合材料中的TiO2为锐钛矿型结构。同时,在2θ=12.0°、19.1°、24.1°、33.3°、35.3°、59.3°等处出现的特征衍射峰与Ni3[Ge2O5](OH)4的衍射结果相一致[17]。由此可以说明制备样品为锐钛矿型TiO2与Ni3[Ge2O5](OH)4的复合物。
2.2 TiO2、Ni3[Ge2O5](OH)4和TiO2/Ni3[Ge2O5](OH)4的扫描电镜分析

图1 TiO2、Ni3[Ge2O5](OH)4和 TiO2/Ni3[Ge2O5](OH)4的XRD图谱Fig.1 XRD patterns of TiO2, Ni3[Ge2O5](OH)4 and TiO2/Ni3[Ge2O5](OH)4
在图2中,图2(a)~(h)分别为纯TiO2、Ni3[Ge2O5](OH)4、样品TN1、样品TN2、样品TN3、样品TN4、样品TN5的SEM照片和样品TN4的能谱图。从图中可以看出,通过水热辅助液相沉积法制备的纯二氧化钛颗粒呈现出不规则的形状,有严重的团聚现象。Ni3[Ge2O5](OH)4表现出典型的层状结构,直径约100~300 nm。随着二氧化钛的加入,可以明显地观察到Ni3[Ge2O5](OH)4表面和边缘有二氧化钛附着且样品TN1、TN2、TN3、TN4、TN5的片状样品上分布的颗粒量依次增加,粒径约10~30 nm,这是因为[TiF6]2-水解形成[Ti(OH)6]2-,并与Ni3[Ge2O5](OH)4表面的Ni—OH聚合形成Ni—O—Ti—O[18],可以有效地将TiO2进行分散,防止团聚,从而使TiO2的粒径变小。其中TN1、TN2、TN3、TN4样品中Ni3[Ge2O5](OH)4片上的TiO2颗粒是离散的,TN5样品中Ni3[Ge2O5](OH)4片上的TiO2颗粒有明显团聚。选TN4框选区域进行能谱分析,结果如图2(h)所示。可以看出,TN4样品中有Ni、Ge、O、Ti元素。结合TiO2/Ni3[Ge2O5](OH)4复合材料的制备工艺和扫描电镜及能谱分析结果表明,试验中制备的样品TN1、TN2、TN3、TN4为Ni3[Ge2O5](OH)4片上负载TiO2颗粒,且随TiO2与Ni3[Ge2O5](OH)4摩尔比的增大Ni3[Ge2O5](OH)4片上负载的TiO2颗粒逐渐增多。同时,与相同条件下制备的二氧化钛相比,Ni3[Ge2O5](OH)4片上负载的TiO2颗粒更分散、粒径更小。
2.3 TiO2/Ni3[Ge2O5](OH)4的透射电镜分析
如图3(a)所示,Ni3[Ge2O5](OH)4呈现为六方层状结构,Ni3[Ge2O5](OH)4的片层上分布许多TiO2颗粒,TiO2颗粒均匀分布在Ni3[Ge2O5](OH)4纳米片层和边缘上,经测量,其粒径约10~30 nm。这与扫描电镜的结果相一致。从图3(b)的高分辨结果可以明显看出TiO2颗粒的晶格条纹方向及晶格间距与Ni3[Ge2O5](OH)4明显不同。经测量Ni3[Ge2O5](OH)4晶格间距约为0.72 nm,结合Ni3[Ge2O5](OH)4的晶体结构表明,该面为Ni3[Ge2O5](OH)4的(002)面[17];TiO2晶格间距约为0.35 nm,结合TiO2的晶体结构表明,该面为锐钛矿的(101)面。因为锐钛矿的(101)面是所有晶面中光活性较高的面[19],所以此面具有较高的光利用率。
2.4 TiO2/Ni3[Ge2O5](OH)4的拉曼光谱分析
从图4中可以看出,TiO2/Ni3[Ge2O5](OH)4复合材料的拉曼光谱中在148 cm-1、353 cm-1、395 cm-1、515 cm-1、587 cm-1、637 cm-1、873 cm-1等处存在拉曼散射峰,其中148 cm-1、395 cm-1、515 cm-1、637 cm-1处的拉曼散射峰分别与锐钛矿相的Eg(1)、B1g、A1g、Eg(2)特征振动相对应[19]。表明在Ni3[Ge2O5](OH)4上包覆的TiO2为锐钛矿相。这与XRD测量结果相一致。

图2 不同材料的SEM照片和TN4的能谱图。(a)TiO2;(b)Ni3[Ge2O5](OH)4;(c)TN1;(d)TN2; (e)TN3;(f)TN4; (g)TN5; (h)TN4的能谱图Fig.2 SEM images of different materials and energy spectra of TN4. (a) TiO2; (b) Ni3[Ge2O5](OH)4; (c) TN1; (d) TN2; (e) TN3; (f) TN4; (g) TN5; (h) energy spectrum of TN4

图3 样品TN4的TEM和HTEM照片Fig.3 TEM and HTEM images of the sample TN4
2.5 TiO2和TiO2/Ni3[Ge2O5](OH)4的光催化性能分析
从图5亚甲基蓝的标准曲线中可以看出,亚甲基蓝的5个点浓度C(mg/ L)和吸光度A在 0~10 mg/L范围内具有很好的线性关系。从图6亚甲基蓝的吸收谱图可以看出亚甲基蓝在λ=664 nm时出现最大的吸收峰,所以实验选用λ=664 nm波长处评价亚甲基蓝的光降解率。如表2和图7所示,在避光吸附30 min后,所有光催化剂的吸附已基本达到平衡,保证后续阶段主要由光催化反应起作用。其中TN4的吸附性能最好,30 min亚甲基蓝的吸附率达到51.48%,这有利于后续光催化的进行。TN1、TN2、TN3、TN4、TN5吸附性能均高于TiO2,其主要原因有两点:(1)Ni3[Ge2O5](OH)4提高了TiO2的分散性,使二氧化钛的比表面积和表面能增加;(2)Ni3[Ge2O5](OH)4本身具有一定吸附性。TN1、TN2、TN3、TN4、TN5的吸附性能没有规律性,其原因主要是样品制备时Ni3[Ge2O5](OH)4在去离子水体系中水解,其pH值在7~8之间,而氟钛酸铵和硼酸混合液为弱酸性,两者混合后对Ni3[Ge2O5](OH)4结构有一定破坏,硼酸含量越高对Ni3[Ge2O5](OH)4结构破坏越严重,降低了Ni3[Ge2O5](OH)4的吸附能。同时,随氟钛酸铵和硼酸的增加,样品中Ni3[Ge2O5](OH)4占比降低,TiO2含量增高,TiO2吸附比例提高,两个因素的相互制约造成样品对亚甲基蓝的吸附量依次为:TN4>TN1>TN3>TN2>TN5。

图4 TiO2、Ni3[Ge2O5](OH)4和TiO2/Ni3[Ge2O5](OH)4 拉曼光谱Fig.4 Raman spectra of TiO2, Ni3[Ge2O5](OH)4 and TiO2/Ni3[Ge2O5](OH)4

图5 亚甲基蓝标准曲线图Fig.5 Methylene blue standard curve

表2 TiO2和TiO2/Ni3[Ge2O5](OH)4的吸附性能Table 2 Adsorption properties of TiO2 and TiO2/Ni3[Ge2O5](OH)4
从表3和图7的结果可以看出,所有样品随光照时间增加,亚甲基蓝的光降解率逐渐增加。光催化反应20 min时,各样品对亚甲基蓝的光降解率差别明显;样品TN4的光催化效率最高,光降解率为86.96%,TN1、TN2、TN3、TN5纯TiO2的光降解效率分别为66.22%、66.48%、69.85%、51.8%、74.50%,由此可以得出,当TiO2与Ni3[Ge2O5](OH)4的摩尔比从0.3∶1提升至6.3∶1时,TiO2/Ni3[Ge2O5](OH)4复合材料的光催化效率先升高后降低。光催化反应60 min时,样品对亚甲基蓝光降解率明显上升,所有催化剂的光降解率都已达到95%以上,但只有TN4的光催化效果好于纯TiO2,其主要原因有两点:(1)TiO2/Ni3[Ge2O5](OH)4复合实验在理想条件下,所得TN1、TN2、TN3、TN4、TN5复合材料中二氧化钛的质量分数分别仅为4.86%、10.65%、20.34%、34.54%、51.74%;(2)TiO2与Ni3[Ge2O5](OH)4的摩尔比达到一定值时,二氧化钛会出现团聚,从而使二氧化钛的分散效果降低,导致光催化性能降低。因此,光催化结果表明,TiO2与Ni3[Ge2O5](OH)4的复合有利于提高TiO2的光催化活性,当TiO2与Ni3[Ge2O5](OH)4的摩尔比为3.1∶1时得到的TiO2/Ni3[Ge2O5](OH)4复合材料光催化效果最好,20 min时对亚甲基蓝的光降解率为86.96%,80 min时光降解率为99.81%。
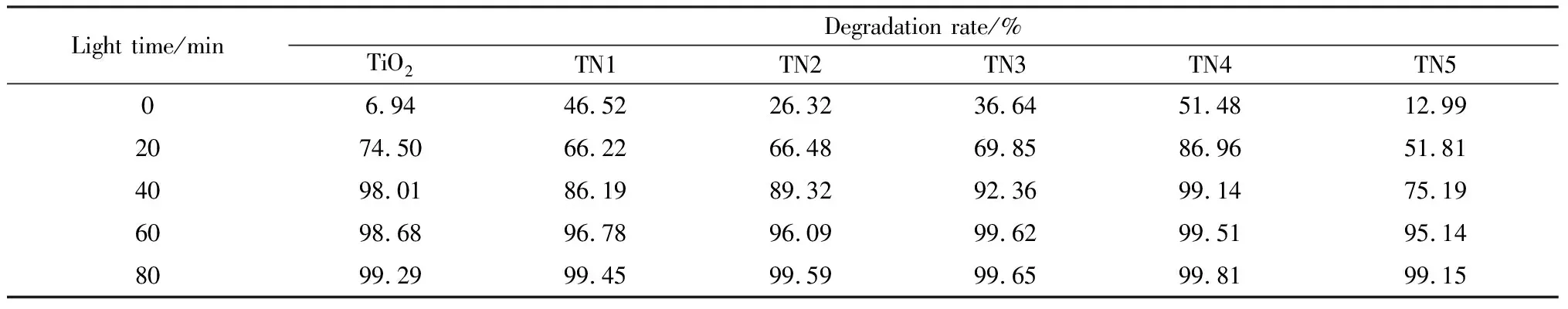
表3 TiO2和TiO2/Ni3[Ge2O5](OH)4的光催化性能Table 3 Photocatalytic performance of TiO2 and TiO2/Ni3[Ge2O5](OH)4

图6 亚甲基蓝光吸收谱图Fig.6 Methylene blue absorption spectrum
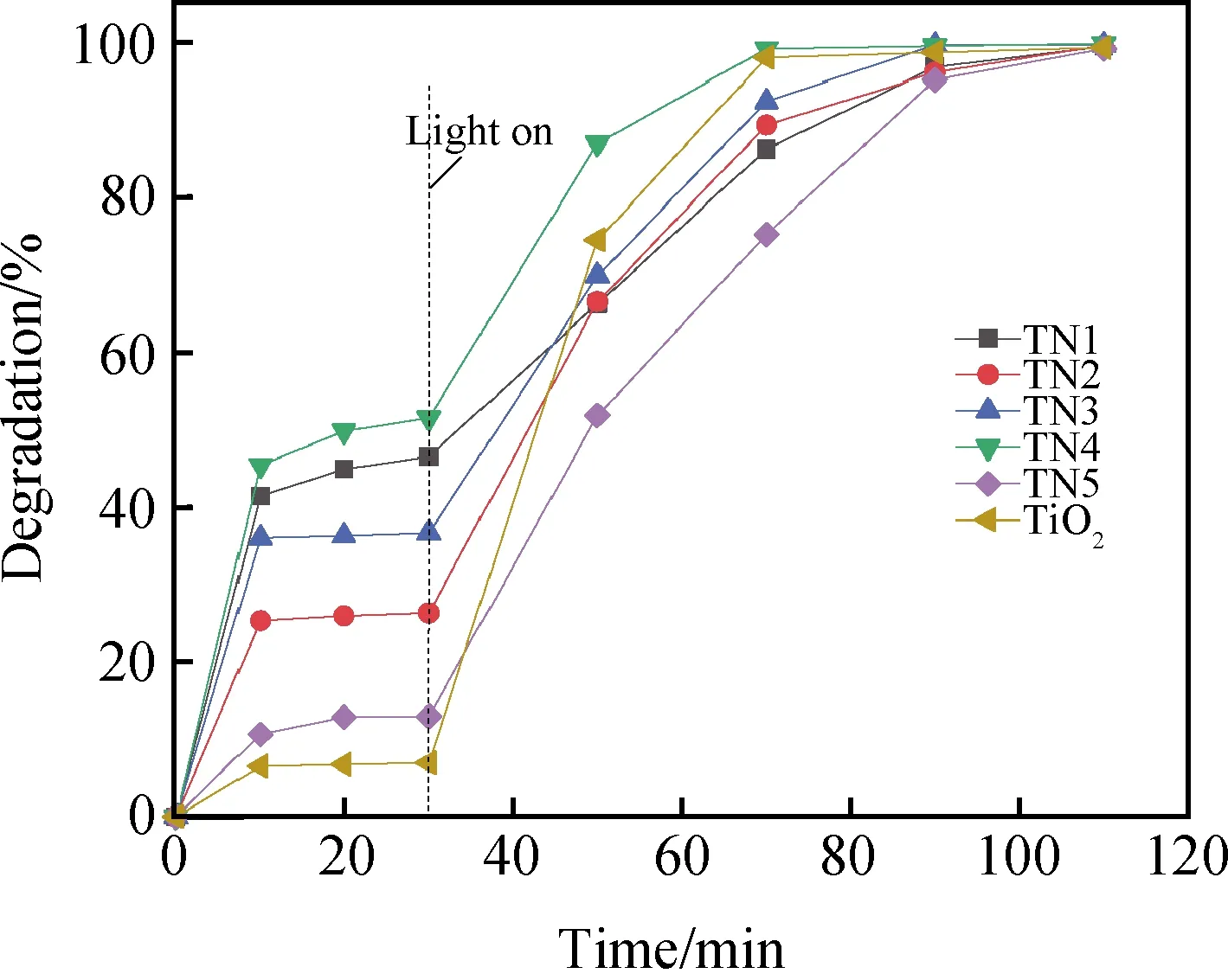
图7 不同催化剂对亚甲基蓝的降解率Fig.7 Degradation rate of methylene blue by different catalysts
2.6 TiO2/Ni3[Ge2O5](OH)4复合材料光催化机理讨论
TiO2/Ni3[Ge2O5](OH)4复合材料的光催化机理主要有三点:
(1)Ni3[Ge2O5](OH)4的吸附作用,由于Ni3[Ge2O5](OH)4为六方层状结构,其比表面积为18.43 m2/g,这种结构有利于纳米TiO2的均匀分散和复合,提高二氧化钛的比表面积和表面能,为光催化反应提供更多的活性点位,进而提高光催化效率;
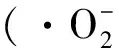
(3)Ni3[Ge2O5](OH)4由Ge—O四面体层和Ni—O(OH)八面体层组成。由文献[20]可知,p-n异质结能够有效抑制光生电子与空穴的复合并提高载流子迁移速率。其中,氧化镍是一种典型的p型半导体材料[21],二氧化钛为n型半导体材料,两者会形成p-n异质结构,导致在二氧化钛上产生的光电子容易偏向氧化镍,从而抑制光生载流子的复合,进而实现更高的光催化率。
3 结 论
(1)以Ni3[Ge2O5](OH)4和氟钛酸铵为原料,通过水热辅助液相沉积法成功制备了TiO2/Ni3[Ge2O5](OH)4复合材料。复合材料实现了锐钛矿相二氧化钛与Ni3[Ge2O5](OH)4的紧密复合与有效分散,且该复合结构能够有效抑制光生载流子的复合,改善材料的吸附性能,进而提高材料的光催化效率。
(2)当TiO2与Ni3[Ge2O5](OH)4的摩尔比为3.1∶1时得到的TiO2/Ni3[Ge2O5](OH)4复合材料对亚甲基蓝的光催化效果最好,20 min对亚甲基蓝的光降解率为86.96%,80 min光降解率为99.81%。

