芦根化学成分及其抗氧化和α-葡萄糖苷酶抑制活性
秦 涛,高祉婧,苏艳芳,张 杰
(天津大学药物科学与技术学院,天津 300072)
芦根为禾本科植物芦苇属芦苇PhragmitescommunisTrin.的干燥根茎,是《中国药典》收载的品种,为常用的药食同源中药,性寒味甘,具有清热生津、除烦、止呕、利尿之功效[1]。临床主要用于治疗发热、支气管炎、尿路感染、止呕等,现代药理学研究表明,芦根具有抗氧化、降血糖、抗肿瘤、保肝等作用[2]。芦根是中医推荐用于治疗新冠肺炎的疏风解毒胶囊的八味组成药材之一[3]。迄今国内外关于芦根的文献集中于其多糖,次生代谢产物的研究鲜有报道,为了进一步阐明芦根的药用物质基础,对芦根醇提物的石油醚、乙酸乙酯和正丁醇萃取部分的化学成分进行分析,共分离得到25个化合物,其中化合物2~11、13~17、20和23~25均为首次从该属和该植物中分离得到,化合物1~4和7具有较强的抗氧化活性,化合物2~4、11和15具有α-葡萄糖苷酶抑制活性。
1 材料
Bruker Avance Ⅲ-400 MHz、600 MHz型核磁共振谱仪(德国Bruker公司);Agilent TOF LC/MS质谱仪(美国Agilent公司);Autopol Ⅱ旋光仪(美国鲁道夫公司);GF254薄层色谱硅胶、柱色谱硅胶(青岛海洋化工厂);聚酰胺(浙江台州路桥四甲生化塑料厂);Sephadex LH-20(美国Amersham Pharmacia公司);ODS 柱色谱硅胶(日本Fuji Silysia公司);D101大孔吸附树脂(天津市海光化工有限公司);ZORBAX SB-C18制备柱、ZORBAX SB-C18分析柱(美国安捷伦公司);Thermo Scientific Multiskan GO 酶标仪(中生华美科技有限公司)。色谱甲醇(天津市康科德科技有限公司);其他试剂均为分析纯。
药材芦根2018年4月采集于河北省保定市白洋淀,由天津中医药大学李天祥教授鉴定为禾本科芦苇属芦苇PhragmitescommunisTrin.的干燥根茎,标本保存在天津大学药物科学与技术学院天然药物化学实验室。
2 提取与分离
干燥的芦根27.1 kg,用95%乙醇冷浸2周,依次用95%乙醇、60%乙醇回流提取2次(每次2 h),得到浸膏4.1 kg,加适量蒸馏水混悬,然后依次用石油醚、乙酸乙酯、正丁醇进行萃取,得石油醚萃取部分(84.0 g)、乙酸乙酯萃取部分(188.0 g)、正丁醇萃取部分(571.0 g)。
取石油醚萃取物(78.0 g),采用硅胶柱分离,石油醚-乙酸乙酯(100∶0~70∶30)梯度洗脱,得到6个部分(Fr.A1~Fr.A6)。将Fr.A2采用硅胶柱分离,以石油醚-丙酮(99∶1)作为洗脱剂,得到13个流分(Fr.a1~Fr.a13)。Fr.a7经过硅胶柱分离,以石油醚-乙酸乙酯(98∶2)作为洗脱剂,共得120个流分(Fr.b1~Fr.b120)。经过硅胶薄层色谱法检识将Fr.b113~Fr.b119与Fr.a8合并,然后通过硅胶柱分离,以石油醚-二氯甲烷(60∶40)作为洗脱剂,再经石油醚纯化后,得到化合物22(7.0 mg)。
取乙酸乙酯萃取物(173.0 g),采用硅胶柱分离,以石油醚-乙酸乙酯-甲醇(100∶0∶0~0∶70∶30)梯度洗脱,得到8个部分(Fr.B1~Fr.B8)。Fr.B3经过硅胶柱分离,以二氯甲烷-乙酸乙酯(100∶0~90∶10)梯度洗脱,得到5个流分(Fr.c1~Fr.c5)。Fr.c1经甲醇重结晶后,得化合物20(3.0 mg)。Fr.c2通过硅胶柱分离,以石油醚-乙酸乙酯(86∶14)作为洗脱剂,再经制备HPLC甲醇-水(30∶70)纯化,得化合物21(5.0 mg)。Fr.c3经二氯甲烷重结晶后,得化合物18(180.0 mg)。Fr.c4经多次Sephadex LH-20柱(甲醇)分离,得化合物11(3.8 mg)、19(4.5 mg)。Fr.c5经二氯甲烷重结晶后,得到化合物12(17.9 mg)。Fr.B4经甲醇重结晶后,得化合物23(70.0 mg)。Fr.B5经丙酮纯化后,得化合物15(27.5 mg)。Fr.B6经硅胶柱分离,以二氯甲烷-甲醇(90∶10)作为洗脱剂,得到4个流分(Fr.d1~d4)。Fr.d1经过制备HPLC甲醇-水(12∶88)纯化,得化合物16(1.5 mg)、17(2.8 mg)。Fr.d2经多次Sephadex LH-20柱(甲醇)分离,得化合物9(2.3 mg)。Fr.d4经多次Sephadex LH-20柱(甲醇)分离,得化合物8(50.0 mg)。Fr.B7通过硅胶柱分离,以二氯甲烷-甲醇(90∶10)作为洗脱剂,再经过多次Sephadex LH-20柱(甲醇)分离,得化合物10(5.0 mg)。
将正丁醇部分分散于水中,过D101大孔吸附树脂柱,依次用水、30%乙醇、95%乙醇进行洗脱,收集各洗脱部分,减压回收,得到水洗脱部分(353.0 g)、30%乙醇洗脱部分(RPB30,54.0 g)、95%乙醇洗脱部分(RPB95,65.0 g)。
取RPB30进行硅胶柱分离,以二氯甲烷-甲醇(9∶1~6∶4)梯度洗脱,得到3个部分(Fr.C1~Fr.C3)。Fr.C1(7.8 g)进行硅胶柱分离,以乙酸乙酯-甲醇(95∶5)作为洗脱剂,得到46个流分(Fr.e1~Fr.e46),合并Fr.e20~Fr.e30(4.0 g)进行ODS反相柱色谱分离(甲醇-水10∶90~0∶100),得到13个流分(Fr.f1~Fr.f13),Fr.f13(220.0 mg)经制备HPLC甲醇-水(30∶70)纯化,得化合物1(35.0 mg)、2(30.0 mg)。Fr.C2(6.5 g)进行Sephadex LH-20柱(甲醇)分离,得到9个流分(Fr.g1~Fr.g9),将Fr.g1~Fr.g3、Fr.e31~Fr.e46与Fr.f3~Fr.f8进行合并(3.3 g),进行ODS反相柱甲醇-水(10∶90~0∶100)分离,得到27个流分(Fr.h1~Fr.h27),Fr.h26(30.0 mg)经制备HPLC甲醇-水(22∶78)纯化,得化合物3(7.0 mg)、4(3.5 mg)。Fr.h11(20.0 mg)经制备HPLC甲醇-水(22∶78)纯化,得化合物5(7.0 mg)、6(2.7 mg)。将Fr.g7~Fr.g9进行合并(890.0 mg),进行聚酰胺柱分离,以二氯甲烷-甲醇(93∶7)作为洗脱剂,得到55个流分Fr.i1~Fr.i55,合并Fr.i18~Fr.i24(240.0 mg),进行Sephadex LH-20柱(甲醇)分离,得到12个流分(Fr.j1~Fr.j12),合并Fr.j9~Fr.j12(30.0 mg),经甲醇重结晶得化合物13(10.0 mg)。将Fr.i35~Fr.i55进行合并(100.0 mg),进行Sephadex LH-20柱(甲醇)分离,得到8个流分(Fr.k1~Fr.k8),合并Fr.k4~Fr.k8(20.0 mg),经甲醇重结晶,然后进行制备HPLC甲醇-水(41∶59)纯化,得化合物14(3.0 mg)。将Fr.g4~Fr.g6进行合并(1.2 g),进行硅胶柱分离,以二氯甲烷-甲醇(86∶14)作为洗脱剂,得34个流分(Fr.l1~Fr.l34),将Fr.l16~Fr.l19进行合样(300.0 mg),进行硅胶柱分离,以乙酸乙酯-甲醇(90∶10)作为洗脱剂,得到20个流分(Fr.m1~Fr.m20),合并Fr.m7~Fr.m8,得化合物24(105.0 mg)。Fr.C3(2.0 g)进行硅胶柱分离,以乙酸乙酯-甲醇(99∶1)作为洗脱剂,得到63个流分 (Fr.n1~Fr.n63),合并Fr.n56~Fr.n63(130.0 mg),经制备HPLC甲醇-水(40∶60)纯化,得化合物7(17.0 mg)。合并Fr.n26~Fr.n54(1.0 g),经丙酮重结晶,得化合物25(200.0 mg)。
3 结构鉴定

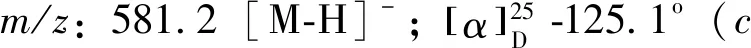
化合物3:白色粉末,紫外吸收254 nm有吸收,365 nm没有吸收,提示可能是木脂素苷类化合物,ESI-MSm/z:581.2[M-H]-。1H-NMR (600 MHz,CD3OD)δ:6.57 (1H,s,H-6),6.38 (2H,s,H-2′,6′),4.30 (1H,d,J=6.0 Hz,H-7′),4.24 (1H,d,J=7.9 Hz,H-1″),3.94 (1H,dd,J=10.0,5.8 Hz,H-9b),3.86 (1H,dd,J=11.9,1.8 Hz,H-6″b),3.85 (3H,s,5-OCH3),3.74 (6H,s,3′,5′-OCH3),3.65 (1H,dd,J=11.9,5.4 Hz,H-6″a),3.52~3.58 (3H,m,H-9a,H-9′),3.32 (3H,s,3-OCH3),3.24~3.36 (3H,m,H-3″,4″,5″),3.17 (1H,dd,J=8.4,7.5 Hz,H-2″),2.78 (1H,dd,J=15.3,4.4 Hz,H-7b),2.57 (1H,dd,J=15.1,11.6 Hz,H-7a),1.88 (1H,m,H-8′),1.84 (1H,m,H-8);13C-NMR (150 MHz,CD3OD)δ:149.0 (C-3′,5′),148.6 (C-5),147.7 (C-3),140.1 (C-4′),139.6 (C-4),134.6 (C-1′),130.1 (C-1),126.5 (C-2),107.7 (C-6),107.0 (C-2′,6′),104.6 (C-1″),78.1 (C-3″),78.0 (C-5″),75.2 (C-2″),74.9 (C-9),71.7 (C-4″),63.3 (C-9′),62.8 (C-6″),60.0 (3-OCH3),56.8 (3′,5′-OCH3),56.6 (5-OCH3),50.1 (C-8′),42.7 (C-7′),38.2 (C-8),34.0 (C-7)。以上数据与文献[5]报道基本一致,故鉴定为(-)-南烛木树脂酚9-O-β-D-葡萄吡喃糖苷。
化合物4:白色粉末,紫外吸收254 nm有吸收,365 nm没有吸收,提示可能是木脂素苷类化合物,ESI-MSm/z:581.2[M-H]-。1H-NMR (600 MHz,CD3OD)δ:6.57 (1H,s,H-6),6.42 (2H,s,H-2′,6′),4.60 (1H,d,J=4.6 Hz,H-7′),4.31 (1H,d,J=7.8 Hz,H-1″),3.85 (3H,s,5-OCH3),3.81~3.89 (2H,m,H-6″b,H-9′b),3.74 (6H,s,3′,5′-OCH3),3.65 (1H,dd,J=12.0,5.7 Hz,H-6″a),3.60 (1H,dd,J=11.5,5.1 Hz,H-9b),3.52 (1H,dd,J=11.5,5.9 Hz,H-9a),3.48 (1H,dd,J=10.0,5.8 Hz,H-9′a),3.22 (3H,s,3-OCH3),3.21~3.39 (4H,m,H-2″,3″,4″,5″),2.96 (1H,dd,J=16.9,5.5 Hz,H-7b),2.71 (1H,dd,J=16.9,11.5 Hz,H-7a),2.13 (1H,m,H-8′),2.00 (1H,m,H-8);13C-NMR (150 MHz,CD3OD)δ:149.1 (C-5),148.5 (C-3′,5′),146.6 (C-3),138.6 (C-4),135.1 (C-4′),134.9 (C-1′),128.1 (C-1),127.2 (C-2),109.5 (C-2′,6′),107.6 (C-6),104.7 (C-1″),78.3 (C-3″),78.1 (C-5″),75.5 (C-2″),72.0 (C-4″),71.5 (C-9′),65.2 (C-9),63.3 (C-6″),60.0 (3-OCH3),57.0 (3′,5′-OCH3),56.5 (5-OCH3),42.1 (C-8′),41.9 (C-7′),35.3 (C-8),34.0 (C-7)。以上数据与文献[6]报道基本一致,故鉴定为(-)-7′-表-南烛木树脂酚9′-O-β-D-葡萄吡喃糖苷。
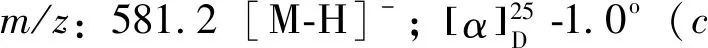

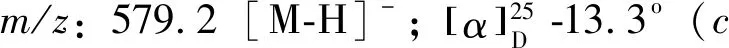
化合物8:浅黄色固体,ESI-MSm/z:417.1[M-H]-。1H-NMR (600 MHz,DMSO-d6)δ:8.20 (1H,d,J=8.9 Hz,H-6′),7.88 (1H,d,J=15.3 Hz,H-β),7.87 (2H,d,J=8.8 Hz,H-2,6),7.77 (1H,d,J=15.3 Hz,H-α),7.09 (2H,d,J=8.8 Hz,H-3,5),6.41 (1H,dd,J=8.9,2.3 Hz,H-5′),6.28 (1H,d,J=2.3 Hz,H-3′),5.37 (1H,d,J=4.9 Hz,2″-OH),5.28 (1H,d,J=7.3 Hz,H-1″),5.14 (1H,d,J=4.6 Hz,3″-OH),5.07 (1H,d,J=5.3 Hz,4″-OH),4.61 (1H,t,J=5.8 Hz,6″-OH),3.70 (1H,m,H-6″b),3.46 (1H,m,H-6″a),3.40 (1H,m,H-5″),3.28 (1H,m,H-3″),3.26 (1H,m,H-2″),3.17 (1H,m,H-4″);13C-NMR (150 MHz,DMSO-d6)δ:191.4 (C=O),166.1 (C-4′),165.8 (C-2′),159.4 (C-4),143.5 (C-β),133.0 (C-6′),130.7 (C-2,6),128.3 (C-1),119.1 (C-α),116.5 (C-3,5),113.0 (C-1′),108.2 (C-5′),103.0 (C-3′),99.9 (C-1″),77.1 (C-3″),76.6 (C-5″),73.2 (C-2″),69.7 (C-4″),60.7 (C-6″)。以上数据与文献[9]报道基本一致,故鉴定为异甘草苷。

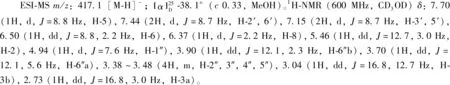
化合物11:黄色固体,ESI-MSm/z:337.1[M-H]-。1H-NMR (600 MHz,CD3OD)δ:7.98 (1H,d,J=15.6 Hz,H-β),7.94 (2H,d,J=8.8 Hz,H-2′,6′),7.56 (1H,d,J=15.6 Hz,H-α),7.50 (1H,s,H-6),6.89 (2H,d,J=8.8 Hz,H-3′,5′),6.47 (1H,s,H-3),6.26 (1H,dd,J=17.8,10.3 Hz,H-2″),5.00 (2H,m,H-3″),3.89 (3H,s,-OCH3),1.49 (6H,s,-CH3×2);13C-NMR (150 MHz,CD3OD)δ:191.9 (C=O),163.5 (C-4′),161.5 (C-4),160.6 (C-2),149.1 (C-2″),142.3 (C-β),132.1 (C-1′),131.6 (C-2′,6′),130.2 (C-6),128.5 (C-5),119.4 (C-α),116.4 (C-3′,5′),115.8 (C-1),110.7 (C-3″),100.9 (C-3),56.1 (OCH3),41.1 (C-1″),27.5 (C-4″,5″)。以上数据与文献[12]报道基本一致,故鉴定为甘草查尔酮 A。
化合物12:浅黄色固体,在365 nm下呈暗紫色荧光,FeCl3乙醇显蓝色斑点,硫酸乙醇显黄色斑点,根据以上结果初步判断是黄酮类化合物,ESI-MSm/z:329.1[M-H]-。1H- NMR (600 MHz,DMSO-d6)δ:7.33 (2H,s,H-2′,6′),6.98 (1H,s,H-3),6.56 (1H,d,J=2.0 Hz,H-8),6.20 (1H,d,J=2.0 Hz,H-6),3.88 (6H,s,-OCH3×2)。以上数据与文献[13]报道基本一致,故鉴定为小麦黄素。
化合物13:浅黄色粉末,ESI-MSm/z:637.2[M-H]-。1H-NMR (600 MHz,DMSO-d6)δ:12.50 (1H,s,12-OH),7.36 (2H,s,H-2′,6′),7.05 (1H,s,H-3),6.86 (1H,d,J=1.9 Hz,H-8),6.48 (1H,d,J=1.9 Hz,H-6),5.08 (1H,d,J=7.5 Hz,H-1″),4.54 (1H,brs,H-1‴),3.89 (6H,s,3′,5′-OCH3),1.07 (3H,d,J=6.3 Hz,5‴-CH3);13C-NMR (150 MHz,DMSO-d6)δ:182.3 (C-4),164.6 (C-2),163.2 (C-7),161.5 (C-9),157.2 (C-5),148.6 (C-3′,5′),140.8 (C-4′),120.4 (C-1′),105.7 (C-10),104.9 (C-2′,6′),104.1 (C-3),100.8 (C-1″),100.2 (C-1‴),99.7 (C-6),95.6 (C-8),76.6 (C-3″),75.9 (C-5″),73.4 (C-4‴),72.4 (C-2″),71.0 (C-2‴),70.6 (C-3‴),69.9 (C-4″),68.6 (C-5‴),66.3 (C-6″),56.7 (3′,5′-OCH3),18.0 (C-6‴)。以上数据与文献[14]报道基本一致,故鉴定为苜蓿素-7-O-芸香糖苷。
化合物14:浅黄色粉末,ESI-MSm/z:637.2[M-H]-。1H-NMR (600 MHz,DMSO-d6)δ:12.95 (1H,s,5-OH),7.34 (2H,s,H-2′,6′),7.01 (1H,s,H-3),6.87 (1H,brs,H-8),6.37 (1H,brs,H-6),5.20 (1H,d,J=7.5 Hz,H-1″),5.12 (1H,s,H-1‴),3.89 (6H,s,3′,5′-OCH3),1.20 (3H,d,J=6.3 Hz,5‴-CH3);13C-NMR (150 MHz,DMSO-d6)δ:182.3 (C-4),164.6 (C-2),163.2 (C-7),161.5 (C-9),157.2 (C-5),148.6 (C-3′,5′),140.5 (C-4′),120.5 (C-1′),105.7 (C-10),104.9 (C-2′,6′),104.1 (C-3),100.8 (C-1‴),100.2 (C-1″),99.7 (C-6),95.6 (C-8),77.2 (C-5″),77.2 (C-2″),76.5 (C-3″),71.9 (C-4″),70.5 (C-4‴),70.4 (C-3‴),69.8 (C-2‴),68.3 (C-5‴),60.6 (C-6″),57.3 (3′,5′-OCH3),18.0 (C-6‴)。以上数据与文献[14]报道基本一致,故鉴定为苜蓿素-7-O-新橙皮糖苷。
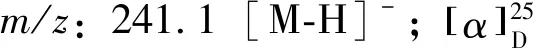

化合物18:浅黄色结晶,ESI-MSm/z:163.0[M-H]-。1H-NMR (600 MHz,CD3OD)δ:7.60 (1H,d,J=15.9 Hz,H-7),7.44 (2H,d,J=8.6 Hz,H-2,6),6.81 (2H,d,J=8.6 Hz,H-3,5),6.28 (1H,d,J=15.9 Hz,H-8)。以上数据与文献[19]报道基本一致,故鉴定为对羟基桂皮酸。
化合物19:白色结晶,ESI-MSm/z:193.1[M-H]-。1H-NMR (600 MHz,CD3OD)δ:7.60 (1H,d,J=15.9 Hz,H-7),7.18 (1H,d,J=1.9 Hz,H-2),7.06 (1H,dd,J=8.2,1.9 Hz,H-6),6.81 (1H,d,J=8.2 Hz,H-5),6.31 (1H,d,J=15.9 Hz,H-8),3.90 (3H,s,OCH3)。以上数据与文献[19]报道基本一致,故鉴定为反式阿魏酸。
化合物20:浅粉色结晶,ESI-MSm/z:271.1[M-H]-。1H-NMR (600 MHz,CDCl3)δ:7.02 (2H,d,J=1.9 Hz,H-2,2′),7.00 (2H,dd,J=8.2,1.9 Hz,H-6,6′),6.90 (2H,d,J=8.2 Hz,H-5,5′),6.88 (2H,s,H-7,7′),5.62 (2H,s,OH),3.95 (6H,s,OCH3);13C-NMR (150 MHz,CDCl3)δ:146.9 (C-3,3′),145.5 (C-4,4′),130.5 (C-1,1′),126.7 (C-7,7′),120.3 (C-6,6′),114.7 (C-5,5′),108.3 (C-2,2′),56.1 (OCH3)。以上数据与文献[20]报道基本一致,故鉴定为(E)-3,3′-二甲氧基-4,4′-二羟基二苯乙烯。
化合物21:浅黄色固体,ESI-MSm/z:181.1[M-H]-。1H-NMR (600 MHz,CDCl3)δ:9.82 (1H,s,CHO),7.16 (2H,s,Ar-H),6.03 (1H,s,OH),3.98 (6H,s,OCH3×2)。以上数据与文献[21]报道基本一致,故鉴定为丁香醛。


化合物24:白色粉末,ESI-MSm/z:179.1[M-H]-。1H-NMR (600 MHz,CD3OD)δ:4.09 (1H,m,H-3),4.09 (1H,m,H-4),4.06 (1H,m,H-5′),4.06 (1H,m,H-6′a),3.92 (1H,m,H-4′),3.87 (1H,m,H-5),3.87 (1H,m,H-6a),3.82 (1H,m,H-3′),3.74 (1H,m,H-1′a),3.74 (1H,m,H-6′b),3.70 (1H,m,H-6b),3.68 (1H,m,H-1a),3.67 (1H,m,H-1′b),3.65 (1H,m,H-1b);13C-NMR (150 MHz,CD3OD)δ:103.2 (C-2),99.2 (C-2′),83.3 (C-5),77.9 (C-4),77.6 (C-3),71.8 (C-4′),71.2 (C-5′),69.5 (C-3′),66.0 (C-1′),64.6 (C-6′),64.5 (C-6),64.2 (C-1)。以上数据与文献[24]报道基本一致,故鉴定为果糖。
化合物25:白色粉末,ESI-MSm/z:235.1[M-H]-。1H-NMR (600 MHz,D2O)δ:4.02 (1H,brs,H-3′),3.95 (2H,s,H-4′,5′),3.87 (1H,d,J=12.6 Hz,H-6′b),3.82 (2H,d,J=1.7 Hz,H-1′a,1′b),3.75 (1H,dd,J=12.6,1.7 Hz,H-6′a),3.55 (2H,m,H-1),1.59 (2H,m,H-2),1.40 (2H,m,H-3),0.94 (3H,t,H-4);13C-NMR (150 MHz,D2O)δ:100.5 (C-2′),69.7 (C-4′),69.2 (C-5′),68.4 (C-3′),63.9 (C-6′),61.4 (C-1′),60.8 (C-1),34.4 (C-2),18.8 (C-3),13.2 (C-4)。以上数据与文献[25]报道基本一致,故鉴定为正丁基-O-β-D-吡喃果糖苷。
4 抗氧化活性筛选
参考文献[26],采用DPPH自由基清除试验,对分离得到的化合物进行抗氧化活性测定并计算半数抑制浓度(IC50)值,以维生素C为阳性对照。10个化合物显示出一定程度的抗氧化活性,见表1,化合物1~4、7表现出较强的抗氧化活性,其IC50值低于阳性对照维生素C。
5 α-葡萄糖苷酶抑制活性试验筛选
参考文献[27],采用PNPG法对分离得到的化合物进行α-葡萄糖苷酶抑制活性测定并计算IC50
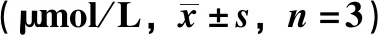
表1 抗氧化活性试验IC50值Tab.1 IC50 values in antioxidant activities tests
值,以阿卡波糖为阳性对照。5个化合物显示出一定程度的α-葡萄糖苷酶抑制活性,见表2,化合物2~4和11表现出较强的α-葡萄糖苷酶抑制活性,其中化合物11的活性最强,其IC50值为180.42 μmol/L。
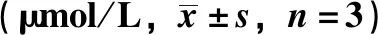
表2 α-葡萄糖苷酶抑制活性试验IC50值Tab.2 IC50 values in α-glucosidase inhibitory activities
6 讨论
本实验从芦根(干)分离鉴定了25个化合物,主要包括木脂素苷类、黄酮类及苯丙素类等成分,其中化合物2~11、13~17、20和23~25均为首次从该植物、该属植物中分离得到。体外生物活性测试结果表明,木脂素苷类、黄酮类、苯丙素类成分具有不同程度的抗氧化活性和α-葡萄糖苷酶抑制活性,其中木脂素苷类成分的含量高,种类多,也表现出强的抗氧化活性和α-葡萄糖苷酶抑制活性。本研究为阐明芦根抗氧化和降血糖作用的物质基础,寻找具有抗氧化活性和降血糖活性的化学成分以及芦根的进一步研究开发提供了科学依据。

