盐酸法钛白粉新工艺副产氯化亚铁制备四氧化三铁
胡骆兴,黄齐茂,2,屈泓佑
(1.武汉工程大学化工与制药学院绿色化工过程教育部重点实验室,湖北武汉430073;2.国家磷资源开发利用工程技术研究中心,湖北武汉 430074)
酸浸法生产钛白粉在中国已有半个多世纪的研 究历史,但是由于整个生产流程还存在着诸多有待改进的地方,至今规模生产企业极少[1]。研究表明,中国钛白粉生产行业面临的主要问题包括酸浸前处理流程复杂、能耗大、浸出率低以及生产过程中危废导致的高污染等问题[2-3]。已有学者对钛白粉行业副产物的处理进行过大量研究,但是对副产固废硫酸亚铁[4-5]和氯化亚铁[6-7]的处理研究,多数还处于实验室小试阶段,大规模的工业化生产还存在很多问题,难以实现产业化。
四氧化三铁磁材料是一种功能材料,在磁记录材料、磁流体的基本材料和磁性颜料等领域被广泛应用[8-10]。磁性四氧化三铁材料由于其良好的吸附性,在废水处理领域也发挥了较好的效果[11-13]。制备四氧化三铁包括制备纳米级四氧化三铁[14-15]和制备四氧化三铁磁粉[16],但是在相关文献报道中对比发现,制备四氧化三铁的方法大多数只处于小试阶段,达到千克级别的实验都很少,主要原因是因为在制备四氧化三铁的过程中,量的增大或者浓度的增高会导致在氧化过程中形成胶体包裹亚铁阻碍其氧化,从而导致放大实验难以成功,只能处于低浓度小试级别,难以实现工业化生产。
黄齐茂等[17]公开了一种通过钛精矿与浓盐酸直接制得钛白粉的方法,加入结晶改良剂,在140 ℃高温高压下以浓盐酸酸解钛精矿,冷却过滤可直接获取钛白粉。该方法解决了酸浸前处理流程复杂、能耗高、浸出率低等问题,但是该方法会伴随大量固体氯化亚铁副产物产生,每生产1 t钛白粉将产生1.5~2.0 t的氯化亚铁危废,不但会污染环境,还导致该工艺路线的经济损失。
为此,本文以盐酸法酸浸钛精矿制备钛白粉新工艺中产生的大量氯化亚铁废料为原料,氧化钙作为pH调整剂,加入分散剂(自制,见文献[18]中的分散剂)破坏氧化过程中形成的胶体来辅助氧化,同时优化工艺条件,将副产废料氯化亚铁制成四氧化三铁磁粉,达到了50 L级别的放大,实现了资源的综合利用。
1 实验部分
1.1 实验原料及设备
原料:四水合氯化亚铁晶体,盐酸法钛白粉新工艺副产氯化亚铁;氧化钙,分析纯;氨水,分析纯;稀盐酸,盐酸法钛白粉新工艺回收废稀盐酸;分散剂,自制。
设备:集热式恒温加热磁力搅拌器,型号DF-101S;真空抽滤泵,型号VP30;空气压缩机,型号OTS-800;电热鼓风干燥箱,型号101-3AB;电子天平,型号AR124CN。
1.2 实验工艺流程及方法
在盐酸法钛白粉新工艺中,酸浸步骤会产生大量含氯化亚铁废液,采用低温冷冻使氯化亚铁晶体析出,氯化亚铁晶体通过离心分离得到,加入去离子水配制成氯化亚铁溶液;加入氧化钙使溶液呈弱碱性同时与氯化亚铁反应生成氢氧化亚铁;通入空气使其氧化成氢氧化铁,同时加入分散剂辅助氧化;氧化完成后的氢氧化铁与一定比例的氢氧化亚铁充分混合,以氨水和稀盐酸调节pH为6~8;进行正压过滤分离,得到的滤饼经过烘干、研磨等处理得到产品四氧化三铁磁粉。
1.3 实验内容
1.3.1 氢氧化亚铁的制备
釜A(20 L):取盐酸法钛白粉新工艺中酸浸步骤的滤出液,通过冷冻分离得到氯化亚铁晶体6 kg,加入去离子水6 kg配制成氯化亚铁溶液,浓度为4.5~5.5 mol/L。按与其物质的量比为1∶1加入氧化钙粉末1.7 kg,充分搅拌均匀后制得氢氧化亚铁,密封保存防止氧化。

1.3.2 氢氧化铁的制备
釜B(50 L):冷冻分离得到氯化亚铁晶体12 kg,加入去离子水12 kg配制成氯化亚铁溶液,浓度为4.5~5.5 mol/L。按与其物质的量比为1∶1加入氧化钙粉末3.4 kg,加入分散剂0.5 kg,同时从溶液底部通入空气氧化,加热搅拌直至氧化完全(溶液为棕褐色),制得氢氧化铁。
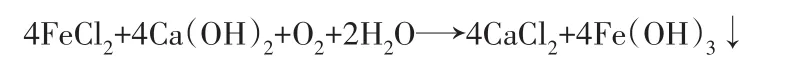
1.3.3 磁铁粉的制备
将釜A中氢氧化亚铁加入釜B中,充分搅拌混合,以氨水和稀盐酸调节pH,混合均匀后采用正压压滤分离,分离后的滤饼放入烘箱中干燥,最后经过研磨等后处理得到黑色的具有磁性的四氧化三铁磁铁粉。

2 反应条件优化
2.1 分散剂投料量
在制备四氧化三铁过程中,反应物投量的增大或者浓度的增加会导致在氧化过程中形成胶体包裹亚铁阻碍其氧化,从而导致放大实验难以成功。因此在进行50 kg级别放大反应时,在其氧化过程中加入分散剂辅助氧化避免胶体包裹抑制氧化。
控制反应条件:氧化温度为80 ℃、氧化钙及分散剂加料时间间隔为1.5 h、氧化时间为8.5 h、固液分离pH为6.5,设计分散剂加入量(制备氢氧化铁步骤中分散剂占氯化亚铁投量的分数)为1%、2%、3%、4%、5%、6%的对照实验。图1为分散剂加入量不同时所得四氧化三铁磁粉的产率。由图1可知,随着分散剂投加量增加,四氧化三铁磁粉的产率逐渐升高,说明在50 kg级别反应中分散剂的加入有效地促进了制备氢氧化铁过程中的氧化过程,在分散剂加入量为制备氢氧化铁步骤中氯化亚铁投量的2%~3%时,分散剂的促进作用随着投量的加大逐渐增加,在分散剂投量达到4%时,对氧化过程的促进作用达到最大值,此时四氧化三铁磁粉的产率达到97%以上。

图1 分散剂投量对四氧化三铁磁粉产率的影响Fig.1 Influence of dispersant dosage on yield of Fe3O4 magnet powder
在此分散剂投量下对反应温度、氧化钙及分散剂加料时间间隔、氧化时间、固液分离pH等影响因素进行单元优化。
2.2 反应温度优化
在氢氧化铁的制备过程中,首先探究反应温度对亚铁离子氧化效率的影响。在其他条件一定时,控制在不同温度下通入空气对亚铁离子进行氧化,以求得一个最佳温度,既能达到理想产率,又能尽可能地减少能耗。
控制反应条件:氧化钙及分散剂加料时间间隔为1.5 h、氧化时间为8.5 h、固液分离pH为6.5,设计氧化温度梯度为60、65、70、75、80、85、90 ℃的对照试验。图2为不同氧化温度下所得到的四氧化三铁磁粉产率。由图2可知,在70 ℃之前,温度对溶液中亚铁离子的氧化速率影响较大,随着反应温度的升高,溶液中的离子与氧原子碰撞更加剧烈,亚铁离子氧化速率逐渐加快;在温度达到70 ℃时,亚铁离子氧化速率增大趋势明显变缓;在温度达到80~85 ℃时达到最大值,此时亚铁离子氧化速率达到最快,且随着温度的继续增加,亚铁离子氧化速率几乎趋于恒定值。故在尽可能减少能耗的前提下,选择氧化温度为80 ℃。

图2 反应温度对四氧化三铁磁粉产率的影响Fig.2 Influence of reaction temperature on yield of Fe3O4 magnet powder
2.3 氧化钙及分散剂加入时间间隔优化
氧化钙及分散剂加入量由反应式按比例配置。在进行50 kg放大反应的过程中,加入氧化钙后溶液中会形成亚铁沉淀胶体减缓亚铁离子氧化速度,因此控制氧化钙及分散剂加入的速度,才能保证溶液中亚铁氧化完全。在制备氢氧化铁阶段采用分4次加入氧化钙及分散剂的方法,每加料一次后,保持一定的时间间隔来进行氧化,保证溶液中亚铁的氧化速率。
控制反应条件:氧化温度为80 ℃、氧化时间为8.5 h、固液分离pH为6.5,设计氧化钙加入时间梯度为0.5、1.0、1.5、2.0、2.5 h的对照试验。图3为加入氧化钙时间间隔从0 h到2.5 h时所得到的四氧化三铁磁粉产率。由图3可知,随着加料时间间隔的增加,亚铁在加料间隙氧化的时间变长,导致磁铁粉的产率随着加入氧化钙及分散剂时间间隔的增加而增大。在时间间隔小于1 h时所得产品产率较低,且暴露在空气中一段时间后变为黄褐色,该现象产生的原因是在反应量级过大时亚铁氧化不完全,产品中存在未被氧化的氢氧化亚铁,在空气中氧化后变为黄褐色的氢氧化铁;加料时间间隔大于1 h的产品显黑色,后处理过后呈黑色粉末状,其主要成分为四氧化三铁磁粉,其产率呈上升趋势;加料时间间隔超过1.5 h时,四氧化三铁磁粉的产率趋于稳定值,此时所得产品为具有磁性的黑色四氧化三铁粉末,故将加入氧化钙及分散剂的时间间隔确定为1.5 h。

图3 时间间隔对四氧化三铁磁粉产率的影响Fig.3 Influence of time interval on yield of Fe3O4 magnet powder
2.4 氧化时间优化
在确定氧化钙加入的时间间隔后,进一步探究加料以后的氧化时间对产品产率的影响。因为在加料过程中氧化已经开始,氧化时间从加料前开始计时(从6 h起),在不影响产品质量及产率的条件下,尽量缩短加料后的氧化时间。
控制反应条件:氧化温度为80 ℃、氧化钙加料时间间隔为1.5 h、固液分离pH为6.5,设计氧化时间(包括加料氧化钙的时间)梯度为6.0、6.5、7.0、7.5、8.0、8.5、9.0 h的对照试验。图4为氧化时间(包括加料氧化钙的时间)对四氧化三铁磁粉产率的影响。由图4可知,在氧化时间(包括加料氧化钙的时间)为6 h时,即加完氧化钙以后直接结束氧化,此时四氧化三铁磁粉产率较低,亚铁氧化不完全,还需继续通入空气进行氧化。随着后续氧化时间的增加,亚铁氧化趋于完全,在氧化时间(包括加料氧化钙的时间)为8.5 h时达到峰值。超过8.5 h后反而起到负作用导致收率开始下滑,故将亚铁的氧化时间(包括加料氧化钙的时间)定为8.5 h。

图4 氧化时间对四氧化三铁磁粉产率的影响Fig.4 Influence of oxidation time on yield of Fe3O4 magnet powder
2.5 固液分离前pH优化
在氢氧化铁与氢氧化亚铁悬浊液混合后,需要对溶液的pH进行调节。选用稀盐酸和氨水来调节溶液pH,因为氯离子的加入不会带来新的杂质,且少量氨在后处理步骤中以气体形式挥发。控制加料时间间隔和氧化时间都在最佳条件下,探究分离之前溶液的pH对最后产品的影响。
控制反应条件:氧化温度为80 ℃、氧化钙及分散剂加料时间间隔为1.5 h、氧化时间为8.5 h,设计固液分离前溶液pH为3、4、5、6、7、8的对照试验。pH对四氧化三铁磁粉产率的影响如图5所示。由图5可知,混合溶液固液分离前溶液的pH对最后产品的影响较大,当溶液pH较小时,此时溶液为酸性,仍存在一部分氢氧化亚铁和氢氧化铁无法分离出来,导致最后四氧化三铁磁粉的产率较低;随着pH增加到6.5~7.0,溶液趋于中性,氢氧化亚铁和氢氧化铁逐渐沉淀完全,此时四氧化三铁磁粉的产率也达到最大值;但是当pH继续增加时,最终产率有下降趋势,且在产品中观察到有白色的氧化钙析出,是因为当溶液为弱碱性时会有部分氢氧化钙伴随沉淀分离出来,导致最终产率降低且有氧化钙析出,故将分离前溶液的pH确定为6.5~7.0。

图5 pH对四氧化三铁磁粉产率的影响Fig.5 Influence of pH on yield of Fe3O4 magnet powder
3 放大实验及产品检测
在优化条件下进行50 kg级别放大实验,采用双釜分开反应。釜A中投料量:氯化亚铁晶体6 kg,水6 kg,氧化钙1.7 kg。釜B中投料量:氯化亚铁晶体12 kg,水12 kg,氧化钙3.4 kg,分散剂0.5 kg。待釜B中氧化结束后,将釜A中物料加入釜B中并搅拌均匀,以氨水和盐酸调节pH,最后正压分离、烘干、研磨得到约6.8 kg的四氧化三铁磁粉产品。
将得到的四氧化三铁产品进行SEM分析,得到的SEM照片如图6所示。由图6可知,所得四氧化三铁产品呈球状聚集体,粒子大小不均一,直径为50~200 nm。

图6 四氧化三铁SEM照片Fig.6 SEM image of Fe3O4
4 结论
对盐酸法钛白粉新工艺中产生的大量氯化亚铁副产物进行利用,经过绿色的简单工艺步骤,将没有经济价值的副产物变成有一定经济价值的新产品四氧化三铁磁粉,变废为宝,进一步完善了盐酸法钛白粉新工艺。
对本工艺进行50 kg级别放大实验,成功制得四氧化三铁产品,产率高。通过加入分散剂破坏氧化过程中形成的胶体,解决了高投料量、高浓度级别反应中胶体包裹抑制氧化的问题,突破了制备四氧化三铁只能处于实验室小试阶段的难题。
本实验采用氧化钙沉淀氧化法以及加入分散剂辅助氧化的方法,以副产物氯化亚铁制备四氧化三铁磁铁粉,优化条件:分散剂投加量为4%、氧化温度为80 ℃、氧化钙及分散剂加料时间间隔为1.5 h、氧化时间为8.5 h、固液分离pH为6.5。在优化条件下进行50 kg级别放大实验,成功制得产品四氧化三铁磁粉,产率达到97%以上。

