NdFeB 磁体表面环保型Zn-Al 涂层的盐雾腐蚀行为
胡娜,谢发勤,吴向清,李淑良,黄科超,贺栋栋,鲁闯
(1.西北工业大学 民航学院,西安 710072;2.宁波职业技术学院,浙江 宁波 315800)
由于NdFeB 磁体具有优异的磁性能,极高的磁能积和矫顽力,性价比高,被广泛应用于电池的驱动材料、医疗设备、现代工业、新能源汽车、航空航天等领域[1-3]。但各相间电位差大,易在潮湿、高温、有氢的环境中腐蚀粉化,导致磁性能下降,彻底失效,严重限制了磁体应用领域的拓展。
目前,提高NdFeB 磁体的耐蚀性能有2 种方法:一种是添加合金元素,能够提高磁体耐蚀性,但提高不显著,并且会破坏磁体[4-6];另一种是在磁体表面制备防护层[7-11],比如电镀、化学镀、达克罗涂层。其中,电镀、化学镀成本低,但是严重污染环境,危害人体健康,成本高;而达克罗涂层具有优良的耐腐蚀特性和力学特性,但含有高致癌和污染环境的物质Cr6+。随着全球范围内对铬的管控越来越严,在未来,达克罗涂层必然会被无铬Zn-Al 涂层代替[12]。
Zn-Al 涂层(又名无铬达克罗),是一种兼具环保性和实用性的防污耐腐蚀强的涂层[13-15]。Tanaka等[16]研究发现,钢上的Zn-Al 合金涂层发生大气腐蚀,产生了由ZHS 和Zn-Al-LDH 组成的颗粒择优取向,形成了致密锈层,进一步抑制了钢的腐蚀。Gou等[17]采用电化学试验和浸泡试验研究发现,当3-glycidoxypropyl-trimethoxy(3–缩水甘油醚氧基丙基甲基二乙氧基硅烷)和methyltrimethoxysilane(甲基三甲氧基硅烷)的混合比为1 时,制备的无铬锌铝涂层在5%(质量分数)NaCl 溶液中的浸泡时间可达58 d。Hu 等[18]采用电化学阻抗谱(EIS)和交流电位测量发现,CFD/steel 在腐蚀前,涂层的保护作用仅在前3 d 保持活性,然后物理屏蔽功能起主导作用。目前,针对Zn-Al 涂层的相关文献多数是关于在钢、铝合金等基体表面通过电镀、磁控溅射等方法的制备技术研究,极少有NdFeB 磁体表面制备Zn-Al 涂层在盐雾环境中腐蚀行为研究的相关报道[19-22]。本文旨在研究NdFeB 磁体表面Zn-Al 涂层在中性盐雾环境中的腐蚀行为,从而为提高NdFeB 磁体的耐腐蚀性,评价环保型Zn-Al 涂层防护性能,预测涂层使用寿命和分析涂层失效机制提供理论依据。
1 试验
1.1 基体前处理
烧结NdFeB 磁体由宁波金科磁业有限公司提供。基体试样规格为φ10 mm×47 mm。经过打磨,除油、除锈,用去离子水冲洗后,自然风干。
1.2 涂料制备
本文Zn-Al 涂料配方分为A、B、C、D 组分,A组分为片状Zn 粉、片状Al 粉、分散剂、KH560、去离子水、乳化剂;B 组分为KH560、甲醇、去离子水;C 组分为磷钼酸钠、去离子水;D 组分为增稠剂、去离子水。Zn 粉和Al 粉在整个涂料中共占35%,其中Zn 粉和Al 粉的质量比为6∶1。按比例称量所述A、B、C、D 组分中的各种物料,并按照一定的顺序混合搅拌均匀后得到Zn-Al 涂料。
1.3 涂层制备
将经过前处理的NdFeB 磁体试样放入搅拌中的Zn-Al 涂料中,静置20~30 s。取出后再静置1 min,直到NdFeB 磁体试样表面的Zn-Al 涂料均匀流平,且没有Zn-Al 涂料滴落。然后放入烘箱100 ℃预热15 min,300 ℃固化30 min,完成制备Zn-Al 涂层的涂覆、预热、固化过程。然后取出,自然或者人工加速冷却后,重复所述涂覆、预热、固化过程3 遍,得到Zn-Al 涂层。
1.4 性能测试
在自然光条件下,目测观察Zn-Al 涂层表面呈现银灰色,涂层宏观上均匀平整,无麻点、剥落、裂纹等缺陷。用ZEISS Gemini 500 场发射扫描电镜观察Zn-Al 涂层的微观形貌,并用其配套的能谱仪(EDS)分析元素的组成及含量。用岛津多晶XRD-7000 型衍射仪对Zn-Al 涂层进行物相分析。用TY9000 拉曼光谱仪对Zn-Al 涂层进行成分分析。用Nicolet iS50 Thermo Fisher/赛默飞世尔傅里叶变换红外光谱仪分析Zn-Al 涂层的有机官能团,光谱的范围为4 000~400 cm-1。根据GB/T 5270—2005,采用划格法和胶带试验法相结合,检测Zn-Al 涂层与基体的结合强度。采用RK2683AN 型四探针电阻率仪测量干态条件下Zn-Al 涂层的电阻率。
依据GB/T 2423.17 的规定,采用y/Q-250 湿热盐雾试验箱进行盐雾试验。试验持续时间为48、168、336、672、1 126 h。
采用普林斯顿公司生产的PARSTAT-2273 电化学工作站,测量涂层的电化学性能。极化曲线扫描速率为0.5 mV/s,起始电位为-0.3 V,终止电位为0.3 V。阻抗频率范围为10 mHz~100 MHz,正弦波激励信号幅值为 5 mV,从高频到低频扫描,扫描速率为2 mV/s,正向扫描至电流达到10–2A/cm2数量级。
2 结果与讨论
2.1 腐蚀过程中Zn-Al 涂层宏观形貌变化
盐雾腐蚀不同时长Zn-Al 涂层试样的表面形貌如图1 所示。由图1 可见,Zn-Al 涂层为银灰色,表面均匀平整,无麻点、裂纹等缺陷(见图1a)。盐雾腐蚀后,Zn-Al 涂层表面出现白锈,失去金属光泽(见1b—e)。腐蚀到1 126 h 时,涂层表面部分区域出现红色锈点,但无裂纹和鼓泡现象(见图1f),检测Zn-Al涂层的电阻率为4.93 kΩ·m,属于半导体涂层,说明Zn-Al 涂层在盐雾环境中能够出现相互电连接,形成闭合回路,起到电化学保护作用,因此Zn-Al 涂层具有优异的耐腐蚀性能。盐雾腐蚀前,Zn-Al 涂层与基体的结合力为0 级,腐蚀1 126 h 后,Zn-Al 涂层与基体的结合力降为1 级。

图1 盐雾腐蚀不同时长Zn-Al 涂层的表面形貌Fig.1 Surface morphology of Zn-Al coatings corroded by salt spray for different duration
2.2 腐蚀过程中Zn-Al 涂层微观形貌及成分变化
盐雾腐蚀不同时长后,Zn-Al 涂层表面的微观形貌如图2 所示。由图2 可见,Zn-Al 涂层表面组织致密,呈黑白相间形貌。局部放大表明,片状Zn 粉和Al 粉分布均匀(见图2a)。图2a 中不同区域的元素检测结果见表1。由表1 可知,图1a 中亮白色片状物为Zn 粉(点1),深黑色片状物为Al 粉(点2),检测到的C、Si 和O 元素表明硅烷膜均匀分布在整个Zn-Al 涂层中。在盐雾腐蚀过程中,可以观察到Zn-Al 涂层表面黑白相间的形貌消失,片状Zn 粉和Al 粉逐渐难以分辨,出现了海绵状组织,腐蚀产物堆积在金属粉周围,填充到涂层表面不平区域,使得涂层变得平整。盐雾腐蚀至672 h 时,涂层更加致密(见图2b—e)。当腐蚀到1 126 h 时,Zn-Al 涂层出现了长裂纹和蜂窝状蓬松结构(见图2f)。

表1 图2 中不同区域的EDS 分析(质量分数,%)Tab.1 EDS results for different regions in fig.2 (mass fraction %)

图2 盐雾腐蚀不同时长Zn-Al 涂层的表面微观形貌Fig.2 Surface micro-morphology of Zn-Al coatings corroded by salt spray for different duration
Zn-Al 涂层在中性盐雾环境中腐蚀不同时长的EDS 分析结果见表2。由表2 可知,Zn、Al、C、Si、Mo 和O 元素分布在Zn-Al 涂层中,无明显团聚现象(见图2a)。随着腐蚀时间的延长,涂层中Zn、Al 元素含量呈明显下降趋势,而O、Cl 和C 元素含量则逐渐增加,说明腐蚀介质逐渐腐蚀涂层,消耗片状Zn、Al 粉。分析认为,片状Zn 粉和片状Al 粉在25 ℃时的标准电极电位分别为-0.763 V 和-1.662 V。在盐雾环境中,首先是片状Al 粉和片状Zn 粉之间由于电位差形成原电池,不断消耗涂层中的Al 粉,保护基体。其次,随着腐蚀的进行,腐蚀产物中Zn5(OH)8Cl2·H2O 的相对含量达到55.35%,由于Zn5(OH)8Cl2·H2O 难溶于水,且在很宽的pH 范围内可保持很强的稳定性,填充并包覆在Zn-Al 涂层中,使涂层的物理屏蔽作用达到最佳效果,涂层的腐蚀速率最低。因此,整个盐雾腐蚀过程中生成的腐蚀产物覆盖在涂层表面,发挥了物理屏蔽保护作用,减缓了涂层中Zn、Al 粉的消耗,保护基体。盐雾腐蚀至1 126 h 后,涂层中出现了Fe 元素,此时腐蚀介质通过微裂纹到达基体,并与基体发生反应,因此涂层表面出现了红锈。

表2 中性盐雾环境中腐蚀不同时长Zn-Al 涂层EDS 分析(质量分数,%)Tab.2 EDS analysis of Zn-Al coatings corroded in neutral salt spray environment for different duration (mass fraction %)
Zn-Al 涂层盐雾腐蚀不同时长的截面微观形貌如图3 所示。由图3a 可见,Zn-Al 涂层中Zn 粉、Al粉相互交叠,形成层片状结构,与基体结合良好,平均厚度为20.78 μm。在盐雾环境中,由于Cl-的侵蚀,Zn-Al 涂层表层的片状金属粉逐渐碎化,腐蚀产物在Zn-Al 涂层表面堆积,形成1~3 μm 的腐蚀层(见图3b)。腐蚀到672 h 时,可以观察到Zn-Al 涂层表面的腐蚀层增厚为5~8 μm(见图3c),而腐蚀层下方的层片状交叠结构依然完整,表明此时Zn-Al 涂层仍具有物理屏蔽作用,可有效地将腐蚀介质与NdFeB 基体阻隔。当盐雾腐蚀1 126 h 后,观察图3d 可见,Zn-Al涂层中出现了微裂纹,并渗透至基体,涂层中Zn 粉和Al 粉已经无法清晰分辨。说明随着盐雾腐蚀时间的延长,涂层中Zn 粉和Al 粉因腐蚀反应大量消耗(表1),涂层中生成的腐蚀产物越来越多,导致体积膨胀,出现裂纹,同时也可以观察到基体表面涂层因腐蚀产物的生成明显增厚。

图3 盐雾腐蚀不同时长Zn-Al 涂层的截面微观形貌Fig.3 Cross-sectional micro-morphology of Zn-Al coatings corroded by salt spray for different duration
2.3 腐蚀过程中Zn-Al 涂层的物相变化
图4 和表3 分别为盐雾腐蚀不同时长后Zn-Al 涂层的XRD 图谱和不同物相相对含量的计算结果。由图4 可见,Zn-Al 涂层由Zn、Al、AlPO4、Zn3(PO4)2、Zn4Si2O7(OH)2相组成。在2θ=43.1°出现了Zn(101)晶面的尖锐峰形,表明Zn-Al 涂层中片状Zn 粉具有高度一致的取向,大部分以单质形式存在,而Zn4Si2O7(OH)2相则表明涂层中含有硅烷膜。相比于原始Zn-Al 涂层,盐雾腐蚀48 h 后的涂层,物相中只有Zn、Al、Zn5(OH)8Cl2·H2O 和Al12(OH)18(AlO4)(Si5O16)Cl,其中Zn、Al 的衍射峰强度随着腐蚀时间的延长而越来越弱。表明在盐雾环境中,Zn-Al 涂层中硅烷膜层遭到破坏,片状Zn 粉和Al 粉在Cl-的侵蚀下,生成越来越多的腐蚀产物Zn5(OH)8Cl2·H2O 和Al12(OH)18(AlO4)(Si5O16)Cl。

图4 盐雾腐蚀不同时长Zn-Al 涂层的XRDFig.4 XRD of Zn-Al coatings corroded by salt spray for different duration

表3 盐雾腐蚀不同时长Zn-Al 涂层物相的相对含量Tab.3 Relative content of phases in Zn-Al coatings corroded by salt spray for different duration%
由表4 可见,随着盐雾腐蚀时间延长,涂层中Zn 粉和Al 粉的含量因腐蚀消耗而显著减少,腐蚀产物Zn5(OH)8Cl2·H2O 和Al12(OH)18(AlO4)(Si5O16)Cl 的含量逐渐增加,并堆积在Zn-Al 涂层表面,因此腐蚀层厚度不断增加,Zn-Al 涂层不断减薄(见图3)。盐雾腐蚀1 126 h 后,腐蚀产物Zn5(OH)8Cl2·H2O 相对含量达到63.49%,通过拉曼光谱(图5)进一步检测可知,涂层表面含有Fe2O3。表明此时O2、Cl-通过涂层的微裂纹渗透至NdFeB 基体,并与之发生反应,烧结NdFeB 在空气中的腐蚀产物为FeO、Nd2O3和CO2[23],但在中性盐雾环境中由于NaCl、O2和H2O存在,经过进一步氧化反应生成了红色的Fe2O3。
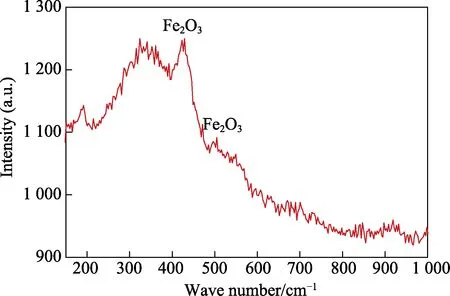
图5 盐雾腐蚀1 126 h 后Zn-Al 涂层试样的拉曼光谱分析Fig.5 Raman spectroscopic analysis of Zn-Al coated samples after salt spray corrosion for 1 126 h
Zn-Al 涂层发生的反应如式(1)—(4)所示。
阳极:
阴极:
2.4 腐蚀过程中Zn-Al 涂层的极化曲线分析
图6 和表4 分别给出了盐雾腐蚀不同时间后Zn-Al 涂层的电化学测试结果。由图6 可见,Zn-Al涂层的Tafel 极化曲线有较明显钝化区,表明Zn-Al涂层表面存在钝化膜,具有优异的耐蚀性能。由表4可知,Zn-Al 涂层在盐雾腐蚀过程中,阴阳极塔菲尔斜率βc、βa变化不大,表明Zn-Al 涂层主要通过物理屏蔽作用来保护基体。在盐雾腐蚀过程中,Zn-Al 涂层的自腐蚀电位发生负移,钝化区消失。腐蚀48 h 后,腐蚀电流密度增大1 个数量级,为9.76×10-6A/cm2。表明由于腐蚀介质的作用,Zn-Al 涂层表面的硅烷膜层、无机盐钝化膜遭到破坏,暴露在盐雾环境中的片状Zn 粉和Al 粉发生电化学腐蚀,在涂层表面生成少量腐蚀产物,造成腐蚀速率增加。此阶段以Zn-Al 涂层牺牲阳极的电化学保护作用为主。
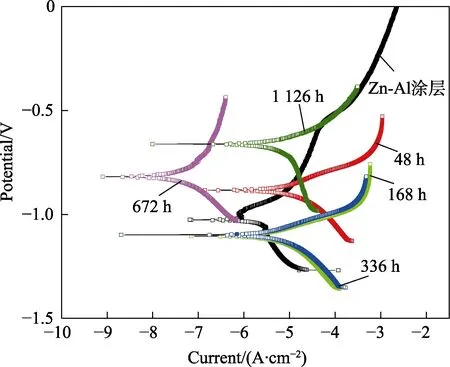
图6 中性盐雾环境腐蚀不同时间Zn-Al 涂层试样的Tafel 极化曲线Fig.6 Tafel polarization curves of Zn-Al coated samples corroded in neutral salt spray environment for different duration

表4 极化曲线的拟合参数Tab.4 Fitting parameters for polarization curves
在中性盐雾环境腐蚀48~336 h 时,自腐蚀电位维持在-1.1 V 左右,自腐蚀电流密度基本保持不变,腐蚀速率稳定,片状Zn 粉和Al 粉持续活化,腐蚀产物覆盖在Zn-Al 涂层表面,形成保护层,起到物理屏蔽作用。当盐雾腐蚀持续到672 h 后,可以发现,Zn-Al涂层的自腐蚀电位正移至-0.82 V,自腐蚀电流密度降低了2 个数量级,为5.64×10-8A/cm2。此时,Zn-Al涂层表面的腐蚀产物层厚度达5~8 µm(见图3c)。腐蚀产物中Zn5(OH)8Cl2·H2O 的相对含量达到55.35%,由于它难溶于水,且在很宽的pH 范围内可保持很强的稳定性[24-26],填充并包覆在Zn-Al 涂层中,使涂层的物理屏蔽和电化学保护作用达到最佳效果,所以此时涂层的腐蚀速率最低。腐蚀到1 126 h 后,Zn-Al 涂层中Zn 粉和Al 粉都转变成腐蚀产物,涂层失去完整的金属片状结构,涂层的电化学保护失去作用。此时,涂层以腐蚀产物为主,涂层组织蓬松,呈海绵状,且出现许多微裂纹,腐蚀介质穿透Zn-Al 涂层,在涂/基界面处,与基体发生反应,生成Fe2O3(见图5)。
2.5 腐蚀过程中Zn-Al 涂层的阻抗谱分析
Zn-Al 涂层试样在中性盐雾环境腐蚀不同时长的EIS 图见图7。高频区容抗弧可以反映腐蚀过程中涂层的物理电阻,半径越大,涂层的物理屏蔽作用越强。低频容抗弧可以反映金属粉的活化状态,半径越小,金属粉的活性越强。腐蚀前,Zn-Al 涂层的低频容抗弧具备明显的Warburg 阻抗特征,说明Zn-Al 涂层表面具有钝化膜,并与硅烷膜组成了结构致密的表面膜[33]。腐蚀进行48 h 后,Warburg 阻抗特征消失,且未检测到硅烷膜的存在(见图4),表明涂层表面膜消失。腐蚀不同时长后,试样的高频容抗弧半径大小依次为:腐蚀672 h 试样>Zn-Al 涂层>腐蚀48 h 试样>腐蚀168 h 试样>腐蚀336 h 试样>腐蚀1 126 h 试样,说明在Zn-Al 涂层腐蚀失效前,盐雾腐蚀672 h时,Zn-Al 涂层的物理屏蔽保护作用最强。进一步观察不同试样的低频容抗弧半径,其大小依次为:腐蚀48 h 试样>腐蚀168 h 试样>腐蚀336 h 试样>腐蚀672 h 试样>腐蚀1 126 h 试样,说明在Zn-Al 涂层腐蚀失效前,盐雾腐蚀672 h 时金属粉的活化作用最弱,涂层的电化学保护与物理屏蔽协同作用在盐雾腐蚀672 h 时达到最佳耐蚀效果,腐蚀速率最小(见表4)。

图7 Zn-Al 涂层在中性盐雾环境不同时间的EIS(a)和Bode 图(b)Fig.7 EIS (a) and Bode (b) of Zn-Al coatings in neutral salt spray environment for different duration
Zn-Al 涂层试样在中性盐雾环境腐蚀不同时间点的EIS 如图8 所示。可以看到,腐蚀进行到672 h 时,高频区容抗弧的半径进一步增大,与图6 中腐蚀进行到672 h,Zn-Al 涂层的自腐蚀电流密度降低2 个数量级,物理屏蔽保护作用达到最佳效果的分析保持一致。

图8 Zn-Al 涂层在中性盐雾环境不同时间点的EISFig.8 EIS of Zn-Al coatings in neutral salt spray environment for different duration
Zn-Al 涂层的阻抗可按照图9 的等效电路模型拟合。其中,Rs是溶液电阻,指测试的电解液中工作电极到鲁金毛细管口之间溶液的电阻;Cc为涂层电容;Rc为涂层电阻;Qm、Rm分别为金属粉表面腐蚀产物层的电容和电阻;Qa和Ra分别为片状Zn 粉和片状Al 粉腐蚀活化的电容和电阻。采用经常使用的相位角元件Q来代替电容,可以获得更好的拟合效果。测得弥散系数n为0.79,相位角代替电容器可补偿系统中的不均匀性。Rs由测试溶液本身决定,对Zn-Al涂层耐腐蚀性能的影响较小。Ra是Rm的一条支路上的电阻,Rm对Zn-Al 涂层耐腐蚀性的影响远大于Ra,所以Zn-Al 涂层耐腐蚀性能主要由Rm决定。
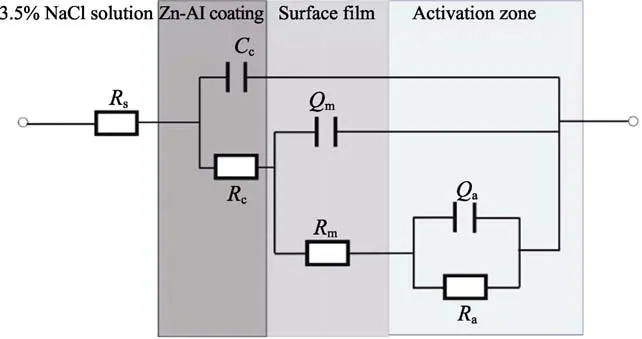
图9 等效电路Fig.9 Equivalent circuit
等效电路图相应的拟合参数见表5。由表5 可见,在盐雾环境中腐蚀不同时间后,涂层的Rm值与原始Zn-Al 涂层相比明显减小,然后缓慢增加。当腐蚀到672 h 时,Rm显著增大(7 812 Ω·cm2),此时腐蚀产物增厚,覆盖在Zn-Al 涂层表面,涂层的电化学保护和物理屏蔽协同作用最佳,因此自腐蚀电流密度降低2 个数量级。腐蚀到 1 126 h 后,Rm减小为74.48 Ω·cm2,此时涂层中片状Zn 粉和Al 粉消耗殆尽,电化学保护作用失效,腐蚀产物堆积在烧结NdFeB 基体上,呈现海绵蓬松状组织,腐蚀介质穿透腐蚀产物层,对基体造成腐蚀。

表5 等效电路拟合参数Tab.5 Fitting parameters of equivalent circuit
3 结论
1)NdFeB 磁体表面制备的环保型Zn-Al 涂层的耐盐雾腐蚀时间不少于1 000 h。
2)在盐雾腐蚀环境中,Zn-Al 涂层表面逐渐被白锈覆盖,失去金属光泽。腐蚀至1 126 h 时,Zn-Al涂层表面出现红色锈点,涂层微观组织呈蜂窝状结构,并出现微裂纹。腐蚀产物由Zn5(OH)8Cl2·H2O、Al9SiAl12(OH)18(AlO4)(Si5O16)Cl、Fe2O3极少量的Zn、Al 组成。
3)盐雾腐蚀初期,Zn-Al 涂层表面钝化膜、硅烷膜层破坏,Zn 粉、Al 粉活化,涂层以电化学保护作用为主。随着腐蚀时间的延长,腐蚀产物产生并覆盖在Zn-Al 涂层表面,形成保护,电化学保护和物理屏蔽保护同时作用。在腐蚀到672 h 时,腐蚀产物膜与Zn-Al 涂层的协同作用,使涂层的腐蚀速率降到最低。腐蚀到1 126 h 后,Zn-Al 涂层失去完整的金属片状结构,对基体失去保护作用。

