肝肿瘤热消融穿刺电磁导航系统研究
姚洁,伍国林,吴水才
北京工业大学 环境与生命学部 生物医学工程系 智能化生理测量与临床转化北京市国际科研合作基地,北京 100124
引言
原发性肝癌是全球第六大常见的癌症,我国肝癌新发病例占全球的45.3%,是我国第5 位常见恶性肿瘤及第2 位肿瘤致死病因[1-3]。目前肝肿瘤手术切除、肝移植和消融治疗已成为原发性肝癌的3 种主要治疗方法[4-7]。肝肿瘤微波和射频消融治疗由于其操作简单、微创、疗效显著等优点,已逐步成为治疗原发性肝癌的有效方法[8]。在术前,医生依据CT、MRI 等断层影像图像构建的三维可视化模型,对患者肝肿瘤消融穿刺路径进行规划;术中,在影像技术引导下,医生凭经验确定经皮穿刺点的位置与深度。在实际消融治疗中,医生往往很难做到穿刺与消融治疗一步到位[9-10]。大量研究表明,消融针穿刺导航系统可在术中为医生提供辅助与指导,提高肝肿瘤热消融治疗穿刺成功率[11-13]。基于此,本文旨在研制一种肝肿瘤热消融穿刺电磁导航系统,用于辅助医生进行肝肿瘤经皮穿刺,提高手术的安全性与有效性。
1 方法
1.1 术中定位技术
在肝肿瘤穿刺中,穿刺位置选取与深度的不恰当可能导致不完全消融和较高的复发率,精准的术中定位对于达到足够的肿瘤消融覆盖和治疗至关重要。手术导航系统术中定位一般有机械定位、超声定位、光学定位与电磁定位[11-14]。电磁定位不易受障碍物遮挡和反光物干扰,可以对非刚性手术器械进行准确定位,且分辨率较高[15-16]。在肝肿瘤热消融穿刺电磁导航系统设计中,选取加拿大NDI 公司生产的Aurora 电磁定位仪来追踪患者与手术器械的物理坐标空间位姿,以提高手术导航的精度。
1.2 空间配准技术
空间配准是为了在不同坐标系之间寻求其转换关系。肝肿瘤热消融导航系统中,三维影像模型、定位设备以及患者均有各自独立的坐标系,通过确定图像系统和定位导航系统之间的转换关系,将消融针按照图像系统显示的术前规划穿刺路径插入病灶靶点,并在这个过程中实时跟踪消融针位置和姿态。
手术导航中的空间配准技术主要有标记点法、标志面法、定位框架法等,标记点法是目前临床中最常用的配准方法[17]。标记点配准法是利用不同坐标系下一定数目的公共点作为配准标记点,寻求不同坐标系下变换误差最小的旋转矩阵和平移矢量。标记点类型主要包括解剖标记点和粘贴于皮肤表面的自定义标记点两种。解剖标记点利用人体的显著特征作为标记点,如鼻根、眼角、下颌角点等[18]。人工粘贴标记点由医生在术前粘贴于患者体表,由成像设备扫描成像后表现出与其周围组织灰度值的明显差异,方便识别、提取图像中的标记点位置信息。
基于不同坐标系下成对点集的刚性空间配准算法,目前常用的主要是奇异值分解(Singular Value Decomposition,SVD)法、最近值迭代法、单位四元数法和主元分析法等,其本质均是求得使误差最小的旋转矩阵和平移矩阵[19-20]。本研究通过在患者腹部粘贴标记点,基于三维影像空间坐标系和电磁导航坐标系下粘贴的标记点作为配准标记点,采用基于SVD 的刚性空间配准算法。
在任意两个相同尺度笛卡尔三维坐标系中,存在P{p1,p2,…,pn}和Q{q1,q2,…,qn}两个匹配点集,pi和qi为两个坐标系中对应的匹配点。本文基于SVD 算法求解配准点集之间所需的刚体变换,即求解旋转矩阵R和平移向量t的最小化,对齐误差如公式(1)所示。
式中,SO(3)为三维旋转群;R∈SO(3)为旋转矩阵;R为正交矩阵,且行列式为1;R3表示笛卡尔三维坐标系。
计算点集P 的中心点和点集Q 的中心点q,计算方式分别如公式(2)和公式(3)所示。
为计算旋转矩阵,需要消除平移向量影响,故需要将点集重新中心化,生成新点集X 和Y,其中xi和yi分别表示新点集中的点,具体计算方式如公式(4)所示。
计算点集X 和Y 之间3×3 的协方差矩阵S=XYT。通过SVD 算法分解S 得到S=U∑VT,其中U 和V 均为3×3 的正交矩阵。基于U 和V,计算两点集之间的旋转矩阵R 如公式(5)所示。
正交矩阵R 可能是旋转矩阵或反射矩阵,通过验证R 的行列式对反射矩阵的情况进一步处理。当det(VUT)=1 时,R 为旋转矩阵;当det(VUT)=-1 时,R 为反射矩阵,为将旋转解转换为旋转矩阵进行处理,得到旋转矩阵如公式(6)所示。将R 带入公式(6),计算得到两点集之间的平移向量t,其计算方式如公式(7)所示。
1.3 肝肿瘤热消融穿刺电磁导航系统的设计
1.3.1 系统整体设计
肝肿瘤热消融穿刺电磁导航系统功能框图如图1 所示,主要由数据管理、空间配准和路径规划3 个模块组成。数据管理模块实现CT 图像的读取、分割处理和三维可视化。路径规划模块完成消融针进针路径的合理规划、交互式调整和实时显示。空间配准模块通过电磁设备读取消融针的空间位置,使消融针沿着规划的路径穿刺进入肿瘤。肝肿瘤热消融穿刺电磁导航系统的主界面如图2所示,包括数据管理、CT 数据显示、系统功能等区域,其中系统主要功能区包括设备管理、图像配准及手术规划实施。
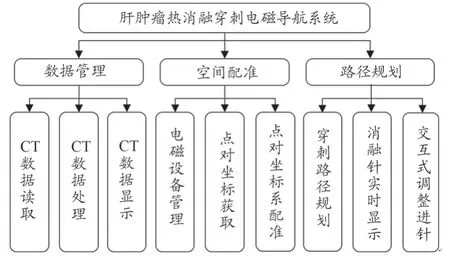
图1 系统功能框图

图2 肝肿瘤热消融穿刺电磁导航系统主界面
肝肿瘤热消融穿刺电磁导航系统硬件由电磁定位系统和PC 端三维影像系统组成。如图3 所示,电磁定位装置为NDI 公司的NDI Aurora 电磁跟踪系统,包括控制器和发射线圈两个部分,可在遮挡的情况下确定患者/腹部体模的实际位置,同时用于实时追踪装有电磁传感器消融针的位姿。装有电磁传感器的消融针将电磁传感器放置于自制电磁传感器放置套中,安装固定在消融针尾端。腹部体模采用的是美国Cirs 071A 穿刺体模,包含12 个肿瘤病灶。系统界面利用MFC 设计实现,系统软件基于ITK、VTK、OpenCV 开源工具包实现,矩阵计算使用Eigen 库。
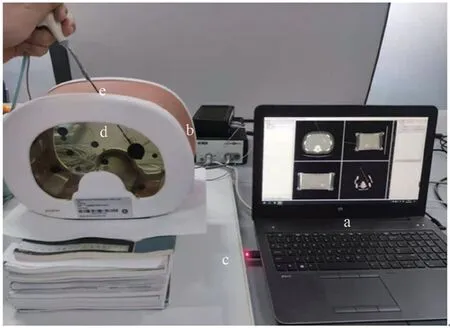
图3 硬件结构图
1.3.2 系统工作流程
肝肿瘤热消融穿刺电磁导航系统工作流程如图4 所示,在三维影像处理系统导入CT 数据后,通过图像处理在数据显示区显示横截面、矢状面和冠状面图像及三维重建后的模型。随后建立三维影像系统与电磁导航系统的通信,通过电磁定位仪获取腹部粘贴标记点在电磁导航坐标系下位姿信息,同时通过三维影像系统获取对应标记点在三维影像空间坐标系下的坐标信息,得到两个对应点集。通过奇异值分解方法求得三维影像空间坐标系和电磁导航坐标系的变换关系。基于三维影像系统对CT 图像处理获得的三维模型,进行穿刺手术路径的规划,通过对消融针的电磁定位实现实时穿刺导航。
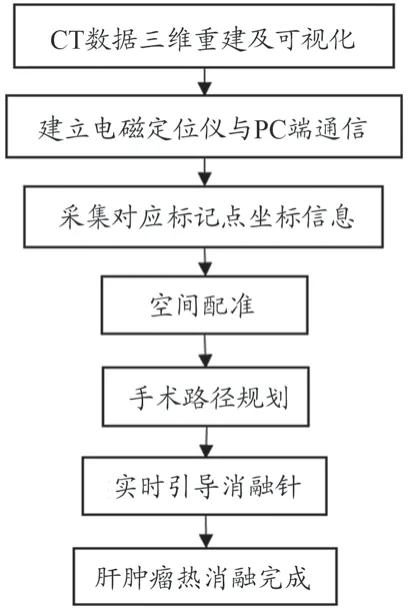
图4 肝肿瘤热消融穿刺电磁导航系统工作流程
2 实验与结果
2.1 空间配准的准确性验证实验
对SVD 算法在肝肿瘤热消融穿刺电磁导航系统的空间配准中准确性进行验证,设计了腹部体模与其CT图像的配准实验来进行测试。
在腹部体模上粘贴6 个标记点(序号1~6)后进行CT 扫描,将扫描得到的图像进行分割和三维重建。通过电磁定位仪采集腹部体模标记点的空间坐标,使用SVD求解旋转矩阵和平移向量。腹部体模与重建的三维模型配准示意图如图5 所示,在腹部体模与重建三维模型两个坐标系中,三维模型中序号1~6 标记点与腹部体模中序号1’~6’标记点一一对应。获取这六对点的空间坐标,通过SVD 变换得到两个空间坐标系的刚性变换。坐标转换精度的评价方式通常是利用转换前后公共点坐标差值的均方根值来进行评价。进行20 次实验,依据每次实验中获取体膜6 个标记点在三维影像坐标系与经转换求得三维影像坐标系下的坐标计算得到均方根误差,将计算误差值与对应实验编号绘制为柱状图(图6),其中实验中最大均方根误差不超过1.5 mm,平均均方根误差为1.262 mm。

图5 体模与重建模型配准示意图

图6 体膜标记点空间配准均方根误差柱状图
2.2 肝肿瘤热消融穿刺电磁导航系统精度验证实验
为评估肝肿瘤热消融穿刺电磁导航系统的精度,本文设计了如图7 所示的模型实验。在对扫描后的腹部体模CT 影像进行三维重建并手动规划穿刺路径后,建立PC 端导航系统软件与电磁定位仪的通信,来获取穿刺消融针的空间位置。在进行肝肿瘤穿刺路径规划后,手持消融针,依据实时映射在三维影像坐标系中的消融针位姿对消融针进针位置与角度进行调整,直至三维影像中消融针与规划路径重合,将消融针沿着规划穿刺路径进针。当三维影像中显示消融针针尖到达肿瘤中心位置时,完成进针引导。
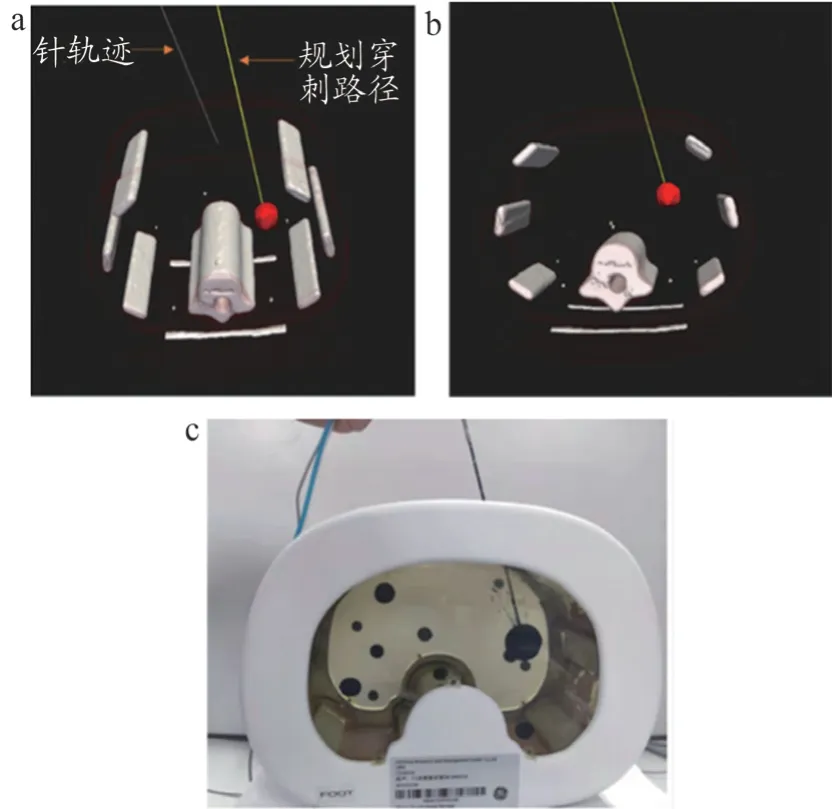
图7 系统引导消融针穿刺示意图
本文选取的5 位操作人员均为之前未接触过该系统且无临床操作经验的实验室人员,参照上述步骤对体模中5 个腹部模拟肿瘤进行了精度验证实验,实验结果如表1 所示,其中目标位置误差为穿刺后消融针针尖位置与规划路径末端位置的均方根误差。由表1 可知,系统最大目标位置误差不超过5.00 mm,平均目标位置误差为3.10 mm。
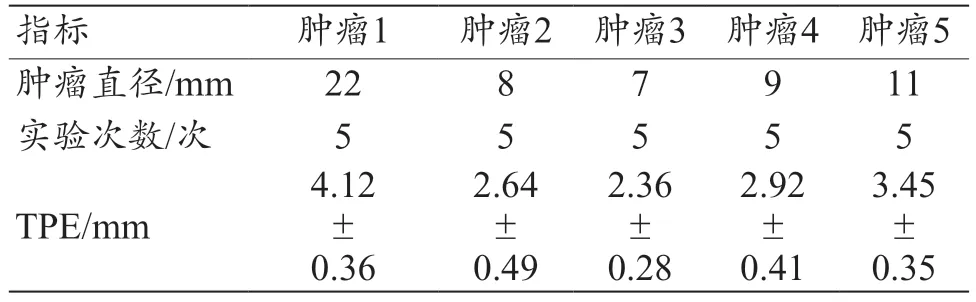
表1 模拟肿瘤穿刺实验结果
3 讨论
本文针对肝肿瘤热消融治疗过程中消融针实时引导问题,开发了一套肝肿瘤热消融穿刺电磁导航系统。实验结果显示,标记点从电磁导航坐标系映射到三维影像坐标系,坐标信息与实际三维影像坐标系对应标记点坐标基本相同,但还存在一定误差。分析出现上述误差的主要原因是在电磁定位针采集腹部体模标记点坐标时,定位针的放置可能存在偏差;同时标记点数量以及体模在磁场空间中放置位置可能会对配准精度造成一定的影响。实验结果表明,配准算法最大均方根误差不超过1.5 mm,平均均方根误差为1.262 mm,算法误差较小,具有较好的精度,可应用本文所设计的导航系统,实现患者与其三维影像的配准。
Teng 等[11]基于电磁导航系统协助医生完成1 例肺肿瘤消融手术,在术后评估中未出现出血、气胸、感染、胸腔积液等并发症,表明电磁导航系统辅助消融手术治疗具有可行性。Zhang 等[16]基于电磁导航系统在CT 引导下进行肝肿瘤热消融手术,实验证明电磁导航系统与徒手穿刺相比可有效减少患者辐射暴露与相关仪器的调整次数,对肝肿瘤热消融手术起到很好的辅助作用。Liu等[21]评估将腹腔镜超声图像、腹腔镜视频和针头轨迹统一于同一视图的增强现实系统,其目标定位误差为11.1 mm,所需平均穿刺针放置时间为22.9 s。Li 等[22]提出了腹部肿瘤穿刺消融手术导航中一种无标记手术配准方法,模拟实验穿刺结果表明,术后CT 图像显示的针尖位置与实际穿刺目标之间的距离平均为4.117 mm。Xiao 等[23]提出一种自动提取腹部表面区域的方法,其对Kinect 的安装有严格的要求,以保证其z轴垂直于CT 床,如果没有基准或测量设备很难实现。梁亮亮等[24]通过电磁定位引导体模内橡胶小球穿刺的实验研究中,体膜的配准精度平均误差为(0.826±0.029) mm。Ringe 等[25]评估了电磁导航系统的准确性,其穿刺平均偏差为(3.2±1.9)mm,与传统CT 引导微波消融相比准确性更高。本研究中的系统最大目标位置误差不超过5.00 mm,平均目标位置误差为3.10 mm,表明本文设计的电磁导航系统能实现消融针的实时导航,对临床操作经验较少的人员具有一定的辅助与指导作用。
但本文系统还需要在以下几方面进一步改进:① 系统对穿刺路径进行手动规划,依赖于医生的临床经验,后续将优化对穿刺路径的规划,实现穿刺路径的自动规划。② 肝脏为非刚性组织,本文未考虑术中呼吸运动与穿刺过程中造成的肝脏形变。构建个性化的呼吸运动模型及针-组织交互模型,在此基础上实现消融针的实时定位更具有临床价值。③ 本系统只使用体模进行实验,系统有效性也存在一定的局限性,后续还需要进行动物和临床实验。④ 系统仍使用徒手穿刺,现有研究结合机械臂进行肝肿瘤热消融穿刺,使得穿刺准确性、安全性均有了一定提升,下一步可结合机械臂进行研究[26]。
4 结论
本文设计了一套肝肿瘤热消融穿刺电磁导航系统,实现了CT 数据的读取和可视化、穿刺路径规划以及基于电磁定位实时反馈消融针的空间位姿。通过腹部体模实验,初步验证了肝肿瘤热消融穿刺电磁导航系统的准确性和可行性。

