用改性壳聚糖同步去除废水中的镉和刚果红 试验研究
郭 娜,廖 兵,卢 涛,4,刘胜兰
(1.成都理工大学 生态环境学院,四川 成都 610059;2.四川建筑职业技术学院 四川省城市污泥建材资源化利用工程研究中心,四川 德阳 618000;3.四川建筑职业技术学院 德阳市建材环保资源化工程技术研究中心,四川 德阳 618000;4.成都环境集团 成都市自来水有限责任公司,四川 成都 610031)
镉(Cd2+)和刚果红(CR)常共存于含电镀企业和印染企业的工业园区废水中,属于对环境和人体危害大、难处理的污染物,是工业废水处理领域的难题之一[1-2]。目前,含Cd2+废水处理技术主要有化学沉淀法[3]、离子交换法[4]、吸附法[5]、电化学法[6]、生物法[7]等。含CR的印染废水的常规处理方法有物理法(混凝沉降法、吸附法)[8]、化学法(AOPs、光催化反应、臭氧氧化)[9]、生物法(好氧生物处理法、厌氧生物处理法)[10]等。相较于其他方法,吸附法因具有对重金属和染料吸附量大、材料来源广泛、价格低廉、经济有效等优点[11],在废水处理领域应用广泛。常用的吸附材料有沸石[12]、硅藻土[13]、活性炭[14]、壳聚糖[15]等。
壳聚糖作为一种环境友好型材料,其分子链上有大量自由的氨基(—NH2)和羟基(—OH),对金属离子具有离子交换和螯合吸附作用,同时能通过氢键、范德华力、静电引力等相互吸附作用与多种类型的染料分子保持很高的亲和性[16]。因此,壳聚糖既能吸附Cu2+、Mn2+、Pb2+、Cd2+等金属离子,也能吸附染料污染物,在水污染处理方面应用广泛。壳聚糖具有生物降解性、细胞亲和性和无毒性等特点,不会造成环境污染[17],但因吸附容量不高、选择性差、性能不稳定、适用pH范围窄等缺陷制约了其应用与发展[18]。
通过化学改性可提高壳聚糖对Cd2+或CR等其他污染物质的吸附性能,即在氨基及羟基上引入其他基团,制备不同性质的改性壳聚糖材料。含硫、氮的硫脲对重金属的吸附选择性较好,吸附容量较高,巯基对极性大的离子或重金属离子有特殊的配合能力,能形成稳定的配合结构,因此可用硫脲对壳聚糖接枝提高其对重金属离子的吸附容量。经环氧氯丙烷交联,制得硫脲改性壳聚糖颗粒,改性后的壳聚糖具有明显的耐酸能力,对Cr6+、Ni2+的吸附效果较好[19]。离子印迹聚合物吸附剂对印迹离子具有特异选择性,可直接用于去除水中某种重金属离子,效果较好[20]。
为了提高壳聚糖的吸附特异选择性、降低溶解性、增加吸附位点并拓宽pH适用范围,试验研究了采用离子印迹、环氧氯丙烷交联、硫脲接枝方法对壳聚糖进行化学改性,并将改性壳聚糖用于吸附去除单独体系和复合体系废水中的Cd2+和CR,同时探究了其吸附动力学及吸附机制。
1 试验部分
1.1 试剂与仪器
主要试剂:壳聚糖(脱乙酰度≥95%,分子量100 000~300 000)、硫化镉、氯化镉、氢氧化钠、氯化钠、乙二胺四乙酸、硫脲、刚果红、异丙醇、环氧氯丙烷,均为分析纯,购于成都科龙化学试剂厂;试验用水为去离子水。
主要仪器:V-1100D型可见分光光度,上海美谱达仪器有限公司;GGX-9型火焰原子分光光度计,北京海光仪器有限公司;SHZ-82型水浴恒温振荡器,常州国宇仪器制造有限公司;85-2型恒温磁力搅拌器,金坛市城东新瑞仪器厂;DF-101S型集热式恒温加热磁力搅拌器,巩义市予华仪器有限责任公司。
1.2 改性壳聚糖的制备及表征
称取2.5 g壳聚糖于三口烧瓶中,加入高浓度(60 mg/L)Cd2+溶液,放入集热式恒温加热磁力搅拌器中搅拌至壳聚糖吸附镉离子饱和;加入1 g硫脲反应4 h,离心后将生成的材料浸于50 mL溶液中(异丙醇与水体积比1∶1),加入5 mL环氧氯丙烷反应2 h;再次投加1 g硫脲,反应一定时间后用0.02 mol/L EDTA溶液进行洗脱;最后用无水乙醇与去离子水清洗数次,在真空干燥箱中于60 ℃下烘干,得改性壳聚糖样品,记作CTS-1。
采用日本JSM-7500F型扫描电子显微镜(SEM)观察CTS-1表面微观形貌(加速电压为0.1~30 kV);采用日本理学Smartlab 9型射线衍射仪(XRD)分析CTS-1晶体结构(Cu靶Kα射线,λ=0.154 nm,电压40 kV,电流35 mA,扫描范围2θ=5°~65°);采用美国Nicolet-1170SX型傅里叶红外光谱仪(FT-IR)分析CTS-1官能团种类;采用英国Axis Ultra型X射线光电子能谱仪(XPS)分析CTS-1表面化学成分。
1.3 吸附试验
试验方法:向100 mL锥形瓶中加入一定浓度的待处理废水50 mL和CTS-1 0.05 g(干重),调节废水pH=5;将锥形瓶置于恒温振荡器中,在25 ℃下以120 r/min速率振荡反应12 h,待吸附结束后,固液分离,测定溶液中Cd2+或CR浓度。
CTS-1对单独体系和复合体系中Cd2+的吸附:单独体系中Cd2+初始质量浓度为40 mg/L,复合体系中Cd2+和CR初始质量浓度分别为40、150 mg/L。
CTS-1对单独体系和复合体系中CR的吸附:单独体系中CR质量浓度为150 mg/L,复合体系中Cd2+和CR初始质量浓度分别为40、150 mg/L。
CTS-1对复合体系Ⅰ和复合体系Ⅱ中Cd2+和CR的吸附:复合体系Ⅰ中Cd2+初始质量浓度固定为40 mg/L,CR初始质量浓度分别为50、100、150、200、250 mg/L;复合体系Ⅱ中CR初始质量浓度固定为150 mg/L,Cd2+的初始质量浓度为10、20、30、40 mg/L。
2 试验结果与讨论
2.1 改性壳聚糖的表征
通过扫描电镜(SEM)观察壳聚糖与CTS-1的微观形貌,结果如图1所示。可以看出:与壳聚糖相比,CTS-1表面粗糙不平,且呈褶皱的多孔结构,多孔结构使表面积增大,结合位点得以充分暴露,有利于吸附废水中的Cd2+和CR。

图1 壳聚糖(a)和CTS-1(b)的SEM分析结果
图2为壳聚糖和CTS-1的XRD图谱。可以看出:壳聚糖在2θ为20°处出现1个较强吸收峰,该峰归属于壳聚糖第2类晶型,在10°处出现1个较弱吸收峰,该峰归属于壳聚糖第1类结晶度较低的水合晶体[21];CTS-1在2θ为20°处出现1个明显衍射峰,且峰形尖锐,说明材料结晶程度好,在28.1°处也出现了1个衍射峰,这与CdS (JCPDS 06-0314)中衍射峰(101)相对应,是由于在CTS-1制备过程中,Cd2+与CTS-1表面的S结合形成了配合物或者CdS纳米颗粒[22]所致,这与文献[23]研究结论中提到的CdS对CR的吸附具有促进作用相一致。

图2 壳聚糖和CTS-1的XRD图谱
2.2 CTS-1对废水中Cd2+和CR的吸附
2.2.1 CTS-1吸附不同体系中的Cd2+
CTS-1对不同体系中Cd2+的吸附效果如图3所示。

图3 CTS-1对不同体系中Cd2+的吸附效果
由图3看出:在单独体系中,CTS-1对Cd2+吸附30 min,Cd2+吸附量即达35 mg/g,120 min左右达吸附平衡,Cd2+吸附量为37.13 mg/g,这与文献[24-25]提到壳聚糖基吸附剂相比,具有吸附速率快,吸附容量高的优点。而在复合体系中,Cd2+吸附量较单独体系有所降低,120 min左右吸附达到平衡,Cd2+吸附量为26.06 mg/g,约为单独体系的70%。这是由于离子印迹作用使得CTS-1上存在Cd2+的特异性吸附位点,即使CR浓度较高条件下,CTS-1也可选择性吸附Cd2+,并保持70%的吸附量;同时,Cd2+和CR在CTS-1的非特异性位点上发生竞争吸附,而CR分子因浓度远高于Cd2+而占优势,导致Cd2+吸附量降低。此外,CR分子中—NH2也可能与废水中Cd2+发生配合,生成氮镉键,限制Cd2+向CTS-1表面迁移。
2.2.2 CTS-1吸附不同体系中的CR
CTS-1对不同体系中CR的吸附效果如图4所示。可以看出:在不同体系中,CTS-1均能全部去除不同体系中的CR,吸附量约为153 mg/g,与其他壳聚糖基吸附剂相比,具有较高的吸附量[26-27];吸附30 min内,CR在复合体系中的吸附速率比单独体系快,随反应继续进行吸附速率变慢。这是因为:Cd2+带正电,被CTS-1吸附后,溶液中阳离子数量减少,根据电荷守恒定律,溶液中质子浓度相应增加,导致溶液pH降低[23];随pH降低,CTS-1上的氨基质子化程度增强,从而促进其对阴离子CR的吸附[28];反应后期,大量CR被吸附到CTS-1上,氨基质子化的促进作用减弱,相应的吸附位点也减少,造成吸附速率降低。
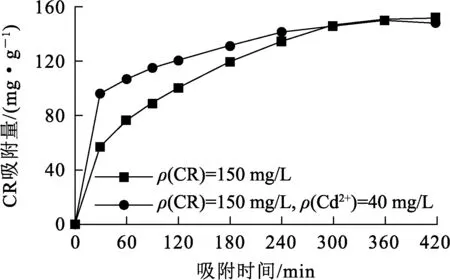
图4 CTS-1对不同体系中CR的吸附效果
2.2.3 CTS-1吸附不同复合体系中的Cd2+和CR
2.2.3.1 复合体系Ⅰ中CR质量浓度对CTS-1吸附Cd2+的影响
复合体系Ⅰ中CR质量浓度对Cd2+吸附量的影响试验结果如图5所示。可以看出,在复合体系Ⅰ中,CTS-1对Cd2+的吸附量随CR质量浓度增大而降低:CR质量浓度为50、100 mg/L时,CR对Cd2+在CTS-1上的吸附影响较小;CR质量浓度为150、250 mg/L时,CR对Cd2+在CTS-1的吸附产生抑制作用,CR质量浓度越高,抑制作用越明显。这是因为:CR质量浓度较低时,CTS-1吸附位点能同时满足对Cd2+和CR的吸附;随CR质量浓度升高,CR会与Cd2+竞争吸附位点,导致Cd2+吸附量降低;此外,CR吸附到CTS-1表面后,还可能会在材料表面产生空间位阻,阻碍Cd2+与CTS-1接触,从而导致Cd2+吸附量降低[28]。

图5 复合体系Ⅰ中CR质量浓度对Cd2+吸附量的影响
2.2.3.2 复合体系Ⅱ中Cd2+质量浓度对CTS-1吸附CR的影响
复合体系Ⅱ中Cd2+质量浓度对CTS-1吸附CR的影响试验结果如图6所示。可以看出:不同Cd2+质量浓度条件下,CTS-1均可有效吸附溶液中的CR;吸附前15 min,CTS-1对CR的吸附速率较快,但随吸附进行,吸附速率逐渐减慢,之后达到吸附平衡;随Cd2+质量浓度增大,CTS-1对CR的吸附速率加快,这可能是因为Cd2+浓度增大改变了复合体系Ⅱ的pH,从而影响了其对CR的吸附行为。

图6 复合体系Ⅱ中Cd2+质量浓度对CR吸附量的影响
由图6还可看出:吸附过程分2个阶段,在吸附15 min内,CR吸附速率较快,这是因为溶液中的Cd2+越多,对溶液pH影响越大,越有利于促进CTS-1对CR的吸附。随反应进行,CR吸附速率变缓,这是因为CR含量减少,向CTS-1内部扩散时的阻力增大。
2.3 吸附机制
2.3.1 吸附动力学
为了进一步探讨CTS-1对Cd2+和CR的吸附机制,同时控制吸附速率的关键步骤,试验利用准一级、准二级动力学模型和颗粒内扩散模型对吸附过程进行拟合。
准一级动力学模型:
qt=qe(1-e-k1t);
(1)
准二级动力学模型:
(2)
颗粒内扩散模型:
qt=k3t0.5+C。
(3)
式中:qe—平衡吸附量,mg/g;qt—吸附t时刻的吸附量,mg/g;t—吸附时间,min;k1—准一级动力学常数,min-1;k2—准二级动力学常数,g/(mg·h);k3—内扩散速率常数,mg/(g·min0.5);C—截距,μg/g,大小与边界层厚度相关。
向100 mL锥形瓶中加入含Cd2+(初始质量浓度40 mg/L)或CR(初始质量浓度150 mg/L)废水50 mL,再加入0.05 g(干重)CTS-1,调节废水初始pH为5;将锥形瓶置于恒温振荡器在25 ℃、以120 r/min速率振荡反应12 h,吸附试验完成后进行固液分离,测定溶液中Cd2+或CR浓度。用上述3个动力学模型对所得试验数据进行拟合,拟合曲线如图7所示,拟合参数见表1、2。

表1 CTS-1对Cd2+的吸附动力学拟合参数

表2 CTS-1对CR的吸附动力学拟合参数

图7 CTS-1对Cd2+(a、c、e)和CR(b、d、f)的吸附动力学拟合曲线

由图7(e)看出,颗粒内扩散模型拟合曲线由3个线段组成,说明CTS-1对Cd2+的吸附为3个阶段[23]:瞬时扩散阶段,Cd2+快速占据CTS-1表面活性位点;孔内扩散阶段,Cd2+占据吸附剂孔内表面活性位点及特异性吸附位点;吸附平衡阶段,吸附剂对Cd2+的吸附趋于平衡。而图7(f)则表明CTS-1对CR的吸附还未达到平衡。由相关拟合参数可知,CTS-1对Cd2+和CR的吸附过程与颗粒内扩散模型均具有一定相关性。
2.3.2 CTS-1吸附Cd2+、CR前后的FT-IR表征


a—吸附前;b—吸附Cd2+后;c—吸附CR后;d—吸附Cd2+、CR后。图8 CTS-1吸附前、后的FT-IR光谱
2.3.3 CTS-1吸附Cd2+、CR前后的XPS表征
为了进一步探究污染物与CTS-1之间的作用机制,对吸附Cd2+、CR前后的CTS-1表面进行XPS能谱分析,结果如图9所示。吸附前后CTS-1中各元素质量分数变化见表3。CTS-1吸附Cd2+、CR前后S 2p的XPS图谱如图10所示。

表3 CTS-1吸附Cd2+、CR前后各元素的质量分数 %

a—吸附前;b—吸附Cd2+后;c—吸附CR后;d—吸附Cd2+、CR后。图9 CTS-1吸附Cd2+、CR前后的XPS能谱

a—吸附前;b—吸附Cd2+后;c—吸附CR后;d—吸附Cd2+、CR后。图10 CTS-1反应前、后S 2p的XPS图谱
由图9(a)看出:有Cd电子峰出现,说明在制备CTS-1过程中生成了CdS,且并成功附着于CTS-1表面,与图2结果一致。对比图9(a)~(d)看出:吸附Cd2+后的CTS-1界面的Cd电子峰强度比吸附前明显增强,说明CTS-1成功吸附Cd2+;吸附CR后的CTS-1界面的S电子峰明显增强,说明CTS-1成功吸附CR。


2.3.4 吸附机制


图11 CTS-1吸附Cd2+和CR的流程
3 结论
1)以壳聚糖为原材料,通过离子印迹技术、环氧氯丙烷交联及硫脲接枝方法制备的改性壳聚糖(CTS-1)比表面积大,表面粗糙,呈现出褶皱的多孔结构。
2)CTS-1可同步吸附废水中Cd2+和CR,且在吸附过程中,Cd2+与CR会相互影响:在Cd2+质量浓度为40 mg/L的复合体系中,CR质量浓度在0~250 mg/L范围内变化时,CTS-1对Cd2+的吸附效果随CR质量浓度增大而降低;在CR质量浓度为150 mg/L的复合体系中,Cd2+质量浓度在0~40 mg/L范围内变化时,CTS-1对CR的吸附速率会随Cd2+质量浓度增加而加快,但在Cd2+质量浓度相同条件下,随反应时间延长而降低。
3)CTS-1对Cd2+和CR的吸附过程符合准二级动力学模型,以化学吸附为主。CTS-1对Cd2+及CR的吸附主要是与CTS-1中的含N、S、O的官能团发生配位作用。CTS-1对Cd2+的吸附机制可能为表面吸附和配合作用,对CR的吸附机制为表面吸附、静电引力及氢键作用。CTS-1对Cd2+和CR吸附具有吸附容量大、吸附速率高等特点,可被广泛应用于含Cd2+或CR废水的治理,具有一定应用前景。

