3D可视化辅助半侧卧后腹腔镜在肾上腺肿瘤切除术中的应用效果*
万 繁,袁仁斌,徐 何,曹 敏,卓 晖
成都市第三人民医院 泌尿外科(成都 610000)
肾上腺肿瘤为临床上常见的肿瘤之一,其在中年人群、老年人群中的发病率分别为4%、10%[1]。目前手术为治疗肾上腺肿瘤的主要方式之一,随着外科微创技术的进展,腹腔镜逐渐被应用于肾上腺相关疾病的治疗,且被公认为肾上腺肿瘤(≤6 cm)手术切除方式的金标准[2]。后腹腔镜肾上腺手术因患者创伤较小,且康复较快,在临床应用广泛。侧卧位入路为手术常用方式,但在此路径中肾脏可阻挡手术视野,术中操作存在一定困难[3-4],而半侧卧位主要在腹侧安置套管,利于病灶显露[5]。以往临床采用二维技术获取的图像并不精确,且操作时缺乏深度感,在操作过程中较依赖手术者经验,易影响手术进程、延长手术时间、造成副损伤[6],因此临床应用存在一定的局限性。3D可视化技术利用术前影像合成图像的新型技术,可辅助术者观察病灶位置、大小及形态,同时可判断周围器官及组织的关系,具有分辨率高、定位准确等优势,有利于临床手术开展。既往临床研究[7-8]多为半侧卧后腹腔镜手术治疗,但关于3D可视化辅助半侧卧后腹腔镜手术研究还较少。因此,本研究探究3D可视化辅助半侧卧后腹腔镜在肾上腺肿瘤(≥3 cm)切除术中的应用效果,现报道如下。
1 资料与方法
1.1 临床资料
选取2017 年2 月至2022 年2 月在成都市第三人民医院收治的接受半侧卧后腹腔镜治疗的134 例肾上腺肿瘤患者进行回顾性分析,根据患者术前是否接受3D可视化分为对照组(n=65)和试验组(n=69)。纳入标准:1)肾上腺肿瘤经B超、CT等影像学确诊;2)影像学图像显示肾上腺肿瘤直径≥3 cm且<10 cm。排除标准:1)双侧病灶患者;2)伴有其他恶性肿瘤或恶性肿瘤疾病史;3)存在确切手术禁忌证;4)伴有严重肝、肾等脏器功能障碍者;5)既往存在肾上腺与肾脏手术者。纳入患者均同意本研究并签署知情同意书,且本研究获成都市第三人民医院伦理委员会审核批准。两组性别、年龄、体重指数、肿瘤类型等一般资料比较,差异无统计学意义(P>0.05)(表1)。
表1 两组一般资料比较[(),n(%)]
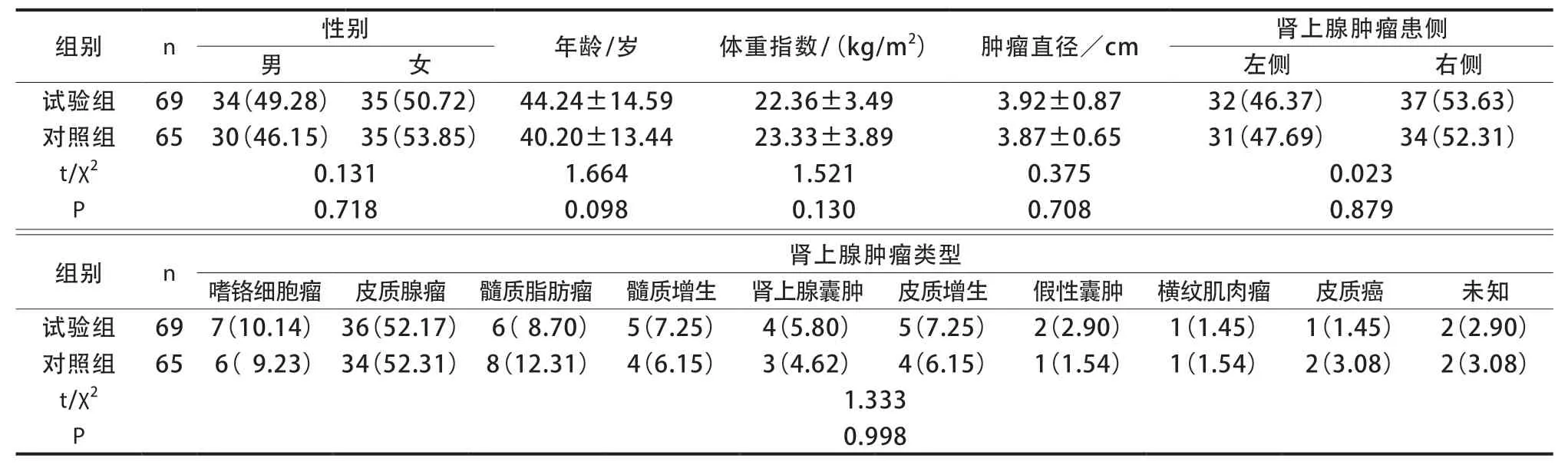
表1 两组一般资料比较[(),n(%)]
?
1.2 方法
术前予以两组患者CT扫描(动脉期、实质期与排泄期)。试验组将CT图像输入成像系统建立3D可视化模型,使用数据云平台进行观看,根据显示的不同颜色对肾上腺、血管走行、肿瘤及周围重要脏器等各种结构进行区分,同时可通过透明化、旋转、放大以获得更好的视觉效果。对照组则不进行3D可视化技术重建。纳入患者均行半侧卧后腹腔镜下手术,具体操作为:气管插管,全麻,嘱患者健侧呈50°~70°半侧卧,建立腹膜后腔,腋中线肋缘下为第一穿刺孔(A点),横向切开1 cm皮肤,撑开腰部肌群,食指将周围筋膜组织分离并向前将腹膜推开;横向切开1 cm皮肤,在食指的指引下清晰避开腹膜,将10 mm套管从腋前2~4 cm处(B点)置入,创立通路,拿出套管后食指由B点进入向前将腹膜推开,横向切开0.5 cm皮肤,腹膜后腔内在食指引导下清除避开腹膜,在A点水平锁骨中线处(C点)置入套管;接着分别于B点、A点位置置入套管,建立腹膜后腔,向前推开腹膜,分离钳穿出C点将套管(5 mm)引入,向上分离(肾前方腹膜外)至肾上极内侧摘除肾上腺,顺着包膜表面分离腺体与病灶,避免对病灶刺激引发不必要的出血。术中使用超声刀对肾上腺动脉分支进行分离,用双重hem-o-lock夹处理肾上腺静脉与其余动静脉,切除肾上腺肿瘤。无出血后将肿瘤装入标本袋,检查肿瘤完整,常规留置引流管。
1.3 观察指标
1)一般资料,包括性别、年龄等两组基线资料;2)手术相关指标,包括预估出血量、副损伤、输血率等;3)术后相关指标,包括拔除引流管、术后开始进食时间与下床活动时间、镇痛药物使用与否等;4)并发症,包括术后肠梗阻、发热、胸膜损伤、感染、切口愈合不佳及腹膜后血肿等情况。
1.4 统计学方法
采用SPSS 25.0统计软件进行统计分析,服从正态分布的定量资料采用()表示,组间比较采用t检验;定性资料采用例数(%)表示,组间比较采用χ2检验或Fihser精确概率。检验水准α除特别说明外均设定为0.05。
2 结果
2.1 两组手术相关指标比较
与对照组比较,试验组估计出血量较少,手术时间较短,差异有统计学意义(P<0.05)。两组副损伤、输血率、中转开放率及血压心率波动率比较,差异无统计学意义(P>0.05)(表2)。
表2 两组手术相关指标比较[(),n(%)]
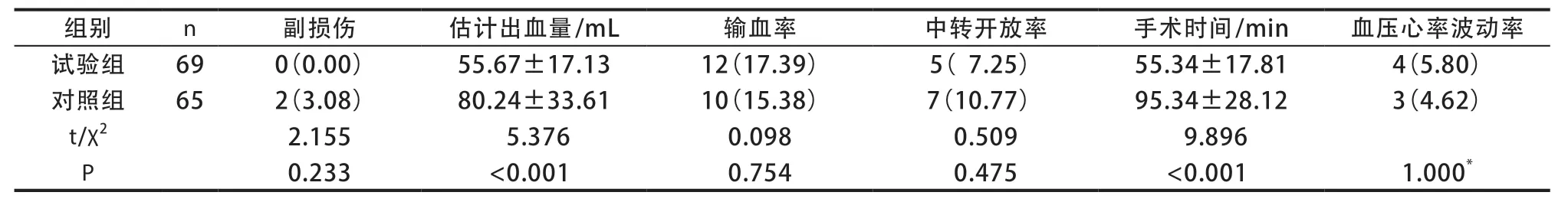
表2 两组手术相关指标比较[(),n(%)]
注:*为Fisher精确概率。
?
2.2 两组术后相关指标比较
试验组术后开始进食时间与下床活动时间短于对照组,差异有统计学意义(P<0.05)。两组拔除引流管时间、术后镇痛药物使用、术后住院时间比较,差异无统计学意义(P>0.05)(表3)。
表3 两组术后相关指标比较[(),n(%)]
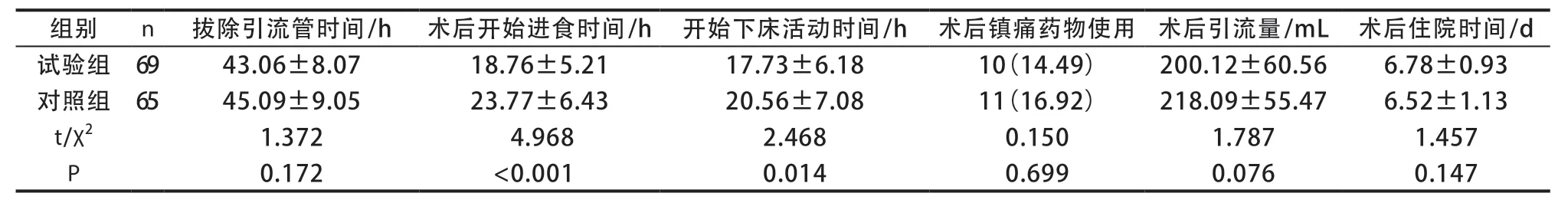
表3 两组术后相关指标比较[(),n(%)]
?
2.3 两组并发症比较
与对照组比较,试验组发热、感染、肠梗阻等并发症的发生率均较低。两组并发症总发生率比较,差异无统计学意义(P>0.05)(表4)。
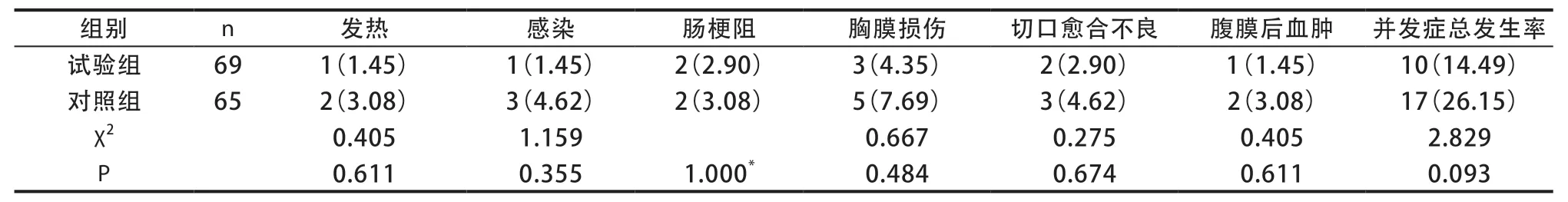
表4 两组并发症比较[n(%)]
3 讨论
有研究[9]显示,肾上腺肿瘤患病率为1.0%~8.7%,且随着年龄的增长其患病率呈上升趋势。腹腔镜因具备独特优势,在肾上腺疾病手术中应用广泛[10]。既往临床多通过经腹入路腹腔镜手术,但经后腹腔入路避免了对其他脏器的干扰,能在观察下直达病灶位置,手术时间更短,且术后患者疼痛较轻,利于术后康复[11]。既往研究[12-14]采用传统腹腔镜系统,该系统获取的是二维平面图像,与直视情况下比较,传统腹腔镜获取的二维图像存在35%~100%的损失,外科医师在观察时无深度感觉,手术定位时需要依赖器械标志或触碰组织进行辨别,不仅阻碍手术进程,还可能对患者组织器官造成损伤,且对于≥3 cm的肾上腺肿瘤患者,二维图像无法成功呈现手术区域复杂的解剖结构。3D可视化技术则可在术前利于外科医师获取患者大量信息,该技术利于术者置管,观察病灶大小、形态、位置及周围情况,构建适合患者的术前计划。较多患者病灶具有内分泌功能,因此要求术者对解剖结构了解透彻,准确定位手术区域,术中精准分离病灶周围组织[15-16]。
本研究结果显示,与对照组相比,试验组估计出血量较少、手术时间、术后开始进食与下床活动时间均较短,差异有统计学意义(P<0.05)。常规CT检查,外科医师仅能对肿瘤周边组织或器官的大致位置进行确定,在肿瘤的干扰下对肿瘤供应血管进行离断较困难,因此需要耗费大量精力与时间,而3D可视化辅助半侧卧后腹腔镜利于手术者精确定位病灶的大小、位置,准确进行手术。另外,术中于肾前方与内上方的位置平面分离,与侧位比较操作空间靠前,避免肾脏对手术入路阻挡,能直接暴露肾上腺、肾上极前内侧或内上方的大病灶,在肾门位置处也可显露切除,手术过程无须添加操作孔[17-18]。而术前常规CT检查下手术者对肿瘤位置与大小较为模糊,手术操作干扰较大,因此试验组术后开始进食时间及下床活动时间均短于对照组。有研究[19-20]采用3D可视化技术对复杂肾肿瘤进行切除发现,与直接进行手术相比,采用3D可视化进行辅助可保留更多肾实质,缩短肾动脉阻断时间,具有良好的临床应用价值,与本研究结果相似,进一步表明采用3D可视化技术在肾上腺肿瘤切除术中应用效果良好。另外,本研究选择肿瘤大小为3~10 cm,更适用于采用后腹腔途径入路。根据3D可视化技术提供的肿瘤血管供应情况,外科医师可对肿瘤相关重要血管进行准确游离;且经腹腔入路具有较大的手术空间,肿瘤占据的视野较少,可在镜下对组织结构进行清晰分辨,快速将肿瘤切除[21-22]。另本研究结果还显示,两组并发症总发生率比较差异无统计学意义(P>0.05),与曹琦等[23]研究存在区别,分析原因可能与本研究纳入样本较少,尤其是肾上腺肿瘤较大的患者较少有关。
综上所述,3D可视化辅助半侧卧后腹腔镜下用于肾上腺肿瘤切除,能有效减少患者出血量,缩短手术时间,且术后开始进食与下床活动时间更短,利于患者术后康复。但由于本研究纳入样本较少,存在一定局限性,后续将通过大样本进一步分析以增加研究可信度。

