固相燃烧法制备LiMg0.02 Mn1.98 O4 正极材料及电化学性能
陈奕妃, 杨 梅, 向明武, 白 玮, 郭俊明
(云南民族大学 云南省高校绿色化学材料重点实验室, 昆明 650500)
锂离子电池作为一种绿色环保的可再充电池,在新能源系统中具有重要的地位.其中,尖晶石型LiMn2O4正极材料因具有锰矿储量丰富、安全环保和晶体结构稳定等优点脱颖而出[1-3].然而,由于存在Jahn-Teller 效应、Mn 溶解和氧缺陷等问题[4-6],LiMn2O4在充放电过程中循环寿命短,特别在高温55 ℃及高倍率下尤为显著,这严重阻碍了其商业化发展.
研究者们发现,元素(如Sc,Ni,Al,Mg 等)掺杂替代尖晶石型LiMn2O4晶格结构中部分高自旋的Mn3+[7-10],会提高Mn 的平均化合态(>+3.5).该方法不仅可以降低Jahn-Teller 效应,还能稳定其晶体结构,提升LiMn2O4的电化学性能.Leong等[7]发现掺杂Sc3+的LiMn2O4材料在0.2 C 倍率、循环50 次后,容量保持率为97.3%,而未掺杂的LiMn2O4容量保持率仅为88.3%.Xu 等[9]制备出的LiAl0.05Mn1.95O4样品在10 C 倍率下,初始放电容量为90.3 mAh/g,循环1 000 次后容量保持率达到80%,而未掺杂的LiMn2O4样品容量保持率仅为66.9%.Mg 在自然界中分布广泛且无毒性,是一种常见的掺杂元素,能有效抑制Jahn-Teller 效应[10-12].另外,掺杂后形成的Mg—O 键能394 kJ/mol 大于Mn—O 键能362 kJ/mol[12],可使[MnO6]八面体骨架更稳定,进而稳定尖晶石型LiMn2O4的晶体结构.Wang 等[12]采用高温固相合成方法合成的LiMg0.04Mn1.96O4材料,在0.1 C 倍率下首次放电容量为113.5 mAh/g,循环500 次后容量保留率为81.05%.王云婷等[13]采用第一性原理计算后发现, 与 LiMn2O4晶格常数(0.825 nm)相比,LiMg0.125Mn1.875O4材料的晶格常数(0.821 nm)和能带间隙(0.006 eV)减小,O 2p和Mn 3d 轨道的成键能力增强,这有效提高了掺Mg 电极材料离子和电子的电导率,还稳定了其晶体结构.Zhao 等[14]采用高温固相法制备的LiMg0.05Mn1.95O4正极材料在1 C 和10 C 倍率下,首次放电比容量分别为 115.3 mAh/g 和72.1 mAh/g,100 次 循 环 后 分 别 有96.8% 和97.5%的容量保持率.此外,解决LiMn2O4正极材料中Mn 溶解问题,除表面包覆外,也可通过调控其单晶颗粒形貌来实现[15-18].Kim 等[18]首次制备出具有高暴露{111}面及少部分{110},{100}面的截角八面体LiMn2O4单晶颗粒形貌正极材料.其中,{111}晶面的Mn 原子排列最紧密,具有最低的表面能[19],可减少LiMn2O4材料中Mn 溶解,提高其晶体结构稳定性;而截角的少部分{110},{100}晶面取向与Li+扩散通道方向相一致,能增加Li+的传输通道数量,提高Li+的传输速率.他们发现,所制备的截角八面体LiMn2O4每次循环均以1 C 充电,10 C 放电,400 次循环后其保持率高达90.8%.Zhu 等[20]采用固相燃烧法合成包含{111},{110}和{100}单晶截角八面体形貌的LiNi0.10Mn1.90O4正极材料,其在10 C 倍率下首次放电比容量为87 mAh/g,经2 500 次超长循环后保持率仍有54.76%.梁其梅等[21]制备的单晶截角八面体LiNi0.08Mn1.92O4正极材料(55 ℃)在1 C及5 C 倍率下,其首次放电比容量分别为109.9 mAh/g 和98.0 mAh/g,循环300 次后容量保持率分别为75.8%和80.5%.上述结果表明,联合元素掺杂和单晶截角八面体形貌调控,既能显著降低尖晶石型LiMn2O4材料的Jahn-Teller 效应,又可有效减缓Mn 溶解,增加Li+传输通道数量,使材料的循环和倍率性能得到提高.然而,关于单元Mg 掺杂单晶截角八面体形貌LiMn2O4材料的研究很少,仅见Llusco 等[22]通过超声辅助Pechini 溶胶-凝胶法合成出包含3 个晶面的单晶截角八面体形貌LiMgxMn2-xO4(x=0 ~0.10)材料,但他们只研究了Mg 掺杂LiMn2O4纳米颗粒的热分解动力学和热力学及其成核和生长,未进行相关电化学性能的探索.
因此,本文中利用元素掺杂和单晶截角八面体形貌控制的策略,采用固相燃烧法制备具有{111},{110}和{100}晶面的LiMg0.02Mn1.98O4样品,以期探究其物相组成、晶体形貌,以及高倍率、长循环的电化学性能和动力学性能等.
1 实 验
1.1 正极材料制备
本实验中以Li2CO3和MnCO3作为原料,Mg(CH3COO)2·4H2O 作为Mg 掺杂剂,并添加原料混合物总质量5%的柠檬酸作为燃料(试剂均为分析纯).按LiMg0.02Mn1.98O4化学计量比,准确称取各物质放于球磨罐中,以无水乙醇为介质,球磨混合10 h 后干燥,可得反应混合物原料粉体.取适量反应混合物放入瓷坩埚中,在恒温500 ℃马弗炉中加热燃烧反应1 h,冷却、研细后,置于700 ℃马弗炉焙烧3 h,而后冷却、磨细得到黑色粉末LiMg0.02Mn1.98O4样品.按照上述相同方法制备纯LiMn2O4正极材料样品,将LiMg0.02Mn1.98O4和LiMn2O4正极材料分别记为LMMO 和LMO.
1.2 材料表征
使用X 射线衍射仪(XRD,D8 ADVANCE 型,德国Bruker)在10°~80°的扫描范围内,扫速为10°/min,分析样品晶体结构(Cu-Kɑ 为辐射源);使用场发射扫描电子显微镜和能谱仪(FESEM 和EDS,NOVA NANOSEM 450 型,美国FEI)对材料的晶体形貌和元素组成进行分析;使用X 射线光电子 能 谱 仪(XPS, K-Alpha+型, 美 国Thermo Scientific)对材料表面的化学组成及元素价态进行分析.
1.3 电化学性能测试
按照1 ∶1 ∶8 的质量比称量黏结剂(聚偏氟乙烯,PVDF)、导电剂(乙炔黑)和正极活性材料,添加适量的溶剂(N-甲基吡咯烷酮,NMP)混匀成浆料,而后均匀涂抹在光面铝箔上,烘干后裁剪成直径14 mm 的正极圆片.在充满高纯Ar 气氛的手套箱中,将正极(正极圆片)、负极(金属锂片)、隔膜(聚丙烯微孔膜,Celgard 2320) 和电解质(1 mol/L LiPF6,EC+DMC+EMC 体积比1 ∶1 ∶1)组装成CR2032 型纽扣电池.采用Land 电池测试系统(CT2001A,武汉金诺电子有限公司)进行恒电流充放电循环性能测试(电压范围3.0~4.5 V,1 C =148 mAh/g).利用电化学工作站(CHI600E,上海辰华仪器有限公司)分别进行循环伏安测试(CV,扫速0.1 mV/s,电压范围3.6 ~4.5 V)和电化学交流阻抗测试(EIS,交流幅值为10 mV,频率范围为1 Hz~100 kHz).
2 结果与讨论
2.1 结构与形貌表征
图1 为LMMO 和LMO 样品的XRD 谱.由图1(a)可知,2 个样品均出现标准尖晶石型LiMn2O4的10 个特征衍射峰(JCPDS No.35-0782),属于立方晶系Fdm 空间群且无杂质峰,这表明Mg 掺杂没有改变LiMn2O4的尖晶石型结构[23].与LMO相比,掺杂Mg 后的LMMO 样品具有较强、较尖锐的衍射峰及较窄的半高峰宽,这是因为Mg 掺杂促进了LiMn2O4晶体的发育[24],使LMMO 样品具有更好的结晶性.从图1(b)中可看出,LMMO 样品的XRD 衍射峰向高角度方向偏移,这说明掺杂Mg 后的LMMO 样品晶格发生收缩.通过Jade 5.0计算可得,LMO 和LMMO 样品的晶格常数分别为0.823 148 nm 和0.821 899 nm, LMMO 样品晶格收缩.这是由于Mg2+(离子半径为0.065 nm)掺杂取代了半径相近的高自旋态Mn3+(0.064 5 nm),而为了维持电中性,半径较小的Mn4+(0.053 nm)数量相对增加[10,24].此外,Mg—O 键能大于Mn—O键能[12],这也会导致LMMO 样品晶格收缩[25].
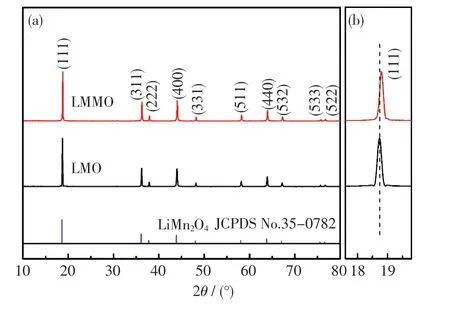
图1 LMO 和LMMO 样品的XRD 谱Fig.1 XRD patterns of LMO and LMMO
图2 为LMO 和LMMO 样品的SEM 图、截角八面体的示意图及LMMO 的EDS 分析结果.从图2(a) 可看出,大多数纯LMO 颗粒是由包含{111},{110}和{100}这3 个晶面的2 个截角八面体形貌颗粒聚集形成的(虚线所示),只有少数为包含{111}和{100}两个晶面(见图中箭头所指)或仅有{111}晶面的标准八面体形貌(见图中虚框所示)的单晶颗粒,并且大部分颗粒发育不完整,没有形成单晶颗粒,颗粒尺寸320 ~390 nm.此外,在晶粒的表面也有极少数形貌不规则的小颗粒.而LMMO 样品颗粒形貌基本均为包含{111},{110}和{100}这3 个晶面的单晶截角八面体,其棱、角更规整,晶界更清晰,颗粒大小分布较均匀,颗粒尺寸约350 nm,但仍有极少数由2个颗粒聚集形成的颗粒,如图2(b)中虚线所示.综上可知,Mg 掺杂促进了LiMn2O4的晶体发育和{110},{100}晶面的择优生长,形成单晶截角八面体颗粒形貌.截角八面体颗粒的晶面是根据图2(c) 建立的八面体面心立方框架的面取向确定[18,26].

图2 LMO 和LMMO 样品的SEM 图、截角八面体的示意图及LMMO 样品的EDS 图Fig.2 SEM images of LMO and LMMO, schematic diagram of a truncated octahedron,and EDS pattern of LMMO
为了检测所合成材料的元素组成,使用能谱仪(EDS)对合成的LMMO 样品进行测试,结果如图2(d)所示.检测到合成产物中有Mn,Mg 和O,Li 的相对分子质量很小,不在检测范围内.所测的金属元素Mn 和Mg 的原子比为1.974 ∶0.020,这与理论合成产物LiMg0.02Mn1.98O4的化学式相符合.
对LMMO 样品中表面元素组成与元素价态进行XPS 分析,结果如图3 所示.由图3(a)和(b)可知,LMMO 材料中存在O,Mn,Mg 和Li,而Mg 1s和Mg 2p 在1 304.1 eV 和49.5 eV 处的特征峰信号,可证明Mg 是以Mg2+的形态掺入LiMn2O4晶格[27].为确定LMMO 样品中Mn 的平均 价 态 及 Mn3+和 Mn4+的 相 对 含 量, 采 用XPSPEAK 对LMMO 的Mn 2p3/2峰进行拟合,得到结合能为641.2 eV 和642.5 eV 的2 个拟合峰,并且分别对应于Mn3+和Mn4+[28].通过进一步分析可知,Mn3+和Mn4+的摩尔分数分别为48.4%和51.6%,这与LMMO 样品的理论值基本一致[见图3(c)].经计算可得,Mn 的平均化合价提高到+3.52,这说明掺杂元素Mg 已经进入LiMn2O4晶格,并对Jahn-Teller 效应起到抑制作用.

图3 LMMO 样品的XPS 图Fig.3 XPS spectra of LMMO
2.2 电化学性能测试
从图4(a)中可看出:LMO 和LMMO 样品的初始放电比容量分别为 122.1 mAh/g 和116.8 mAh/g.这是由于LiMn2O4中作为活性物质的Mn3+被非活性的Mg2+取代,所以LMMO 样品的首次放电比容量略低.在第2 次充放电循环后,LMMO 样品的放电比容量超过LMO 样品,并且随着循环次数的增加,LMMO 样品始终保持较高的容量;经历200 次循环后LMMO 样品容量保持率为78.3%,显著高于LMO 样品的64.8%,展现出较好的循环性能.由图4(b)可知,在3.9 V 和4.1 V处均呈现出2 个特征电压平台,它们分别对应着尖晶石型LiMn2O4电池中Li+的两步脱出和嵌入过程[29-30].根据Yoshio 等[31]提出的首次充电曲线在3.2 V 平台容量(C3.2V)与氧空位(z)之间的定量关系,可以得到LMO 和LMMO 样品的氧空位分别为0.028 和0.024,这表明LMMO 样品的氧缺陷在Mg 掺杂后得到了一定程度的补偿[32].
从图4(c)中可看出,2 个样品的放电比容量随着倍率由0.5 C 逐渐升高到10 C,呈阶梯式下降的趋势,这是由于电极材料的极化作用随着倍率增大而增强[33].在较低的0.5 C 和1 C 倍率下,2 个样品的放电比容量相差不大;但在5 C 和10 C 倍率下,LMMO 样品表现出较为优异的倍率性能.这是因为Mg 掺杂增加了材料的离子及电子电导率,同时还减弱了材料的极化作用,使LMMO 材料在高倍率下仍然保持较高的放电比容量.LMMO 材料在0.5 C倍率时的初始放电比容量为119.9 mAh/g,经不同倍率的30 次充放电循环后,再次回到0.5 C 倍率时仍有97.3%的可逆容量,其展现出较好的电化学可逆性.
为进一步研究样品在高倍率下的长循环性能,在5 C 和10 C 倍率下对2 个样品进行充放电测试,结果如图4(d)和(e)所示.从图中可看出:在5 C 倍率下LMO 和LMMO 样品的初始放电比容量分别为83.5 mAh/g 和102.3 mAh/g,循环1 000次后LMMO 样品的放电比容量仍有初始放电比容量的64.2%,明显优于LMO 样品的52.7%; 在 10 C 倍 率 下, LMMO 样 品 有90.3 mAh/g的初始放电比容量,且1 000 次循环后仍有56.3%的容量保持率,这显著高于LMO 样品(78.3 mAh/g,38.7%),表现出优良的倍率性能和循环稳定性.
为探究Mg 掺杂对LiMn2O4材料高温电化学稳定性的影响,在55 ℃和1 C 倍率下对LMO 和LMMO 样品进行高温性能测试,结果如图4(f)所示.与室温和1 C 倍率下的测试相比,该条件下LMO 和LMMO 样品均拥有较高的初始放电比容量,分别为124.4 mAh/g 和123.0 mAh/g,这是Li+在高温下有较高的迁移速率和电极材料有良好的化学反应活性所致[21].虽然LMO 样品的初始放电比容量比LMMO 样品的略高,但第3 次循环后LMMO 样品的放电比容量始终高于LMO 样品,循环200 次后LMMO 样品的容量保持率有58.0%,明显高于LMO 样品的53.8%,这表明Mg掺杂改善了其高温电化学性能[34].
综上可知,LMMO 材料的高倍率性能及长循环寿命均得到显著的提高.主要原因如下:Mg 掺杂取代了部分Mn3+,有效抑制了Jahn-Teller 效应;Mg 掺杂促进了尖晶石型LiMn2O4样品的晶体发育及{110}和{100}晶面的择优生长,导致单晶截角八面体形貌的产生,降低了Mn 溶解并增加了Li+扩散通道的数量;此外,Mg—O 键能比Mn—O 键能大,对LiMn2O4的晶体结构稳定性起到增强作用.
2.3 动力学性能测试
从图5 中可以观察到,2 个样品均出现两对氧化还原峰,对应于图4(b)充放电曲线的2 个电压平台[29-30],但循环前LMMO 电极的峰面积略小于LMO 电极的峰面积,与图4(a)中首次放电比容量略低于LMO 电极的结果一致.在5 C 倍率下充放电循环1 000 次后,LMO 和LMMO 电极的峰电流和面积均减小,但LMMO 电极的CV 曲线的峰值电流和面积均比LMO 的大得多,且其峰仍保持较好的对称性.上述结果表明LMMO 样品的电化学极化较小,有较好的电化学循环可逆性,这与电化学循环性能结果一致.
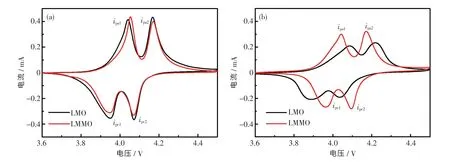
图5 LMO 和LMMO 电极的CV 曲线Fig.5 CV curves of LMO and LMMO electrode materials
为了研究电极材料的动力学过程和内部阻抗,对LMO 和LMMO 样品进行电化学交流阻抗(EIS)测试,结果见图6 和表1.图中高频区截距Rs为电解质溶液的欧姆电阻,中高频区半圆Rct为电荷转移电阻,而低频区直线归于Warburg 阻抗Wo,与Li+扩散系数相关[35].图6 显示了在5 C倍率下1 000 次循环前后样品的Nyquist 曲线,表1 为阻抗的相应拟合结果.可以发现,在循环前后,LMMO 样品均具有较小的电荷转移电阻(Rct分别为102.66,89.82 Ω),较小的Rct值表现出更快的Li+传输速率,这说明Mg 掺杂减少了Li+脱/嵌过程中的阻力,提高了LMMO 的倍率性能,与充放电循环性能结果一致.

表1 LMO 和LMMO 样品的阻抗和Li+扩散系数Table 1 Impedance and Li+diffusivity of LMO and LMMO
为了进一步深入探讨LiMg0.02Mn1.98O4电极材料具有优异倍率性能和长循环稳定性的原因,采用EIS 数据,根据下式计算电极反应的Li+扩散系数DLi+[36].
式中:Z′为Warburg 阻抗;σω为Warburg 常数;ω为角频率,ω=2πf;DLi+为Li+扩散系数cm2/s;R为气体常数,取8.314 J/(mol·K);T为绝对温度,取198.15 K;A为浸入电解液的正极材料面积,取1.5 cm2;n(LiMn2O4,n≈1)为反应过程中转移的电子数;F为法拉第常数,取96 485 C/mol;CLi为Li 在电极中的浓度,取0.023 78 mol/cm3(从4.3 g/cm3理论密度而得).根据式(1)可求出直线斜率σω,代入式(2)可计算出LMO 和LMMO 样品的DLi+分别为6.16×10-16,1.65×10-15cm2/s.LMMO 样品有更大的Li+扩散系数,这是由于Mg掺杂使Li+在LiMn2O4晶格中迁移速率更快,同时也与单晶截角八面体形貌可提供更多的Li+传输通道,以及Mg 掺杂可增加材料的离子、电子电导率等有关,上述结果与LMMO 材料具有良好的倍率性能相佐证.
化学反应的速率与活化能Ea密切相关.通常活化能越大,反应发生所需要的能垒越高,相应的反应速率就越小.为了探究LiMn2O4材料发生电化学反应时Li+脱/嵌所需要的能量,在不同温度下对LMO 和LMMO 样品进行阻抗测试,计算相应的Li+迁移表观活化能[37].
式中:i0和A分别为交换电流和与温度无关常数.根据式(3)和(4),可以求得LMO 和LMMO 样品的Ea分别为33.70,30.67 kJ/mol(见图7).LMMO较小的活化能证明其能够降低Li+在LiMn2O4晶格中迁移过程的反应能垒,这也暗示LMMO 材料具有更好的电化学性能.
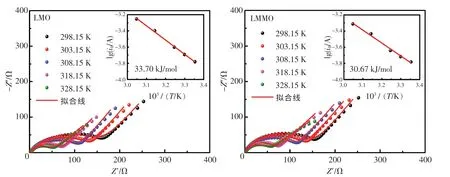
图7 样品在不同温度下的EIS 图Fig.7 EIS spectra of the samples at different temperatures
2.4 循环后的结构分析
为了研究LiMn2O4电极材料在充放电循环过程中的晶体结构变化,对LMO 和LMMO 样品在5 C倍率下循环1 000 次前后的极片进行XRD 表征.由图8(a)和(b)可知: 除集流体Al 箔的衍射峰外,所有电极显示出的衍射峰均与LiMn2O4的特征衍射峰相吻合[23];经1 000 次长循环后,2 个样品的衍射峰强度均降低,但纯LMO 样品的衰减程度较大,如(111)晶面的衍射峰强度仅为循环前的64.6%,而LMMO 样品为75.6%.从图8(c)中可以看出,循环后LMMO 电极材料的颗粒仍然为截断八面体,晶面棱角清晰,与循环前颗粒基本一致.图8(d) 是循环后LMMO 样品XPS 的Mn 2p3/2峰拟合结果.其Mn3+和Mn4+的摩尔分数分别为45.1%和54.9%,与循环前相比,Mn3+的摩尔分数仅降低3.3%.综上分析可知,大倍率充放电循环过程中的Jahn-Teller 效应及Mn 溶解会造成LMO 样品的部分晶体结构坍塌,导致晶格中的Li+迁移通道被破坏,样品的容量快速衰减,而截角八面体颗粒形貌可使LMMO 样品保持较好的晶体结构稳定性.
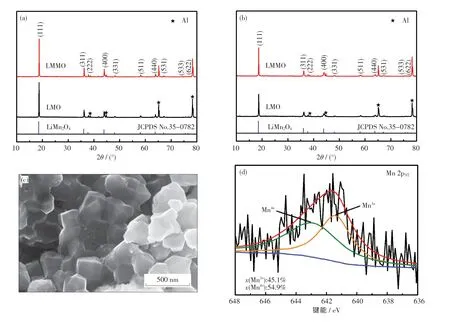
图8 LMO 和LMMO 电极5 C 循环1 000 次后的XRD、SEM 和XPS 图Fig.8 XRD patterns, SEM image and XPS spectra of LMO and LMMO electrode materials after 1 000 cycles at 5 C
3 结 论
(1)采用固相燃烧法制备出具有{111},{110} 和{100} 晶 面 的 单 晶截 角八 面体 形 貌LiMg0.02Mn1.98O4正极材料,Mg 掺杂有效抑制了Jahn-Teller 效应,使Mn 溶解减缓,Li+的迁移通道数量得以增加,同时还促进了其晶体的发育和{110},{100}晶面的择优生长,有利于单晶截角八面体颗粒形貌的形成及晶体结构的稳定.
(2)电化学测试结果表明,Mg 掺杂显著提高了LiMn2O4正极材料的高倍率性能和长循环寿命.在5 C 和10 C 高倍率下,LiMg0.02Mn1.98O4样品首次放电比容量分别为102.3,90.3 mAh/g,1 000次循环后容量保持率仍有64.2%和56.3%.在55 ℃、1 C 倍率及循环200 次后,容量保持率为58.0%.
(3)动力学测试结果表明,LiMg0.02Mn1.98O4样品具有较好的电化学循环可逆性,主要包括较小的电化学极化、较大的Li+扩散速系数(1.65×10-15cm2/s)和较低的表观活化能(30.67 kJ/mol).

