小儿消积止咳口服液治疗儿童慢性咳嗽的机制与效果
瞿 志,李世富,崔庆浩
1.曲靖市妇幼保健院质控部,曲靖 655000;2.曲靖市妇幼保健院门诊部,曲靖 655000;3.曲靖市妇幼保健院药学部,曲靖655000
慢性咳嗽是儿童常见的呼吸系统疾病之一,反复、阵发性咳嗽且病程≥4 周,常伴鼻塞、流涕及打喷嚏等症状[1]。小儿消积止咳口服液是一种祛痰止咳的中成药,已有研究显示,其对慢性咳嗽患儿的临床症状具有良好的改善作用[2]。临床研究结果显示,慢性咳嗽的发生及发展与慢性炎症密切相关,嗜酸性粒细胞(eosinophils,EOS)浸润及炎症细胞激活后释放出大量炎性介质,如降钙素原(procalcitonin,PCT)、肿瘤坏死因子-α(tumor necrosis factor-α,TNF-α)、干扰素-γ(interferon-γ,IFN-γ)和白细胞介素(interleukins,ILs)等,炎性介质过表达可破坏气道结构,从而导致病情进展[3-5]。本研究采用小儿消积止咳口服液治疗慢性咳嗽患儿,并检测外周血免疫指标、炎症指标及肺功能指标变化,旨在为小儿慢性咳嗽的诊疗提供参考依据。
1 资料与方法
1.1 一般资料
选取在本院就诊的慢性咳嗽患儿110 例。
纳入标准:①符合《中国儿童慢性咳嗽诊断与治疗指南(2013年修订)》[1]中的诊断标准;②咳嗽病程≥4 周;③年龄为4~14 岁;④患儿依从性良好,能够配合临床治疗与相关检查、评估;⑤患儿家长知情同意,并且签署了知情同意书。
排除标准:①合并先天性心脏病、先天性呼吸系统疾病者;②合并慢性咽炎、扁桃体炎及其他呼吸系统疾病者;③合并严重心肺功能不全、肝肾功能障碍者;④合并免疫系统疾病、血液系统疾病及重度营养不良者;⑤合并精神疾病或沟通交流障碍者。
1.2 分组
将110 例患儿按照随机数字表法分为对照组与观察组,每组55 例。观察组:男33 例,女22 例,年龄为4~14岁,平均(5.63±0.82) 岁;病程为5~12周,平均(8.14±1.66) 周;发病季节:春季发病20例,夏季发病5 例,秋季发病7 例,冬季发病23 例。对照组:男36 例,女19 例,年龄为4~14 岁,平均(5.77±0.89) 岁;病程为5~12 周,平均(8.02±1.53) 周;发病季节:春季发病21例,夏季发病3例,秋季发病4例,冬季发病27例。另选同期年龄、性别匹配的健康体检儿童55 例作为健康组。3 组儿童的年龄、性别比较差异无统计学意义,且观察组与对照组的病程、发病季节比较差异无统计学意义(P>0.05)。本研究获得医院伦理委员会批准。
1.3 治疗方法
对照组患儿均接受常规抗感染治疗,并口服盐酸氨溴索糖浆,年龄<6 岁的患儿每次2.5 mL,每日3 次;≥6 岁的患儿每次5 mL,每日3 次。观察组在对照组治疗的基础上,口服小儿消积止咳口服液,≤4 岁患儿每次10 mL,每日3 次;>4 岁的患儿每次20 mL,每日3 次。2 组患儿的疗程均为2 周。
1.4 标本采集
在治疗前及治疗后(疗程结束后2 d 内),采集2 组患儿清晨空腹静脉血3~5 mL,健康组于体检当日采血,置于含抗凝剂的真空采集管中,常温下摇匀,用离心机以3 000 r·min-1离心10 min,分离血清,置于-20 ℃冰箱中保存待测。
1.5 检测方法
用全自动血液分析仪检测EOS;用放射免疫法检测血清TNF-α;用酶联免疫吸附试验(enzyme linked immunosorbent assay,ELISA)检测血清PCT、IFNγ、IL-4 和IL-8 水平,ELISA 试剂盒由上海酶联生物科技有限公司提供。用免疫扩散法检测外周血免疫球蛋白(immunoglobulin, Ig)A、IgG、IgM 水平。正常参考范围:EOS 为(0~0.8)×109·L-1(占白细胞总数的1%~5%),PCT 为<0.5 μg·L-1,TNF-α为0.74~1.54 ng·mL-1,IFN-γ为1.21~5.51 μg·L-1,IL-4 为0.45~1.11 ng·mL-1,IL-8 为8.1~21.3 μg·L-1。
用肺功能仪检测肺功能指标,包括用力肺活量(forced vital capacity,FVC)、第1 秒用力呼气量占用力肺活量百分比(the percentage of forced expiratory volume in the first second/FVC%,FEV1/FVC%)和呼气峰值流速(peak expiratory flow rate,PEF)。
1.6 观察指标
①观察并记录观察组与对照组患儿体温恢复正常的时间、肺啰音消失时间及咳嗽消失时间;②治疗前及治疗2 周后,评价咳嗽症状评分:无咳嗽为0 分,日间偶尔咳嗽或仅夜间咳嗽为1 分,频繁咳嗽且轻度影响睡眠及生活为2 分,严重咳嗽且明显影响睡眠及日常生活为3 分;③治疗前及治疗2 周后,用匹兹堡睡眠质量指数(Pittsburgh sleep quality index,PSQI)评价睡眠质量,总分为0~21 分,分值越高表示睡眠质量越差;④根据临床症状及体征评价疗效。治愈:咳嗽消失,肺啰音恢复正常,停药2 个月未见复发;显效:咳嗽频率下降≥2/3,肺啰音消失或明显减轻,停药2 个月无症状加重;有效:1/3≤咳嗽频率下降<2/3,停药2 个月无症状加重;无效:未达上述标准或疾病恶化。总有效率=[(治愈例数+显效例数+有效例数)/总例数]×100%。⑥安全性:观察记录用药期间不良反应的发生情况,随访统计咳嗽相关并发症的发生情况。
1.7 统计学方法
采用SPSS 22.0 统计学软件进行数据分析。无序分类计数资料如不良反应、疗效等用“例(%)”表示,组间比较采用χ2检验;计量资料用(±s)表示,比较采用t检验。P<0.05 为差异有统计学意义。
2 结果
2.1 2 组患儿临床症状消失时间的比较
观察组的体温复常时间、肺啰音消失时间、咳痰消失时间及咳嗽消失时间均较对照组缩短,组间比较差异有统计学意义(P<0.05)。见表1。
表1 2 组患儿临床症状消失时间的比较 (n=55,±s)Tab.1 Comparison of the disappearance time of clinical symptoms between the 2 groups of children (n=55, ±s)

表1 2 组患儿临床症状消失时间的比较 (n=55,±s)Tab.1 Comparison of the disappearance time of clinical symptoms between the 2 groups of children (n=55, ±s)
项目观察组对照组tP体温复常时间/d 2.13±0.85 3.07±1.02 5.250<0.001咳痰消失时间/d 3.64±1.25 4.31±1.72 2.337 0.021肺啰音消失时间/d 5.02±1.04 6.48±1.27 6.596<0.001咳嗽消失时间/d 7.17±1.24 9.33±1.58 7.976<0.001
2.2 2 组治疗前后咳嗽及PSQI 评分的比较
治疗前2 组患儿咳嗽评分及PSQI 评分比较,差异均无统计学意义(P>0.05);治疗后,2 组患儿评分均明显下降,且观察组的下降幅度大于对照组,组间比较差异有统计学意义(P<0.05)。见表2。
表2 2 组治疗前后咳嗽及PSQI 评分的比较 (n=55,±s)Tab.2 Comparison of cough and PSQI scores between the 2 groups before and after treatment (n=55, ±s)

表2 2 组治疗前后咳嗽及PSQI 评分的比较 (n=55,±s)Tab.2 Comparison of cough and PSQI scores between the 2 groups before and after treatment (n=55, ±s)
项目观察组对照组tP咳嗽评分/分治疗前2.69±0.42 2.57±0.41 1.516 0.132治疗后0.65±0.13 0.99±0.34 6.927<0.001 t 34.411 21.999 P<0.001<0.001 PSQI 评分/分治疗前10.05±2.33 9.72±2.19 0.765 0.446治疗后4.11±1.25 6.18±1.02 9.515<0.001 t 16.660 10.867 P<0.001<0.001
2.3 2 组临床疗效的比较
观察组的总有效率较对照组明显提高(P<0.05)。见表3。
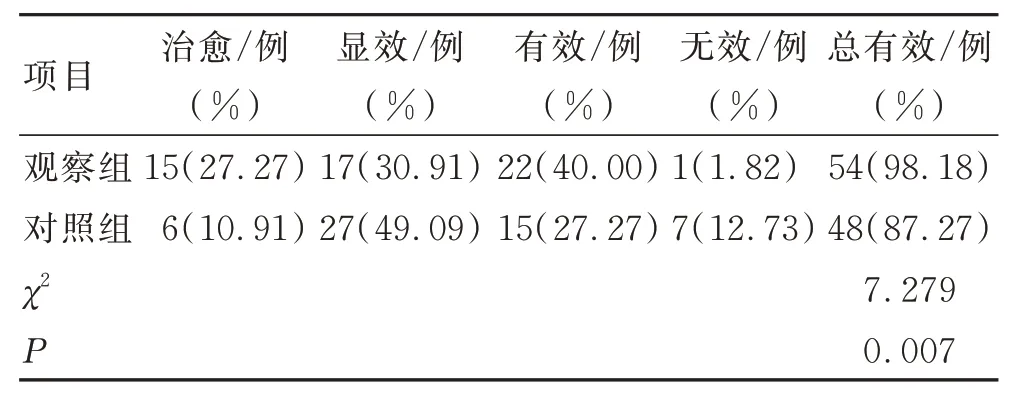
表3 2 组临床疗效的比较 (n=55)Tab.3 Comparison of clinical efficacy between the 2 groups(n=55)
2.4 3 组外周血各指标的比较
治疗前,观察组与对照组患儿的外周血EOS、PCT、TNF-α、IL-4 和IL-8 水平均高于健康组(P<0.05),IFN-γ水平均低于健康组(P<0.05);治疗后,2 组患儿的外周血EOS、PCT、TNF-α、IL-4和IL-8 水平均下降,IFN-γ水平均升高,且观察组的改善幅度明显优于对照组,2 组比较差异有统计学意义(P<0.05);观察组治疗后各指标水平与健康组比较差异无统计学意义(P>0.05)。见表4。
表4 3 组外周血各指标的比较 (n=55,±s)Tab.4 Comparison of the indicator levels in peripheral blood among the 3 groups (n=55, ±s)

表4 3 组外周血各指标的比较 (n=55,±s)Tab.4 Comparison of the indicator levels in peripheral blood among the 3 groups (n=55, ±s)
注:与健康组比较,aP<0.05;与本组治疗前比较,bP<0.05;与对照组比较,cP<0.05。
项目健康组观察组治疗前治疗后对照组治疗前治疗后EOS/(×109·L-1)0.25±0.04 0.43±0.09a 0.28±0.05bc 0.41±0.09a 0.35±0.08b PCT/(μg·L-1)0.39±0.05 0.97±0.23a 0.45±0.12bc 0.95±0.21a 0.61±0.16b TNF-α/(ng·mL-1)0.85±0.23 1.82±0.51a 0.89±0.33bc 1.76±0.46a 1.42±0.37b IFN-γ/(μg·L-1)4.69±1.33 2.42±1.03a 4.54±1.32bc 2.65±1.12a 3.79±1.25b IL-4/(ng·mL-1)0.66±0.21 2.71±0.58a 0.72±0.23bc 2.56±0.54a 1.03±0.31b IL-8/(μg·L-1)12.32±3.04 33.74±6.54a 14.69±3.13bc 31.96±5.98a 19.21±4.25b
2.5 3 组免疫球蛋白水平的比较
治疗前,观察组与对照组患儿的IgA、IgG 和IgM水平均低于健康组(P<0.05);治疗后,2 组患儿的IgA、IgG 和IgM 水平均升高,且观察组的改善幅度均明显大于对照组(P<0.05)。见表5。
表5 3 组免疫球蛋白水平的比较 (n=55,±s)Tab.5 Comparison of immunoglobulin levels among the 3 groups (n=55, ±s)

表5 3 组免疫球蛋白水平的比较 (n=55,±s)Tab.5 Comparison of immunoglobulin levels among the 3 groups (n=55, ±s)
项目健康组观察组治疗前治疗后对照组治疗前治疗后IgA/(g·L-1)2.01±0.34 1.31±0.14 1.95±0.26 1.34±0.16 1.71±0.21 IgG/(g·L-1)12.98±2.05 7.11±1.03 12.24±1.85 7.23±1.15 10.31±1.79 IgM/(g·L-1)1.79±0.35 1.29±0.24 1.69±0.29 1.31±0.25 1.45±0.27
2.6 3 组肺功能参数的比较
治疗前,观察组与对照组患儿的FVC、FEV1/FVC%和PEF 均低于健康组(P<0.05);治疗后,2 组患儿的FVC、FEV1/FVC%和PEF 均升高,且观察组的改善幅度均明显大于对照组(P<0.05)。见表6。
表6 3 组肺功能参数的比较 (n=55, ±s)Tab.6 Comparison of pulmonary function parameters among the 3 groups (n=55, ±s)

表6 3 组肺功能参数的比较 (n=55, ±s)Tab.6 Comparison of pulmonary function parameters among the 3 groups (n=55, ±s)
项目健康组观察组治疗前治疗后对照组治疗前治疗后FVC/L 2.89±0.55 1.42±0.23 1.92±0.43 1.45±0.24 1.66±0.29 FEV1/FVC%92.21%±5.04%76.42%±3.13%88.45%±5.07%78.23%±3.24%84.01%±4.78%PEF/(L·s-1)3.73±1.02 2.12±0.25 3.48±0.94 2.16±0.28 2.97±0.54
2.7 观察组与对照组并发症发生情况的比较
用药期间,2 组患儿均未发生明显不良反应。随访6 个月,观察组发生1 例支气管炎、1 例支气管扩张,并发症发生率为3.64%;对照组发生3 例支气管炎、2 例支气管扩张、1 例肺炎、1 例咳嗽变异性哮喘,并发症发生率为12.73%。观察组的并发症发生率低于对照组,组间比较差异有统计学意义(χ2=4.354,P=0.037)。
3 讨论
临床研究证实,机体免疫-炎症反应紊乱与儿童慢性咳嗽的发生、发展密切相关,大部分慢性咳嗽患儿伴有不同程度的免疫功能失调及持续气道炎症反应[6]。同时,持续炎症反应进一步刺激气管、支气管平滑肌,导致咳嗽反复发作或持续[7]。因此,在儿童慢性咳嗽发生及发展过程中对于免疫反应性慢性炎症的观察与控制成为临床研究的热点。
EOS 以及肥大细胞浸润是儿童慢性咳嗽的主要病理特征之一,EOS 过高被认为是慢性咳嗽发生的危险因素[8]。本研究中,慢性咳嗽患儿的外周血EOS 明显高于健康组(P<0.05),证实了上述观点。PCT 能较为敏感地反映全身炎症反应活跃程度,对于细菌感染的诊断及抗菌治疗效果评估具有一定的参考价值[9]。TNF-α是炎症“瀑布效应”的始动因子,可诱导气道内皮细胞生成黏附分子,刺激气道黏液的分泌及组织纤维增生,诱发气道狭窄[10]。IL-8可对嗜碱性粒细胞以及T 淋巴细胞产生趋化作用而参与炎症调节,可刺激气道壁增厚并使气道管腔狭窄,诱发或加重咳嗽等症状[11]。本研究中,慢性咳嗽患儿的血清PCT、TNF-α和IL-8 水平均明显高于健康组,表明炎症反应参与了慢性咳嗽的发生及发展过程。IFN-γ可激活中性粒细胞、巨噬细胞以及自然杀伤细胞等清除病原微生物,又可协同诱导TNF-α和IL-1β等炎症因子的释放而扩大炎症反应[12]。IL-4可增强淋巴细胞、单核细胞和EOS 等与内皮细胞的结合,促进局部组织的炎症细胞浸润,且可趋化肺泡巨噬细胞,加重气道炎症反应[13]。同时,IL-4 可激活B 淋巴细胞,促进IgG 及IgE 的生成,进一步刺激炎症介质的释放[14]。另有研究发现,IL-4 可刺激黏液糖蛋白的合成,促进杯状细胞的增生以及气道黏液的分泌,还可提高血管通透性,加速平滑肌细胞的增生以及成纤维细胞的趋化,从而参与气道炎症反应以及气道重构过程[15]。部分研究结果显示,IFN-γ低表达而IL-4 过表达可能加重肺损伤[16]。
在本研究中,慢性咳嗽患儿的血清IL-4 水平较健康组明显升高,而IFN-γ水平较健康组明显降低,证实了儿童慢性咳嗽中的Th1/Th2 失衡学说,且以Th2 细胞因子呈优势,这可能是其气道损伤及咳嗽不止的主要原因。与此同时,慢性咳嗽患儿的IgA、IgM、IgG 水平均低于健康组,提示慢性咳嗽患儿存在免疫功能低下现象,考虑为长期咳嗽及伴随症状可导致机体处于高消耗状态,导致免疫功能下降,这也将加重机体免疫相关性炎症反应,进一步增加治疗难度。
本研究结果显示,观察组患儿在加用小儿消积止咳口服液治疗后,体温恢复正常的时间、肺啰音消失时间、咳痰消失时间及咳嗽消失时间均较对照组明显缩短,总有效率较对照组明显提高,且观察组治疗后咳嗽评分及PSQI 评分均较对照组明显降低,表明小儿消积止咳口服液治疗小儿慢性咳嗽可提高临床疗效,促进临床症状及体征的缓解。随访结果显示,观察组的并发症发生率较对照组降低,考虑与观察组咳嗽控制效果更好有关。分析其原因,儿童慢性咳嗽属于中医“久咳”“久嗽”等范畴,病机主要为肺失宣降和气机上逆,病久易损伤肺气而致表卫不固,故可导致咳嗽反复发作。小儿消积止咳口服液由山楂、枳实、槟榔等10 味中药制成,槟榔和山楂具有消食导滞的功效,为君药;瓜蒌、桔梗、枇杷叶及连翘具有宣散肺气、清肺化痰之功,为臣药,且桔梗能够引药直达病灶,兼使药之功;葶苈子、莱菔子与蝉蜕具有泻肺平喘、降气化痰等功效,共为佐药。全方可发挥清肺化痰、止咳平喘、宣肺止咳等功效,可对症治疗该病。药理学研究显示,小儿消积止咳口服液具有抗炎、抗病毒、抗感染、抗氧化及调节机体免疫等作用,故可针对性治疗咳嗽[17-18]。复测治疗后炎症因子亦显示,2 组患儿的外周血EOS、PCT、TNF-α、IL-4 和IL-8 水平均下降,而IFN-γ、IgA、IgG 和IgM水平均明显升高,且观察组的改善幅度明显大于对照组,提示小儿消积止咳口服液能更好地纠正慢性咳嗽患儿的免疫性炎症反应紊乱,也证实慢性炎症与慢性咳嗽的发生及转归有一定相关性。气道高反应性是儿童慢性咳嗽的主要病理基础之一,这与小儿免疫功能、气道结构及功能发育不完善有关,而免疫功能失调及持续炎症反应势必诱发或加重气道高反应性[19]。在本研究中,慢性咳嗽患儿的FVC、FEV1/FVC%和PEF 均较健康组降低,考虑为咳嗽发生时气道平滑肌收缩,致使PEF 下降,而反复发作的咳嗽可导致FVC 和FEV1/FVC%持续降低,进一步增加疾病治疗的难度。经治疗后,2 组患儿的FVC、FEV1/FVC%和PEF 较治疗前明显升高,且观察组的改善优于对照组,考虑为小儿消积止咳口服液的应用能更好地降低气道反应性,缓解气道痉挛,使肺呼吸功能得以恢复,这可能也是观察组预后优于对照组的主要原因之一。
综上所述,慢性咳嗽患儿的外周血EOS、PCT、TNF-α、IL-4 及IL-8 过表达而IFN-γ低表达,应用小儿消积止咳口服液能纠正免疫性炎症反应紊乱,促进临床症状的缓解,提高临床疗效并改善患儿的睡眠质量,这对临床诊疗方案的确定具有参考价值。

