超高效液相色谱-四极杆-飞行时间高分辨质谱用于化妆品中18种非甾体抗炎药筛查和测定
黄佳颖,李杨杰,方继辉,肖树雄,徐新军
(1. 中山大学 药学院,广东 广州 510006;2. 广东省药品检验所,国家药品监督管理局化妆品风险评估重点实验室,广东 广州 510163)
非甾体抗炎药(NSAIDs)外用具有抗炎、抗过敏、祛痘等功效[1],临床上可单独或与糖皮质激素制剂联合使用,以减少糖皮质激素停药后的“反跳现象”[2],也可用于治疗接触性皮炎[3]。但使用不当易引起药物不良反应,轻者表现为药疹,重者则引起继发感染,甚至危害人体生命安全[4-6]。近年来,为了使化妆品达到更快速、显著的美白、消炎等效果,不法分子在化妆品中违法添加禁用物质、国家法定检验方法项目种类内的化学物质时有报道[7-9],其中包括非那西丁等[10]。NSAIDs 若被添加至化妆品中,消费者在不知情下使用存在一定的安全风险。
目前,NSAIDs 的检测方法主要有高效液相色谱法(HPLC)、气相色谱法(GC)、高效液相色谱-串联质谱法(HPLC-MS/MS)、气相色谱-串联质谱法(GC-MS/MS)等[11-17],但大多用于中成药和保健食品检测领域,化妆品中NSAIDs 检测方法的研究较少,我国也未制定化妆品中NSAIDs 的标准检验方法。李静等[18]建立了HPLC 法同时测定牙膏中的4 种NSAIDs,熊爽等[19]建立了UPLC-MS/MS 法测定祛痘类化妆品中氨基比林和保泰松的含量,董亚蕾等[20]采用UPLC-MS/MS 测定了化妆品中的6 种镇痛类化学成分。虽然上述方法的专属性强,但HPLC 法难以满足定性筛查需求;UPLC-MS/MS 仅适用于已知目标物的分析,质谱优化过程繁琐,在无对照品的情况下难以快速初筛判断。超高效液相色谱-四极杆-飞行时间高分辨质谱(UPLC-Q-TOF MS)具有更强的抗基质干扰和高通量检测能力,在无对照品情况下,可结合谱库快速实现样品中未知物的初筛检测,同时通过一级母离子精确质量数进行定量分析[21]。目前,采用UPLC-Q-TOF MS 筛查和测定化妆品中NSAIDs 尚未见报道。因此,建立NSAIDs 的高通量筛查测定方法具有重要意义,可以提高化妆品风险监测靶向性,为化妆品风险预警提供技术支持。
本研究建立了同时测定化妆品中18 种NSAIDs 的UPLC-Q-TOF MS 法,简化了前处理和质谱条件,并对色谱条件进行了优化。所建方法能准确定性和定量测定化妆品中18 种NSAIDs,可为化妆品风险识别提供技术支持。
1 实验部分
1.1 仪器设备
Agilent 1290 InfinityⅡ-6546 超高效液相色谱-四极杆-飞行时间质谱仪(美国安捷伦科技有限公司);X3R 高速冷冻离心机(美国赛默飞世尔公司);Milli-Q Reference 超纯水发生器(美国Millipore 公司);XS205DU电子天平(瑞士Mettler公司);MS3 basic涡旋振荡器(德国IKA公司)。
1.2 材料与试剂
甲酸(质谱纯,德国CNW 公司);甲醇和乙腈(色谱纯,德国CNW 公司);乙酸铵(质谱纯,美国Sigma 公司);甲酸铵(质谱纯,阿拉丁生化科技股份有限公司);实验用水为屈臣氏纯净水;舒林酸、对乙酰氨基酚、酮洛芬、非那西丁、安替比林、普拉洛芬、4-甲氨基安替比林、异丙安替比林、艾瑞昔布、氨基比林、洛索洛芬钠、吡罗昔康、氯诺昔康、氯芬那酸丁酯、美洛昔康、醋氯芬酸、吲哚美辛对照品来自中国食品药品检定研究院;辛可芬对照品购自Alfa Aesar公司。
1.3 实验条件
1.3.1 液相色谱条件色谱柱:ACQUITY UPLC BEH C18(100 mm×2.1 mm,1.7 μm);柱温:40 ℃;流动相A:0.1%甲酸水,流动相B:0.1%甲酸乙腈;流速:0.35 mL/min;进样量:5 μL。梯度洗脱程序:0~1 min,2% B;1~5 min,2%~30% B;5~10 min,30%~40% B;10~15 min,40%~70% B;15~20 min,70%~98% B;20~22 min,98% B;22~22.1 min,98%~2% B;22.1~25 min,2% B。
1.3.2 质谱条件离子源:双喷雾电喷雾离子源(Dual-ESI 源);采集模式:正离子模式;干燥气温度:320 ℃;雾化气压力:241.32 kPa;干燥气流速:8 L/min;毛细管电压:4 000 V;鞘气温度:350 ℃;鞘气流速:12 L/min;喷嘴电压:1 000 V;毛细管出口电压:175 V;锥孔电压:65 V;八极杆电压:750 V;碰撞气:氮气;一级全扫描范围:m/z100~500;二级Target MS/MS 扫描范围:m/z20~500。
1.3.3 对照品溶液的配制分别精确称取18 种NSAIDs 各10 mg 至10 mL 容量瓶中,加入甲醇于室温超声溶解,定容至刻度,摇匀,4 ℃避光贮存。该对照品储备溶液的质量浓度为1 000 mg/L。分别取适量对照品储备溶液,用60%乙腈水配制成质量浓度分别为2.0、5.0、10.0、20.0、50.0、100.0、200.0 μg/L的对照品溶液。
1.3.4 18 种NSAIDs 筛查谱库的建立18 种NSAIDs 的母离子加合方式均为[M+H]+,配制18 种NSAIDs 的对照品溶液,采用正离子模式下TOF 数据采集模式进行扫描分析,识别18种NSAIDs 的一级母离子精确质量数和保留时间,再采用Target MS/MS 模式,在低、中、高3 种碰撞能量下扫描获取18种NSAIDs的二级碎片离子精确质量数和离子丰度比等质谱信息。将各化合物在3种碰撞能量下的子离子谱图导入PCDL 软件中,补充各化合物的中英文名称、分子式、分子量、结构式mol 文件、保留时间、CAS号等信息,在PCDL软件中构建18种NSAIDs的筛查谱库。18种NSAIDs的质谱参数见表1。
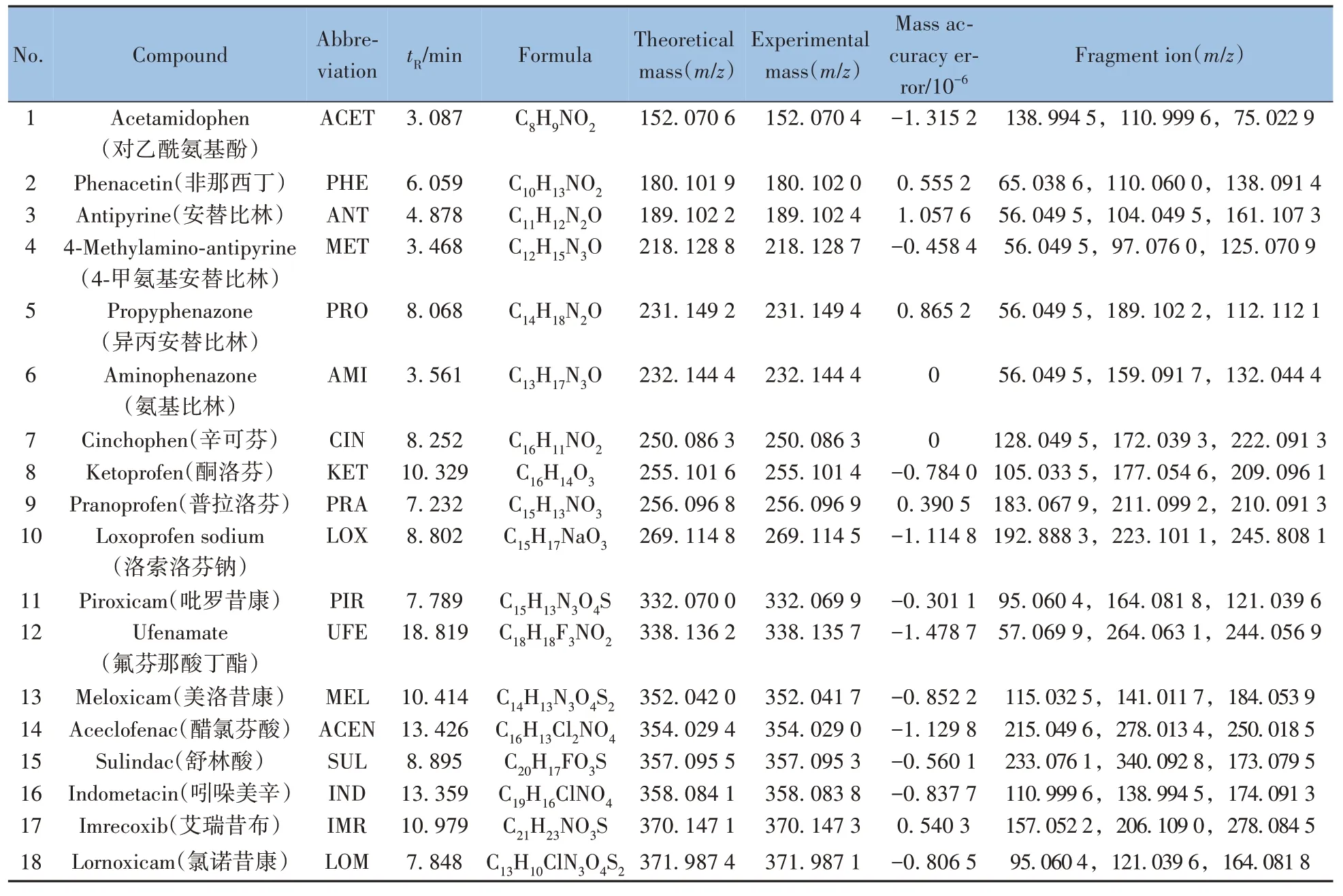
表1 18种化合物的UPLC-Q-TOF MS分析参数Table 1 Analytical parameters of 18 compounds by UPLC-Q-TOF MS
1.3.5 样品的筛查确证与测定取化妆品约0.2 g,精密称定置于10 mL 具塞比色管中,加入60%乙腈水溶液5 mL,涡旋30 s,定容,超声提取15 min,涡旋混合摇匀。取上清液经0.22 μm 滤膜过滤后得供试品溶液,将供试品溶液上机检测进行一级全扫描,得到各化合物的母离子质荷比、保留时间、同位素等信息。通过安捷伦MassHunter 工作站的定性软件匹配数据库分析,同时对保留时间和精确质量数进行检索,设置化合物一级质谱数据打分条件为保留时间偏差小于2 min,母离子质量数偏差小于10 ppm,同位素丰度比差异<5%,综合匹配得分90 分以上则作为疑似阳性样品进行二级子离子扫描;若二级子离子质谱数据分析确证为阳性样品,确证后的目标物则通过外标法定量计算。
2 结果与讨论
2.1 样品提取方法的优化
膏霜和水剂是化妆品的常见基质,本实验通过基质加标考察不同提取条件下18 种NSAIDs 在两种基质中的提取效果。分别考察了化妆品分析常用的两种提取溶剂甲醇和乙腈,通过代入溶剂标准曲线计算提取回收率,结果见图1。由图1可见,4-甲氨基安替比林、氨基比林、氟芬那酸丁酯在甲醇中的提取效率明显高于乙腈,其余化合物均是在乙腈中的提取效率高于甲醇或相当。为兼顾所有化合物的提取效率,使用乙腈作为提取溶剂进行后续实验。

图1 18种NSAIDs在不同提取溶剂中的提取效率Fig.1 Extraction efficiencies of the 18 NSAIDs using different solvents
18 种NSAIDs 的酸碱性存在差异,在酸性条件下有利于酸性或中性化合物溶于有机溶剂,抑制化合物水解[22]。为进一步提高提取效率,考察了不同体积分数(0%、0.1%、0.2%、0.3%、0.5%)的甲酸乙腈溶液对NSAIDs提取回收率的影响。结果表明,随着甲酸体积分数的增加,4-甲氨基安替比林的回收率逐渐降低,这可能是因为其为碱性化合物,加入甲酸可促进离子化,导致检测含量降低。当甲酸为0.5%时,膏霜类化妆品中绝大多数化合物的质谱响应差,回收率异常。因此,本实验选择不加入甲酸的纯乙腈进行提取优化。
进一步考察了不同体积分数(20%、50%、60%、80%、90%、100%)的乙腈水溶液对膏霜和水剂类化妆品样品提取回收率的影响。结果表明,乙腈与水的体积比对对乙酰氨基酚的影响较大。以60%乙腈水溶液为提取溶剂时,对乙酰氨基酚的提取回收率达到最大,当乙腈的比例进一步提高时,对乙酰氨基酚的提取回收率下降,以纯乙腈提取时其回收率在50%以下。其余绝大部分NSAIDs以60%乙腈水溶液为提取溶剂时的回收率均达到80%以上,提取效果较佳。综合多组分的提取效果,最终选用60%乙腈水溶液作为提取溶剂。
2.2 色谱条件的优化
本研究考察了不同流动相体系,包括2 种有机相(甲醇、乙腈)、3 种流动相添加剂(乙酸铵、甲酸铵、甲酸)对18种NSAIDs色谱分离的影响。结果表明,以甲醇为有机相时,氟芬那酸丁酯的洗脱时间超过20 min;乙腈的洗脱能力强于甲醇,以乙腈为有机相时,18 种目标物在20 min 内均被洗脱出来,且各化合物分离良好,因此选择乙腈为有机相。根据前期文献研究[23],在质谱ESI+扫描模式下,甲酸可促进[M+H]+生成,同时流动相中加入挥发性盐也能够提高化合物的离子化效率,故本实验进一步考察了乙腈与水、乙酸铵、甲酸铵、甲酸水溶液等多种流动相条件下的色谱分离效果。结果显示:在水相中加入0.1%甲酸,绝大多数化合物的离子化效率提高,且在有机相中加入0.1%甲酸可进一步改善18 种NSAIDs 的色谱行为;在0.1%甲酸水中加入乙酸铵或甲酸铵溶液时,非那西丁、安替比林、4-甲氨基安替比林、艾瑞昔布的离子响应均下降。因此确定以0.1%甲酸水与0.1%甲酸乙腈为流动相。
由于18 种NSAIDs 的分子结构和化学性质存在差异,实验考察了18 种物质在Waters ACQUITY UPLC HSS T3(100 mm×2.1 mm,1.8 μm)、Waters ACQUITY UPLC BEH C18(100 mm×2.1 mm,1.7 μm)、CAPCELL CORE C18(100 mm×2.1 mm,2.7 μm)、ZORBAX Eclipse Plus C18(50 mm×2.1 mm,1.8 μm)4 种色谱柱上的分离效果。结果显示,采用 BEH C18色谱柱时,美洛昔康、氯诺昔康的峰形较好,不拖尾。此外选用100 mm 色谱柱比50 mm 色谱柱更能实现有效分离,本实验选择BEH C18柱进行色谱分离。
实验发现,纯乙腈溶解时,部分目标物不能在色谱柱上很好的保留洗脱,因此将对照品混合溶液等比例稀释以降低溶剂效应,改善色谱行为。分别考察了不同体积分数的乙腈水溶液(0%、20%、50%、60%、80%、90%、100%)作为进样溶剂时的色谱分离效果。结果表明,当乙腈比例降至60%时,非那西丁、安替比林、普拉洛芬、舒林酸的峰形得到改善,其余化合物的峰形均正常。但当乙腈比例降至60%以下时,绝大多数化合物的质谱响应显著下降。综合考虑,选用60%乙腈水溶液作为稀释溶液。
2.3 质谱条件的优化
18 种NSAIDs 均含有电负性基团,在质谱ESI+扫描模式下易结合氢离子形成准分子离子[M+H]+。在优化的色谱条件下,以UPLC-Q-TOF MS 的一级MS采集模式对目标化合物的单个对照品溶液进行全扫描,通过优化毛细管出口电压以获得最佳响应一级母离子,确定各化合物的保留时间,然后在Target MS/MS 采集模式下对18 种NSAIDs 进行扫描,设定碰撞能量分别为10、20、40 V,获得18 种NSAIDs 的母离子和子离子图谱,得到离子精确质量数和丰度比。将各化合物在3种碰撞能量下的子离子谱图导入PCDL软件中,结合各化合物名称、分子式、分子量、结构式mol文件、CAS号、保留时间等数据构建18种NSAIDs的筛查数据谱库。图2为18种NSAIDs混合对照品溶液在最优条件下的提取离子流色谱图。从图中可以看出,18 种NSAIDs 色谱干扰少,具有较好的分离度和灵敏度,有利于后续准确定量。
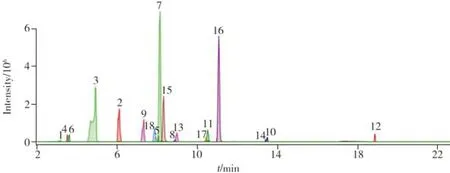
图2 18种化合物的提取离子流色谱图Fig.2 Extract ion chromatogram of 18 compounds peak identification:1.acetamidophen;2.4-methylamino-antipyrine;3.aminophenazone;4.antipyrine;5.phenacetin;6.pranoprofen;7.piroxicam;8.lornoxicam;9.propyphenazone;10.cinchophen;11.loxoprofen sodium;12.sulindac;13.ketoprofen;14.meloxicam;15.imrecoxib;16.indometacin;17.aceclofenac;18.ufenamate
2.4 方法学评价
2.4.1 基质效应考察化妆品的基质较为复杂,样品分析时常存在基质效应,表现为目标离子响应抑制或增强,影响分析结果的准确性。消除基质效应的方法包括同位素内标校正、基质匹配标准曲线、加入分析保护剂等,其中基质匹配标准曲线法操作较为方便[24]。本实验通过对膏霜类和水剂类化妆品的空白基质匹配标准曲线与纯溶剂标准曲线的斜率之比进行比较。若ME<100%,表明基质对分析物存在抑制作用;若ME>100%,表明基质对分析物存在增强作用;若ME=100%,表明不存在基质效应。结果表明,经该前处理方法处理后,4-甲氨基安替比林和氨基比林在水剂化妆品基质中存在基质增强效应,其余组分在两种基质中均存在基质抑制效应(见图3)。为克服基质效应,采用基质匹配工作溶液定量分析。

图3 18种化合物的基质效应Fig.3 Matrix effects of 18 compounds
2.4.2 线性范围、检出限与定量下限本实验分别采用膏霜和水剂化妆品空白样品为基质,配制混合基质标准工作溶液,以化合物的质量浓度(μg/L)和峰面积进行线性拟合,绘制基质匹配标准工作曲线。18种NSAIDs的线性范围、检出限和定量下限见表2。结果表明,非那西丁、安替比林、异丙安替比林、氨基比林、辛可芬、普拉洛芬、吡罗昔康、美洛昔康、氯诺昔康的线性范围为2.00~100.00 μg/L,其余9种化合物的线性范围为5.00~200.00 μg/L,相关系数(r2)均大于0.99。将18种NSAIDs混合基质标准工作溶液逐级稀释至信噪比(S/N)≥3 时确定检出限,S/N≥10 时确定定量下限[25],得到18 种NSAIDs 的检出限为0.001~0.050 μg/g,定量下限为0.004~0.150 μg/g。本方法具有较高的灵敏度,适用于膏霜类和水剂类化妆品中18种NSAIDs的测定。
2.4.3 回收率与相对标准偏差分别选取膏霜和水剂化妆品空白基质样品,进行0.5、1、2.5 μg/g 3个水平的加标回收实验,每个浓度水平平行测定6次,计算18种NSAIDs的平均回收率。在相同实验条件下,连续3 天每天测定6 次,计算18 种NSAIDs 的日内和日间相对标准偏差(RSD)。表3 结果表明,膏霜及水剂两种基质在3 个加标水平下的平均回收率为70.7%~116%,日内RSD(n=6)为0.70%~7.5%,日间RSD(n=3)为3.0%~14%。

表3 18种化合物的回收率及相对标准偏差Table 3 Recoveries and relative standard deviations of the 18 compounds
2.5 实际样品测定
在销售环节采购500 批次化妆品,样品种类包括婴幼儿类、祛痘类、祛斑美白类、舒缓类等,样品性状为无色透明液体、无色凝露、白色膏霜等。应用本方法进行快速筛查检验,在3 个婴幼儿类化妆品中检出对乙酰氨基酚。采用Agilent Q-TOF 的Target MS/MS 采集模式进行质谱分析,用仪器自带软件对样品中化合物的保留时间、母离子及碎片离子精确质量信息、同位素丰度比等与自建谱库进行匹配。设置保留时间偏差为±0.2 min,母离子精确质量数偏差为10 ppm,同位素丰度比差异<5%及其它打分参数。如图4所示,以其中一个样品为例,该样品在3.053 min处出峰,与对照品的保留时间相对应,一级质谱图中存在m/z152.070 4,对应对乙酰氨基酚的[M+H]+峰,且与谱库中对乙酰氨基酚信息一致,初步判断其为阳性样品。

图4 阳性样品中对乙酰氨基酚的提取离子色谱图(A)与一级质谱图(B)Fig.4 Extracted ion chromatogram(A) and MS spectrum(B) for acetaminophen in a positive sample
样品的碎片离子图谱与对乙酰氨基酚对照品的碎片离子图谱见图5,通过与对乙酰氨基酚对照品的二级质谱图对比,发现该样品在高能量通道下既存在对乙酰氨基酚的分子离子峰,又存在二级碎片离子m/z93.033 1 和m/z65.038 4,与对照品的碎片离子图镜相匹配达90%以上,质量数偏差小于10 ppm,通过保留时间、母离子、同位素丰度比、碎片离子等对比确证该样品含有对乙酰氨基酚。通过一级母离子定量分析,3个样品中对乙酰氨基酚的检出含量分别为785、13 822、11 491 μg/g。

图5 对乙酰氨基酚阳性样品(A)和对照品(C)的二级质谱图及镜像对比图(B)Fig.5 MS/MS spectra for acetaminophen from positive sample(A) and standard(C) and mirror comparison spectrum(B)
3 结 论
本研究采用UPLC-Q-TOF MS 建立了化妆品中18 种NSAIDs 的筛查和测定方法,经实际样品考察,该方法前处理步骤简单高效、准确度好、分析速度快,可用于大批量化妆品中18 种NSAIDs 的快速定性定量分析。目前关于化妆品中非甾体抗炎药物检验检测的研究尚少,本方法在一定程度上可为化妆品风险识别提供技术支持。

