镁改性水生植物生物炭吸附水中的微囊藻毒素-LR*
陈 刚 朱赫特 陈浩然 郭雅欣 鲜啟鸣
(1.南方电网电力科技股份有限公司,广州,510080;2.污染控制与资源化国家重点实验室,南京大学环境学院,南京,210023)
微囊藻毒素(microcystins,MCs)是一类由蓝藻产生的环状七肽天然毒素,其中微囊藻毒素-LR(MC-LR)是毒性最强、分布最为广泛的MCs 变体之一[1−2].夏季富营养化的湖泊容易发生蓝藻暴发从而产生较高浓度的MCs,这会给人体健康和生态环境造成危害.MCs 的化学结构稳定,在天然水体中虽然能在光照和微生物的作用下降解,但降解缓慢[3];因此需要采取一些人工手段进行水体治理以去除MCs,减少MCs 带来的危害和风险.常用的MCs 去除方法通常应用于水处理厂,如活性炭吸附、混凝沉淀、化学氧化、超滤、生物膜反应器等[3-4],若在湖泊水体中开展大规模治理,上述方法会有诸多限制.生物炭由于原料来源广泛、制备方便、成本低廉,有较强的污染物吸附能力,此外还具有固碳减排、改良土壤或底质等多重环境效益,近年来在环境领域受到越来越多的研究和应用[5−6].因此,用生物炭来吸附去除水体中MCs 是较为可行的方法.
制备生物炭的原料有农林植物废料、畜禽粪便、餐厨垃圾、沼渣污泥等,水生植物残体也是制备生物炭的常见原料[7].水生植物是湿地生态系统的重要组成部分,具有分布广、产量大、生长快的特点;但到秋冬季节,水生植物往往会枯萎,残体若不及时处理,会腐烂释放出营养物质造成水体污染[8].因此,将水生植物制成生物炭再投放到水体吸附MC-LR,既实现水生植物资源化利用,又能改良水体.
直接热解得到的生物炭的吸附性能通常十分有限,往往不能满足实际工作中去除特定污染物的应用需求[9].为了提升其吸附性能,可通过改性来改善其理化性质[10].氯化镁由于无毒害、腐蚀性小、成本低,是一种较为理想的改性剂[11].将氯化镁用于生物炭改性去除水体中的无机营养盐和重金属有较多的研究,镁改性能在生物炭表面负载含镁矿物,这能增强静电吸引、离子交换、表面络合、化学沉淀从而加强对无机污染物的吸附性能[12−14].虽然将镁改性生物炭用于有机污染物的去除研究较少,但Tao 等研究认为镁改性可用于提升对可离子化有机污染物的吸附性能[15].
目前,利用水生植物生物炭去除MC-LR 的研究较少,而利用镁改性生物炭吸附MC-LR 的研究未见相关报道.本研究在这一方面做新的尝试,利用2 种常见的水生植物苦草(Vallisnerianatans)和狐尾藻(Myriophyllumverticillatum)制备氯化镁改性生物炭,开展其吸附MC-LR 的研究,结合生物炭的表征和吸附特性,探索其改性和吸附机理.
1 材料与方法(Materials and methods)
1.1 材料和仪器
材料:苦草和狐尾藻采集自江苏省无锡市太湖贡湖湾湿地公园.
试剂:MC-LR(≥95%)购自Taiwan Algal Science Inc.;氯化镁(AR)购自上海凌峰化学试剂有限公司;微囊藻毒素检测试剂盒购自Beacon Analytical Systems Inc.;其他试剂均为分析纯.
仪器:酶标仪(Tecan Infinite 200 PRO)、全自动比表面及孔隙度分析仪(Micromeritics ASAP 2460)、有机元素分析仪(Elementar vario EL Ⅲ)、傅里叶变换红外光谱仪(Nicolet Nexus 870)、X 射线光电子能谱仪(Thermo Fisher Nexsa)、X 射线衍射仪(Thermo X'TRA)、马弗炉、pH 计、恒温摇床等.
1.2 实验方法
1.2.1 生物炭的制备
先将采集到的苦草和狐尾藻清洗,去除表面泥沙,晒干并60 ℃烘干至恒重,粉碎至小于20 目.将植物碎末填充到坩埚中,加入与植物碎末质量(g)等数值体积(mL)的MgCl2溶液浸渍24 h,分别设置0.5、1.0、2.0、4.0 mol·L−1的MgCl2浸渍浓度.然后将坩埚置于马弗炉中以3 ℃·min−1升温速率加热至500 ℃,维持3 h 热解.热解完成后冷却至室温,用超纯水清洗、烘干后研磨过筛,取100—200 目颗粒并再次清洗烘干,得到粒度较为均一的氯化镁改性生物炭.用K 指代苦草,H 指代狐尾藻,按照浸渍浓度分别将镁改性苦草生物炭分别标记为KB-0.5Mg、KB-1.0Mg、KB-2.0Mg、KB-4.0Mg;镁改性狐尾藻生物炭分别标记为HB-0.5Mg、HB-1.0Mg、HB-2.0Mg、HB-4.0Mg.
对应地制备500 ℃热解未改性生物炭KB、HB,方法见本课题组先前的研究[16].
1.2.2 生物炭的表征
全自动比表面积孔隙度分析仪测定77 K 温度下生物炭对N2的吸附等温线;有机元素分析仪测定生物炭中C、H、N、O 含量(其中O 元素用氧模式测定);KCl 压片法测定生物炭的傅里叶变换红外光谱(FTIR),波数区间为4000—400 cm−1;X 射线光电子能谱仪对生物炭进行XPS 全谱扫描(结合能1350—0 eV)和特定元素精细谱的扫描;对生物炭进行X 射线衍射(XRD),扫描范围5°—90°,速率10(°)·min−1;采用pH 漂移法测定生物炭的零电荷点(pHpzc)[17−19].
1.2.3 吸附实验
(1)吸附去除率
为了使体系的pH 在吸附过程中维持稳定,以pH 7 磷酸缓冲液(使用0.001 mol·L−1NaH2PO4配制,并用NaOH 调节至pH 7)作为背景溶液配制10 μg·L−1的MC-LR 溶液.取2.0 mg 生物炭添加到上述50 mL MC-LR 溶液中,用螺口玻璃瓶盛装,密封后以180 r·min−1转速25 ℃恒温振荡24 h 后取样.
(2)吸附动力学
取4.0 mg 生物炭添加到上述100 mL 10 μg·L−1MC-LR 溶液中,密封后以180 r·min−1转速25 ℃恒温振荡,每间隔一段时间进行取样.
(3)吸附等温线
以pH 7 磷酸缓冲液为背景溶液配制0—100 μg·L−1不同浓度的MC-LR 溶液,取2.0 mg 生物炭添加到上述不同初始浓度50 mL MC-LR 溶液中,密封后以180 r·min−1转速恒温(分别设置25 ℃和35 ℃)振荡72 h 后取样.
(4)pH 的影响
配制10 μg·L−1MC-LR 溶液,以0.001 mol·L−1NaH2PO4为背景溶液,并用H2SO4/NaOH 调节pH 为4、6、8、10.取2.0 mg 生物炭添加到50 mL 上述不同pH 的MC-LR 溶液中,密封后以180 r·min−1转速25 ℃恒温振荡24 h 后取样.
(5)溶解性有机质(DOM)的影响
用富里酸(CAS: 479-66-3)、单宁酸(CAS: 1401-55-4)、没食子酸(CAS: 149-91-7)做为模式DOM,探讨不同分子量大小DOM 对吸附的影响.配制10 μg·L−1MC-LR 溶液,以pH 7 磷酸缓冲液为背景溶液,分别添加上述DOM 使溶液中DOM 浓度为2 μmol·L−1.取2.0 mg 生物炭添加到50 mL 上述含有不同DOM 的MC-LR 溶液中,密封后以180 r·min−1转速25 ℃恒温振荡24 h.
上述所有吸附实验均进行平行实验,所有样品取约2 mL 用0.45 μm 针头滤器过滤,将滤液保存在玻璃小瓶中,测定溶液在吸附前后MC-LR 浓度.
1.2.4 MC-LR 测定
思政课是思想政治教育的主要阵地,而教师和家长是主导者。“工学结合”模式下,学生一旦走出校门,如果企业尚未形成相应的思想政治教育机制,学生的思想政治教育很可能被忽略。这就要求我们尽可能地转移思想政治教育的战场,与企业联合,拓展丰富的思想政治教育路径,在企业实践中,建立对学生行之有效且符合企业实际的思政教育监管机制,如表1、2、3所示。
使用酶联免疫吸附法(ELISA)测定MC-LR,利用Beacon 公司生产的ELISA 试剂盒进行检测.若样品浓度较高超过试剂盒量程(2.0 μg·L−1),先对样品进行适当比例稀释,再依据说明书的操作流程进行加样、孵育、洗版、显色,用酶标仪测定450 nm 吸光度最终计算MC-LR 浓度,检测限为0.1 μg·L−1.所有样品及平行样品均进行复孔测定.
2 结果与讨论(Results and discussion)
2.1 生物炭表征
2.1.1 比表面和孔隙度分析
对未改性生物炭KB、HB 和镁改性生物炭KB-2.0Mg、HB-2.0Mg 进行N2吸附等温线(77 K)的测定,利用BET 模型计算生物炭的比表面积SBET,根据等温线P/P0≥0.99 处的N2吸附量计算生物炭的总孔孔容Vtot,利用DFT 模型计算生物炭的孔径分布.根据孔径分布计算出微孔(孔径≤2 nm)孔容Vmic和中孔(2 nm<孔径≤50 nm)孔容Vmes.其中未改性生物炭的部分表征结果引自本课题组先前的研究[16].
从孔径分布图(图1)可以看出,镁改性生物炭在不同孔径下对应的孔容均高于未改性生物炭.表1也表明,镁改性生物炭比表面积和孔容明显高于未改性生物炭,且中孔的增加明显,说明氯化镁改性能够促进生物炭孔隙的形成.研究表明,氯化镁改性能够使生物炭表面产生鳞片状MgO 颗粒,该结构有助于提升生物炭的比表面积[20].此外,MgCl2在高温下能与H2O 反应,形成Mg(OH)2、Mg(OH)Cl、MgO 等产物,并释放HCl 气体,该过程会改变生物炭的孔隙结构,促进孔容的增加[21−22].

表1 生物炭的比表面和孔径分析Table 1 Specific surface and pore size analysis of biochar
2.1.2 元素分析
生物炭的元素分析结果见表2.其中C、H、O、N 元素含量由元素分析仪测定得到的质量分数,而Mg 元素含量由XPS 全谱扫描分析得到的原子数占比.通常,O/C 和(N+O)/C 可反映生物炭的亲水性和极性,O/C 和(N+O)/C 的值越大表示亲水性和极性越强;H/C 可反映生物炭的芳香性,值越小则芳香性越强[23−24].结果显示,氯化镁改性使生物炭的极性和亲水性增加,而芳香性降低.改性苦草生物炭中Mg 元素含量比改性狐尾藻生物炭更高,可见不同植物材料会影响改性过程中Mg 元素的负载.
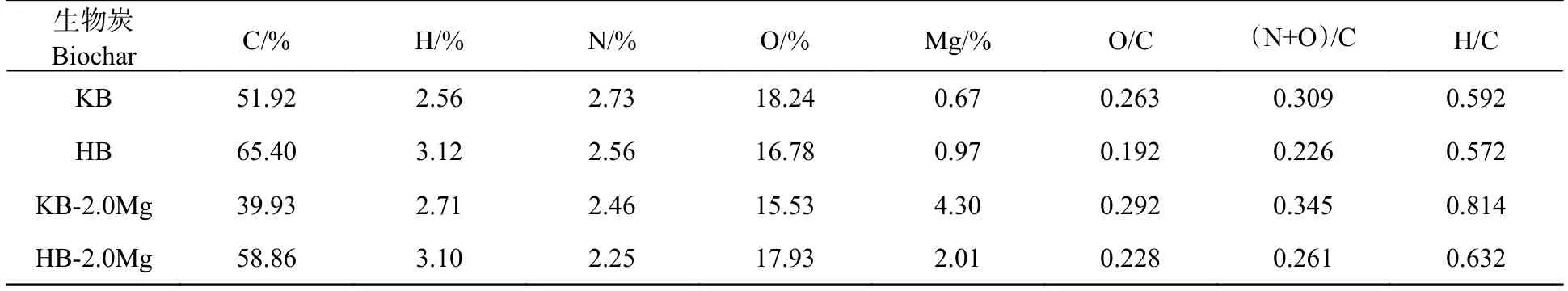
表2 生物炭元素分析Table 2 Elemental analysis of biochar
2.1.3 官能团和元素形态分析
XPS 表征结果见图3.图3(a,b)是XPS 全扫图,可以看出未改性生物炭中除了含有C、N、O 元素,还存在Si、Al、Ca、Na 等矿物盐类元素;氯化镁改性使生物炭的XPS 全谱中出现明显的Mg(1s)谱峰,也带入一定量的Cl 元素.将生物炭的C(1s)精细谱用Avantage 软件进行分峰拟合,结果见图3(c,d).峰值为284.8 eV 的峰代表C—C 中的C 元素;286.1—286.2 eV 处代表C—O;287.5—287.6 eV 处代表醛或酮的C=O;288.8 eV 处代表羧基或酯基的O—C=O[34−35].此外,290.0—290.2 eV 处是π−π*峰,是芳环中的离域电子跃迁形成的[34,36].这说明生物炭具有富π 电子的表面,能与MC-LR 分子中含共轭结构的胍基发生π+−π 电子供体-受体(π+−π EDA)相互作用而利于吸附[37].氯化镁改性使C—C 中C 元素占总C 元素的比例下降,而C—O 和O—C=O 占比上升,这表明氯化镁改性使生物炭的含氧官能团增加.图3(e,f)是Mg(1s)的分峰拟合谱图,可以看出镁改性生物炭的Mg(1s)谱峰明显强于未改性生物炭,且Mg 元素主要以Mg(OH)2和MgO 的形式存在,1303.3—1303.4 eV 的峰代表Mg(OH)2,1304.0—1304.2 eV 的峰代表MgO[38−40].
对未改性生物炭KB、HB 和镁改性生物炭KB-2.0Mg、HB-2.0Mg 进行XRD 表征,并通过比对ICDD PDF-2 2004 标准谱图进行物相鉴定,结果见图4.从图4 可以看出,镁改性生物炭中含有Mg(OH)2(PDF 卡号:44-1482)和MgO(PDF 卡号:45-0946)的衍射峰,这说明镁改性生物炭中含有Mg(OH)2和MgO 结晶,这也进一步佐证了XPS 中的分析结果.此外,生物炭中还含有CaCO3(PDF 卡号:05-0586)和SiO2(PDF 卡号:46-1045)等矿物成分.

图4 生物炭的XRD 谱Fig.4 XRD spectra of biochar
2.1.4 零电荷点
用pH 漂移法测定生物炭的零电荷点(pHpzc),其测定原理是将生物炭投加到不同初始pH 的Na2SO4电解质溶液中,当溶液的pH<pHpzc时,生物炭会净吸附H+,使溶液pH 升高;当溶液的pH>pHpzc时,生物炭会净吸附OH−,使溶液pH 下降;而pH=pHpzc时,则溶液pH 不变[41].因此,以溶液初始pH(Initial pH)为横坐标、混合24 h 之后的pH(Final pH)为纵坐标作图,用曲线连接,曲线上Initial pH=Final pH 的点即pHpzc[17−18],结果见图5.可以看出,未改性生物炭和镁改性生物炭的pHpzc>7,这说明在中性水体中生物炭表面会净吸附H+而带正电[42],而MC-LR 分子在中性条件下带负电[43],因此生物炭与MC-LR 分子之间存在静电吸引作用.镁改性生物炭的pHpzc高于未改性生物炭,且苦草和狐尾藻制得的生物炭在镁改性后pHpzc值基本相同.研究表明Mg(OH)2和MgO 有较高的pHpzc,分别在10.8—12 和9.8—12 之间[44],因此改性负载MgO 和Mg(OH)2能提高生物炭的pHpzc.
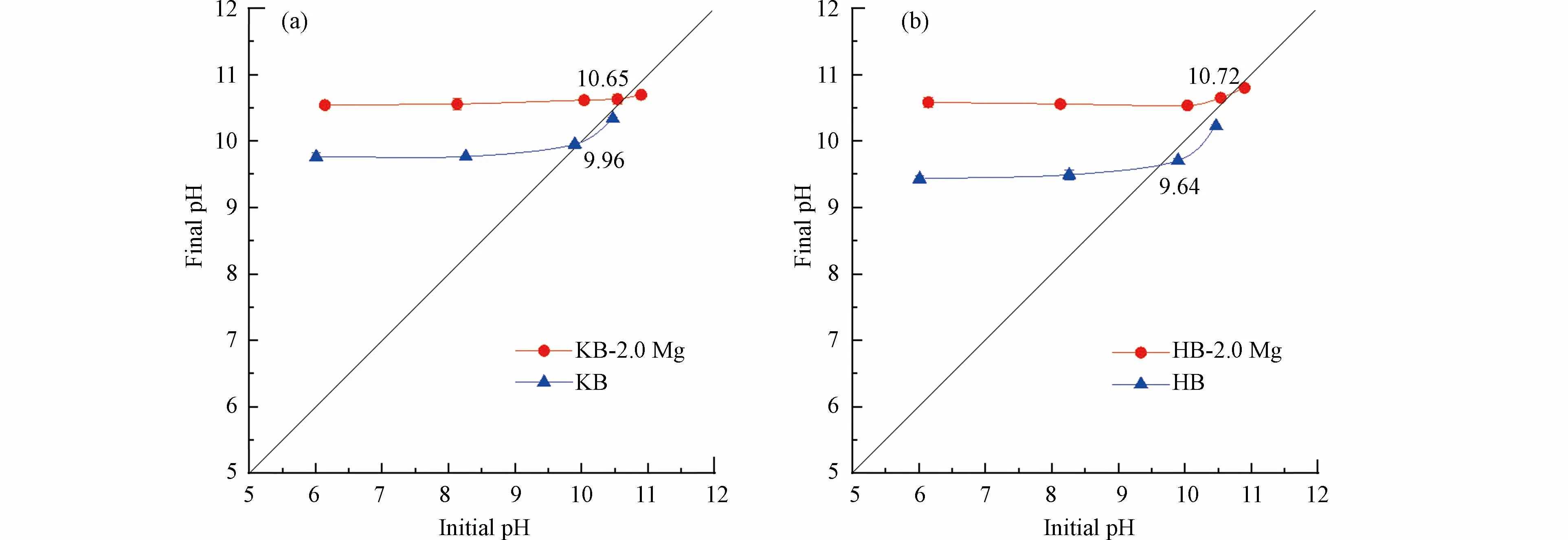
图5 生物炭的零电荷点测定(a)苦草生物炭Vallisneria biochar;(b)狐尾藻生物炭Myriophyllum biocharFig.5 pHpzc determination of biochar
2.2 生物炭对MC-LR 的吸附去除率
比较未改性生物炭和不同镁浸渍浓度制备的镁改性生物炭对MC-LR 的吸附去除性能,投炭量为2.0 mg/50 mL,MC-LR 去除率见图6.从图6 可以看出,MgCl2浸渍浓度为2.0 mol·L−1制备得到的镁改性生物炭对MC-LR 的吸附性能最佳;与未改性生物炭相比,镁改性生物炭对MC-LR 吸附性能有明显的提高.研究表明,MC-LR 的分子尺寸为1.9 nm×1.5 nm×1.1 nm[45],由于体积排阻效应MC-LR 分子无法进入微孔,中孔填充是生物炭吸附MC-LR 的重要机制[34,37].生物炭的表征结果已表明,镁改性使生物炭的比表面积增大,尤其中孔孔容增加明显,从而提升了生物炭的吸附性能;此外,生物炭表面的含氧官能团能与MC-LR 中的氨基、羧基形成氢键[46],而镁改性能使生物炭的含氧官能团增加,有利于对MC-LR 的吸附.镁改性生物炭的pHpzc要高于未改性生物炭(图5),表明镁改性生物炭在溶液中能吸附更多H+而带有更多的正电荷[41],能与带负电的MC-LR 分子产生更强的静电吸引力,有利于吸附.

图6 未改性生物炭和不同MgCl2 浸渍浓度制备的镁改性生物炭对MC-LR 的去除率(投炭量2.0 mg/50 mL,图中K 和H 分别表示苦草和狐尾藻生物炭,浸渍浓度标记为0 的表示未改性生物炭)Fig.6 The removal rate of MC-LR of unmodified biochar and Mg-modified biochar prepared with different MgCl2 soaking concentration(carbon addition: 2.0 mg/50 mL.K and H represented Vallisneria and Myriophyllum biochar respectively,and the soaking concentration marked 0 represented the unmodified biochar)
2.3 吸附动力学
研究未改性生物炭KB、HB 和镁改性生物炭KB-2.0 Mg、HB-2.0 Mg 对MC-LR 的吸附动力学.用式1 计算吸附量,使用OriginPro 2018 软件将动力学数据用式(2—5)拟合[47−49]:
式中,t表示吸附时间(h);qt为t时刻的吸附量(μg·g−1);C0和Ct分别为初始MC-LR 浓度和t时刻的MC-LR 浓度(μg·L−1);V代表溶液体积(L);m代表生物炭的质量(g).qe、k1、k2、α、β、ki、Ci则是各模型拟合计算得到的参数,其中qe代表计算得到的平衡吸附量(μg·g−1).
准一级、准二级动力学和Elovich 模型的拟合图形见图7(a,b),拟合参数见表3.通过比较拟合优度R2,KB 和KB-2.0Mg 的吸附过程用准一级动力学拟合效果较好,而HB 和HB-2.0Mg 的吸附过程则更符合Elovich 和准二级动力学模型.通常,准一级动力学用于描述物理作用主导的吸附,如液膜扩散机制等[50−51];准二级动力学用于描述化学吸附作用,如配位络合、电子的得失和共享、化学键的形成等机制[52];Elovich 可反映发生在异质性表面的化学吸附[49,53].
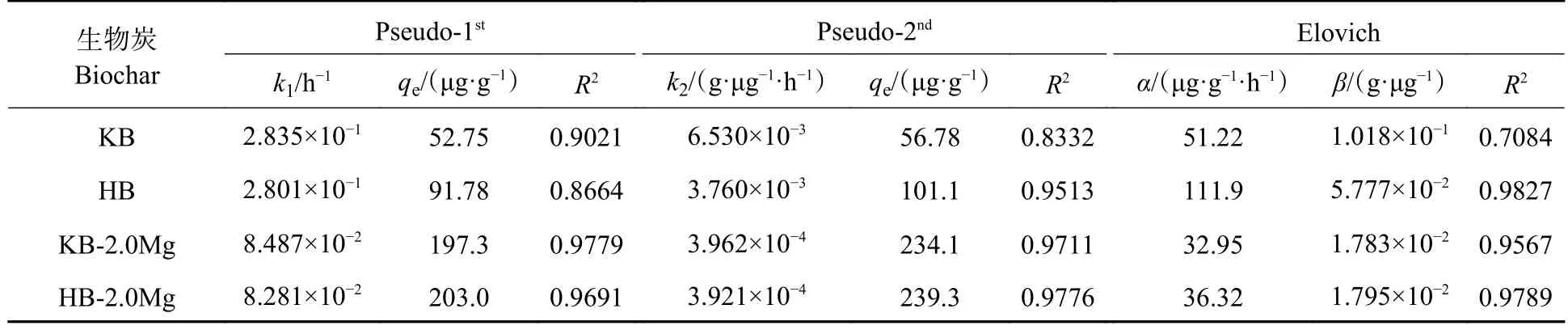
表3 吸附动力学拟合参数Table 3 Fitting parameters of adsorption kinetics
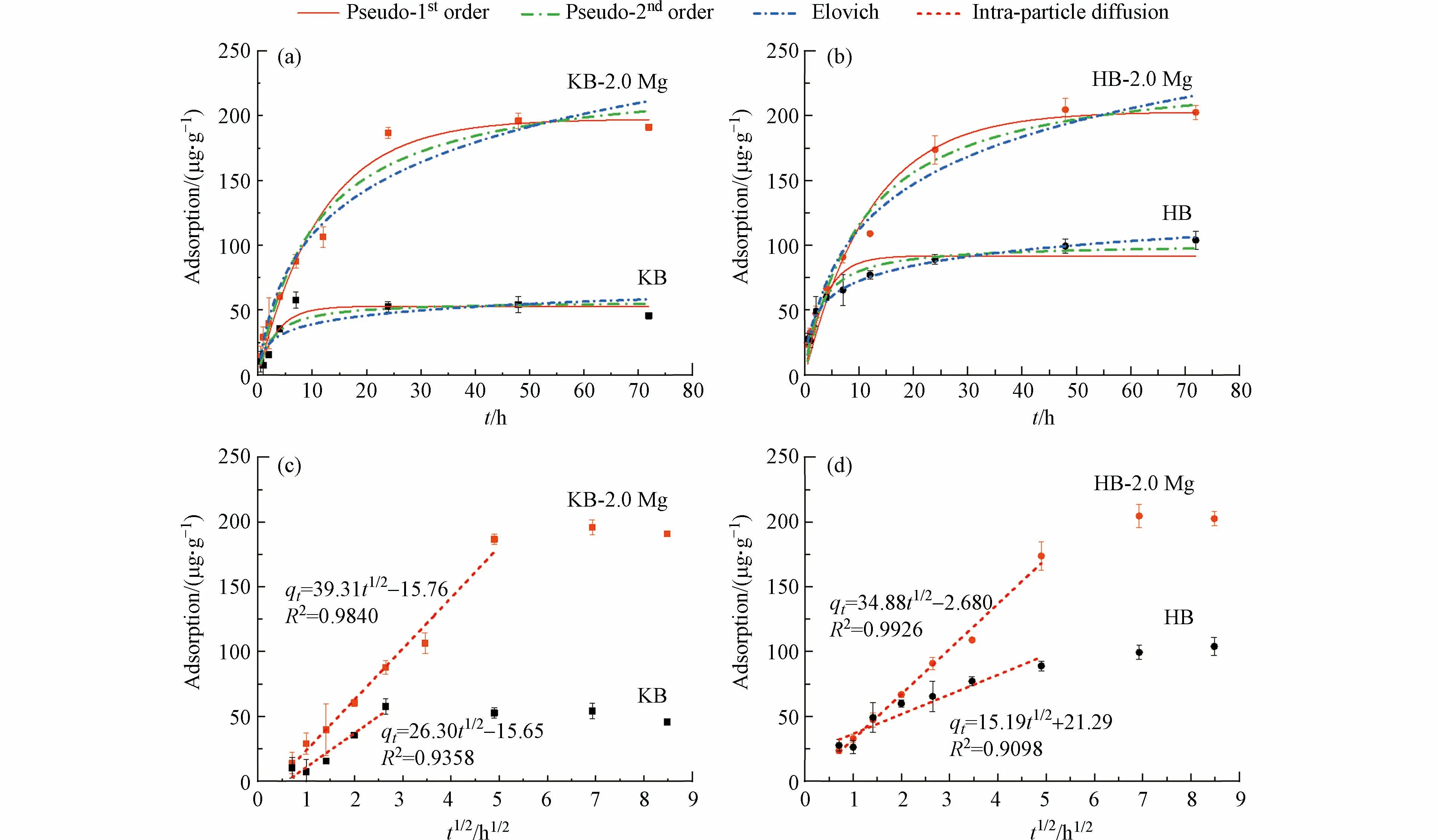
图7 镁改性及未改性生物炭吸附MC-LR 的吸附动力学苦草(a)和狐尾藻(b)生物炭准一级、准二级动力学和Elovich 模型拟合;苦草(c)和狐尾藻(d)生物炭的颗粒内扩散模型分阶段拟合Fig.7 Adsorption kinetics of MC-LR on Mg-modified and unmodified biocharfitting of pseudo-1st order,pseudo-2nd order,Elovich models of Vallisneria(a)and Myriophyllum(b)biochar;fitting of intra-particle diffusion model of Vallisneria(c)and Myriophyllum(d)biochar in stages
吸附过程一般可分为外部液膜扩散阶段、颗粒内扩散阶段、吸附平衡阶段[54].从图7(c,d)可以看出,在前期吸附未达到平衡时的阶段,颗粒内扩散模型较好地拟合,由此可见颗粒内扩散也是吸附的重要阶段性机制.
2.4 吸附等温线
测定并计算在不同吸附平衡浓度下生物炭对MC-LR 的吸附量(式6),利用Langmuir 和Freundlich 模型(式7—8)拟合绘制吸附等温线[55−56]:
式中,qe为平衡吸附量(μg·g−1),Ce为平衡浓度(μg·L−1),qm、KL、KF、n均为模型拟合得到的参数,其中qm代表拟合计算得到的最大吸附量(μg·g−1).
等温线拟合参数列于表4,拟合图形见图8.Langmuir 模型假设吸附过程是发生在均质表面的单层吸附,且吸附质分子间无相互作用力;Freundlich 模型是经验模型,对非均质表面以及多层吸附有较好的拟合效果,对物理吸附和化学吸附均适用[57].对于KB 和HB,Langmuir 模型和Freundlich 模型的R2相差不大,说明生物炭吸附MC-LR 机制是复杂的,既存在均一的单层吸附,也存在发生在非均质表面上的多层吸附.35 ℃的qm要高于25 ℃,表明提高温度能提升生物炭对MC-LR 的吸附容量.
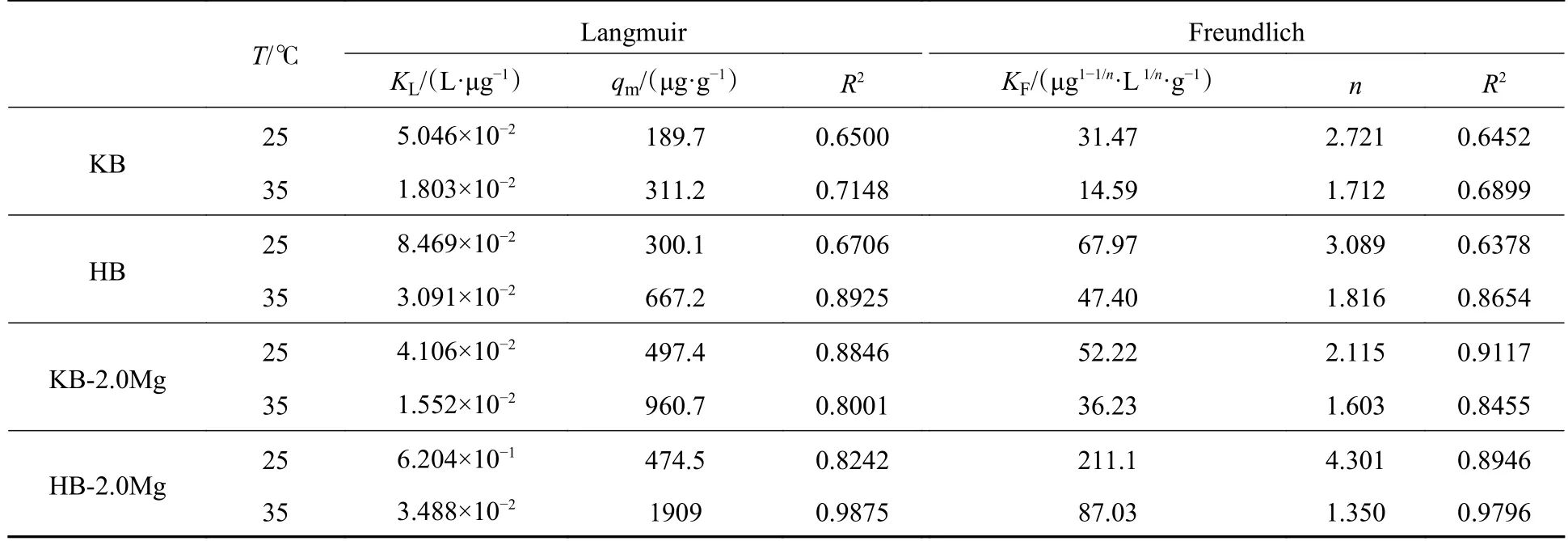
表4 吸附等温线拟合参数Table 4 Fitting parameters of adsorption isotherm
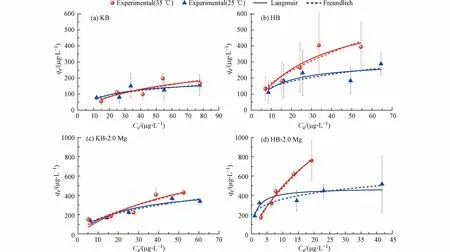
图8 吸附MC-LR 的吸附等温线KB(a)、HB(b)、KB-2.0Mg(c)和HB-2.0Mg(d)的Langmuir 和Freundlich 模型拟合Fig.8 Adsorption isotherm of MC-LR adsorption: fitting of Langmuir and Freundlich models of KB(a),HB(b),KB-2.0Mg(c)and HB-2.0Mg(d)
2.5 吸附影响因素
2.5.1 pH 的影响
图9 显示了不同pH 条件下生物炭对MC-LR 的去除率.由图9 可以看出,不同pH 会影响去除率的大小,由于MC-LR 在强酸碱条件下仍能保持稳定不易分解[58],说明实验结果去除率的差异取决于生物炭吸附的差异.pH 升高对未改性生物炭的吸附性能有抑制作用,尤其在pH 10 的条件下其对MCLR 的去除率明显下降;而镁改性生物炭受pH 的影响较小,仅pH 升高到10 时其吸附性能略有下降.研究表明,MC-LR 分子中的羧基和氨基在不同pH 下会发生电离或离子化,使分子带有不同的净电荷:pH<2.09 主要以MCLR+形式存在,pH 2.09—2.19 主要是MCLR0,pH 2.19—12.48 主要是MCLR−,pH>12.48 则主要是MCLR2−[43].可见在pH 4—10 区间主要以MCLR−存在.由于镁改性生物炭的pHpzc>10,其在pH 4—10 带正电,与MC-LR 分子存在静电吸引;未改性生物炭pHpzc9—10,其在pH 4—8 带正电与MC-LR 分子存在静电吸引,而在pH 10 生物炭几乎不带电或带轻微负电,存在静电排斥.研究表明,pH 的降低能使生物炭表面的净正电荷增加[59],从而增强静电吸引,这可能是较低pH 下有着较高的吸附去除率的原因.此外,pH 降低还能使MC-LR 分子发生卷曲,使分子体积减小,从而促进吸附[60].
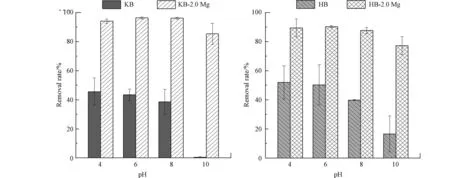
图9 pH 对生物炭吸附去除MC-LR 的影响Fig.9 The effect of pH on the removal of MC-LR by biochar
2.5.2 DOM 的影响
由于天然水中存在DOM,为探讨DOM 对吸附的影响,选用没食子酸(GA)、富里酸(FA)、单宁酸(TA)做为模式DOM 开展研究,结果见图10.从图10 可以看出,添加GA 对生物炭吸附MC-LR 的几乎没有影响,而添加FA 和GA 对吸附有明显的抑制作用.MC-LR 的分子量为995.2 g·mol−1,分子尺寸为1.9 nm×1.5 nm×1.1 nm[45],如前文所述主要占据生物炭的中孔;而GA 分子量(170.12 g·mol−1)和分子尺寸(0.90 nm×0.63 nm×0.28 nm)较小,主要占据微孔[61],与MC-LR 的吸附几乎不会发生竞争作用,因此GA 的添加对吸附的影响小;FA 的分子量(308.24 g·mol−1)大于GA,竞争作用加强,导致生物炭吸附MC-LR 减弱;TA 分子量(1701.2 g·mol−1)和分子尺寸(1.93 nm×1.73 nm×1.32 nm)较大,依赖中孔填充吸附[61],与MC-LR 分子竞争吸附明显,其更大的体积还会阻塞孔道,使MC-LR 分子难以进入合适大小的孔隙[62−63],因此TA 的添加能产生明显的抑制作用.DOM 对未改性生物炭的抑制作用表现为TA>FA>GA;而对于镁改性生物炭,TA 与FA 的抑制作用相近,这可能是因为氯化镁改性使生物炭的中孔增加,使其不再那么“稀缺”,因而在一定程度缓解了TA 和MC-LR 对中孔的竞争.

图10 DOM 对生物炭吸附去除MC-LR 的影响Fig.10 The effect of DOM on the removal of MC-LR by biochar
3 结论(Conclusions)
(1)用MgCl2溶液浸渍水生植物苦草和狐尾藻,热解制备镁改性生物炭.氯化镁改性使生物炭的比表面积和孔容增加,尤其是中孔的增加,表面含氧官能团增加.镁改性生物炭表面负载了MgO 和Mg(OH)2,并具有更高的pHpzc值.
(2)镁改性生物炭比未改性生物炭对MC-LR 有更强的吸附性能,以2.0 mol·L−1的MgCl2浸渍制备的生物炭对MC-LR 有最佳的去除效果.准一级、准二级动力学、Elovich 和颗粒内扩散模型能在不同程度较好地描述吸附过程.吸附等温线符合Langmuir 和Freundlich 模型,且较高的温度能提升吸附容量.较高的pH 和较大分子量的DOM 会抑制生物炭对MC-LR 的吸附,镁改性生物炭会使pH 和DOM 对吸附的影响减弱.
(3)生物炭对MC-LR 的吸附机理是复杂的,可能同时存在物理吸附和化学吸附作用,既存在均一的单层吸附,也可能在非均质表面上发生多层吸附.此外,颗粒内扩散是吸附的重要阶段性过程.中孔填充是生物炭吸附MC-LR 的重要机制,生物炭和MC-LR 分子间可能存在氢键、静电吸引和π+−π EDA 相互作用力.镁改性能增强中孔填充作用,并加强氢键和静电吸引力从而增强吸附.

