乳腺癌患者保乳术中放疗与术后全乳放疗的疗效、安全性及美容效果比较
赵 阳 杨红杰 孔舒欣 韩 倩
在女性妇科肿瘤中,以乳腺癌较为常见。据调查显示,全球每年乳腺癌新发病例达226万人,在妇科肿瘤中的占比约为1/4,已成为女性的首要健康杀手[1]。该病主要表现为乳房胀痛、乳头溢液,如未及早施治,致使病灶转移,可增加预后不良风险。近年来,随着诊断效力的不断提升,早期乳腺癌检出率愈来愈高[2]。目前,对于本病早期患者已由既往的根治性手术转向保乳手术。保乳术结合放疗为保乳的重要前提,已成为专家的统一共识。保乳术后全乳放疗为一种常规的放疗方法,可提高病灶控制效果,降低术后复发的可能性[3]。但此方法治疗时间长达5周,费用较高,且放疗后患者可能出现患侧乳腺萎缩、皮肤色泽改变等问题,使乳房的美观度受到影响,部分患者较难接受,尤其是青年女性[4]。近年来,加速部分乳腺放射治疗(accelerated partial breast irradiation,APBI)受到肿瘤科治疗领域关注。APBI优势在于一次性小范围照射,可在缩短治疗总时长的同时,减少正常组织的受照射剂量[5]。术中放疗为一项新的APBI方法,可在术中直接对瘤床予以一次性的大剂量照射,因术野暴露充分,可实现精准照射治疗,并对周围组织进行最大化的保护[6]。为了解不同放疗方式的应用优劣,本研究对比分析乳腺癌患者保乳术中放疗与术后全乳的效果,现报告如下。
1 资料与方法
1.1 一般资料
本研究为非同期对照研究,选择2019年5月至2021年8月在本院行保乳术的98例乳腺癌患者为研究对象,按入院顺序将2019年5月至2020年6月、2022年7月至2021年8月收治的各49例乳腺癌患者分别设为A组、B组,两组一般资料比较,差异无统计学意义(P>0.05),见表1。
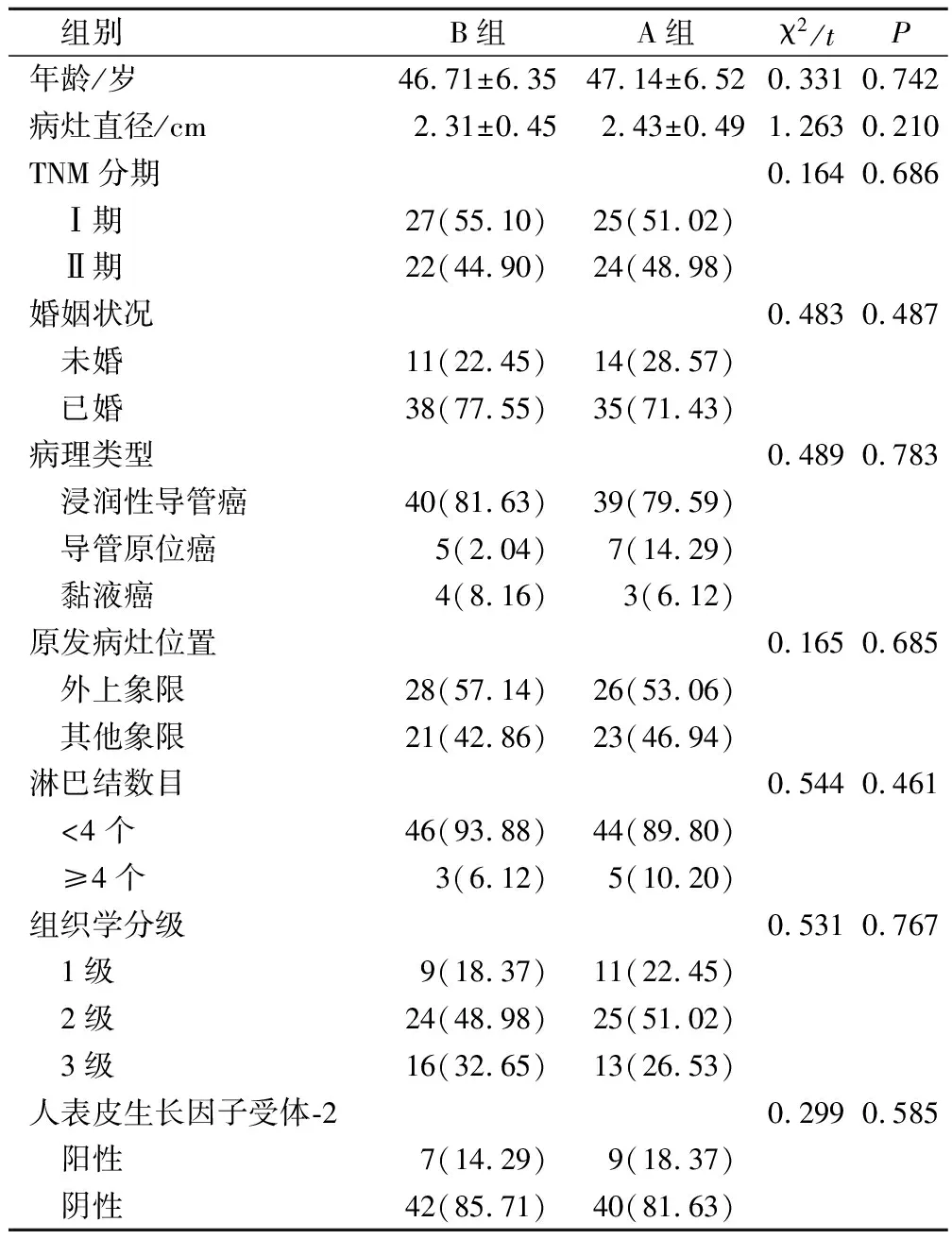
表1 两组一般资料比较
1.2 纳入标准
①符合有关乳腺癌的诊断标准[7];②单发病灶,且病灶直径不超过3 cm;③乳腺癌肿瘤淋巴结转移(tumor lymph node metastasis,TNM)分期Ⅰ或Ⅱ期;④均为女性,有保乳需求;⑤病灶切缘阴性;⑥诊疗及随访数据完整。
1.3 排除标准
①复治者;②存在其他肿瘤;③因器质性病变或患有其他重症疾病而无法耐受手术及放疗;④病灶侵犯或接近乳头;⑤乳房发育异常;⑥处于妊娠期。
1.4 方法
所有患者均行保乳术,患者处于平卧姿势,全麻后结合冰冻病理结果明确病灶边缘,实施腋窝淋巴结清扫。依据病灶所在位置确定切口,如对于病灶处于中上象限者,可做和乳晕平行的弧状切口。对于病灶处于中下象限者,可做放射状切口。在病灶外2 cm左右开展肿瘤切除术,结合实际情况行乳腺叶切除,确保无病灶残余。于腋下4 cm做斜切口并实施淋巴结清扫,直至达到LevelⅡ水平,最后在腋窝与胸壁下留置引流管,关闭切口并妥善包扎。A组术后实施全乳放疗,术后2周开展,放疗时由锁骨上部照射到乳腺褶皱下3 cm,结合患者情况设定参数,选用8 MeV电子线,照射剂量50 Gy,2 Gy/次,5次/周。B组实施术中放疗,照射范围为病灶及其附近2 cm、下部1 cm 正常组织,治疗剂量为18~21 Gy,选用9 MeV或12 MeV的电子线。放疗过程中结合瘤床大小选用适宜的限光筒,将其由切口置入,使其覆盖病灶前后1 cm与附近2 cm,照射所用剂量率为10 Gy/min,单次照射,时间持续3~5 min。
1.5 观察指标
①并发症。观察两组术后有无脂肪液化、创面水肿、放射性皮炎、急性血液毒性、肺损伤等并发症;②美容效果。术后6个月,判定两组美容效果。优:双侧乳房的外形、色泽基本无差异,乳头水平间距的差异不足2.0 cm;良:双侧乳房的外形、色泽存在轻微差异,乳头水平间距的差异为2~3 cm;双侧乳房的外形、色泽的差异明显,但仍在可接受范围内,乳头水平间距的差异超过3 cm;差:未达到上述标准[8]。计算优良率;③肿瘤标志物水平。采集术前及术后8周患者空腹静脉血,采血量为4 ml。对血液进行常规离心后。采用酶免法(试剂盒均购自上海瑞番生物科技有限公司)测定血清糖类抗原(carbohydrate antigen,CA)125、癌胚抗原(carcinoembryonic antigen,CEA)水平;④远期预后。观察2组术后2年内局部复发、转移、生存情况。
1.6 统计学方法
2 结果
2.1 两组并发症情况比较
B组并发症发生率为8.16%,显著低于A组的24.49%(P<0.05),见表2。

表2 两组并发症情况比较(例,%)
2.2 两组美容效果比较
B组美容优良率为89.80%,显著高于A组的65.31%(P<0.05),见表3。
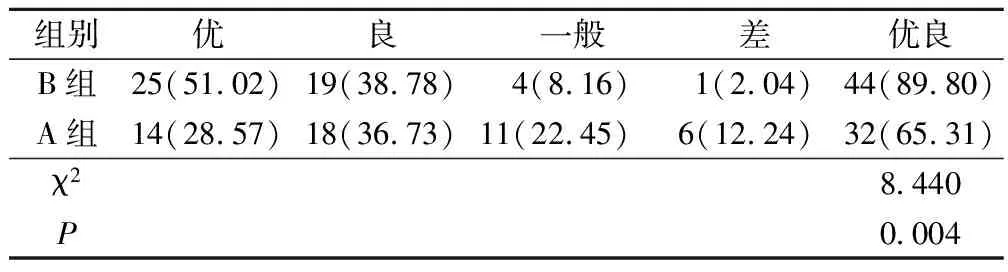
表3 两组美容效果比较(例,%)
2.3 两组术前后肿瘤标志物水平
术后8周,两组血清CA125、CEA水平均较术前降低(P<0.05),组间比较无差异(P>0.05),见表4。
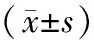
表4 两组术前后肿瘤标志物水平比较
2.4 两组远期预后比较
两组局部复发、转移及生存率比较无差异(P>0.05),见表5。
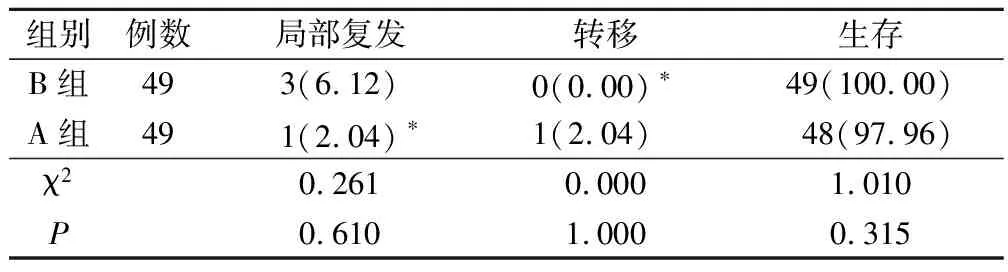
表5 两组远期预后比较(例,%)
3 讨论
保乳术仅做局部切除,手术范围小,可最大化保留乳房,与传统的根治术相比,其更能满足女性对乳房美观的要求[9]。故此术式成为早期乳腺癌治疗的首选。但保乳术后可能有癌细胞残留,故为充分清除病灶,达到根治疾病的目的,临床常辅助应用放疗。常规的放疗模式为于保乳术后以切线野的方式对整个乳房实施照射,单次照射剂量为2.0 Gy,每周5 d,总照射剂量为50 Gy,这意味着术后整个放疗时间长达5周。部分患者可能因无法较好地依从放疗而导致预后受到影响[10]。且术后放疗需于创面愈合后方可开展,这种放疗时间上的滞后可能增加局部复发的概率[11]。此外,此放疗模式易导致照射部位皮肤红肿、色泽改变及发生纤维化,继而损害乳房的外形,部分患者可能为此而于术后拒绝开展放疗。
Bernstein等[12]研究发现,保乳术后复发主要发生于术区。故为预防肿瘤复发并缩短放疗总时长,APBI逐渐受到关注并成为研究焦点。现阶段常用的APBI方法主要有三维适形放疗、调强放疗及术中放疗,前两种治疗可减轻常规放疗中大范围照射所造成的不必要损伤,但呼吸及体位等因素可对患者照射产生影响[13]。术中放疗为一种创新性的APBI方法,区别于其他APBI方法,其可实现和保乳术同步开展,且可避免呼吸及体位对照射的干扰,能提高放疗的精准度[14]。研究显示,术中放疗中以一定剂量对病灶区予以一次性照射,可有效杀死残余病灶,且患者术后无需因放疗而再度入院,能明显缩短治疗用时,缓解患者经济压力[15]。
本研究以术后常规放疗为对照,分析了保乳术中放疗的应用效果及安全性,结果显示,B组放射性皮炎、急性血液毒性、肺损伤等并发症的总发生为8.16%,和A组的24.49%相比明显更低,提示保乳术中放疗可减少放射性并发症的发生。究其原因,在术中将病灶切除后立即对病灶与附近可能受到侵犯的部位实施大剂量的照射,在精准作用于靶组织的同时可减少正常组织的受照射量,避免附近器官受到损害,故能降低放射性并发症的发生概率[16]。在美容效果上,B组的美容优良率为89.80%,和A组的65.31%相比明显更高,徐晓帆等[17]研究亦显示,术中放疗对乳房的美容效果较术后常规放疗佳。这是由于术中放疗仅照射乳房局部,与全乳放疗相比,可避免出现患侧乳腺萎缩、皮肤色泽改变等现象,患者术后乳房美观度基本不受影响。作为常见的肿瘤标志物,CA125、CEA含量在正常组织内极低,而在乳腺癌组织内处于高表达状态,且表达水平越高,恶化程度越高。研究显示,其水平和TNM分期、远期预后关系密切[18]。在本研究中,术后8周,两组血清CA125、CEA水平均降低,组间比较无差异;两组术后2年内局部复发(6.12%比2.04%)、转移(0.00%比2.04%)及生存率(100%比97.96%)比较均无差异,亦有研究指出,术中一次性放疗剂量20 Gy等效于术后常规分割放疗的50 Gy[19]。原因可能为术中放疗开展中靶区定位准确且剂量分布均匀;通过提前放疗时间,可降低术后癌细胞扩增的可能性,且一次性大剂量放疗可避免分次照射中残余病灶的增殖,继而可获得较佳的生物学效应[20]。
综上所述,保乳术中放疗可获得和术后全乳放疗相当的远期效果,但术中放疗可减少放射性并发症的发生,并使患者术后乳房获得更好的美观度。本研究纳入病例仅来自一所医院,有着一定的同质性,可能导致统计结果出现偏倚。故未来计划和其他医院合作开展多中心研究,以确保研究更加可信。

