上皮性卵巢癌患者肿瘤细胞减灭术术后复发的影响因素
沈冰燕,沈 谦,徐玲玲
(江苏省启东市妇幼保健院 妇产科,江苏 启东,226299)
卵巢癌为妇科常见的恶性肿瘤,其为妇科恶性肿瘤患者死亡的主要原因[1]。卵巢癌临床症状特异性较差,因此在早期难以被发现和诊断,而晚期卵巢癌因为复发率较高[2-3],导致预后较差,因此寻找有效治疗方法降低卵巢癌复发概率及改善卵巢癌预后、延长患者生存期限为妇科肿瘤学者们关注的重点问题。肿瘤细胞减灭术(CRS)指比较大的肿瘤或是肿瘤产生一些显著的压迫症状,且无法完全切除肿瘤、通过切除部分肿瘤减轻症状,减轻肿瘤负荷的手术[4]。利用细胞减灭术治疗卵巢癌,可以使体内残留癌细胞得到杀灭或是抑制,可延长患者生存期。但是也有研究[5-6]发现,该种模式治疗下的卵巢癌患者1年内复发率较高,争议较多。1年内复发的原因主要与术前患者分期、手术结局、术后化疗等危险因素有关。基于此,本研究探讨术前新辅助化疗联合CRS治疗卵巢癌患者术后1年复发的独立危险因素。
1 资料与方法
1.1 一般资料
选取 2018年 6 月—2021年6月行CRS治疗的卵巢癌患者90例为研究对象。所有患者均在化疗结束后随访1年,以是否复发将90例卵巢癌患者分为复发组(54例)和无复发组(36例)。
1.2 方法
所有患者均采用CRS治疗,手术包含阑尾与转移灶、大网膜、全子宫双附件等,并联合采用TC方案进行术前新辅助化疗,术后1个月采用紫杉醇+卡铂(TC方案) 化疗:第1天采用紫杉醇(北京协和药厂,LLC,批准文号H10980068) 135~175 mg/m2,卡铂(昆明贵研药业有限公司生产,国药准字H20053908 ); 第2天采用静脉滴注生理盐水,1个疗程为3周,共治疗3个疗程。化疗结束后随访1年。
1.3 观察指标
比较2组的一般资料(年龄、分期等,其中分期按照国际妇产科联合会FIGO进行)、术式(开腹、腹腔镜等)等情况,然后利用多元回归分析来对上皮性卵巢癌患者CRS化疗结束后随访1年复发的独立危险因素进行分析,并以相关危险因素建立卵巢癌CRS治疗预后的预测模型。
本研究采用FIGO分期,按照肿瘤在盆腹腔的侵犯程度以及是否远处转移,分为Ⅰ~Ⅳ期。卵巢癌肿瘤局限在卵巢为Ⅰ期,当扩散到盆腔脏器时为Ⅱ期,侵犯腹腔内脏器时则为Ⅲ期,如出现远处转移,比如肺、胸腔、肝、骨转移时为Ⅳ期。
1.4 统计学分析

2 结 果
2.1 2组一般资料比较
90例上皮性卵巢癌患者均采用术前新辅助化疗,术后紫杉醇加卡铂化疗,从化疗结束后开始随访,随访1年,复发54例,复发率为60.00%。2组一般资料比较,差异无统计学意义(P>0.05)。见表1。

表1 2组患者的一般资料比较[n(%)]
2.2 2组术前分期比较
术前,复发组高分期患者占比高于未复发组,差异有统计学意义(P<0.05)。见表2。

表2 2组患者的术前分期比较[n(%)]
2.3 术式和术中淋巴结的清扫
采用开腹或是腹腔镜CRS治疗,复发组和无复发组比较,差异无统计学意义(P>0.05)。无复发组患者清扫淋巴结比例高于复发组,差异有统计学意义(P<0.05)。见表3。

表3 2组患者的术式比较[n(%)]
2.4 2组的术前部分血清指标比较
复发组的血清CA125、HE4、CEA及AMH水平均高于无复发组,差异有统计学意义(P<0.05)。见表4。
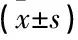
表4 2组的术前部分指标的比较

表5 上皮性卵巢癌患者CRS术后1年复发的多因素非条件Logistic回归分析
2.5 2组术前新辅助化疗次数
复发组的术前新辅助化疗次数为(3.23±1.21)次,无复发组为(3.14±1.03)次。2组术前新辅助化疗次数比较,差异无统计学意义(P>0.05)。
2.6 上皮性卵巢癌患者CRS术后1年复发的影响因素分析
回归设计:为了对各个变量的综合效应加以正确估计,混杂因素干扰结果的情况得到有效控制,文章采用似然比检验分析前述单因素中P<0.05的变量,采用多因素非条件Logistic回归分析,用逐步后退方法,以P<0.05为保留条件拟合回归方程。此外,考虑到本研究样本量较小,故对纳入的自变量采取降维处理,即原为连续型数值变量的术前血清CA125、术前血清HE4、术前血清CEA、AMH等,均参考2组总均值或中位数转化为二分类变量,多分类变量也适当合并成二分类,以提高回归的稳健性。
分析结果,最终被纳入回归模型的因素有:术前分期、清扫淋巴结及术前血清CA125、术前血清HE4、术前血清CEA、AMH等指标。年龄、术前分期、清扫淋巴结及术前血清CA125、HE4、CEA、AMH均为上皮性卵巢癌患者CRS术后1年复发的影响因素(因果关系)或关联影响因素(果因关系)(P<0.05)。见表5。
2.7 评估上皮性卵巢癌患者CRS术后1年内复发的预测价值
进一步探讨上述4个指标(术前血清CA125、HE4、CEA、AMH等)预测上皮性卵巢癌患者CRS术后1年复发中的应用价值:以复发组54例为阳性样本,以未复发组36例为阴性样本,建立ROC预测分析模型。① 单独应用:上述4个指标均为临床和既往文献中所见,划分成若干个组段,然后用软件来拟合,得到ROC曲线后对约登指数最大值点加以读取,对各项参数和理论阈值(适当取整)进行测算,并根据实测样本对敏感度、准确度和特异度加以计算。② 联合应用(LogP模式):以前述Logistic回归结果,建立回归风险评估/预测模型,以其Log[P/(1-P)]=术前血清CA125+1.276×术前血清HE4+0.979×术前血清CEA+0.840×AMH为联合应用的虚拟概率量指标,再行ROC分析。联合应用虚拟指标的阈值系依据该Log[P/(1-P)]模型(无常数项)计算所得,其中各指标阳性阈值按二分类化后的变量形式读取,即均为1。③ 分析结果显示:术前血清CA125、术前血清HE4、术前血清CEA、AMH等指标单独及联合预测的曲线下面积(AUC,95%CI)分别为0.740(0.516~0.937)、0.730(0.467~0.990)、0.731(0.477~0.977)、0.743(0.515~0.967)和0.884(0.829~0.924)。见表6、图1。

图1 上皮性卵巢癌患者CRS术后1年复发的预测因素/指标的预测评估价值

表6 上皮性卵巢癌患者CRS术后1年复发的预测因素/指标的预测评估价值分析
3 讨 论
上皮卵巢癌在女性生殖系统恶性肿瘤中病死率居于首位,且可能会出现输卵管、大网膜、子宫等盆腹腔脏器的转移[7-8]。既往研究对卵巢癌的诊断价值成果比较集中,对其CRS术后1年内复发的危险因素的研究和预测模型研究较少。本研究探讨术前新辅助化疗联合CRS治疗卵巢癌术后1年复发的独立危险因素及部分血液检测指标对化疗结束后随访1年复发的预测评估价值。
卵巢癌属于高龄段多发者,即随着年龄的增高,卵巢癌的发病率和复发率均随之升高[9-11]。因此本研究将年龄作为配比因素,以控制年龄对术后复发的混杂作用[12-13]。社会经济地位(SES)作为一个综合指标,其数值的高低与多数肿瘤的发生密切相关。研究[14-16]发现,SES往往与其他一些因素相关,如地区分布、生活方式、发育情况、职业分布、营养状况、医疗保障水平、饮食习惯等,而这些因素均可能与卵巢癌的发生有关。因此,本研究将地区、职业与文化程度作为因素进行相关性分析,结果发现,这些因素与术后1年内复发情况无显著相关性。既往研究[17-19]认为,分期、术中未清扫淋巴结等均是术后1年内复发的主要原因。故本研究纳入了术前分期和清扫淋巴结等情况作为观察术后1年内复发因素的指标,结果发现,术前分期和清扫淋巴结均与上皮性卵巢癌患者CRS术后1年内复发有相关性。本研究发现,2组间在开腹或是腹腔镜CRS治疗方面比较无显著差异(P>0.05),说明上皮性卵巢癌患者CRS术后1年内复发与术式无关,分析原因可能与样本量和近年腹腔镜手术开展较多有关。本研究发现年龄、术前分期、清扫淋巴结及术前血清CA125、HE4、CEA、AMH均为上皮性卵巢癌患者CRS术后1年内复发的影响因素或关联影响因素(P<0.05),提示应在术前新辅助化时对术前血清CA125、HE4、CEA、AMH等指标进行监测。
研究认为AMH是CRS术后复发的独立危险因素,提示其与患者1年内后复发密切相关。AMH是直接表征卵巢功能之一的指标,故本研究将其纳入预测指标模型。AMH是由卵巢中小卵泡的颗粒细胞分泌的一种激素,其代表卵巢的储备功能,即检查AMH可了解卵巢的储备功能。当卵巢当中小卵泡比较多时,日后可以排卵的卵泡就会越多。AMH越高,提示储备功能越好; 反之,则卵巢的储备功能较差。通常大于35岁的女性卵巢功能开始逐渐衰退,储备功能下降。如果AMH特别低,容易发生卵巢早衰,怀孕的概率随之较小,需及时改善卵巢功能。
综上所述,血清CA125、HE4、CEA、AMH联合预测上皮性卵巢癌患者CRS术后1年内复发的AUC为0.884(0.95CI:0.829~0.924)。血清CA125、HE4、CEA、AMH联合预测的诊断效能高,其AUC及灵敏度、特异度、准确度均高于上述指标单独预测。

