副干酪乳杆菌的益生特性及其机制研究进展
王一帆,薛云德,张宝平,李欢,王彦波*
(1.浙江工商大学 食品与生物工程学院,浙江 杭州 310018;2.东营市一大早乳业有限公司,山东 东营 257400)
副干酪乳杆菌(Lactobacillusparacasei)是一种革兰氏阳性同型发酵乳酸菌,常见于人类肠道、口腔中,通常用于乳制品发酵领域,因其丰富的益生特性,而成为研究的热点。近年来,副干酪乳杆菌开始应用于食品和医疗领域[1],其具有的益生特性有进一步的应用空间。随着研究的逐渐深入,副干酪乳杆菌的益生特性得到更深入地揭示。副干酪乳杆菌能够调节免疫系统,改善脂质代谢,并且具有抗氧化和抑菌作用。同时,由副干酪乳杆菌制备的后生元也具有一定的益生特性。由于具有上述的益生特性,副干酪乳杆菌可以有效地维持宿主机体健康,进而在食品和医疗领域发挥作用。但是,由于副干酪乳杆菌的益生特性及其相关的作用机制并没有得到很好的归纳与解析,无法为后续的研究与应用提供一个清晰的理论支撑。基于此,本文详细并系统归纳副干酪乳杆菌的益生特性,探讨副干酪乳杆菌的益生特性对应的作用机制,以期为副干酪乳杆菌后续的研究与应用提供理论依据并指明发展方向,进一步完善副干酪乳杆菌在食品和医疗领域的产品形式。
1 副干酪乳杆菌的免疫调节作用及其机制
1.1 副干酪乳杆菌的免疫调节作用
调节免疫系统是副干酪乳杆菌的主要益生特性之一。副干酪乳杆菌可以缓解炎症、治疗过敏、抑制癌症和抗增殖等,可有效地调节宿主免疫系统平衡,提高宿主机体免疫力。
副干酪乳杆菌可以缓解结肠炎、皮炎、肝炎和神经性炎症等多种炎症。研究表明,在皮肤气囊小鼠模型中副干酪乳杆菌K5 诱导了小鼠体内促炎性细胞因子白细胞介导素-1α(interleukin-1α,IL-1α)、白细胞介导素-1β(interleukin-1β,IL-1β)、白细胞介导素-6(interleukin-6,IL-6)、肿瘤坏死因子-α(tumour necrosis factorα,TNF-α)、趋化因子CXC 基序配体2(C-X-C motif chemokine ligand 2,CXCL2)、黏附反应分子(serum intercellular adhesion molecula,sICAM)和金属肽酶抑制剂-1(sissue inhibitor of metalloproteinase 1,TIMP-1)的表达,从而缓解小鼠炎症[2]。Huang 等[3]的研究表明副干酪乳杆菌R3 通过调节辅助性Th17 细胞(t helper cell 17,TH17)和调节性T 细胞平衡,显著改善结肠炎小鼠的症状和病理损害,并提高小鼠的免疫功能。Chen 等[4]研究发现,给小鼠喂食副干酪乳杆菌NTU 101 可以通过增强总抗氧化剂谷胱甘肽还原酶(glutathione reductase,GR)、谷胱甘肽(glutathione,GSH)、过氧化氢酶(catalase,CAT)、超氧化物歧化酶(superoxide dismutase,SOD)和丙二醛(malondialdehyde,MDA)的抗氧化能力,并抑制促炎细胞因子如TNF-α、IL-6、以及γ 干扰素(interferon-γ,IFN-γ)和白细胞介导素-12(interleukin-12,IL-12)的分泌,抑制了葡聚糖硫酸钠引起的氧化应激反应,从而减缓了炎症引起的小鼠体质量降低症状,调节免疫活性。此外,口服副干酪乳杆菌KBL382 可显著缓解皮炎小鼠的相关皮肤病变、表皮增厚等症状,并且降低血清免疫球蛋白(immunoglobulins E,IgE)水平和免疫细胞浸润。处理后小鼠的T helper type 1(Th1)、T helper type 2(Th2)和T helper type 17(Th17)细胞比例降低,肠系膜淋巴结中CD4+CD25+Foxp3+调节性T 细胞的比例上升,以上都证明了小鼠皮炎症状得到一定程度的改善[5]。Boonyarut 等[6]研究发现副干酪乳杆菌MSMC39-1 改善了肝炎大鼠的肝脏损伤。除了上述功能,副干酪乳杆菌还可以缓解神经性炎症。蓖麻籽和副干酪乳杆菌NK112 组成的功能食品混合物下调小鼠的丝裂原活化蛋白激酶(mitogenactivated protein kinase signaling,MAPKs)和核因子-kB通路(nuclear factor kappa-B,NF-κB),上调Nrf2 抗氧化(nuclear factor erythroid 2-related factor 2,NRF2)和血红素氧合酶1(heme oxygenase 1,HO-1)信号通路,从而抑制脂多糖诱导的小胶质细胞BV2 细胞的神经炎症反应[7]。副干酪乳杆菌KW3110 还可以保护人视网膜色素上皮细胞免受慢性炎症应激引起的细胞损伤,并可能改善包括眼疲劳在内的慢性眼部疾病[8]。总之,副干酪乳杆菌被证实可以缓解多种炎症。
过敏反应的机理与免疫细胞的分化活化高度关联,副干酪乳杆菌可以缓解多种过敏症状。Lin 等[9]研究发现副干酪乳杆菌HB89 对细颗粒物PM2.5(2.5-micrometer particulate matter,PM2.5)刺激的呼吸道过敏反应起到缓解作用,肺内免疫细胞增殖减慢,免疫球蛋白水平降低。副干酪乳杆菌IJH-SONE68 产生的胞外多糖可以预防和缓解患者的慢性过敏症状[10]。研究表明,口服副干酪乳杆菌还可以降低儿童因过敏遗传而导致的过敏风险[11]。此外,副干酪乳杆菌L9 能够通过调节性树突状细胞介导的主动抑制来缓解机体对β-乳球蛋白的过敏症状。副干酪乳杆菌L9 上调了CD4+CD25+Foxp3+Treg 细胞的应答并调节了小鼠的Th1/Th2 细胞的失衡,同时还显著诱导肠系膜淋巴结、派尔结和脾脏中CD103 的表达,抑制树突状细胞的成熟状态[12]。
副干酪乳杆菌在抑制癌症和抗增殖方面的作用也逐渐受到人们的关注[13]。研究表明,副干酪乳杆菌SD1 对人结直肠腺癌细胞(Cancer coli-2,Caco-2)结肠癌细胞的黏附能力较强,对Caco-2 细胞的增殖抑制作用呈时间和剂量依赖性[14]。Da Silva Duarte 等[15]研究发现,副干酪乳杆菌DTA81 可改善结肠癌小鼠模型早期阶段的症状,改善肠道免疫状态。副干酪乳杆菌的细胞壁蛋白组分可以诱导Caco-2 细胞系的凋亡[16],胞外囊泡可通过pyruvate dehydrogenase kinase isoform 1(PDK1)/ RAC serine/threonine-protein kinase(AKT)/ Bcell lymphoma-2(Bcl-2)信号通路抑制结直肠癌细胞的生长、增殖、迁移、侵袭并诱导其凋亡[17]。
除了上述免疫调节功能,副干酪乳杆菌还具有其他的免疫功效。副干酪乳杆菌对鼠伤寒沙门氏菌感染具有保护作用,口服副干酪乳杆菌降低和减少了小鼠模型的死亡率、体质量减轻、移位到靶器官(肝和脾)和回肠损伤,同时维持肠道菌群平衡[18]。副干酪乳杆菌可缓解肠易激综合征患者的胃肠道症状并改善患者的心理健康状况[19]。副干酪乳杆菌通过抑制NF-κB-肌球蛋白轻链激酶(myosin light chain kinase,MLCK)途径的激活和增加产生短链脂肪酸的肠道菌群丰度来缓解腹泻[20]。持续服用副干酪乳杆菌还可以减轻患者的感冒症状[21]。
1.2 副干酪乳杆菌的免疫调节机制
副干酪乳杆菌可以通过影响细胞因子水平来调节免疫系统,细胞因子可以在细胞间传递信号,在免疫系统中发挥着重要作用。副干酪乳杆菌产生的胞外囊泡可诱导内质网应激相关蛋白的表达,抑制内毒素的促炎作用,同时胞外囊泡降低了促炎细胞因子IL-1α、IL-1β、IL-2 和肿瘤坏死因子TNF-α 的表达,增加了抗炎细胞因子白介素-10(interleukin-10,IL-10)和转化生长因子-β(transforming growth factor-β,TGF-β)的表达,降低炎症相关蛋白的表达水平[22]。副干酪乳杆菌产生的胞外多糖也可以刺激皮炎小鼠模型中的IL-10 的产生[23],通过促进IL-10 的产生而抑制炎症复合体活性成分半胱天冬酶1(cysteinyl aspartate specific proteinase1,Caspase1)的激活和促炎细胞因子IL-1β 的产生[24]。副干酪乳杆菌诱导产生的IL-10 可抑制炎症对巨噬细胞中线粒体形态的破坏和炎症引起的线粒体功能障碍,包括膜电位下调、活性氧诱导和呼吸功能障碍,并阻止了内毒素诱导的包括冠状结构在内的线粒体形态的破坏[25]。副干酪乳杆菌刺激巨噬细胞产生的IL-10 还与巨噬细胞的吞噬作用有关[26]。副干酪乳杆菌还可以作用于肠道细胞,促进细胞发育。副干酪乳杆菌的代谢产物可以增加跨上皮电阻来增强上皮屏障功能,从而提高上皮通透性[27]。此外,副干酪乳杆菌还可以作用于肠道菌群,抑制细菌对肠道细胞的黏附和侵袭,从而缓解肠道炎症[28],并改变肠道菌群结构,上调短链脂肪酸含量[27]。例如,副干酪乳杆菌扩大了肠道中丁酸产生菌的丰度,导致丁酸含量增加,并抑制IL-6/ signal transducer and activator of transcription 3(STAT3)信号通路,进而减轻结肠炎的炎症反应,详细机制见图1[29]。
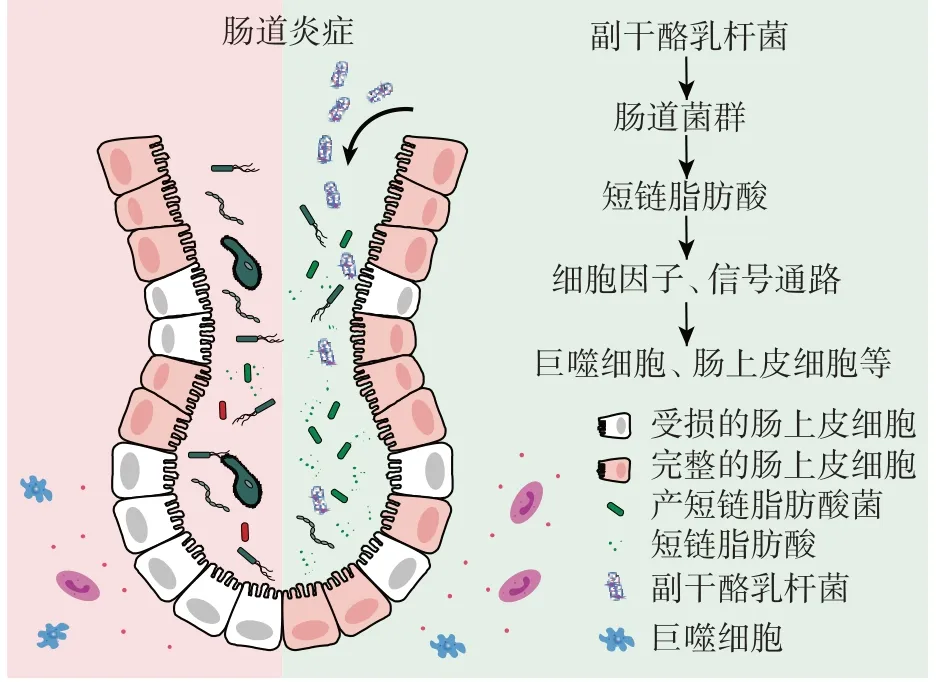
图1 副干酪乳杆菌治疗肠道炎症Fig.1 Treatment of intestinal inflammation by Lactobacillus paracasei
与此同时,炎症和癌症是相互影响的。研究表明,相同的胞外多糖可以发挥双重作用,在抑制免疫细胞炎症的同时,抑制肿瘤细胞的增殖[30-31]。副干酪乳杆菌产生的胞外囊泡和胞外多糖等生物成分可以用于调节免疫系统。首先,副干酪乳杆菌可以诱导细胞凋亡。抗增殖作用可能是通过调节特定的Bcl-2 家族蛋白的表达来诱导细胞凋亡[32]。副干酪乳杆菌SR4 分泌的上清液通过上调凋亡基因Bcl-2 蛋白家族成员(Bcl2-Associated X,BAX)、Bcl-2 蛋白家族成员(Bcl-2-antagonist of cell death,BAD)以及Caspase1、Caspase3、Caspase8 和Caspase9 的表达,下调Bcl-2基因的表达,对宫颈癌细胞具有良好的抑制作用,机制见图2[33]。
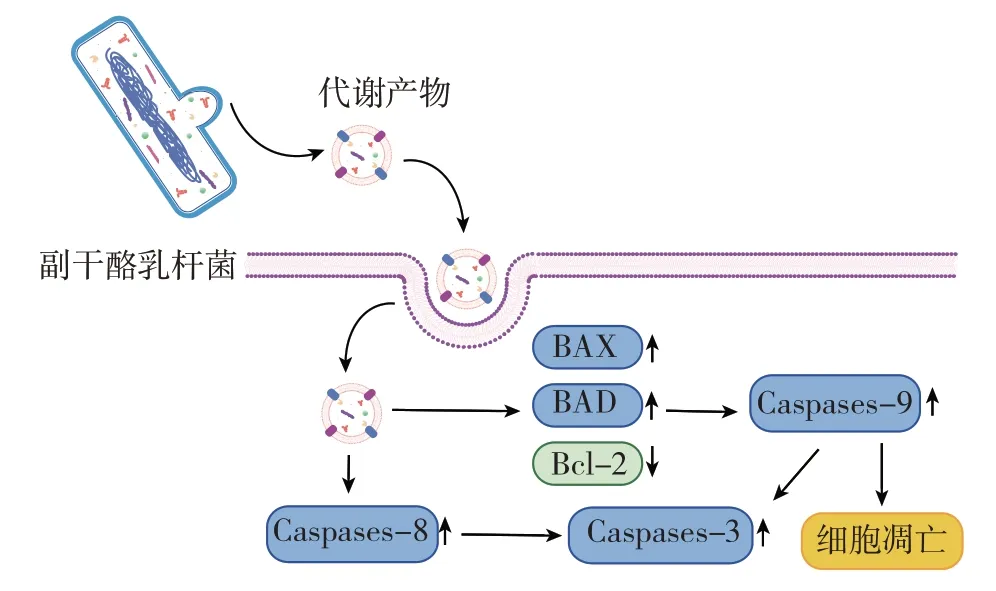
图2 副干酪乳杆菌的代谢产物诱导细胞凋亡Fig.2 Cell apoptosis induced by metabolites of Lactobacillus paracasei
半胱氨酸天冬氨酸特异性蛋白水解酶是细胞凋亡的中心机制[34]。同时,副干酪乳杆菌具有选择性细胞毒性。副干酪乳杆菌的生物活性成分可以显著降低癌细胞存活率,而对结肠上皮细胞无任何细胞毒性作用[35]。经40 mg/mL 的副干酪乳杆菌和短乳杆菌的胞外多糖处理后,细胞L929 存活率均在60% 以上而细胞HT29 的存活率不到20%[36]。副干酪乳杆菌还可以通过引起细胞周期停滞来杀死目标细胞。副干酪乳杆菌X12 通过抑制细胞周期蛋白E1,同时增强细胞周期蛋白p27,使细胞周期停滞于G1期,这一作用是由mammalian target of rapamycin(mTOR)/4E binding protein 1(4EBP1)信号通路介导的[37]。副干酪乳杆菌具有的抗氧化性可以调节免疫系统来抑制肿瘤和癌症的恶化。肿瘤细胞的内源性活性氧的不断生成,促进了肿瘤细胞的存活和增殖,加强了上皮细胞向间充质的转化和侵袭,促进了基因组的不稳定性和血管生成。而副干酪乳杆菌的胞外多糖可以作为抗氧化剂阻断活性氧,有效延缓甚至防止肿瘤恶化。
2 副干酪乳杆菌的脂质代谢调节作用及其机制
2.1 副干酪乳杆菌的脂质代谢调节作用
脂质代谢与降血糖、缓解糖尿病密切相关,通过调整脂质代谢,可以改善胰岛素的敏感性,有助于控制血糖水平。副干酪乳杆菌可以促进机体的脂质代谢。副干酪乳杆菌治疗显著降低了高脂小鼠的体质量和脂肪沉积,减少内脏脂肪和肝脏脂质,改善了血脂水平和肝脏脂肪变性,减少了肝脏氧化应激损伤和炎症反应,并调节了脂肪代谢相关因素[38]。研究表明,副干酪乳杆菌JY062 对高糖脂诱导的小鼠体质量增加和空腹血糖升高有一定的抑制作用,可改善高糖高脂饮食所致的高脂血症和糖耐量异常,并能降低肥胖相关因素的风险,降低总胆固醇、甘油三酯、低密度脂蛋白胆固醇,升高高密度脂蛋白胆固醇。副干酪乳杆菌Jlus66 可以通过调节肠道菌群来减轻氧化应激和炎症,从而改善非酒精性脂肪肝[39]。补充副干酪乳杆菌HII01 可能有助于改善高胆固醇血症患者的血脂状况,降低内毒素水平,并影响免疫激活[40]。Gu 等[41]研究发现,副干酪乳杆菌IMC502 能显著降低血糖、糖化血红蛋白和血脂水平,改善胰岛素抵抗和糖耐量异常,调节与糖异生、脂肪生成和phosphatidylinositol 3'-kinase(PI3K)/Akt途径相关的肝脏关键酶的mRNA 表达,修复胰腺和肝脏组织的损伤,从而缓解糖尿病。
2.2 副干酪乳杆菌的脂质代谢调节机制
副干酪乳杆菌通过多种机制途径来进行脂质代谢调节,肠道菌群在其中发挥着重要作用,其调控机制见图3。
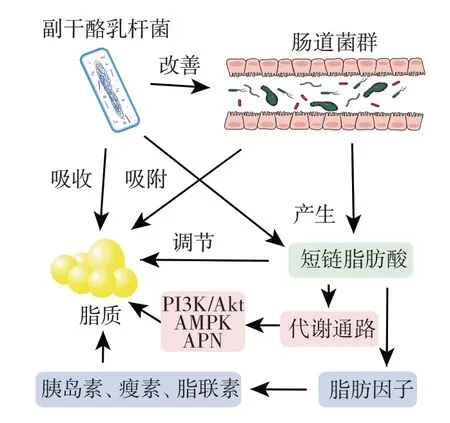
图3 副干酪乳杆菌调节脂质代谢Fig.3 Lipid metabolism regulated by Lactobacillus paracasei
副干酪乳杆菌LP24 通过激活相关基因的表达水平和通过肠-肝轴调节肠道微生物群来调节脂质代谢,从而缓解肥胖[38]。副干酪乳杆菌FZU103 通过改变肠道菌群组成,调节肝脏相关基因的表达,包括初级胆汁酸生物合成、脂肪酸降解和脂肪酸生物合成,对高脂血症具有一定的改善作用[42]。副干酪乳杆菌DTA81 增加肠道菌群中细菌和球菌的丰度,显著降低炎性细胞因子IL-6 水平,降低空腹血糖。肠道菌群失衡可能导致肠道微生物结构和组成变化,副干酪乳杆菌可以对其进行干预和恢复。肠道微生物群可以通过参与机体的新陈代谢来调节机体的糖脂水平。副干酪乳杆菌还可以直接同化吸收胆固醇,将其转化为自身成分[43]。副干酪乳杆菌可以调节机体内脂肪因子和胰岛素的水平来调节脂质代谢。通过副干酪乳杆菌治疗的高脂小鼠体内的瘦素、胰岛素和游离脂肪酸的含量较低,脂联素和胰高血糖素样肽-1 的含量相对升高。副干酪乳杆菌可以影响代谢通路来影响脂质代谢。副干酪乳杆菌可以激活adiponectin(APN)-(AMP-activated protein kinase)AMPK通路,抑制固醇调节元件结合蛋白-1c(sterol regulatory element binding protein 1c,SREBP-1c)的表达,下调其靶基因FAS和ACC,并减少脂质合成。副干酪乳杆菌还可以通过PI3K/Akt 信号和AMPK 激活来缓解糖尿病大鼠的高血糖[44]。在动物模型和临床实验中,短链脂肪酸在预防和治疗肥胖症和二型糖尿病方面发挥了关键作用。乙酸是血清中含量最丰富的短链脂肪酸,它可以缓解炎症,抵抗病原体的侵袭,抑制脂肪的蓄积,而丙酸可以刺激瘦素降低总胆固醇水平,丁酸可促进胃肠激素的释放,从而改善高脂饮食诱导的肥胖和胰岛素敏感性[45]。此外,丁酸可激活肝脏AMPK 信号通路,促进脂肪酸氧化,抑制糖异生和脂肪产生。
3 副干酪乳杆菌的抗氧化作用及其机制
3.1 副干酪乳杆菌的抗氧化作用
副干酪乳杆菌具有较强的抗氧化活性。副干酪乳杆菌发酵果汁中β-胡萝卜素含量、2,2-联苯基-1-苦基肼基(2,2-diphenyl-1-picrylhydrazyl,DPPH)自由基清除活性、铁还原抗氧化能力和脂质过氧化抑制能力均高于未发酵的果汁[46]。Wang 等[47]研究发现,副干酪乳杆菌对α-淀粉酶(82.21%)、α-葡萄糖苷酶(84.29%)和二肽基肽酶-4(42.51%)具有显著的抑制活性,对自由基、总抗氧化活性和超氧化物歧化酶活性具有较高的清除活性。副干酪乳杆菌可以提高老年人的抗氧化酶、超氧化物歧化酶和谷胱甘肽过氧化物酶的mRNA 水平。线粒体功能也受到氧化应激的影响,氧化应激随着年龄的增长而增加。蛋白质羰基的水平是氧化应激重要和直接的生物标志,而服用副干酪乳杆菌可以提高体内的蛋白质羰基水平[48]。
3.2 副干酪乳杆菌的抗氧化机制
副干酪乳杆菌的生物活性成分含有的化学基团使其具有抗氧化性。副干酪乳杆菌的胞外多糖含有羟基、碳自由基和硫酸基[49]等化学基团使其具有高抗氧化性。副干酪乳杆菌的发酵产物具有较高的自由基清除能力。副干酪乳杆菌通过上调其抗氧化酶的基因表达来发挥其抗氧化作用,如硫氧还蛋白、超氧化物歧化酶和谷胱甘肽过氧化物酶等。此外,抗氧化酶的活性也会受到影响。
4 副干酪乳杆菌的抑菌作用及其机制
4.1 副干酪乳杆菌的抑菌作用
副干酪乳杆菌具有较强的抑菌作用。含有副干酪乳杆菌的发酵乳和黄连发酵液联合使用可降低患者体内幽门螺杆菌的密度,改善组织学炎症反应。服用副干酪乳杆菌后可以显著降低幽门螺杆菌的感染率,并降低感染小鼠的血清IL-8 水平和胃炎症[50]。此外,副干酪乳杆菌产生的ZFM54 对鼠伤寒沙门氏菌、黄氏微球菌和单增李斯特菌等食源性致病菌具有广谱抑制作用[51]。
4.2 副干酪乳杆菌的抑菌机制
副干酪乳杆菌产生的代谢产物在抑制细菌方面发挥着关键作用,其中细菌素和有机酸是其重要组成部分,相关机制如图4 所示。
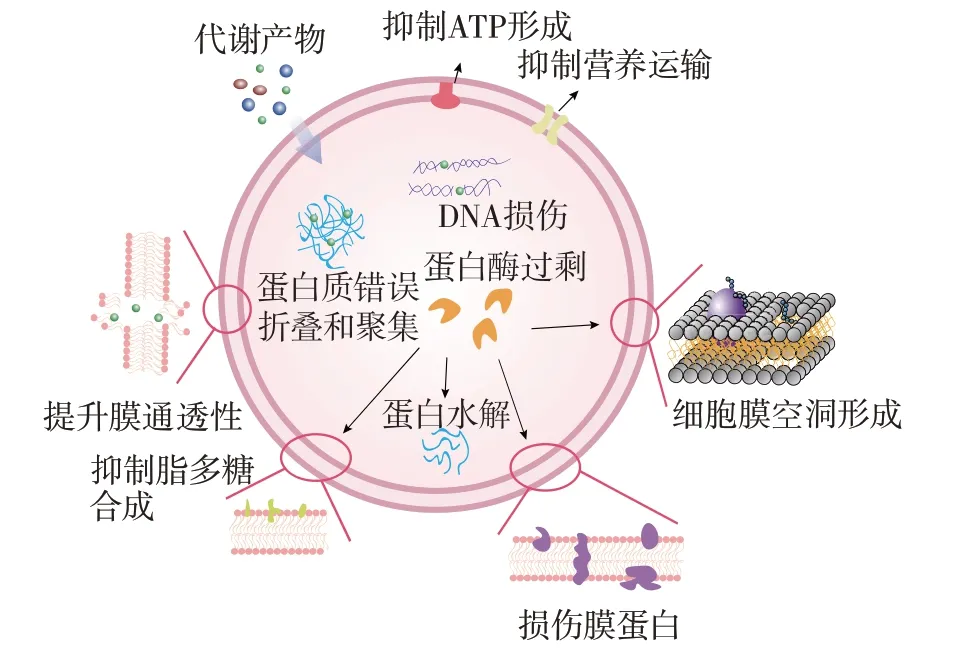
图4 副干酪乳杆菌的代谢产物抑菌机制Fig.4 Antibacterial mechanism of metabolites of Lactobacillus paracasei
副干酪乳杆菌的代谢产物展现了多方面的功能,构成了副干酪乳杆菌对细菌的强大抗菌机制。副干酪乳杆菌通过抑制胞外多糖的产生[52],影响了细菌的生物被膜形成过程[53]。这一作用不仅限于防止新生物被膜的形成,还包括消除已形成的生物被膜,从而影响细菌的生存环境。副干酪乳杆菌所产生的细菌素具有独特的杀菌机制。细菌素诱导细菌细胞膜的孔洞形成[51],同时细菌素通过上调参与膜损伤(FtsH、ClpX)和蛋白质水解(Lon、DnaJ、GroEL)的关键基因和蛋白质,导致DNA 损伤和代谢紊乱,并通过抑制营养物质的运输和能量代谢来抑制细菌[54]。副干酪乳杆菌产生的细菌素在破坏细菌细胞膜后还可以与细胞质中的基因组DNA 结合,以此实现快速杀菌[55]。
5 副干酪乳杆菌的后生元作用及其机制
后生元是指对宿主健康有益的无生命微生物和(或)其成分的制剂[56]。相较于益生菌,后生元更稳定和安全,因此近年来也逐渐受到人们的关注。由副干酪乳杆菌制备而成的后生元同样具备其作为益生菌的免疫调节、脂质代谢、抗氧化和抑菌等益生特性。灭活的副干酪乳杆菌KW3110 可能通过增强趋化因子受体CCR-7(C-C motif chemokine receptor 7,CCR-7)和programmed cell death 1 ligand 2(PD-L2)的基因表达来加速树突状细胞向区域淋巴结的迁移并抑制Th2 细胞因子的产生,进而抑制过敏症状[57]。Lee 等[58]研究表明,连续6 周补充副干酪乳杆菌活菌或后生元都可以防止肌肉损伤后的力量损失,改善血液肌肉损伤和降低炎症标志物水平,具有保护性、加速恢复和抗疲劳的功能,但相较之下,副干酪乳杆菌后生元的效果更强。灭活的副干酪乳杆菌可以通过调节肠道菌群和肝脏相关基因的表达来调节脂质代谢,因此对脂肪性肝病具有防护作用[59]。热灭活的副干酪乳杆菌对变形链球菌多糖的合成以及生物膜的形成有抑制作用,这与未灭活的副干酪乳杆菌的抑菌机制一致。由副干酪乳杆菌制备的后生元具有多种成分,包括肽聚糖、表面蛋白、细胞壁多糖、分泌蛋白、细菌素和有机酸,它们可以对宿主进行正向调控,如免疫调节、脂质代谢、抗氧化和抑菌等功能[60],其组成成分和益生菌类似,因而机制也类似。
6 总结与展望
副干酪乳杆菌由于其具有优异的益生特性而被认为是一种具有研究价值和开发前景的益生菌。研究表明,副干酪乳杆菌可以在免疫系统、脂质代谢、抗氧化和抑菌方面发挥益生作用。此外,副干酪乳杆菌的益生特性是多种机制综合的结果。其中,副干酪乳杆菌的代谢产物发挥着重要作用,副干酪乳杆菌作为后生元也能具有相同的益生特性。通过对机制的深入探究和总结,进一步形成机制架构,以此为副干酪乳杆菌的后续研究与应用提供全面的理论支持和清晰的研究导向。但是,副干酪乳杆菌的作用机制的研究还不够深入,未来可以在抗氧化和菌株肽段等小分子方面进行进一步的研究。此外,副干酪乳杆菌的代谢产物如胞外多糖,具有广阔的研究前景,可以将其与后生元这一新兴的研究热点相结合。同时还可以针对不同菌种的副干酪乳杆菌进行详细研究,进而形成一套完整的产品体系,充分发挥副干酪乳杆菌的多种益生特性。

