甲氨蝶呤/层状双金属氢氧化物的性能调控及细胞生物实验研究
霍晓磊 柳素青 李淑萍
(江苏省生物医药功能材料协同创新中心,江苏省生物功能材料重点实验室,南京师范大学化学与材料科学学院,南京210097)
0 引 言
层状双金属氢氧化物(Layered Double Hydroxide,LDH),也称类水滑石 (hydrotalcite like compounds),是一类由带正电荷的金属氢氧化物层和层间充斥的可交换阴离子所构成的层状化合物,化学通式可表示为:[M2+1-xM3+x(OH)2]x+[An-]x/n·mH2O,其中 M2+表示+2价金属离子,M3+表示+3价金属离子,An-表示层间阴离子,x为每摩尔LDH中M3+的摩尔数;m是每摩尔LDH中结晶水的摩尔数[1-4]。由于LDH具有层间阴离子的可交换性和层间空间的可调性,因此,可以将某些无机、有机、配合物阴离子以及一些生物药物分子等插入其层间,且LDH独特的层板结构,能够有效地保护插入其中的分子或离子[5-8]。LDH为药物载体不仅可以提高药物的安全性、有效性,还可以提高药物的稳定性和溶解度,控制药物的释放速率,因而具有广泛的应用价值,是近年来新发展的一个非常活跃的领域[9-12]。
甲氨蝶呤(Methotrexatum,简称MTX)是一类抗叶酸类抗肿瘤药,主要通过对二氢叶酸还原酶的抑制而达到阻碍肿瘤细胞DNA的合成,从而抑制肿瘤细胞的生长与繁殖,主要适用于急性白血病、乳腺癌、绒毛膜上皮癌及恶性葡萄胎、头颈部肿瘤、骨肿瘤、白血病脑膜脊髓浸润、肺癌、生殖系统肿瘤、肝癌、顽固性普通牛皮癣、系统性红斑狼疮、皮肌炎等自身免疫病[13]。MTX价格便宜、药效显著,但它具有不良反应严重、体内半衰期短、组织分布广泛、器官靶向性差等缺点[14-15]。因此,减少MTX的不良反应,提高其生物利用度,成为医药界和科学界的研究热点。研究表明,甲氨蝶呤(MTX)嵌入LDH层间后,因静电相互作用而使其稳定性大为增加;相同药物浓度下,MTX/LDH复合物的药效约为MTX本身的5 000倍[16]。Choy等[16-17]以LDH为载体,采用共沉淀法成功合成了MTX/LDH纳米复合物,并分别将MTX和MTX/LDH作用于人类骨肉瘤细胞(SaOS-2)中,研究发现MTX/LDH抑制肿瘤细胞生长的效率远远高于纯MTX的,且体内释放半衰期延长,器官靶向性增强。
制备MTX/LDH纳米复合物最常用的方法是共沉淀法。共沉淀法具有操作简单、条件容易控制等优点,但同时存在着粒径分布难以控制、易团聚、单分散性差等缺点[18],对实际应用造成了很大的影响。我们课题组采用了改进的共沉淀法[19-20]成功制备出了单分散性好,粒径分布均一的MTX/LDH复合物。从应用层面上看,一种新型的载药系统无论其具有多么优良的理化及药剂学特性,最终均应以生物效应来评价其实际应用。本文采用了改进的共沉淀法,并通过控制水热处理时间的方式来调控MTX/LDH纳米复合物的性能,重点研究了MTX/LDH纳米复合物对肺癌细胞A549的抑制作用。我们的研究结果发现MTX/LDH纳米复合物的物化性能与抗癌效果之间存在着某种密切的关系,我们首次利用分散系数ε对此进行了量化,这为MTX/LDH纳米复合物的结构-药效相关性的研究打下了坚实的基础。
1 实验部分
1.1 仪器与试剂
仪器:用D/max-2500PC型XRD仪测定样品的相结构,靶压200 kV,靶流 100 mA,Cu Kα射线源为光源,λ=0.154 06 nm,用石墨单色器滤波;H-7650-HITACHI型TEM仪观察粒子的大小和形貌,工作电压为200 KV;Bruker Tensor 27型FT-IR光谱仪,样品与KBr质量比为1∶100;Cary50型紫外可见分光光度计,单波长测量,波长为306 nm,5%CO2培养箱,超净工作台;TCL-16C离心机。
试剂:Mg(NO3)2·6H2O(固含量不少于 99%),分析纯,广东汕头市西陇化工厂有限公司;Al(NO3)3·9H2O(固含量不少于99%),分析纯,上海新宝精细化工厂;NaOH(固含量不少于96%),分析纯,天津市化学试剂三厂;甲氨蝶呤(MTX),浙江省湖州展望药业有限公司;乙醇(含量不少于 99.7%),分析纯,上海国药集团化学试剂有限公司;二甲亚砜(DMSO),分析纯,上海生物工程有限公司;小牛血清(BB001),上海生物工程有限公司;DMEM(编号PB0680)培养基,上海生物工程有限公司;MTT(Sigma编号T0793),上海生物工程有限公司;胰蛋白酶(PB0680),上海生物工程有限公司;酶标仪(Thermo MK4,USA);实验用水均为去离子水。
1.2 共沉淀法合成MTX/LDH
称取 0.769 2 g Mg(NO3)2·6H2O、0.562 7 g Al(NO3)3·9H2O溶于乙醇与水体积比为1∶3的混合溶液中,并转移至三颈烧瓶中,在恒定温度为60℃的条件下磁力搅拌,并通以氮气。将0.340 8 g的MTX溶于20 mL乙醇与2 mL 5%的氨水混合液中,迅速倒入三颈烧瓶中,用10%的氨水作为沉淀剂,控制沉淀剂以0.1 mL·s-1的滴加速率滴加到上述混合溶液中,调节溶液的pH值至9.5,恒温继续搅拌,保温1小时。待反应结束后,在4 000 r·min-1转速下将所得产物用无水乙醇离心洗涤2遍,并用去离子水离心洗涤3遍,每次离心时间为3 min,以清除吸附在表面的MTX。将沉淀分散于25 mL水中,转移至50 mL反应釜(内衬为聚四氟乙烯)内,80℃条件下水热处理6~48 h。水热处理完毕之后,干燥得到产物。
1.3 缓释性能研究
根据测出的载药量计算出做缓释性能实验所需的MTX/LDH的量,将称量好的MTX/LDH纳米复合物置于pH值为7.4(500 mL)的磷酸缓冲液(按照中国药典2005年版第二部附录XIVE方法配置)中,在(37±0.5)℃下恒温搅拌,一定的时间间隔内,取3 mL溶液10 000 r·min-1下离心30 s后取其上清液,用紫外-可见分光光度计在306 nm处测其吸光度,并根据标准曲线 A=0.051 85c+0.000 62(r=0.999 99,n=7)计算 MTX 的累积释放量。
1.4 MTT细胞生物实验
人肺癌A549细胞接种于100 mL的培养中,培养基为含有10%小牛血清的DMEM,置于37℃,5%CO2恒温培养箱内培养箱孵育,用显微镜观测待细胞长满培养瓶的80%~90%,用0.25%的胰蛋白酶消化,传代。用10%DMEM将悬浮的细胞接种到96孔板,每孔体积100 μL,正常培养24 h后吸走废液,加入不同浓度的 MTX和MTX/LDH,如 20、40、60、80、120 μg·mL-1(用 DMEM 稀释),每组设 6 孔重复,对照组加 100 μL DMEM(无血清),分别培养 24 h后弃除96孔板中的残药和DMEM,每孔加入新鲜DMEM(无血清)90 μL,10 μL MTT(5 mg·mL-1,pH=7.4的 PBS配制),继续培养4 h后,终止培养,小心吸弃孔内培养上清液,每孔加100 μL DMSO,震荡5 min,用酶标仪检测。
2 结果与讨论
2.1 XRD分析
图1为不同水热处理时间下制备的MTX/LDH的XRD图,考察了100℃下水热处理时间分别为6、12、24、36 和 48 h 下得到的 MTX/LDH 纳米复合物的性能。从图中可以看出水热处理时间较短(6 h)时,所得产物的XRD特征衍射峰峰值较低。12~48 h下制备的MTX/LDH纳米复合物都具有尖锐的(003)、(006)面特征衍射峰,基线低且平稳,衍射峰峰型窄且尖,表明制备的MTX/LDH纳米复合物晶相单一,晶体结构一致,晶面生长的有序程度高,结晶度好。分析XRD图可知,水热处理6 h后得到的样品,其衍射峰强度最低,结晶度最差,水热处理12 h后的样品衍射峰强度最高,峰形最好,这说明水热处理12 h后得到的MTX/LDH纳米复合物的晶型发育最完整。
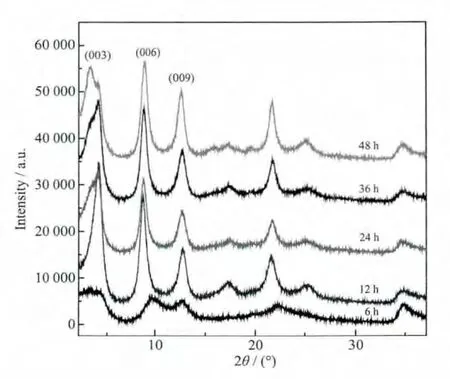
图1 不同水热处理时间下制得的MTX/LDH纳米复合物的XRD图Fig.1 XRD patterns of MTX/LDH nanohybrids obtained at different hydrothermal treatment time
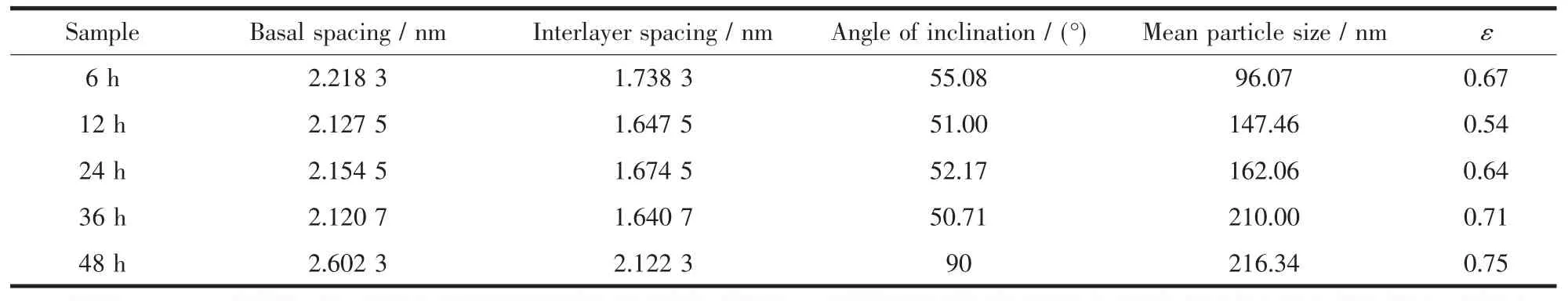
表1 不同水热处理时间下制备的MTX/LDH的晶体结构数据Table 1 Characteristic data of MTX/LDH nanohybrids obtained at different hydrothermal treatment time
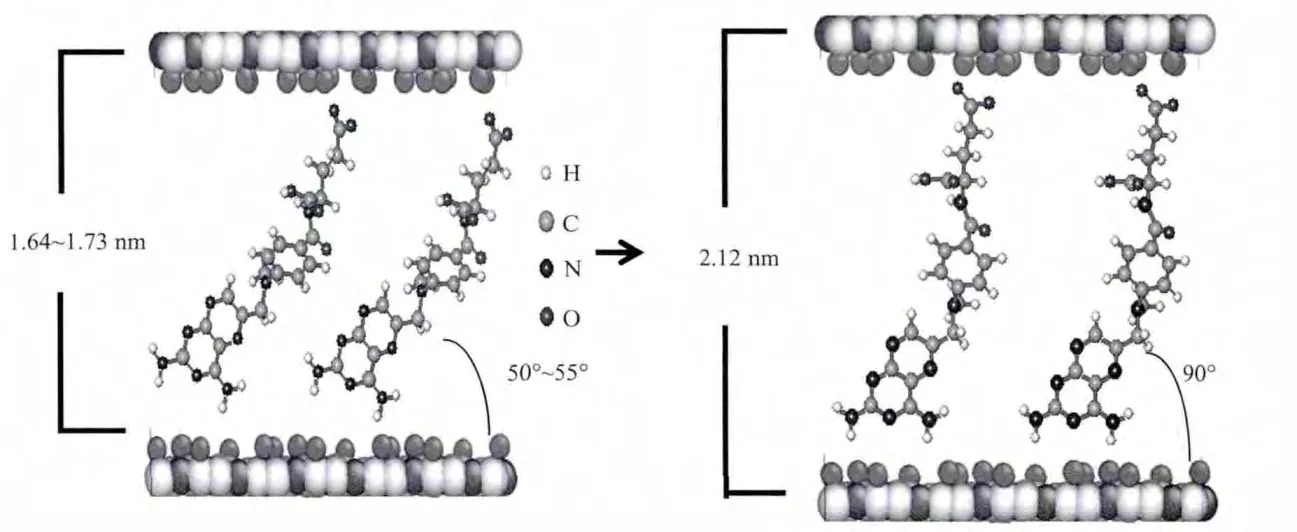
图2 不同水热处理时间下得到的MTX/LDH纳米复合物的排列方式示意图(左)6~36 h;(右)48 hFig.2 Scheme of the arrangement of MTX/LDH nanohybrids obtained at different hydrothermal treatment time(left)6~36 h;(right)48 h
表1为不同水热处理时间下得到的MTX/LDH纳米复合物的特征数据及平均粒径。根据布拉格公式可以计算出MTX/LDH的层间距,由于LDH层板厚度为0.48 nm[21],可以得到样品的通道高度随着水热处理时间的延长分别为 1.738 3、1.647 5、1.674 5、1.640 7 和 2.122 3 nm。甲氨蝶呤分子的长度为2.12 nm[22],据此我们模拟了不同水热处理时间下制得的MTX/LDH纳米复合物空间排列示意图,如图2所示:随着水热处理时间的增加,MTX在LDH层间从单分子倾斜排列变化到垂直单分子排列。平均粒径是通过测定多张(>50,保证200个粒子以上)TEM图中粒子的粒径得到的,也列于表1。从中可以看出:不同的处理时间对产物的层间距有非常大的影响,当水热处理时间较短时(6~36 h),MTX以单层倾斜的方式排列,当时间增加到48 h时,层间距急剧增大,MTX以单层垂直的方式排列。
2.2 FT-IR分析
图3显示了不同水热处理时间下得到的MTX/LDH纳米复合物的FT-IR光谱图。从图3可以看出,3 400 cm-1处的宽峰对应于LDH层板上和层间水分子的OH伸缩峰[23]。1 614 cm-1和1 456 cm-1处的吸收峰对应于MTX中芳香环的C=C伸缩振动峰[21],这些峰的出现表明MTX已经成功插层到LDH层间。1 207 cm-1处的吸收峰为MTX的C-N键。在低频振动区间,出现的吸收峰对应着点阵振动模式(Al-O,Mg-O,Al-O-Mg 等)。
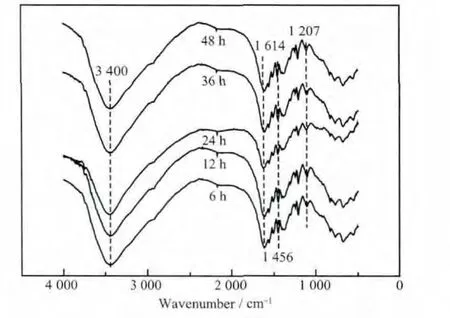
图3 不同水热处理时间下得到的MTX/LDH纳米复合物的FT-IR光谱Fig.3 FT-IR spectra of MTX/LDH nanohybrids obtained at different hydrothermal treatment time
2.3 TEM图分析
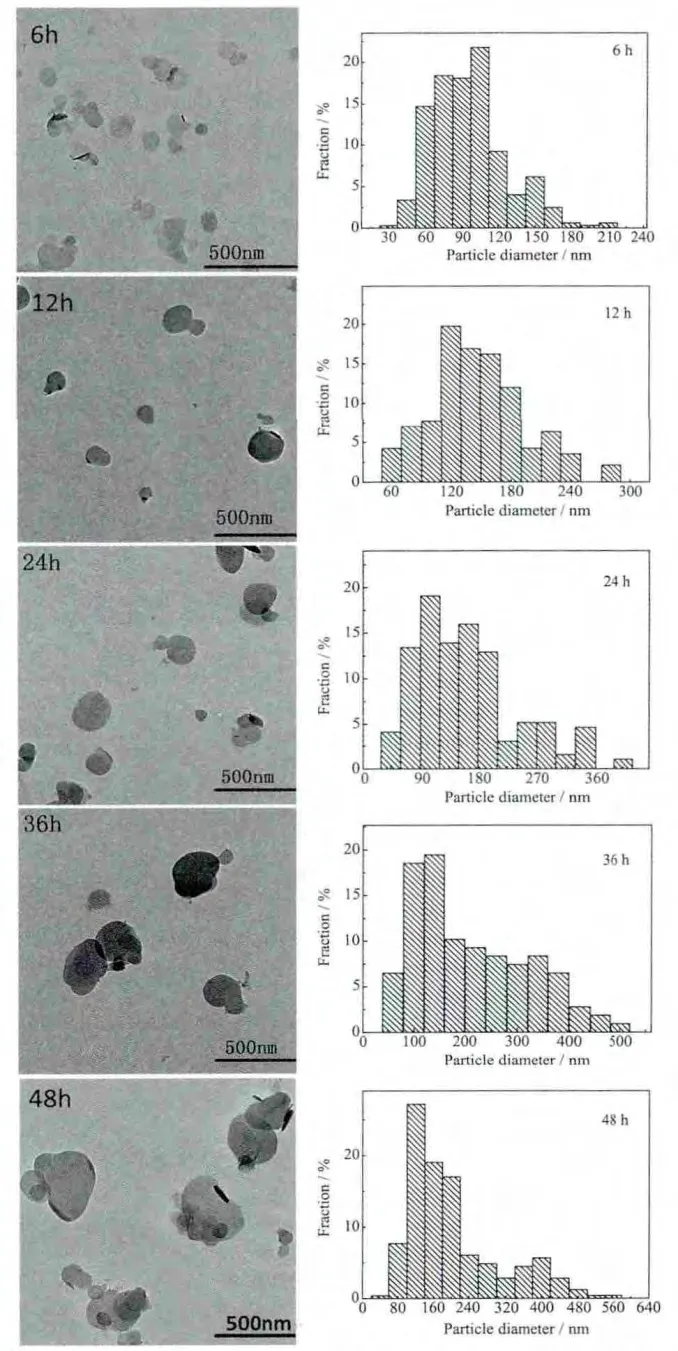
图4 不同水热处理时间下制备的MTX/LDH纳米复合物的TEM图和粒径分布图Fig.4 TEM images and distribution of particle size of MTX/LDH nanohybrids obtained at different hydrothermal treatment time
图4为不同水热处理时间下制备的MTX/LDH纳米复合物的形貌及相应的粒径分布图。从TEM图中可以观察到不同水热处理时间下制备的MTX/LDH纳米复合物基本呈圆形,水热处理时间的不同导致了粒子粒径发生变化。随着水热处理时间的延长,粒子粒径逐渐变大。但水热处理时间过短或过长则会导致单分散性降低、形貌不规则程度的加剧。不同水热处理时间下得到的MTX/LDH纳米复合物的平均粒径列于表1中。从表中可以看出,随着水热处理时间的延长,MTX/LDH粒子的平均粒径逐渐增大,增加速率先快后慢。48 h时粒径最大。从TEM图中可看出处理时间为6 h或超过24 h后,粒子单分散性变差,粒径均匀度变差。12 h和24 h得到的粒子单分散性好且粒子形状均匀。综上所述,从粒子形貌、单分散性、结晶度等角度来分析,12 h样品的物化性能最为优良。
2.4 缓释性能研究
首先对不同水热处理时间得到的5种样品进行了载药量的测定,6~48 h样品的载药量分别为42.6%、52.3%、47.6%、52.7%和 51.5%,据此可以看出,LDH是一类载药能力很强的载体,复合物的平均粒径与其载药量之间并无直接关系。图5为这5种样品的缓释曲线图。从图中可以看出,5种样品均呈现出良好的缓释性能,释放速率先快后慢,前150 min是一个较为快速的释放过程,而以后的150~500 min释放速率缓慢,整个过程中未出现突释现象。这种释放模式非常适合临床应用,开始时的快速释放能满足最初的治疗目的,而后来的控释-缓释模式则能保持体内药物浓度的稳定,从而达到最佳的治疗。其中48 h样品释放速率最慢,从表1可以看出,48 h样品与36 h样品粒径相近,分别为216.34 nm 和 210.00 nm,而 MTX 在 LDH 层间排列方式有较大差异,36 h样品中MTX在LDH层间的倾斜角度为50.71,48 h样品MTX在LDH层间以单层垂直方式排列。从图5中可以看出36 h样品的释放速率远远大于48 h样品的释放速率:100 min时,36 h的释放达到63%,而48 h样品仅为54%,500 min时,36 h最终释放率为75%,48 h样品仅达到66%。这说明了层间排列方式的不同导致了其释放速率不同,层间倾斜角度越大,释放速率越慢,与段雪等人的结论一致[24],段雪的研究表明层间阴离子在层间的不同排布方式会极大地影响其释放速率。
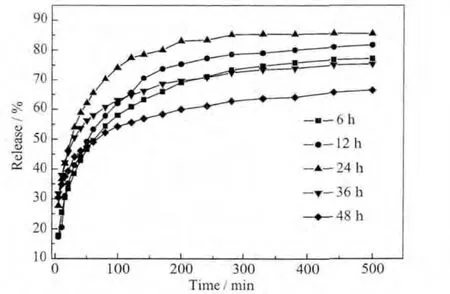
图5 不同水热处理时间制得的MTX/LDH纳米复合物的释放曲线图Fig.5 Release profiles of MTX/LDH nanohybrids obtained at different hydrothermal treatment time
2.5 动力学模拟
一般来讲,生物药物/LDH纳米复合物的释药机制主要有两种:离子交换机理和LDH片层的溶蚀[25]。为了探索MTX/LDH纳米复合物的释药机理,通常采用以下4种常用的数学模型对MTX/LDH的释放过程进行拟合[26-27]。
(1)一级方程:ln(1-Mt/M∞)=-kt,多用于描述释放基质溶解所引发的药物释放行为和离子交换过程;
(2)Higuchi方程:Mt/M∞=kt0.5,它是以 Fickian 扩散定律为基础提出的动力学方程,适用于遵循扩散控释机理的释药过程;
(3)Bhaskar方程:ln(1-Mt/M∞)=-kt0.65,用于描述不规则扩散或者粒内扩散机理;
(4)Ritger-Peppas方程:Mt/M∞=ktn,其中 n 为表征释放机制的特征参数。当 0.45<n<0.89 时,药物的释放机制为non-Fickian扩散,即扩散与溶蚀并存;当 n<0.45 时,为 Fickian 扩散;当 n>0.89 时,为骨架溶蚀机制;
以上4个方程中,其中Mt为t时间的累积释放量,M∞为∞时累积释放量,Mt/M∞为t时累积释放率,k为释放常数。
采用这4种常用的数学模型对MTX/LDH的体外释放数据进行动力学拟合,其结果示于图6,拟合数据列于表2。由拟合结果可知,采用First-order方程拟合得到的拟合因子R均较小,从图6中可看出其拟合数据点离散严重,说明MTX/LDH纳米复合物的释药机制不符合First-order方程。相对于Firstorder方程,采用Bhaskar方程拟合得到的拟合因子相对较高(仅 24 h 样品的 R<0.95),初步判断 MTX/LDH纳米复合物在pH=7.4的磷酸缓冲液中释放出MTX分子的机制属于扩散机制。进一步采用Ritger-Peppas方程,从拟合结果 R>0.96 及 n<0.45 可判定,MTX/LDH纳米复合物的释药机制属于离子交换机理,且释放过程为扩散控制过程。最后采用parabolic-diffusion模型拟合得到了最高的拟合因子(R>0.98),说明MTX/LDH纳米复合物的释药机制为粒内扩散或表面扩散所引起的扩散控制过程;也就是说,MTX/LDH纳米复合物在释放过程中主要是介质中的HPO42-、H2PO4-将LDH层间的MTX阴离子置换出来,使得层间的MTX阴离子进入到缓释介质中。综上,MTX/LDH在模拟体液中释放出MTX的机理为基于离子交换的多相扩散过程,parabolicdiffusion模型能很好地阐述其释放机理。
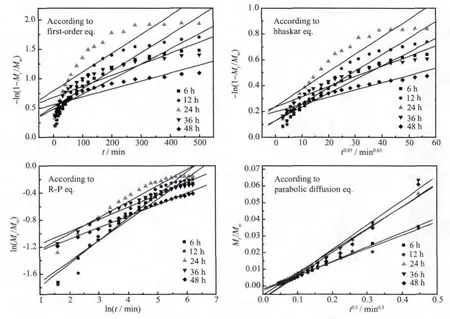
图6 不同水热处理时间下得到的MTX/LDH纳米复合物释放过程的动力学拟合直线Fig.6 Plots of different kinetic models for the release of MTX from the MTX/LDH nanohybrids obtained at different hydrothermal treatment time
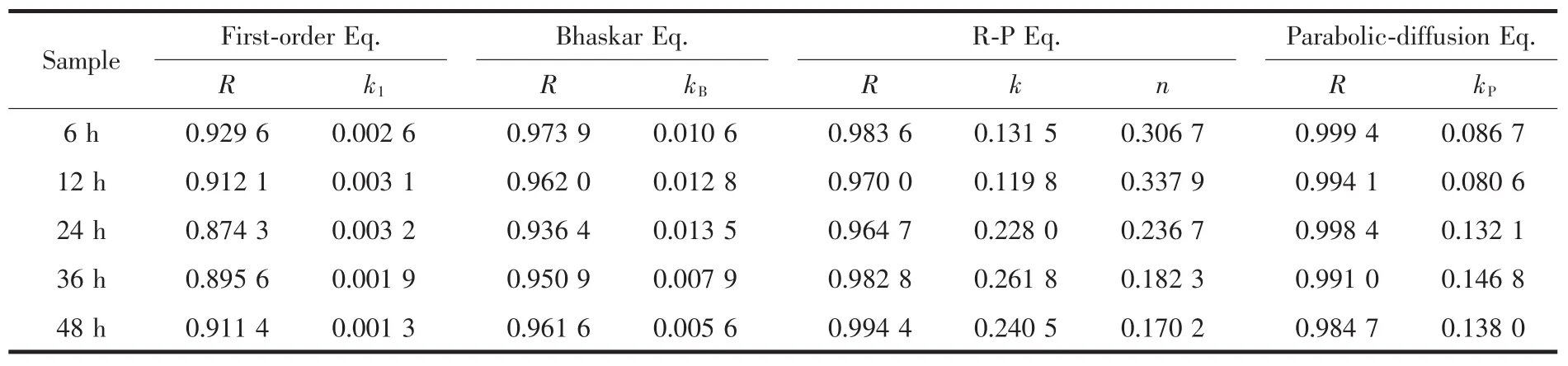
表2 不同水热处理时间下制得的MTX/LDH纳米复合物释放过程的动力学拟合数据Table 2 Fitting parameters of different kinetic models for the release of MTX from the MTX/LDH nanohybrids obtained at different hydrothermal treatment time
2.6 细胞生物实验探索
MTX/LDH纳米复合物对某些癌细胞有非常明显的抑制效果,关于MTX/LDH纳米复合物抗癌-抑癌作用的研究,韩国科学家Choy等作出了大量的工作,他的研究结果表明,LDH母体即使在很高的浓度下对人体也是无害的,MTX/LDH纳米复合物的抗癌效果随着作用时间的延长而增加,随着复合物浓度的增加而增强;粒径在100~300 nm之间的复合物对癌细胞的摄入和治疗效果最佳[16-17,28]。但是影响复合物抗癌-抑癌效果的关键因素目前还未有相关的报道,我们试图进行这方面的探索性研究。因而我们引入了一个新的参数:分散系数ε,ε与粒子的粒径和单分散性有关。ε值的提出鉴于这样的出发点:合成的复合物粒子粒径越均匀,它对癌细胞的抑制作用越均匀与稳定;粒径越小,因表面效应而产生的抑癌效果越明显。其定义式如下:

其中D是平均粒径,D为所测粒子的半径,n为所测粒子的数目,δ为标准偏差,ε值越小表明该体系的分散性越好。不同水热处理时间下得到复合物的ε值列于表1,同时复合物对肺癌细胞A549的抑制效果与ε的关系见图7。从图7可以看出,复合物的抗癌效果与ε值密切相关,ε值越小,复合物的抑癌-抗癌效果越明显;而复合物的平均粒径与其抗癌效果之间并无直接关系。从我们的研究结果还可以看出抗癌效果最好的12 h样品,其粒子形貌最规则、单分散性最好、晶型发育最完整、载药量也很高。这说明MTX/LDH纳米复合物的物化性能与抗癌效果之间存在着某种密切的关系。而这种关系我们首次利用分散系数ε进行了量化处理。我们试图通过这个参数来量化构建MTX/LDH纳米复合物的结构-药效相关性,当然其科学性和准确性还需进一步的研究确认。
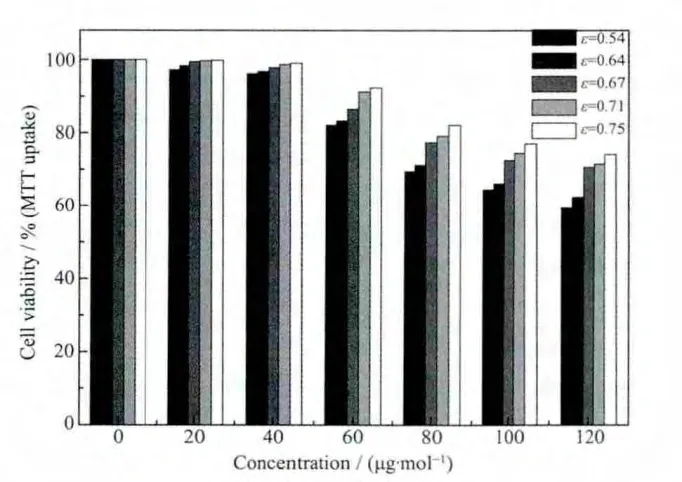
图7 MTX/LDH纳米复合物的抗癌效果与ε值的关系Fig.7 Comparison of Cell viability tests for MTX/LDH nanohybrids with different ε values
3 结 论
通过改变水热处理时间来调控MTX/LDH纳米复合物的粒径以及单分散性,研究表明水热处理时间的不同会导致复合物的粒径、单分散性以及结晶度的不同,据此在宏观上可以通过控制水热处理时间来制备不同性质的MTX/LDH纳米复合物。将得到的5种MTX/LDH纳米复合物作用于肺癌细胞A549进行细胞生物实验,对实验结果首次采用分散系数ε构建MTX/LDH纳米复合物的结构-药效相关性。研究表明,ε值越小,该复合物体系的分散性越好,相应地对肺癌细胞A549的抑制效果越明显。
[1]Iyi N,Sasaki T.Appl.Clay Sci.,2008,42:246-251
[2]Kang H L,Huang G L,Ma S L,et al.J.Phys.Chem.C,2009,113:9157-9163
[3]Zhao M Q,Zhang Q,Jia X L,et al.Adv.Funct.Mater.,2010,20:677-685
[4]Oh J M,Biswick T T,Choy J H.J.Mater.Chem.,2009,19:2553-2563
[5]JIA Chun-Xiao(贾春晓),ZHANG Xiao-Qing(张晓晴),LI Shu-Ping(李淑萍).Chinese J.Chem.(中国化学),2012,30:277-282
[6]Bubniak G A,Schreiner W H,Mattoso N,et al.Langmiur,2002,18:5967-5970
[7]Wei M,Shi S,Duan X,et al.J.Solid State Chem.,2004,177:2534-2541
[8]Leroux F,Besse J P.Chem.Mater.,2001,13:3507-3515
[9]Choy J H,Kwak S Y,Jeong Y J,et al.Angew.Chem.Int.Ed.,2000,39:4041-4045
[10]Yang J H,Han Y S,Park M,et al.Chem.Mater.,2007,19:2679-2685
[11]Katherine M T,Scott S R,Emmanuel G P.J.Controlled Release,2004,95:501-507
[12]Kwak S Y,Kriven W M,Wallig M A,et al.Biomaterials,2004,25:5995-6001
[13]Edward W B,Jeffes III,Jerry L,et al.J.Invest.Dermatol.,1995,104:183-188
[14]Chow M,Koo J,Ng P,et al.Mutat.Res.,1998,413:251-264
[15]Seitz M.Curr.Opin.Rheumatol.,1999,11:226-232
[16]Oh J M,Park M,Kim S T,et al.J.Phys.Chem.Solids,2006,67:1024-1027
[17]Oh J H,Choi S J,Kim S T,et al.Bioconjugate Chem.,2006,17:1411-1417
[18]DU Xue-Yan(杜雪岩),CHEN,Yin-Ze(陈尹泽),MA Y-X(马应霞),et al.Appl.Chem.Ind.(应用化工),2008,37:1449-1452
[19]QI Feng-Lin(齐凤林),LI Shu-Ping(李淑萍),ZHANG Xiao-Qing(张晓晴).Acta Chim.Sinica(化学学报),2012,70:2162-2168
[20]WANG Ji-Qin(王继芹),LI Xin(李鑫),LI Shu-Ping(李淑萍),et al.Acta Chim.Sinica(化学学报),2011,69:137-144
[21]Aisawa S,Takahashi S,Ogasawara W,et al.J.Solid State Chem.,2001,162:52-62
[22]Choy J H,Jung J S,Oh J M,et al.Biomaterials,2004,25:3059-3064
[23]Li B X,He J,David G,et al.Appl.Clay Sci.,2004,27:199-207
[24]MENG Jin-Hong(孟锦宏),ZHANG Hui(张慧),DUAN Xue(段雪),et al.Chinese Sci.Bull.(科学通报),2005.50:208-214
[25]Xu Z P,Lu G Q.Pure Appl.Chem.,2006,78:1771-1779
[26]Zhang H,Pan D K,Duan X.J.Phys.Chem.C.,2009,113:12140-12148
[27]Li F S,Jin L,Han J B,et al.Ind.Eng.Chem.Res.,2009,48:5590-5597
[28]Choi G,Kim S Y,Oh J M,et al.J.Am.Ceram.Soc.,2012,95:2758-2765

