铂类抗肿瘤药物的研发进展及市场情况
张建忠 柯樱 沈佳琳
(上海医药集团股份有限公司 上海 200020)
铂类药物的研究最早兴起于40年前,1967年美国密执安州立大学教授Roserlberg等[1]首次发现顺铂具有抗肿瘤活性。这一发现迅速引起了肿瘤界的广泛兴趣,之后铂类抗肿瘤药物的研究成为热点,随着一个个有历史意义的试验结果的公布,肿瘤化疗疗效有了大幅度地飞跃。1995年WHO对上百种抗肿瘤药物进行排名,顺铂在疗效及市场等方面的综合评价位于第二位。有统计数据表明,我国所有的化疗方案中有70%~80%以铂为主或有铂类药物参加配伍[2]。同时,铂类金属药物也是当前抗肿瘤药物最为活跃的研究开发领域之一,新的铂类抗肿瘤药奥沙利铂、洛铂等已相继推出。铂类药物的抗肿瘤作用机制也有了进一步了解。现就其作用机制、国内外上市开发现状、国内外销售情况及国内研究开发进展等进行综述。
1 作用机制
1.1 细胞生物学机制
几乎所有的肿瘤细胞都具有一个共同的特点,即与细胞增殖有关的基因被开启或激活,而与细胞分化有关的基因被关闭或抑制,从而使肿瘤细胞表现为不受机体约束的无限增殖状态。从细胞生物学角度,诱导肿瘤细胞分化,抑制肿瘤细胞增殖或者导致肿瘤细胞死亡的药物均可发挥抗肿瘤作用。
1.2 铂类抗肿瘤药物的抗肿瘤作用机制
铂类抗肿瘤药物的抗肿瘤作用机制与传统的抗肿瘤药不同,通过大量的研究和实验,初步确定铂类抗肿瘤药物的抗癌机制可分为4个步骤:跨膜转运、水合解离、靶向迁移、作用于DNA,引起DNA复制障碍,从而抑制癌细胞的分裂。与其他抗肿瘤药一样,铂类抗肿瘤药影响DNA合成的作用是非特异性的。但癌细胞比正常细胞增殖快,合成DNA迅速,并且DNA受损后的修复功能不完善,因此,癌细胞对抗肿瘤药的细胞毒作用更为敏感,从而显示出药物的抗肿瘤作用[3]。
铂类化合物的抗肿瘤作用主要在于其类似双功能基烷化剂,DNA是其作用的关键靶点。以顺铂为例,其进入体内后在低氯环境中氯解离,形成水合阳离子,主要与DNA等生物大分子结合形成共价键。DNA上主要的结合位点是G和A的N7,由于DDP与两个位点结合,故理论上可以形成链内交联、链间交联、DNA一蛋白质分子间交联,从而使DNA链局部扭结或解旋,阻止DNA聚合酶推进,致使DNA复制、转录失败,造成肿瘤细胞死亡。其中链内交联占大部分,链间交联的形成不到5%。由此可见,铂类化合物是一类周期非特异性抗肿瘤药物。虽然铂类重金属化合物抗肿瘤作用机制类似,但不同铂类化合物的适应证、毒性反应不尽相同。铂配合物进入肿瘤细胞后水解成水合物,该水合物进一步去质子化生成羟基化的配位离子,这些离子均活泼,在体内与DNA的两个鸟嘌呤碱基N-7位络合成一个封闭的五元螯合环,从而破坏了两条多核苷酸链上嘌呤和胞嘧啶之间的氢键,扰乱DNA的正常双螺旋结构,使其局部变性失活而丧失复制能力[4]。
2 国内外铂类抗肿瘤药的上市现状
目前国内外已上市的主要铂类抗肿瘤药情况见表1。
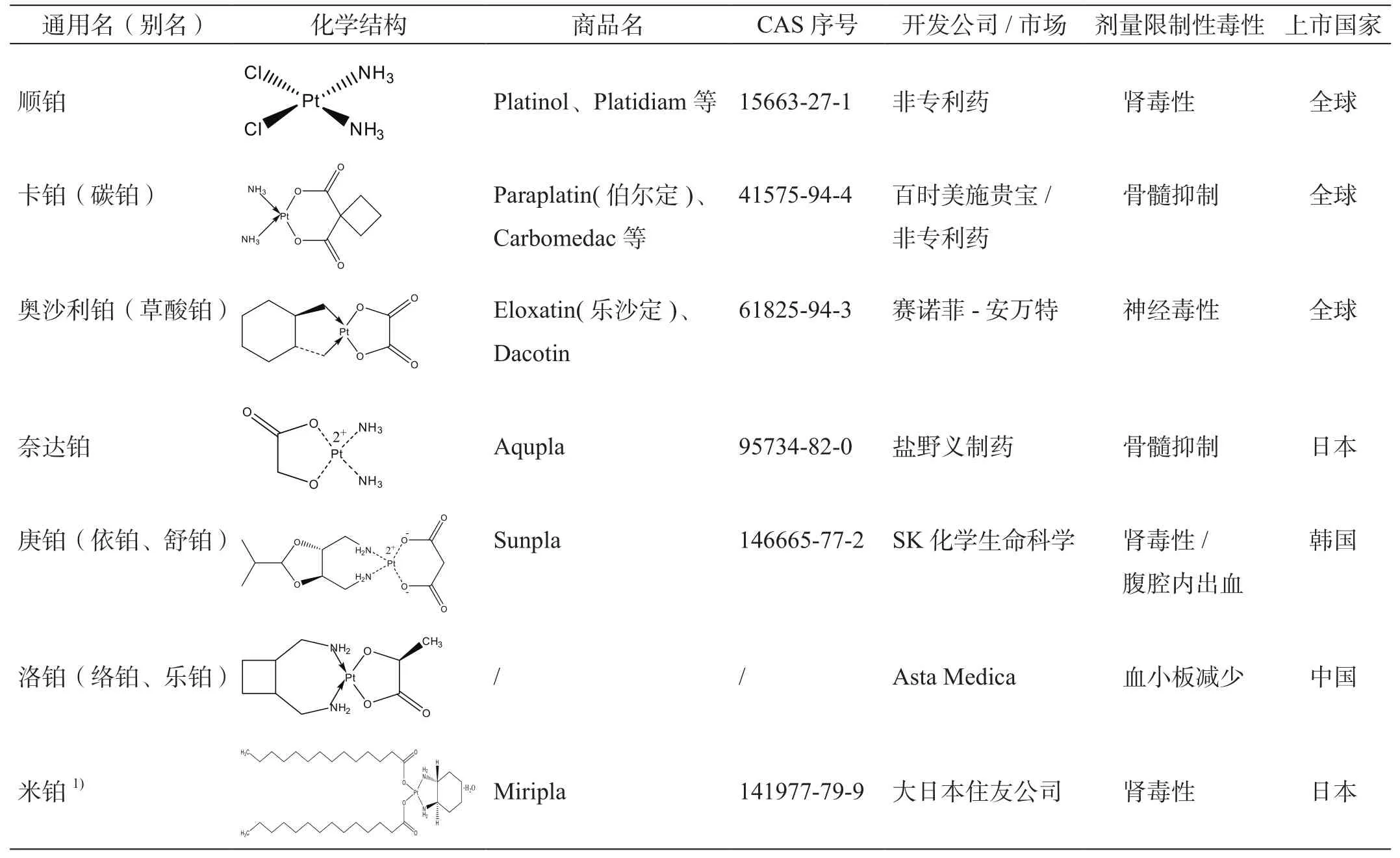
表1 国内外已上市的铂类抗肿瘤药概况[5]
2.1 顺铂 (cisplatin,DDP)
顺铂是顺二氯二氨合铂(Ⅱ)的简称,缩写为DDP或CDDP(Ⅱ)。1979年首次在美国上市,是第一个上市的铂类抗肿瘤药物,目前已被收录入中、美、英等国的药典。在我国以顺铂为主或有顺铂参与配伍的化疗方案占所有化疗方案的70%~80%。顺铂仍是目前应用最广泛的药物之一,含铂类化疗方案是晚期非小细胞肺癌的首选方案,亦是小细胞肺癌的主要组方之一。顺铂是头颈癌单药有效率最高的药物之一;顺铂加五氟尿嘧啶(5-FU)是头颈癌化疗的标准方案之一,联合紫杉醇、 吉西他滨亦是非常有前景的头颈癌化疗方案。顺铂及卡铂一直是治疗睾丸癌(尤其是非精原细胞性)、卵巢癌的主要治疗药物。顺铂与其他化疗药物联合是侵袭性膀胱癌、骨肉瘤、食管癌、胃癌等的标准化疗方案。
如今,顺铂是治疗睾丸癌、卵巢癌、膀胱癌、头部和颈部肿瘤、小细胞和非小细胞肺癌最广泛使用的抗癌药物之一。尽管顺铂临床上有很好的疗效,但它缺乏对肿瘤组织的选择性,导致一些严重的副作用,如肾功能损害,神经毒性,耳毒性(平衡/听力损失)。此外,长期或大剂量顺铂治疗可能引起严重的贫血。为了解决这些问题,新的顺铂类似物,第二代和第三代铂类药物在过去30年多年被开发出来[5]。
此外,Okuda等[6]用顺铂联合长春瑞滨治疗晚期非小细胞肺癌伴有间质性肺疾病(ILD)急性发作的患者,共19例,结果显示应答率为42.1%,无进展生存时间为4.4个月,中位生存时间为7.4个月,1年生存率为36.8%。中性粒细胞减少症是最常见的3到4级的毒性,在63.2%的患者之间发生;化疗相关的ILD急性加重有3例(15.8%)发生,导致1个病人死亡(5.3%)。结论是顺铂和长春瑞滨联合化疗可作为晚期非小细胞肺癌患者有ILD的治疗选择。
2.2 卡铂 (carboplatin,CBP)
卡铂是由美国施贵宝公司、英国癌症研究所及Johnson Matthey公司于20世纪80年代合作开发,是进入临床的第2个铂类络合物。卡铂结构上以CBDCA取代顺铂分子上的两个氯离子,增加了化合物的水溶性。卡铂毒副作用小,疗效与顺铂相似。卡铂的化学稳定性好,与顺铂相比,肾、耳、神经毒性明显降低,剂量限制性毒性为骨髓抑制,毒性作用呈剂量依赖性,作用机制相同,因此可替代顺铂用于某些肿瘤的治疗;与非铂类抗肿瘤药物无交叉耐药性,可与多种抗肿瘤药物联合使用。卡铂除可作为非小细胞肺癌(NSCLC)、小细胞肺癌(SCLC)、卵巢癌(上皮)、胚细胞瘤、肝胚细胞瘤5种肿瘤的首选治疗药物外,还可作为膀胱癌、子宫内膜癌、子宫颈癌、生殖细胞癌、肾癌、头颈部癌、成神经细胞癌、成视网膜细胞癌8种肿瘤的次选治疗药物[7],临床推荐剂量为300 ~ 400 mg/m2。
Tsubamoto等[8]在一项多中心Ⅱ期临床试验进行卡铂联合伊立替康治疗卵巢上皮癌患者的化疗,采用静脉注射伊立替康和卡铂的方法,在2005至2009年之间,跟踪统计了40例卵巢癌患者,平均年龄59岁,结果显示总体反应率为43%,其中患者在最近1次治疗后无铂类治疗间隔期小于6个月,反应率为21%,中位无进展生存期为3.7个月,而患者在最近1次治疗后无铂类治疗间隔期大于等于6个月的,反应率为52%,中位无进展生存期为9.1个月,3至4级的毒性包括中性粒细胞减少65%,血小板减少48%,发热性中性粒细胞减少5%,恶心5%,腹泻5%和疲劳5%。
2.3 奥沙利铂(oxaliplatin,L-OHP)
奥沙利铂是草酸-(反式-1-1,2 -环己烷二胺)合铂的全称,是由瑞士Debiopharm公司研制开发,法国Sanofi公司生产销售。它作为一种稳定的、水溶性铂类烷化剂,是第一个明显对结肠癌有效及在体内外均有广谱抗肿瘤活性的铂类抗肿瘤药物,对耐顺铂的肿瘤细胞亦有作用。它最初于 1996年在法国上市,用于治疗结(直)肠癌等肿瘤。国家食品药品监督管理局于2000年批准了该国产药在国内上市。由于奥沙利铂突出的疗效 ,美国 FDA于2002年也正式批准了其在美国的临床应用。与顺铂、卡铂相比,奥沙利铂具有口服吸收良好、无交叉耐药性、抗肿瘤活性谱广等优点[5]。
2.4 奈达铂 (nedaplatin,CDGP)
奈达铂由日本盐野义制药公司研制开发,研发代号254-S,于1995年6月首次在日本上市,我国对该药物的研究较早,2003年由南京东捷药业(后被先声并购后并入先声东元制药)最先实现国产化,商品名捷佰舒,全称是顺式-乙醇酸-二氨合铂(Ⅱ),缩写CDGP。
在日本,奈达铂获准的适应证有头颈部癌、小细胞肺癌、非小细胞肺癌、食管癌、膀胱癌、睾丸癌、卵巢癌、子宫颈癌等。最大耐受量80 mg/m2。有临床研究显示奈达铂联合其他化疗药物治疗复发或顺铂耐药的生殖细胞肿瘤、头颈部鳞癌等有显著疗效。一项研究将奈达铂与多西紫杉醇联合化疗作为复发或耐药的食管癌二线治疗,结果显示此方案安全性与有效性较好,不良反应低。奈达铂的剂量限制性毒性为骨髓抑制所致的血小板减少。由于其肾、消化道系统毒性均明显低于顺铂,不需要水化利尿,故对于老年人及合并肾功能不全的肿瘤患者可被认为是一种安全、有效的药物[9]。
Ⅲ期试验证实顺铂/长春碱和奈达铂/长春碱治疗NSCLC的疗效相似。有人用小剂量奈达铂/5-FU联合放疗治疗食管癌,部分应答率为80%,完全应答率为50%。另有实验证明,紫杉醇+奈达铂方案对人卵巢癌的疗效比紫杉醇+卡铂或顺铂方案更好。
2.5 庚铂 (heptaplatin,sunpla)
庚铂(SKI-2053R)又名依铂(eptaplatin)或舒铂(sunpla,sunplatinum),由韩国Sunkyong工业研究中心开发,于1999年在韩国上市,化学名为顺丙二酸双氨甲基异丙基二氧戊环合铂(Ⅱ) (cis-malonato[(4R,5R)-4,5-bis(aminomethyl)-2-isopropyl-1,3-dioxolane]platinum(Ⅱ)),其水溶性好,稳定性高,与DNA 交联后阻止DNA 复制和转录,抑制细胞有丝分裂,为非周期特异性抗肿瘤药。
临床试验表明,其对胃癌有一定的疗效,与氟尿嘧啶联用治疗胃、肠道癌和子宫癌、小细胞癌的疗效与顺铂相似,不良反应小于卡铂。临床常见不良反应有恶心、呕吐等胃、肠道反应,少数有腹泻、头痛、失眠及皮疹等现象;白细胞降低和血小板减少等血液毒性、骨髓抑制及肾毒性损害等为剂量限制性毒性,停药后症状可迅速恢复[9]。
2.6 洛铂(lobaplatin, D-19466)
洛铂又名络铂或乐铂,化学名二氨甲基-环丁烷-乳酸合铂,该药由德国Asta Medica AG Frankfurt开发。其作用机制除影响DNA的合成、复制以外,还可以影响原肿瘤基因c-mye基因的表达。该药的抗肿瘤效果与顺铂和卡铂的作用相当或者更好。洛铂对多种肿瘤有效,许多对顺铂和卡铂有应答的患者对洛铂也有应答,无论是初治或经最初的治疗病情未缓解者。洛铂与顺铂无交叉耐药,而且还能克服某些临床肿瘤模型对顺铂的耐药性。骨髓抑制是其剂量限制性毒性,主要表现为可恢复性血小板减少。它的最大耐受剂量为60 mg/m2,每3~4周1次。也可见剂量依赖性的恶心、呕吐、厌食、嗜睡等不良反应发生。临床上主要用于治疗慢性粒细胞性白血病、不能手术的转移性乳腺癌、转移性小细胞肺癌[5]。
2.7 米铂 (miriplatin)
米铂注射液(miriplatin hydrate)是大日本住友制药株式会社开发的脂溶性铂复合物抗癌药,于2009 年10月16 日获得日本厚生劳动省批准,用于治疗肝细胞癌。本品专用混悬液已于同年8 月20 日获得批准。2010 年1月20 日,米铂注射液及其专用混悬液同时上市销售,商品名为miripla。本品是溶于专用碘化罂粟子油脂肪酸乙酯、肝动脉内给药的抗癌药物,其与碘化罂粟子油脂肪酸乙酯的亲和性高,且肝动脉内给药后滞留于肿瘤部位,混悬液中的铂成分可长时间缓慢释放进入血液或组织中,铂二价化合物与DNA 结合,通过阻止DNA 合成抑制癌细胞增殖,提高了抗癌效果。Ⅱ期A 阶段临床试验结果表明:本品给药后血中总铂浓度(ng)等级极低,属微量且维持时间长,给药后约1 年Cmax大约降至17%。未见等级4 的严重不良反应,所见不良反应几乎都在给药后4~6周消失,可控且在耐受范围。本品对肝细胞癌的疗效(TE)良好,CR 率达60%[10]。 Aramaki等[11]将米铂与表柔比星注射液对照治疗经导管肝动脉化疗栓塞术(TACE)局部控制的肝癌患者,42例采用表柔比星、27例采用米铂治疗。显示结果,应答率(患者完全缓解和部分缓解)表柔比星组和米铂组分别为85.7%和81.5%,无进展生存期分别为5.1个月和7.5个月。
3 国外在研的铂类抗肿瘤药
3.1 研发进展
当顺铂(DDP)被发现有抗肿瘤作用后,科学家就不懈地在以铂为中心的结构上竭尽变化,其根本目的在于降低毒性、克服耐药性、扩展抗瘤谱。共衍生出下列铂类化合物及其进入临床的代表药物(表2)。

表2 铂类药物的类别及进入临床的代表药物
自20世纪60年代发现顺铂具有抗肿瘤活性以来,铂类金属抗肿瘤药物的应用和研究得到了迅速的发展。但作为抗肿瘤药物投入临床的仅30种左右,其中20多种因抗肿瘤活性弱或毒性过强而被淘汰,表2中多数代表药物也在淘汰之列。目前有6个药物仍在临床试验阶段,极有可能获得批准,其中沙铂和吡铂处在Ⅲ期临床试验,试验中都表现出了良好的疗效,且口服有效;NDDP和BBR 3464处在Ⅱ期(表3)。另外两个药为prolindac和lipoplatin,如果获批,它们将是最先上市的多聚体或脂质体铂类化合物[12]。
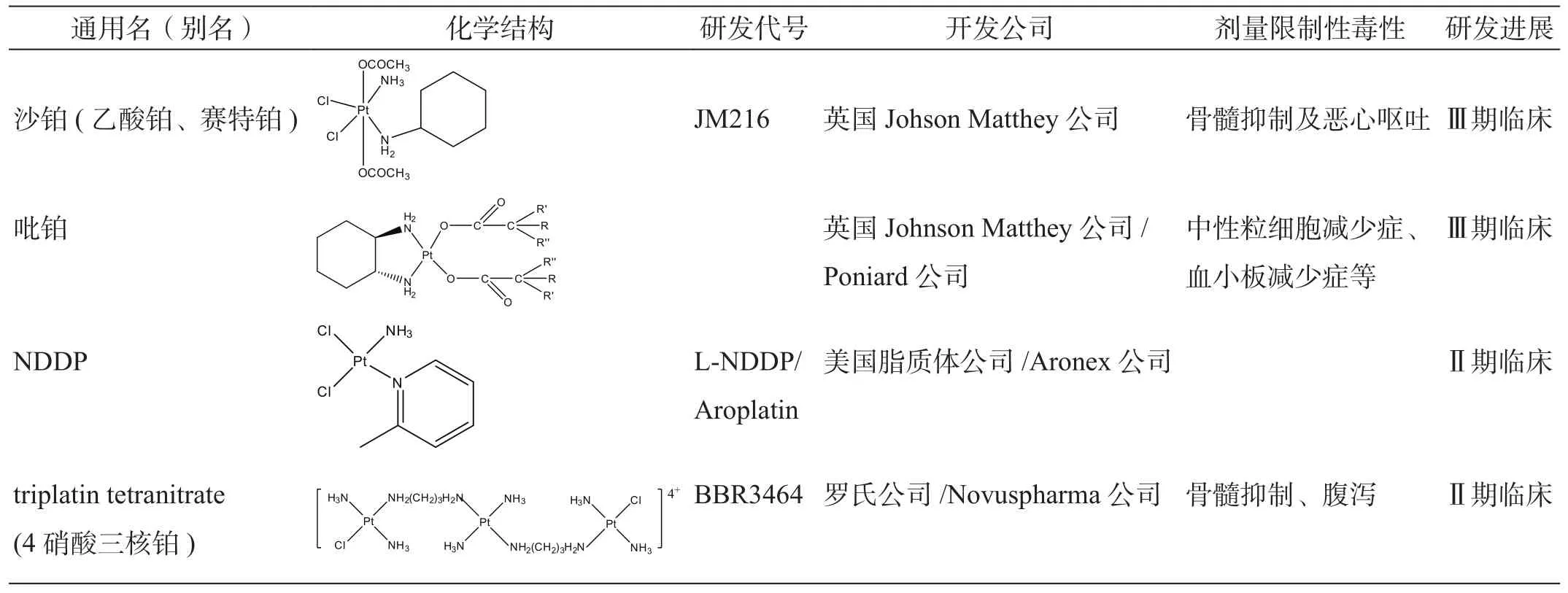
表3 国外在临床并有上市前景的铂类抗肿瘤药
3.2 沙铂(satraplatin, JM216)
沙铂又名乙酸铂或赛特铂,化学名为顺式-二氯-反式-乙酸(氨环己胺)合铂。由美国施贵宝公司、英国Johson Matthey公司和美国癌症研究所共同开发。JM216的结构已完全不同于顺铂或卡铂,而是混胺二羧酸4价铂的配合物,合成比顺铂或卡铂复杂得多,包括多步取代和氧化反应。JM216在1992年就进入了临床试验,是第一个进入临床验证的口服铂类药物。与鬼臼素有协同抗肿瘤作用。其剂量限制性毒性为骨髓抑制及恶心呕吐。Ⅱ期单药临床研究可以看出,该药对SCLC和激素抵抗的前列腺癌(HRPC)有效。Ⅲ期临床试验预计考察沙铂与泼尼松联合方案治疗HRPC的疗效。原计划入组380例病例,但由于施贵宝公司投资终止,只完成了50例,结果显示沙铂和泼尼松联合用药与泼尼松单独组相比,导致PSA反应显著增加(33%比9%;P= 0.046)和中位数无进展生存期(PFS)(5.2个月和2.5个月;P= 0.023)。沙铂总的中位生存时间为15个月,泼尼松组约12个月。沙铂至今还没有在任何一个国家获批准。目前沙铂联合多西他赛治疗前列腺癌、联合紫杉醇治疗非小细胞肺癌、联合卡培他滨治疗晚期实体瘤等的各期临床试验仍在进行中,疗效有待进一步验证。该药口服抗肿瘤活性高,疗效与顺铂相当而且与顺铂不产生交叉耐药,是一种具有开发前景的第三代铂类抗肿瘤药[13]。
3.3 吡铂 (picoplatin)
吡铂是一种能够克服铂类耐药的铂类似物,吡铂是为对抗谷胱甘肽介导的耐药而设计研发,它的独特构象使其免受亲核基团尤其是巯基的攻击。体外实验证实它作用于顺铂、卡铂和奥沙利铂耐药的细胞仍有效。吡铂于1997 年进入临床试验,最大耐受剂量为150 mg/m2,剂量限制性毒性主要是中性粒细胞减少症、血小板减少症、恶心和呕吐。一项比较吡铂联合最佳支持治疗(BSC)与BSC对比的Ⅲ期临床试验(SPEAR研究)最近被公布,选择既往铂类化疗在6个月内进展的SCLC患者,共401例,按照2∶1比例随机分组,吡铂组和BSC组的中位生存时间分别为21 周和20 周(P=0.09)。既往治疗未缓解或在45天内复发的患者生存期有改善,两组的PFS和TTP均无统计学差异。研究者认为生存未达到统计学意义可能和后续治疗不均衡有关,回顾性分析显示对于既往治疗未缓解或在45天内复发的患者生存期有显著改善。研究结果表明其一线和二线治疗晚期非小细胞肺癌、二线治疗小细胞肺癌均无效。目前吡铂和氟尿嘧啶、甲酰四氢叶酸联合治疗结肠癌,和多西他赛联合治疗前列腺癌,治疗进展或复发的非小细胞肺癌的临床试验仍在进行中[14]。
3.4 NDDP
属环己二胺类化合物,全称是顺式-双-新癸酸-反式-R,R-1,2-环己二胺合铂,为亲脂性配合物,由美国脂质体公司开发,是第一个进入临床实验的亲脂性铂同系物。其胶囊脂质体L-NDDP 在小鼠白血病模型上与顺铂无交叉耐药性。其Ⅰ期临床实验为通过腹腔内注射途径来治疗腹膜转移癌及肉瘤病,显示L-NDDP腹腔内注射全身吸收很少且缓慢,腹膜-血浆药物浓度百分比高,并推导出Ⅱ其临床试验的用药方案为每28 d 400 mg/m2,已进入Ⅱ期临床研究。由Aronex 公司研究的NDDP 的另一种脂质体Aroplatin克服了顺铂的耐药性及部分毒性,也已进入了Ⅱ期临床试验[15]。
3.5 triplatin tetranitrate(BBR3464)
BBR 3464(4硝酸三核铂)是由罗氏公司和弗吉尼亚联邦大学联合开发的一种铂复合物类抗癌药。意大利Boehringer Mannheim公司,现改名为Novuspharma公司已经从罗氏公司获得该产品的授权,并已在欧洲完成Ⅰ期临床试验,适应证为实体瘤。Novuspharma公司在意大利和英国已经开始治疗非小细胞肺癌的Ⅱ期临床试验。2001年1月在美国开始了一项治疗小细胞肺癌的Ⅱ期临床试验。此外,在欧洲还在进行治疗卵巢癌和胃癌的Ⅱ期临床试验。针对胰腺癌的Ⅱ期临床试验也已经在美国开始病人募集工作。多核铂类化合物在结构上和顺铂有差异,其作用机制和顺铂也有不同,这样的化合物有可能克服顺铂或卡铂的耐药性。双核铂类化合物包含两个活性铂中心,两者由二元胺长链相连,它可以和DNA 形成特殊形式的加成物,如“长距”、链内或链间交联,这是传统的单核铂类化合物所见不到的。三核铂类化合物是在双核复合物的alkanediamine 骨架上引入了第三个铂中心,其目的是提高复合物和DNA的结合能力。BBR 3464就是一种三核铂类化合物,是两个单功能[trans-PtCl(NH3)2]铂单元经由一个铂四胺单元[trans-Pt(NH3)2(NH2(CH2)6NH2)2]2+连接形成。三核铂类化合物显示了比顺铂更强的抗肿瘤活性,特别是对那些经常会对其它抗癌药产生耐药性的肿瘤类型,如肺癌和非小细胞肺癌[16]。
在Ⅰ期临床试验,剂量限制性毒性为骨髓抑制、腹泻。37例小细胞肺癌患者纳入到一项多中心研究。血液学毒性包括嗜中性白血球减少症(62%),发热性中性粒细胞减少(16%),贫血(10%),疲劳(5%)和低血钾(5%)。在34例可评估的患者中,11例患者疾病稳定,23例患者出现持续的疾病进展。结果显示在治疗小细胞肺癌病单独使用BBR 3464,疗效不确切,不支持进入Ⅱ期临床[17]。
3.6 奥沙利铂聚合体(prolindac)
奥沙利铂聚合体( prolindac) 是一种纳米聚合体,由奥沙利铂的活性部分结合到HPMA 上形成的,提高了对癌细胞的透过能力和停留能力。该聚合体在生理pH 值环境下稳定,但含氧量低的肿瘤细胞胞外环境中pH 值较低,导致活性部分持续减少。动物实验证实了较奥沙利铂而言,prolindac 的生长抑制能力更强,对普通细胞的毒性较低,血药浓度更高更持久,肿瘤内有更多的药物活性部分。
Nowotnik等[18]的Ⅰ/Ⅱ期临床试验评价了prolindac单药治疗既往接受过至少2 次铂类治疗的晚期卵巢癌患者的效果。由于每周方案会使药物半衰期延长,所以该试验改为每2~3 周连续静脉点滴2 h 方案。结果显示治疗耐受性很好,有临床意义的疾病稳定发生率为42%。该试验结果优于或至少不亚于奥沙利铂的试验结果。所有患者均发生不良反应,但都为1~2级的轻微不良反应。它和氟尿嘧啶、吉西他滨、多西他赛、SN-38 的联合化疗都显示出了协同作用。目前prolindac 还在进行Ⅱ期临床试验。
3.7 顺铂脂质体(lipoplatin)
为了减少顺铂的系统不良反应,在增加剂量的同时提高疗效,研究者们制造出脂质体包裹的顺铂,命名为lipoplatin。这种纳米脂质体比顺铂更容易穿过细胞膜,同时不易被免疫原识别。由于体液中循环时间长和分子更小,因此有更多的机会进入肿瘤细胞。
Kosmas等[19]在不含鳞癌的非小细胞肺癌Ⅲ期临床试验中同样验证了lipogem 方案疗效略优于cisgem方案,同时发现lipogem 方案的不良反应包括肾毒性、神经毒性和虚弱均少于cisgem 方案。Koukourakis 等[20]将lipoplatin、氟尿嘧啶和放疗联合治疗12 例局部晚期胃癌患者,几乎无肾毒性和中性粒细胞减少,接受5 周期化疗后80% 患者的肿瘤消失,该结果支持进一步的相关研究。
4 国外铂类抗肿瘤药的市场情况
多个铂类药物的全球销售数据见表4,总额达到30亿美元左右,因顺铂、卡铂、尤其是奥沙利铂销售额的下降,铂类药物2012年销售额同比下降13%左右。
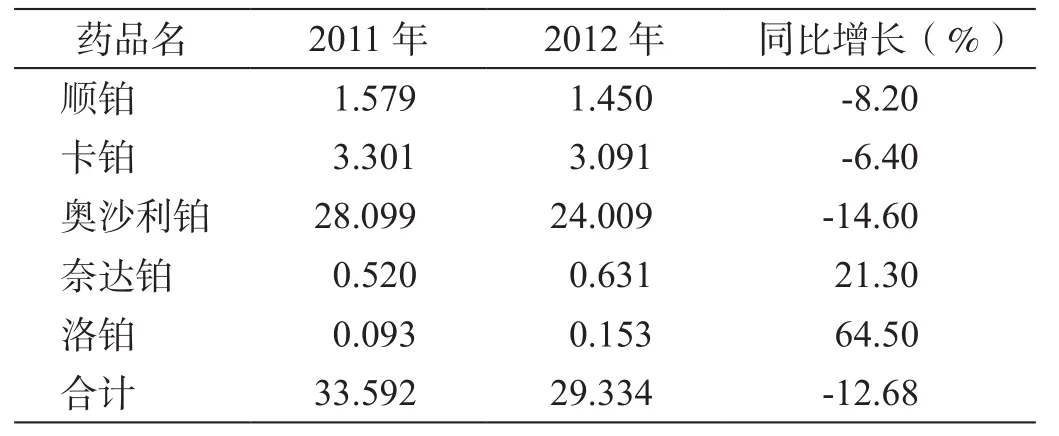
表4 多个已上市铂类药物全球销售额(亿美元)2)
4.1 上市情况
目前国内批准的铂类药物国产药物见表5。
4.2 市场情况
从IMS数据可得知,2012年抗肿瘤剂市场销售为238.17亿元,同比增长22.91%;其中铂类药物市场销售约为15亿元,同比增长10%左右,与烷化剂的44%、抗代谢物的33%和单抗类抗肿瘤剂的32%相比,还是有较大的差距。

表5 批准国产的铂类药物情况3)
部分国内已上市抗肿瘤剂在国内样本医院的销售数据见表6。
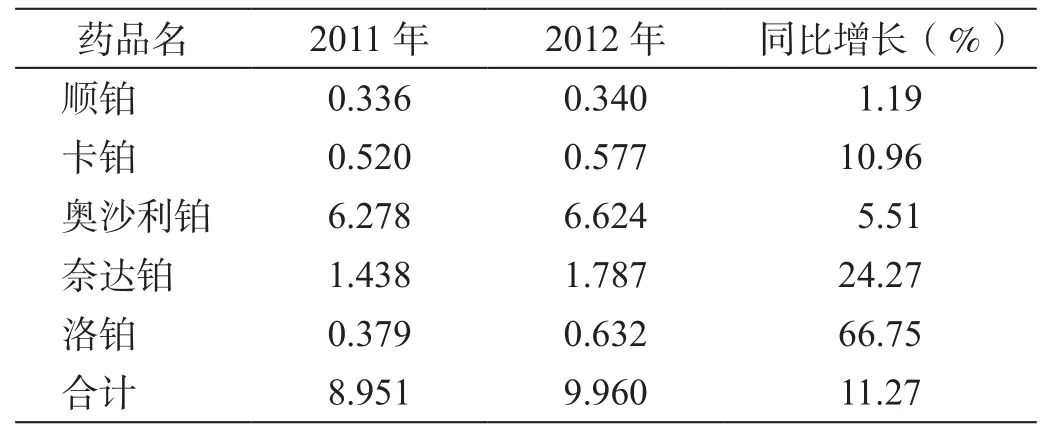
表6 国内已上市抗肿瘤剂样本医院销售额(亿元)4)
4.3 开发注册情况
国内开发铂类药物最有亮点的是双环铂(dicycloplatin,DCP),双环铂是由我国自主研发的国家化药1类抗癌新药的超分子化合物。双环铂最初由北京大学研发,其研制是基于分子生物学的观点,利用癌细胞中DNA的解旋酶的浓度和活性异常的特点研发成功的铂类抗癌新药。在肿瘤细胞复制过程中,聚集在肿瘤细胞核中DNA周围高浓度的DNA解旋酶将双环铂的氢键打开,释放的卡铂与DNA形成加和物,导致肿瘤细胞凋亡。这种取得靶向的方式也可以理解为分子开关。所以双环铂系的结构是在卡铂的基础上,以强氢键将环丁二羧酸基团(CBDCA)和另一个环丁二羧酸结合,作为一个新的铂络合物申报。目的是增加水溶性、提高稳定性、降低毒性、提高抗肿瘤活性。临床前研究结果表明其具有抗瘤活性。该药物申请单位北京市兴大科学系统公司于2003年3月获得SFDA核发的临床试验批件并开展临床试验,2012年5月获得国家食品药品监督管理局的1.1类新药证书国药证字H20120020。抗肿瘤新药双环铂与传统抗肿瘤药物顺铂、卡铂、奥沙利铂相比,具有不可比拟的性能优点:①毒性低,比世界王牌抗癌药顺铂小22倍,且几乎不产生化疗反应[21]。②抗癌活性高,乳腺癌的抗癌数据显示大于卡铂3倍以上。③水溶性好、水中稳定性好,事实证明,双环铂可制成水剂长期保存。④剂量低,显效率达60%~90%。对癌症晚期的治愈率达30%。
2005年12月,北京三思维尔高科技开发有限公司申报1.1类西茜铂的临床批文,2010年5月国家食品药品监督管理局给予不批准,后北京三思维尔申请复审,国家食品药品监督管理局做出维持原不批准的审评结论。此外,还有4家企业申报了3.1类新药米铂的临床批文,目前正在审评中。
5 展望
新型铂类化合物的出现进一步扩大了重金属化合物治疗的临床适应证,且有低毒高效的趋势,对于提高患者的生活质量,延长生存期有重要的意义。随着技术的进步,研究者可从分子水平研究铂类抗肿瘤药物的体内、外活性,研制出抗肿瘤活性高、 不良反应小的新型铂类药物,同时研究出新的给药方式,如缓释技术、靶向给药系统及开发有效的新联合用药方案等,以满足临床治疗的需要。进一步研究现有铂类药物的联合用药方案,以扩大它们在癌症治疗中的适应证和提高疗效则是医务工作者大有可为的课题。
[1]Rosenberg B, Camp V, Grimley EB,et al.The inhibition of growth or cell division inEscherichia coliby different ionic species of platinum(IV) complexes[J]. J Biol Chem, 1967,242(6): 1347-1352.
[2]杨一昆, 普绍平, 高文桂.顺铂的应用及铂族金属抗癌药物的研究进展[J]. 中国新药杂志, 1999, 8(12): 797-800.
[3]翁琳, 陈凌亚.铂类金属抗肿瘤药物的应用与研究进展[J].中国药学杂志, 2005, 40 (16): 1205-1208.
[4]祝兴勇, 张文萍, 尤启冬, 等.铂(Ⅱ)类抗肿瘤药物[J].化学进展, 2008, 20 (9): 1324-1334.
[5]Ali I, Wani W, Saleem K ,et al.Platinum compounds: a hope for future cancer chemotherapy[J]. Anticancer Agents Med Chem, 2013, 13(2): 296-306.
[6]Okuda K, Hirose T, Oki Y,et al. Evaluation of the safety and efficacy of combination chemotherapy with vinorelbine and platinum agents for patients with non-small cell lung cancer with interstitial lung disease[J]. Anticancer Res, 2012, 32(12):5475-5480.
[7]陈竹红.铂类抗肿瘤药物的发展历程及临床评价[J]. 中国药业, 2009, 18(5): 62-64.
[8]Tsubamoto H, Kawaguchi R, Ito K,et al. Phase II study of carboplatin and weekly irinotecan combination chemotherapy in recurrent ovarian cancer: a Kansai clinical oncology group study(KCOG0330) [J]. Anticancer Res, 2013, 33(3): 1073-1079.
[9]叶瑞萍, 杨扬, 陈振东.铂类抗肿瘤药物研究进展[J]. 国际肿瘤学杂志, 2008, 35 (9): 674-677.
[10]中国新特药网.新药推荐: Miripla(Miriplatin Hydrate, 米铂注射液)[EB/OL]. (2012-03-20) [2013-08-13]. http://www.oneyao.net/article/2012/0320/29045.html.
[11]Aramaki T, Moriguchi M, Bekku E,et al. Comparison of epirubicin hydrochloride and miriplatin hydrate as anticancer agents for transcatheter arterial chemoembolization of hepatocellular carcinoma[J]. Hepatol Res, 2013, 43(5): 475-480.
[12]林晓雯, 张艳华.铂类抗肿瘤药的进展与临床评价[J] . 中国医院用药评价与分析, 2011, 11(1): 4-7.
[13]Doshi G, Sonpavde G, Sternberg CN. Clinical and pharmacokinetic evaluation of satraplatin[J]. Expert Opin Drug Metab Toxicol, 2012, 8(1): 103-111.
[14]汉宁医药网.研发纵览:铂类抗癌药研发的现在与未来[EB/OL]. (2010-07-02)[2013-06-15]. http://www.cnhney.com/hneyinformation/Details_158450.html.
[15]Wang XY, Guo ZJ. Targeting and delivery of platinum-based anticancer drugs[J]. Chem Soc Rev, 2013, 42(1): 202-224.
[16]华源医药网.新药评价:三核铂抗癌药物:BBR 3464[EB/OL]. (2004-09-23)[2013-06-15]. http://www.hyey.com/yanfa/rddeep/newdrugevaluation/200409/47777.html.
[17]Monneret C. Platinum anticancer drugs. From serendipity to rational design[J]. Ann Pharm Fr , 2011, 69(6): 286-295.
[18]Nowotnik DP, Cvitkovic E. ProLindac ( AP5346 ) : a review of the development of an HPMA DACH platinum polymer therapeutic[J]. Adv Drug Deliv Rev, 2009, 61(13): 1214-1219.
[19]Kosmas C, Angel J, Athanasiou A,et al. Phase Ⅲ study of lipoplatin plus gemcitabine versus cisplatin plus gemcitabine in advanced NSCLC; interim analysis[J]. Eur J Cancer Suppl,2009, 7(2) : 531.
[20]Koukourakis M, Giatromanolaki A, Pitiakoudis M,et al.Concurrent liposomal cisplatin (Lipoplatin), 5-fluorouracil and radiotherapy for the treatment of locally advanced gastric cancer: a phase I/II study[J]. Int J Radiat Oncol Biol Phys,2010,78 (1): 150-155.
[21]双环铂学术交流网. 国家1.1类抗肿瘤新药双环铂注射 液[EB/OL]. (2013-07-01)[2013-10-11]. http://www.shuanghuanbo.net.

