合并严重心血管疾病老年骨科手术患者的围术期评估和处理
贾水淼,孟赛克,王利民,刘宏建
随着我国逐渐步入老龄化社会,临床上合并严重心血管疾病的高龄患者越来越多,且非心脏手术患者中合并严重心血管疾病者所占比例较大[1],骨科患者中合并严重心血管疾病者也越来越常见。严重心血管疾病造成的负面影响较大,有时可影响非心脏手术的进程[2],恰当地评估和处理骨科围术期患者合并的严重心血管疾病对于提高其对手术、麻醉的耐受性,降低并发症发生率及病死率,改善预后有重要意义,临床医师应加以重视。目前,国内外关于非心脏手术患者合并严重心血管疾病的围术期评估和处理的研究报道较多,但针对骨科患者的研究报道较少。因此,本研究对郑州大学第一附属医院骨科近年收治的老年患者的临床资料进行回顾性分析,旨在提高临床医师的正确认识并为术前合理决策提供参考。
1 对象与方法
1.1研究对象选择2010年6月—2012年1月郑州大学第一附属医院骨科收治的老年患者(年龄≥60岁)76例,均接受手术治疗并经心内科医师会诊明确有无严重心血管疾病;将其中未合并其他系统并发症的38例患者纳入对照组,合并严重心血管疾病的38例患者纳入观察组。对照组中男19例,女19例;年龄(69.0±9.5)岁。观察组中男16例,女22例;年龄(70.5±9.2)岁;不稳定型冠状动脉综合征15例(心肌梗死9例,心绞痛6例),失代偿性心力衰竭10例,严重的心律失常9例,严重心脏瓣膜疾病4例。两组患者的性别(χ2=1.580,P=0.201)、年龄(t=1.02,P>0.05)比较,差异均无统计学意义。
1.2诊断标准严重心血管疾病的诊断参照美国心脏学院(ACC)和美国心脏协会(AHA)联合制定的非心脏手术围术期心血管评估指导意见[3],包括不稳定型冠状动脉综合征(不稳定型或严重的心绞痛和心肌梗死)、失代偿性心力衰竭〔美国纽约心脏病协会(NYHA)心功能分级Ⅲ级和Ⅳ级〕、严重的心律失常〔高度房室传导阻滞(莫氏Ⅱ型二度房室传导阻滞、三度房室传导阻滞)、有症状的心室率不受控制的室性心律失常或室上性心律失常(包括心房纤颤),静息状况下心室率>100次/min及有症状的心动过缓或室性心动过速〕、严重的心脏瓣膜疾病〔严重的主动脉狭窄和有症状的左房室瓣狭窄及瓣膜置换术后长期服用抗凝药(如华法林)〕。
1.3方法回顾性分析两组患者的临床资料,记录其一般情况;对两组患者随访6个月~2年并按照手术部位(颈椎、腰椎、四肢大关节、四肢小关节)记录其手术时间、术中出血量、切口愈合时间、术后功能恢复情况等。颈、腰椎术后功能恢复情况按照日本骨科协会(JOA)评分标准,以改善率>60%为优,25%~60%为良,<25%为差;四肢关节术后功能恢复状况按照各个关节各自的通用评价标准[4]。
1.4围术期评估和处理术前合并心血管疾病是60岁以上骨科手术患者的危险因素[5],两组患者均经过术前积极评估及治疗,术前制定周密详细的手术计划,严密监护,采取积极措施,合理用药,有效控制和改善病情以提高手术耐受力。不稳定型冠状动脉综合征患者先行动态心电图和超声心动图检查,再行64排冠状动脉成像检查及放射性核素冠状动脉造影,冠状动脉狭窄程度>70%者先行经皮冠状动脉介入治疗,再行骨科手术。心肌梗死发作后l~2个月内不宜手术,6个月后若无心绞痛发作,就可按一般冠心病施行手术;但对危及生命的急诊手术和癌症根治术等有绝对手术指征的患者,在术前检查心脏储备能力,严密心电监测和充分治疗下也可以安排手术。失代偿性心力衰竭患者待心功能改善,耐受力提高并稳定之后再行骨科手术;药物治疗期间加强监测,避免水电解质失衡,注意药物应用的适应证和禁忌证,及时发现并处理药物不良反应。严重心律失常患者中有2例为病窦综合征,在安装起搏器后行骨科手术治疗;为防止对起搏器的干扰,围术期注意保持水电解质平衡,术中尽量采用双极电刀,使用单极电刀时注意电极板的位置,不要使电刀电流通过起搏器,坚持低电能短时间短间隔的原则使用电刀。
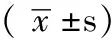
2 结果
2.1手术情况两组患者均顺利完成手术,无死亡患者,均安全度过围术期。
2.2观察指标两组中颈椎手术、腰椎手术、四肢大关节手术、四肢小关节手术患者手术时间、术中出血量、切口愈合时间及术后功能恢复情况比较,差异均无统计学意义(P>0.05,见表1)。

表1 两组不同手术部位患者观察指标比较
注:*为u值
3 讨论
老年人随着年龄增长,组织器官结构及功能退化,合并疾病较多,尤其是合并严重心血管疾病患者手术耐受性差,手术风险较高,手术相关的病死率较高。随着对疾病认识及诊疗手段的提高,经过积极评估和治疗,老年手术患者并没有明显增加手术难度、手术时间、术中出血量及术后恢复不佳的风险[6]。
3.1不稳定型冠状动脉综合征不稳定型冠状动脉综合征常提示冠状动脉狭窄,是一个重要的术前危险因素。本组15例不稳定型冠状动脉综合征患者均行动态心电图和超声心动图检查,前者可明确患者是否存在心肌缺血和心律失常,后者可明确患者各心腔大小、室壁运动情况,测定射血分数;64排冠状动脉成像检查及放射性核素冠状动脉造影对了解冠状动脉狭窄程度有重要意义。15例不稳定型冠状动脉综合征患者经检查后发现有5例冠状动脉狭窄程度>70%,遂先行经皮冠状动脉介入治疗,再施行骨科手术。
射血分数降低与术后心血管事件发生率和病死率相关,当左心室射血分数<40%时会明显增加心血管事件的发生率,如心源性死亡、非致命性心肌梗死、不稳定型心绞痛、充血性心力衰竭、室性心动过速等,需经过内科综合治疗后再行骨科手术[7]。
心肌梗死患者围术期内最大的问题是再度梗死。ACC和AHA推荐心肌梗死后7 d为急性期,7 d~1个月为亚急性期,只要患者近期运动负荷试验提示残存心肌不存在发病风险,术后发生再度梗死的概率较低,建议心肌梗死后4~6周再施行手术[4]。为安全起见,本研究患者心肌梗死发作后1~2个月内原则上不宜手术;6个月后,只要无心绞痛发作就可以按一般冠心病施行手术;本组5例心肌梗死患者的手术均安排在心肌梗死6个月之后。
3.2失代偿性心力衰竭失代偿性心力衰竭包括Ⅱ度和Ⅲ度心功能不全,引起心力衰竭的原因很多,包括冠状动脉疾病、高血压、心律失常、心脏瓣膜疾病等,治疗主要为针对病因的治疗。高容量性心力衰竭应采用血管紧张素转换酶抑制剂(ACEI)、血管紧张素受体拮抗剂(ARBs)、β-受体阻滞剂等。ACEI不但能降低慢性心功能不全患者的病死率,还能阻止疾病进展,是慢性心功能不全患者的首选用药[8];ARBs通过阻断血管紧张素Ⅱ 1型受体而起作用,具有与ACEI相似的血流动力学效应和逆转心肌重构的作用,可降低患者病死率,延缓疾病进程[9],但服用这两类药物的患者在麻醉诱导时容易发生低血压,应加以注意。β-受体阻滞剂是治疗慢性心力衰竭的Ⅰ类A级药物,围术期应用越来越多,有临床随机试验显示β-受体阻滞剂适用于以下患者:心肌缺血、心律失常、高血压及有这些病史的高危心脏病患者和在围术期检查中发现心肌缺血的非心脏手术患者[4]。患者发生急性失代偿性心力衰竭时除标准治疗外还要应用镇静止痛药物、正性肌力药物、利尿剂、扩血管药物,以迅速缓解症状;出现肺水肿时可以短期应用呼吸道正压通气[10];待患者心功能改善、耐受力提高并稳定之后再行手术。药物治疗期间应加强监测,避免水电解质失衡,注意药物的适应证和禁忌证,及时发现并处理药物的不良反应。
3.3严重的心律失常
3.3.1心脏传导阻滞莫氏Ⅰ型二度房室传导阻滞对阿托品或异丙肾上腺素反应较好,如药物不能缓解症状且患者反复发生Adams-Stokes综合征或心功能衰竭,应考虑安装心脏起搏器;而莫氏Ⅱ型二度房室传导阻滞麻醉下更易发展为三度房室传导阻滞,莫氏Ⅱ型二度及三度房室传导阻滞患者应在安装起搏器的前提下施行麻醉,备好提升血压、增加心率的药物,如麻黄素、阿托品、异丙肾上腺素等,不宜使用新斯的明等拮抗肌松药[11]。本组9例严重心律失常患者中有2例为病窦综合征,均在安装起搏器后行骨科手术治疗,安全度过围术期。
3.3.2室上性心动过速可采取刺激迷走神经的方法终止,常用药物有艾司洛尔、维拉帕米或胺碘酮,若药物无效,则应给予同步除颤,起始量为100 J。
3.3.3心房纤颤关键在于维持正常的室性心律,术前应通过洋地黄化控制室性心律,术中可应用艾司洛尔、普萘洛尔、维拉帕米或胺碘酮等药物。
3.3.4室性期前收缩偶发室性期前收缩(也可见于正常人)应注意观察,暂不予处理;5~6次/min以上或多源性室性期前收缩可静脉注射利多卡因,1~2 mg/kg或39~60 μg·kg-1·min-1静脉维持,无效者可采用普罗帕酮。
3.3.5室性心动过速情况严重者应立即处理,因室性心动过速不仅降低心输出量,还会导致心室纤颤;其治疗包括同步除颤、利多卡因或胺碘酮。利多卡因1~2 mg/kg稀释后静脉注射,5 min后可重复;效果不佳时可选用普鲁卡因酰胺(静脉给药不超过50 mg/min)或溴苄铵(5 mg/kg静脉缓慢注射)。
3.4严重心脏瓣膜疾病主动脉瓣狭窄明显增加非心脏手术患者手术风险,严重左房室瓣狭窄或反流增加了心力衰竭的风险[12]。严重心脏瓣膜疾病患者心功能较差,术前应采用洋地黄类药物强心及利尿剂、扩血管药物改善心功能,避免水电解质紊乱;合并心律失常时需要控制好心律后再行手术。
本组患者中有3例心血管介入及心脏机械瓣置换术后长期服用华法林抗凝药物,均在择期手术前停用华法林7 d,使国际标准化比值(INR)自然下降,停药第2天起复查INR,当INR下降到抗凝临界值(即正常抗凝作用下限)时应接受静脉肝素治疗。这种情况多数发生在术前1 d或手术当天;术前至少12 h停用低分子肝素或至少6 h停用普通肝素,使术前INR维持在1.3左右;如术晨INR>2.0应考虑延迟手术或输注新鲜冷冻血浆,同时请血液科会诊[13]。本组2例严重心脏瓣膜疾病患者术前INR均达标,术中出血量没有明显增加,术后引流量正常,安全完成腰椎和股骨近端手术。术中术后应根据患者具体情况补液,补液时应注意晶体液胶体液比例适当,不能单纯输入含大量血红蛋白的红细胞,因为骨科患者多为高龄患者,且四肢关节术后血液处于高凝状态,大量输注含高血红蛋白的红细胞会增加血液黏滞度,增加术后心脑血管栓塞的发生风险;输注红细胞时需结合输注血浆,以补充循环血量,纠正低血容量,同时有助于术后止血。
进食状况能够间接反映患者的营养水平,营养不良患者常发生免疫功能低下、电解质失衡,术后出现感染的概率增大;进食状况良好的老年患者血清清蛋白及血红蛋白水平明显高于进食状况较差的老年患者,术后并发症发生率明显降低[14]。因此,围术期应鼓励患者调整饮食,加强营养,注重饮食治疗。Goldman等[15]认为由于手术时间、失血量、体液重新分配及手术操作等因素,再加上老年人心血管功能储备和代偿能力减低,术中任何应激反应如牵拉脏器、输液速度过快或过慢等都可能导致心功能紊乱,增加心血管事件发生率。因此,术前应严格选择适应证及手术时机,制定周密的手术计划及有效的个体化手术和麻醉方案,术中严格止血,在尽量保证术后功能恢复的情况下采用简单术式,控制手术时间及手术创伤,减少失血量,必要时输血以保证患者各项心功能指标稳定在代偿期,减少围术期心血管意外的发生。
根据非心脏手术风险分级[4]及骨科手术特点,合并严重心血管疾病老年患者骨科手术风险分度如下:(1)高危险度:急诊大手术、血管性手术;(2)中危险度:根治性肿瘤切除术、脊柱畸形矫形术、联合前后路手术大范围脊柱重建、大关节置换后翻修术、长骨骨折复位内固定术、膝以上关节截肢术、脊柱病变(颈、胸、腰椎管狭窄及骨折、滑脱、结核)、单纯前路或后路椎体次全切病灶清除、根管扩大椎间盘摘除、全椎板切除减压椎弓根钉内固定或植骨融合术、关节置换等;(3)低危险度:部分颈椎手术如颈前路椎间盘摘除术、关节镜手术、肌腱吻合术、截指/趾术、腕管及神经松解术、外固定器械闭合复位、金属植入物取出术、经皮球囊扩张椎体成形术、踇外翻矫形术等。合并严重心血管疾病老年患者骨科手术多数为中低危险度。
3.5术前评估(1)首先判断是否为急诊手术,急诊手术不允许进一步做心脏评估或治疗,应立即手术并做好围术期监测及术后危险评估。(2)非急诊手术应询问患者病史并进行体格检查、实验室检查,了解患者是否合并严重心血管疾病,合并严重心血管疾病者应先进行心功能评估和治疗后再考虑手术,可能会导致手术延期或取消,但必须明确合并的严重心血管疾病并得到合理治疗后再施行手术;不稳定型冠状动脉综合征患者多需要接受冠状动脉造影检查以确定下一步治疗方案。(3)未合并严重心血管疾病者应判断是否为低危险度手术,如是则按原计划择期手术。(4)非低危险度手术则应判断患者是否具有良好的心脏功能及相应的临床症状,若患者活动能力≥4能量代谢当量(MET)且无相应临床症状则可以按原计划进行手术治疗。(5)心功能较差、有临床症状或心功能未知患者若具备心脏临床危险因素则需进一步评估,不具备心脏临床危险因素者可以按原计划手术而不需要更改治疗方案;如患者具备1~2个心脏临床危险因素,可以在β-受体阻滞剂控制心率下进行手术,亦可考虑推迟手术以进行相应的心功能评估和处理;如患者具备3个或以上心脏临床危险因素,则术中心血管风险就值得重视,需进一步检查和评估,必要时应改变治疗方案。心脏临床危险因素包括缺血性心脏病病史、代偿性心力衰竭病史、脑血管疾病病史、糖尿病和肾功能不全等[4]。
总之,多科室紧密合作、术前积极评估、精心准备、合理用药、有效控制和改善病情、制定周密详细的手术计划、选择安全、有效、个体化的手术和麻醉方案,术中行心电图、心率、血压及血氧饱和度监测、操作轻柔、控制手术时间、减少失血量,术后缩短卧床时间、早期离床并进行功能锻炼,才能使合并严重心血管疾病的老年骨科手术患者安全度过围术期,得到良好的临床恢复。
1Rihal CS.The role of myocardial revascularization preceding noncardiac surgery[J].Prog Cardiovasc Dis,1998,40(5):383-404.
2Fleisher LA,American College of Cardiology/American Heart Association.Cardiac risk stratification for noncardiac surgery:update from the American College of Cardiology/American Heart Association 2007 guidelines[J].Cleve Clin J Med,2009,76(Suppl 4):S9-S15.
3Fleisher LA,Beckman JA,Brown KA,et al.ACC/AHA 2007 Guidelines on Perioperative Cardiovascular Evaluation and Care for Noncardiac Surgery:Executive Summary:A Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines(Writing Committee to Revise the 2002 Guidelines on Perioperative Cardiovascular Evaluation for Noncardiac Surgery)Developed in Collaboration with the American Society of Echocardiography,American Society of Nuclear Cardiology,Heart Rhythm Society,Society of Cardiovascular Anesthesiologists,Society for Cardiovascular Angiography and Interventions,Society for Vascular Medicine and Biology,and Society for Vascular Surgery[J].J Am Coll Cardiol,2007,50(17):1707-1732.
4刘志雄.常用骨科分类法和功能评定[M].北京:北京科学技术出版社,2010:9.
5Richardson JD,Cocanour CS,Kern JA,et al.Perioperative risk assessment in elderly and high-risk patients[J].J Am Coll Surg,2004,199(1):133-146.
6何建苗,蒲永东,曹志宇.老年病人腹部外科手术时的围手术期处理[J].中华老年多器官疾病杂志,2002,1(2):129.
7Halm EA,Browner WS,Tubau JF,et al.Echocardiography for assessing cardiac risk in patients having noncardiac surgery.Study of Perioperative Ischemia Research Group[J].Ann Intern Med,1996,125(6):433-441.
8McMurray JJ,Adamopoulos S,Anker SD,et al.ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure 2012:The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2012 of the European Society of Cardiology.Developed in collaboration with the Heart Failure Association(HFA)of the ESC[J].Eur Heart J,2012,33(14):1787-1847.
9Pfeffer MA,Swedberg K,Granger CB,et al.Effects of candesartan on mortality and morbidity in patients with chronic heart failure:the CHARM-Overall programme[J].Lancet,2003,362(9386):759-766.
10Allen LA,O′Connor CM.Management of acute decompensated heart failure[J].CMAJ,2007,176(6):797-805.
11袁联文,周建平.老年心血管系统病理生理改变及常见心血管疾病围手术期处理[J].中国实用外科杂志,2008,28(2):97-99.
12Auerbach AD,Goldman L.Assessing and reducing the cardiac risk of noncardiac surgery[J].Circulation,2006,113(10):1361-1376.
13Douketis JD.Perioperative anticoagulation management in patients who are receiving oral anticoagulant therapy:a practical guide for clinicians[J].Thromb Res,2002,108(1):3-13.
14兰秀夫,王爱民,孙红振,等.760例骨科老年患者手术风险因素分析[J].重庆医学,2008,37(5):493-495.
15Goldman L,Calilera DL,Nussbaum SR,et al.Multifactorial index of cardiac risk in noncardiac surgical procedures[J].N Engl J Med,1977,297(16):845-850.

