炔丙基醇类化合物的无溶剂微波法合成
戚兰君 陈 莉 崔冬梅
(浙江工业大学药学院,浙江 杭州 310014)
炔丙基醇类化合物作为重要有机合成中间体,被广泛应用于前列腺素、类固醇、类胡萝卜素等天然产物的合成中[1,2,3]。目前文献报道的炔丙基醇类化合物的常规合成方法有炔烃类化合物与醛酮类化合物的加成反应;如在丁基锂催化条件下或在氯化锌和三乙胺的催化体系下的加成反应,能够得到较高收率[4];也有报道使用叔丁醇钾作为催化剂,在DMSO溶剂中,通过加成反应得到相应的炔醇类化合物,同样可以得到较好收率[5];之后有报道直接使用无溶剂研磨法同样可以得到满意的结果[6]。
近年来关于微波法应用于有机反应的实例越来越多,大量的有机反应在使用微波法后收率明显提高,并且所需反应时间更短,反应条件更为温和,操作简便且易于控制[7-11]。本文使用无溶剂室温微波照射,以端基炔烃与酮类化合物为原料合成相应的炔醇类化合物 (3a~3k,Scheme 1),通过与无溶剂研磨法进行比较,发现微波法具有明显的优势。各类产物结构经1H NMR进行了表征。
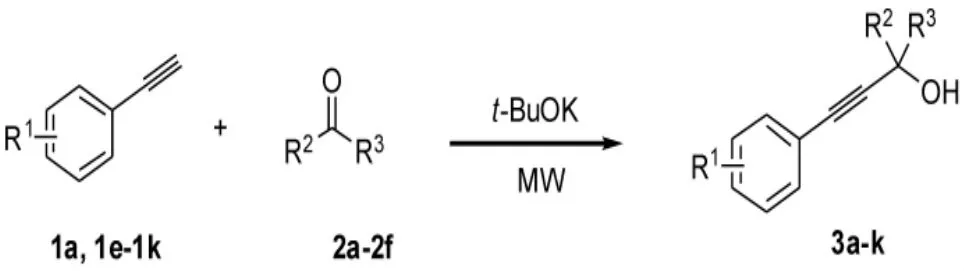
Scheme1
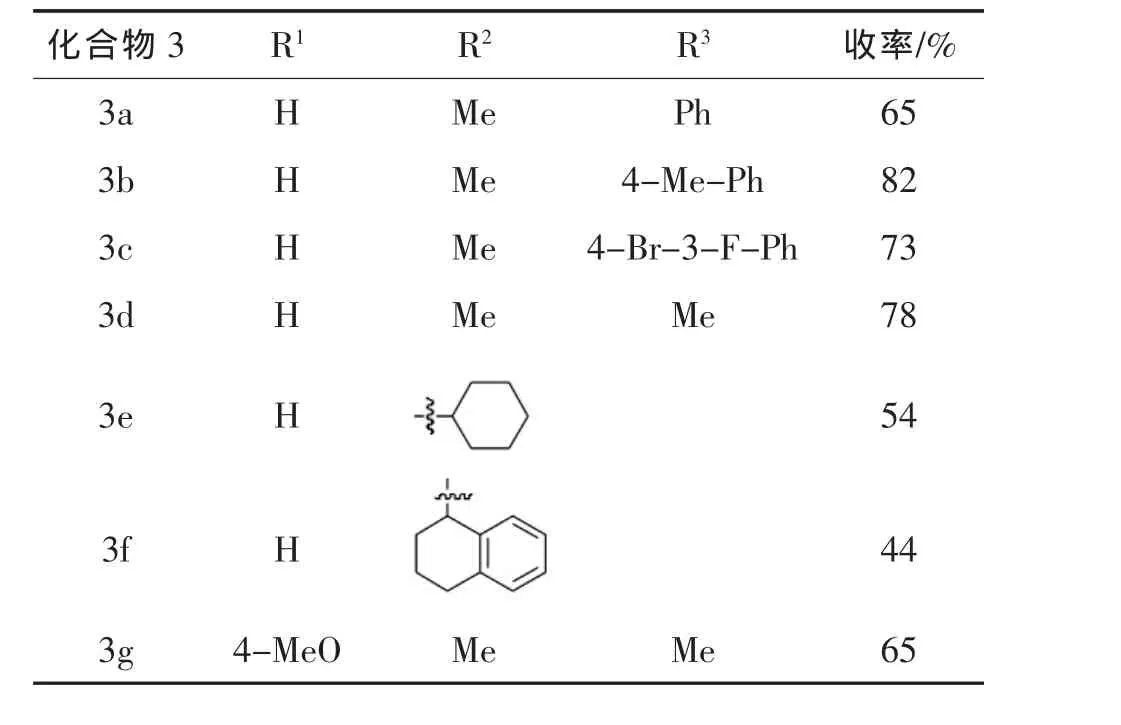
表1 微波合成炔丙基醇类适用范围Table1 substrate scope of synthesis of propargylic alcohols by microwave
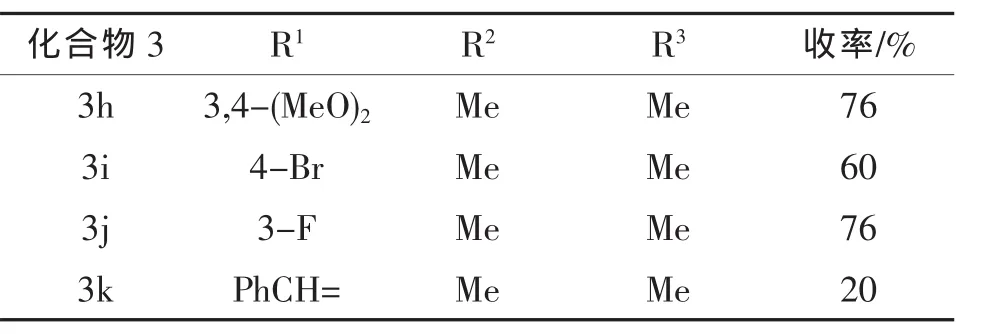
续上表
1 实验部分
1.1 仪器与试剂
Breker AC-8025O MHz~500 MHz型核磁共振仪(CDCl3为溶剂,TMS为内标);
所用试剂均为化学纯。
1.2 合成方法
1.2.1 微波法制备炔醇
在圆底烧瓶中依次加入1a (2.5 mmol)、2a(2.5 mmol),在超声条件下缓慢加入叔丁醇钾 (2.5 mmol),室温微波反应约2 h。停止反应,加入一定量的乙酸乙酯溶解,用饱和NH4Cl溶液水洗,分液,水层用乙酸乙酯萃取三次,合并有机层,再用饱和食盐水洗涤一次,有机层用无水硫酸钠干燥。过滤,减压蒸馏,得到粗产物,柱层析分离(石油醚:乙酸乙酯 =10:1),得到目标产物3a。
用类似方法合成3b~3k。
3a:淡黄色油状液体;产率:65%;1H NMR(500 MHz,CDCl3)δ 7.74~7.72 (m,2H),7.49~7.48(m,2H),7.41~7.32 (m,6H),2.47 (s,1H),1.87(s,3H)。
3b:淡黄色油状液体;产率:82%;1H NMR(500 MHz,CDCl3)δ 7.62~7.59 (m,2H),7.48~7.45(m,2H),7.32~7.29 (m,3H),7.19~7.17 (m,2H),2.55(s,1H),2.49(s,3H),1.85(s,3H)。
3c:黄色油状液体;产率:73%;1H NMR(500 MHz,CDCl3)δ 7.56~7.46 (m,4H),7.40~7.32(m,4H),2.55(s,1H),1.84(s,3H)。
3d:无色油状液体;产率:78%;1H NMR(500 MHz,CDCl3)δ 7.44~7.42 (m,2H),7.32~7.29(m,3H),2.03(s,1H),1.64(s,6H)。
3e:黄色固体;产率:54%;1H NMR(500 MHz,CDCl3)δ 7.44~7.42 (m,2H),7.32~7.30 (m,3H),2.07 (br,1H),2.03~1.98 (m,2H),1.76~1.72(m,2H),1.69~1.57(m,6H)。
3f:淡黄色油状液体;产率:84%;1H NMR(500 MHz,CDCl3)δ 7.86~7.84 (m,1H),7.45~7.43(m,2H),7.31~7.28 (m,3H),7.27~7.13 (m,2H),7.13~7.11(m,1H),2.87~2.83(m,2H),2.37(s,1H),2.31~2.29 (m,2H),2.09~2.06 (m,1H),2.00~1.97(m,1H)。
3g:黄色油状液体;产率:55%;1H NMR(500 MHz,CDCl3)δ 7.34(d,J=9.0 Hz,2H),6.82(d,J=9.0 Hz,2H),3.80(s,3H),2.32(br,1H),1.61(s,6H)。
3h:淡黄色油状液体;产率:76%;1H NMR(500 MHz,CDCl3)δ 7.02 (dd,J=8.0,1.5Hz,1H),6.92(d,J=1.5 Hz,1H),6.78(d,J=8.0 Hz,1H),3.88 (s,3H),3.87 (s,3H),2.14 (br,1H),1.62(s,6H)。
3i:黄色油状液体;产率:60%;1HNMR(500MHz,CDCl3)δ 7.44 (d,J=8.5 Hz,2H),7.28(d,J=8.5Hz,2H),1.62(s,6H)。
3j:黄色油状液体;产率:76%;1H NMR(500 MHz,CDCl3)δ 7.27~7.24 (m,1H),7.20~7.18(m,1H),7.12~7.10(m,1H),7.02~7.01(m,1H),2.15(s,1H),1.62(s,6H)。
3k:淡黄色油状液体;产率:20%;1HNMR(500MHz,CDCl3)δ 7.39~7.28(m,5 H),6.94(d,J=16.5 Hz,1H),6.18 (d,J=16.5 Hz,1H),2.02(br,1H),1.60(s,6H)。
1.2.2 研磨法制备炔醇
在研钵中依次加入1a(2.5 mmol)、叔丁醇钾(2.5 mmol)、和 2f(2.5 mmol),室温研磨反应约 1 h,反应过程中使用TLC监测。停止反应,加入一定量的乙酸乙酯溶解,用饱和NH4Cl溶液洗,分液,水层用乙酸乙酯萃取三次,合并有机层,再用饱和食盐水洗一次,所得有机层用无水硫酸钠干燥。过滤,减压蒸馏,得到粗产物,用柱层析法分离(石油醚:乙酸乙酯=5:1)得到目标产物3f。
2 结果与讨论
2.1 微波反应的适用范围
首先,我们探讨了无溶剂微波法的适用范围。由表1中可见,不同类型的酮均能很好的适应该反应,且收率较好;当使用萘酮时,收率有所降低,为44%;其次,我们探讨了不同的炔烃对反应影响,芳香族炔的苯环上不论带有供电性基团,还是吸电子基团,反应收率均较好;肉桂炔对反应的适用性较差,收率只有20%,可能是烯炔的端位氢与芳香族炔烃的端位氢相比活性较低,在叔丁醇钾碱性条件下较难形成碳负离子。
2.2 微波法和研磨法的比较
作者尝试将微波法与研磨法进行比较,探讨了改研磨为微波法后,收率的变化情况见表2。由表2可见,尝试的三组不同的底物,研磨法的收率较微波法都有较大幅度的降低。且微波的有以下优势:(1)反应较充分,减少了原料的浪费,更为经济环保;(2)操作简便;(3)避免了因研磨时暴露在空气中的叔丁醇钾会吸收水分,使催化效果降低。

表2 微波法和研磨法的比较aTable2 Comparison of synthetic methods between microwave irradiation and pestle reaction for 3
3 结论
综上所述,对于耗时耗力的研磨法,微波法有明显的优势,在收率方面有较大的提高,减少了原料的浪费,操作更为简单,是合成炔醇的一种理想方法。
[1]Fried J,Lin C,Mehro M,et al.Synthesis and biological activity of prostaglandin antagonists[J].Sci.1971,180:38.
[2]Johnson W S,Brinkmeyer R S,Kapoor U M,et al.Asymmetric total synthesis of 11 -alpha -hydroxyprogesterone via a biomimetic polyene cyclization[J].J.Am.Chem.Soc.,1977,99:8341.
[3]Chan K K,Cohen N C,Denoble J P,et al.Synthetic studies on (2R,4'R,8'R)-alpha-tocopherol facile syntheses of optically-active, saturated, acyclic isoprenoids via stereospecific[3,3]sigmatropic rearrangements[J].J.Org.Chem.,1976,41:3497.
[4]Jiang B,Si Y G.Alkynylation of carbonyl compounds with terminal acetylenes promoted by ZnCl2and Et3N:simple,mild and efficient preparation of propargylic alcohols[J].Tetrahedron Lett.,2002,43;8323–8325.
[5]Babler J H,Liptak V P,Phan N.Alkoxide-catalyzed addition of terminal alkynes to ketones[J].J.Org.Chem.,1996,61:416.
[6]Hisakazu Miyamoto,Shunpei Yasaka,Koichi Tanaka.Solvent-free addition of ethynylbenzene to ketones[J].Bull.Chem.Soc.Jpn.,2001,74:185–186.
[7]Winum J Y,Kamal M,Leydet A.Homologation of carboxylic acids by Arndt-Eistert reaction under ultrasonic waves[J].Tetrahedron Lett.,1996,37:1781.
[8]Ando T,Cork D G,Kimura T.Sodium percarbonate(SPC)as a hydrogen-peroxide source for organic-synthesis[J].Chem.Lett.,1986,173:665.
[9]FuentesA,Sinisterra JV.Single electron transfer mechanism of the Cannizzaro reaction in heterogeneous phase,under ultrasonic conditions[J].Tetrahedron Lett.1986,27:2967.
[10]Jayasree J,Rao J M.Sonochemical acetylation reactions of tertiary alkyl halides[J].Synth.Commun.,1996,26:1103.

