奥利司他原料药制备过程中的杂质分析*
石其德,朱骊安,姜俊云,董惠钧
(1.鲁南制药集团股份有限公司,山东 临沂 276006;2.聊城大学医学院,山东 聊城 252000)
奥利司他是一种强效和长效脂肪酶抑制剂,能抑制肠道内脂肪酶活性,减少摄入脂肪的消化和吸收。作为一种新型减肥药,它不会影响中枢神经系统,毒副作用也比较小[1]。目前国内奥利司他原料药有2种工业化生产方法,即半合成法和全化学合成法。半合成生产工艺[2-3]为经微生物发酵获得奥利司他前体物利普司他汀,初步分离精制获得利普司他汀粗品,催化氢化利普司他汀转化为奥利司他,最后经有机溶剂结晶精制获得奥利司他合格成品。本研究中以半合成法生产奥利司他为例,对生产工艺中的杂质种类和来源进行了分析,提出了对工艺杂质和降解产物有效控制的策略和方法。由于奥利司他属于新药,2010年版《中国药典》尚未收录,因此本研究对于奥利司他生产过程中的质量控制具有借鉴和指导意义。
1 仪器与试药
Agilent 1100型(紫外检测器)高效液相色谱系统。奥利司他对照品为自制,纯度大于99.6%;乙腈为色谱纯,甲醇、庚烷、过氧乙酸、盐酸和氢氧化钠等试剂均为分析纯。
2 方法与结果
2.1 色谱条件
色谱柱:Agilent C18柱(250 mm ×4.6 mm,2.5 μm);流动相:乙腈 -水(80∶20);紫外检测波长:195 nm;流速:1.2 mL/min;进样量:20 μL。
2.2 工艺杂质分析
原料药的工艺杂质主要是指反应副产物、未反应的原料或中间体及溶剂等。特别是对发酵原料药而言,其工艺杂质来源和种类更为复杂和多样,对这类原料药工艺杂质的控制一直是项具有挑战性的工作。另外,原辅料引入的杂质和反应过程中接触设备或容器引入的杂质也是工艺杂质的可能来源。
利普司他汀发酵引入的杂质:前体物利普司他汀发酵不可避免地会引入杂质,给下游奥利司他的纯化带来困难。这些杂质主要是毒三素链霉菌次级代谢产物,与利普司他汀的相对保留时间分别为 0.67,0.75,0.80,0.94,1.10,1.26,这些杂质的性质与利普司他汀很相似,在高效液相色谱图上的保留时间也非常相近(见图1),单纯利用层析或萃取方法很难去除。按照人用药品注册技术规范国际协调会(ICH)的质量要求,未知杂质应控制在0.1%以下,故应通过优化发酵培养基和发酵调控来有目的地控制和降低这些杂质的含量。再就是微生物代谢产生的水溶性和脂溶性色素,对于脂溶性色素可通过层析结合结晶的方法去除,只要下游纯化工艺合理有效,这些色素杂质不会对产品的最终质量产生影响。

图1 毒三素链霉菌发酵液中利普司他汀和主要杂质色谱图
氧化作用产生的杂质:奥利司他从分子式组成上看属于酯类物质,在接触空气或氧化性物质条件下,容易发生氧化反应。本研究中用含20%体积的3%过氧乙酸甲醇溶液溶解奥利司他,配制成1 g/L的质量浓度,置振荡器中处理60 min,模拟加速氧化过程,20 μL进样、分析。结果见图2和表1。与标准品相比,多出5个杂质峰,与主峰的相对保留时间分别为 0.42,0.47,0.49,1.20,1.32,而且主峰面积明显减少,表明奥利司他发生了显著分解。其中前3个杂质峰先于奥利司他出现,后2个杂质在奥利司他之后出峰,因此在生产过程中除了缩短制备时间、防止接触氧化物质和充填氮气来防止氧化外,对于前3个杂质,利用结晶法能够比较容易去除;而对于极性弱于奥利司他的后2个杂质,则需要结合结晶和层析的方法才能去除得比较彻底。

图2 不同处理条件下奥利司他高效液相色谱图
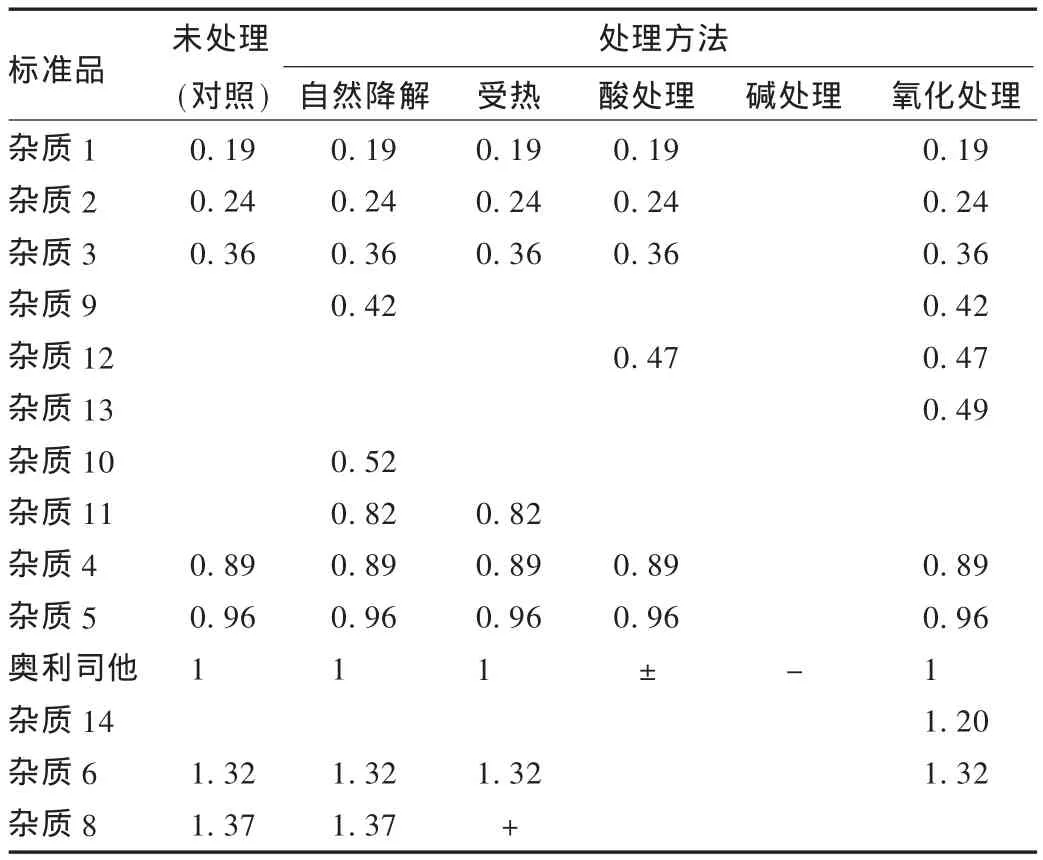
表1 不同处理方法处理后的奥利司他原料杂质分析(相对保留时间)
自然降解产生的杂质:用含有20%(V/V)水的甲醇溶液溶解奥利司他,配制成1 g/L的质量浓度,置振荡器中处理48 h,取20 μL进样,分析。结果见图2和表1,表明在含水的醇溶液中,奥利司他会发生水解,特征性杂质峰的相对保留时间为0.82,其他杂质还有0.42,0.52,而在不含水的醇溶液中奥利司他不发生水解(数据未列)。故在奥利司他制备过程相对保留时间0.82的杂质会成为主要杂质,增加纯化的难度。故应尽量减少含水溶剂的使用,即使使用也应减少对奥利司他的作用时间。对于相对保留时间为0.82的杂质去除,最有效的方法是硅胶层析或利用中等极性有机溶剂进行反溶剂层析结晶。
受热分解产生的杂质:用纯甲醇溶解奥利司他配制成1 g/L的质量浓度,放置在60℃水浴中处理24 h,取20 μL进样、分析。由于在制备工艺中存在减压浓缩等工序,奥利司他会受热作用。结果见图2和表1,显示相对保留时间1.37的杂质明显增大,另外相对保留时间为0.82的杂质也增大。因此要控制减压浓度温度不能过高,同时处理时间尽可能短,或使用高效的降膜浓缩设备以减少受热时间。对于相对保留时间为1.37的杂质,通过非极性溶剂结晶方法能够去除。
遇酸性物质产生的杂质:用含有20%2 mol/L盐酸的甲醇溶液溶解奥利司他,配制成1 g/L的质量浓度,置振荡器中处理60 min,取20 μL进样,分析。在酸性环境中,奥利司他发生明显分解,相对保留时间为0.82的杂质峰显著增大,而奥利司他主峰后的2个杂质峰也发生酸解(图2和表1)。故无论在制备过程还是成品保藏中,应杜绝接触酸性物质。
遇碱性物质产生的杂质:用含有20%2 mol/L氢氧化钠的甲醇溶液溶解奥利司他,配制成1 g/L的质量浓度,置振荡器中处理60 min,取20 μL进样,分析。与其他处理条件相比,碱性环境对奥利司他的破坏分解作用最强。图2显示奥利司他完全分解消失,在相对保留时间0.58处出现1个明显的杂质峰。故奥利司他遇碱最不稳定,应在各个制备和保藏环节避免接触碱性物质。
包装材料杂质分析:在奥利司他的生产过程中,由于会使用能溶解聚乙烯等塑性材料的有机溶剂,如庚烷、丙酮和石油醚等,因此在与物料直接接触的生产设备或器皿、密封材料和包装材料的选择上,要优先选择不锈钢或耐有机溶剂腐蚀的材料。已有文献报道了因奥利司他包装材料的质量问题而引入的杂质[4],对于此类杂质的防范,只需严格避免使用或接触塑性材料即可。本研究中选用不同的包装材质在恒温、干燥条件下保藏奥利司他30 d,取样利用高效液相色谱法分析奥利司他原料药中的杂质情况。结果(表2和图3)表明,用聚乙烯、硅橡胶和乳橡胶等包装材料,会在奥利司他原料药中引入数量和种类不同的杂质,而采用聚丙烯或聚酰胺类包装材料则不会引入杂质。

表2 不同包装材料在奥利司他原料药中引入杂质的高效液相色谱鉴别

图3 不同包装材料贮存奥利司他的高效液相色谱图
3 讨论
奥利司他是一种新型减肥药,进口胶囊剂已在我国上市多年,但由于工艺复杂和质量不稳定,国内仿制药于2011年才获得国家食品药品监督管理局的批准。奥利司他是经过微生物发酵和化学转化获得的,步骤多,工艺控制严格,且由于原研厂商生产的奥利司他原料药的杂质控制水平达到0.1%以下,对国内的仿制者来说是非常大的挑战。目前,国内领先的原料药厂商海正药业和联邦制药主要通过动态轴向压缩柱技术制备单杂在0.1%以下的奥利司他原料药[5-6]。本研究通过试验确定了奥利司他从生产到包装过程中可能引入杂质的种类和可能的途径,为奥利司他质量控制标准的建立提供了科学依据。在此基础上,采取源头控制降低发酵工艺杂质、重视中间流程控制杂质变化及升级核心技术去除手性杂质等措施,不采用制备色谱技术实现大规模生产单杂在0.1%以下的高品质奥利司他原料药。
[1]Goese M,Eisenreich W,Kupfer E,et al.Biosynthetic origin of hydrogen atoms in the lipase inhibitor lipstatin[J].The Journal of Biological Chemistry,2000,275(28):21 192-21 196.
[2]杨小波,陈再新,张奕华.奥利司他的全合成研究进展[J].有机化学,2005,25(8):902-912.
[3]韩俊茹,陈锡永.Lipstatin高产菌株筛选[J].中国抗生素杂志,2007,32(8):459-461.
[4]谭晓世,王栋海,王 旻,等.毒三素链霉菌发酵产物中有关物质的结构鉴定[J].江苏药学与临床研究,2006,14(3):176-177.
[5]许勇煌,彭 韪,王德刚,等.一种奥利司他的制备方法:中国,201110047178.8[P].2011-02-28.
[6]朱国荣,应雪肖,邓传亮,等.一种提纯奥利司他的方法:中国,200910169508.3[P].2009-09-08.

