黄芩苷口崩片的制备及质量标准研究
宋卫中,杨 磊,刘 蔚,张 瑜
(河南大学中药研究所河南开封475001)
黄芩苷口崩片的制备及质量标准研究
宋卫中,杨 磊,刘 蔚,张 瑜
(河南大学中药研究所河南开封475001)
目的 筛选黄芩苷和β-环糊精包合物的最佳比例,解决黄芩苷溶出度低的难题,提高黄芩苷的临床应用。方法 用喷雾干燥的方法,制备了黄芩苷-β环糊精1∶1、1∶2、1∶3、2∶1的包合物。用紫外分光光度法测定其含量,用智能溶出仪测定其溶出度,以累积溶出率与包合物的包载量等因素为指标,对各比例的包合物进行筛选。以崩解时间为指标,采用Lg(34)正交设计法优选口崩片处方,通过对口崩片中主要有效成分黄芩苷的含量测定,确定制剂的质量标准。以外观,含量,崩解时限和溶出参数为考察指标进行质量检查。结果 1.黄芩苷-β-环糊精包合物在溶出介质蒸馏水中有较高的溶出度,与黄芩苷原料药比较,各比例包合物在15 min内溶出度已达90%以上,溶出速率快,溶出更完全。2.黄芩苷-环糊精口崩片在45 min内溶出度达到85%以上,溶出度比单纯黄芩苷的溶出度高。3.最优崩解剂为交联聚维酮(PVPP),用量6%,采用内外加法。黏合剂为PVP,用量1%,硬度控制在4.0 kg,矫味剂甘露醇和阿斯巴甜比例为1∶1。结论 用本法制备黄芩苷口崩片可操作性强,制备工艺稳定可行且黄芩苷释放度良好,口感不错,具有良好的应用前景。
黄芩苷;口崩片;β-环糊精包合物;处方工艺,质量评价
黄芩苷是从唇型科植物黄芩中提取的一种黄酮类化合物,具有抗变态反应、抑菌抗炎、清热解毒、利尿、降压等多种药理作用。并且在抗HIV、抗肿瘤、抗氧化以及治疗心血管疾病等方面均具有开发应用价值。黄芩苷在水中的溶解度极差,经胃肠道吸收缓慢[1]。目前黄芩苷上市的品种主要是片剂和胶囊,在体内的吸收率很低,极大的限制了黄芩苷类药物在临床上的应用。该剂型与普通片剂相比,可提供一种新的服用方法,由于该剂型口感好、服用方便、剂量准确、携带方便,因而是广大患者乐于接受的一种剂型,研制黄芩苷口腔崩解片具有很重要的临床意义。
1 仪器与试药
1.1 仪器
78X片剂四用检测仪(上海黄海制药厂);ZP17E型旋转压片机(上海天和制药机械有限公司),RCZ-8A智能溶出仪(天津大学精密仪器厂),WFZ UV-2000紫外分光光度计(龙尼柯上海仪器有限公司), FT-2000A脆碎度检查仪(天津大学无线电厂),LB-2B崩解时限测定仪(上海黄海药检仪器厂),AB135-S型电子分析天平(瑞士Mettler Toledo仪器公司), 101-4AB电热鼓风干燥箱(北京中兴伟业仪器有限公司)。
1.2 试药
黄芩苷(四川省玉鑫药业有限公司 批号: 080508);β-环糊精(孟州市华兴生物化工有限责任公司批号:090712);氢氧化钠(天津市福晨化学试剂厂批号:110802);无水乙醇(安徽安特食品股份有限公司批号:1204073601);蒸馏水(自制批号:130112)。可压性淀粉(曲阜市天利药用辅料有限公司 批号: 120130),硬脂酸镁(高密市晟荣昌化工销售有限公司批号120516),羧甲基淀粉钠(CMS-Na)(天津市科密欧化学试剂有限公司批号:120416),交联聚乙烯吡咯烷酮(PVPP)(东营市鸿亚化工有限公司批号: 111203),低取代羟丙级纤维素(L-HPC)(郑州市华耀生物科技有限公司批号:120303),聚乙烯吡咯烷酮(PVP)(天津市科密欧化学试剂有限公司批号: 120322),甘露醇(天津市科密欧化学试剂有限公司批号:110922),阿司巴甜(江苏维多股份有限公司批号:120518)。
2 方法与结果
2.1 黄芩苷口崩片的制备
2.1.1 口崩片的基本处方 根据文献资料,结合黄芩苷-β-环糊精包合物的主药含量,初步确定口崩片的基本处方为:黄芩苷包合物5 g;待筛选崩解剂适量;5%PVP乙醇溶液适量;可压性淀粉适量;硬脂酸镁0.15;甘露醇适量;阿司巴甜适量;制成50片。固定包合物占口崩片总量33%,硬脂酸镁用量1%,片重为0.3 g。
2.1.2 制备方法 采用湿法制粒压片工艺。将研碎的主药、与稀释剂、崩解剂(加入一半),矫味剂混匀,混入粘合剂(加入崩解剂另一半)制成软材后过20目尼龙筛。于50~60℃干燥约60 min后整粒后于硬脂酸镁混合均匀,压片。控制片重0.3 g,硬度控制4~6 kg。
2.1.3 崩解剂筛选[2]以口崩片的崩解时限为指标结合溶出度测定对崩解剂进行筛选,根据文献分别备选CMS-Na,PVPP,L-HPC作为崩解剂制备口崩片,用量为0.45 g。根据口腔崩解片的崩解特点,参考中国药典2010版二部附录分散片崩解时间的测定方法,对口腔崩解片的崩解时间测定方法作了适当修改。把小杯装在溶出度试验仪上,加入蒸馏水100 m L作为介质,使温度达到20℃,并加入一片口崩片到杯中,用秒表开始记时,直到口崩片完全彻底崩解成颗粒并通过2号筛的时间为崩解时间,并且对口崩片的分散均匀性进行观察,结果见表1。

表1 黄芩苷包合物口含片中崩解剂筛选结果
对上述制备得到的含不同崩解剂的口崩片进行 体外溶出度测定,结果见图1。

图1 不同崩解剂制得口崩片的体外溶出度测定
由表1图1结果可见,采用PVPP为崩解剂时,口崩片的崩解速度及体个溶出速度均最优,因此选择PVPP为崩解剂进一步进行处方工艺优化。
2.1.4 处方工艺优化 研究发现,口崩片的质量受口崩片制备时处方工艺中的崩解剂用量、黏合剂用量及片剂硬度影响较大,因此,在前面初步筛选得到的崩解剂基础上,对崩解剂用量、黏合剂用量及片剂硬度进行正交设计优化筛选。按照表4中三因素三水平采用L9(34)进行正交设计,以崩解时限作为指标,对试验结果进行直观分析和方差分析,结果见表2和表3。

表2 黄芩苷包合物口崩片处方优化因素水平表
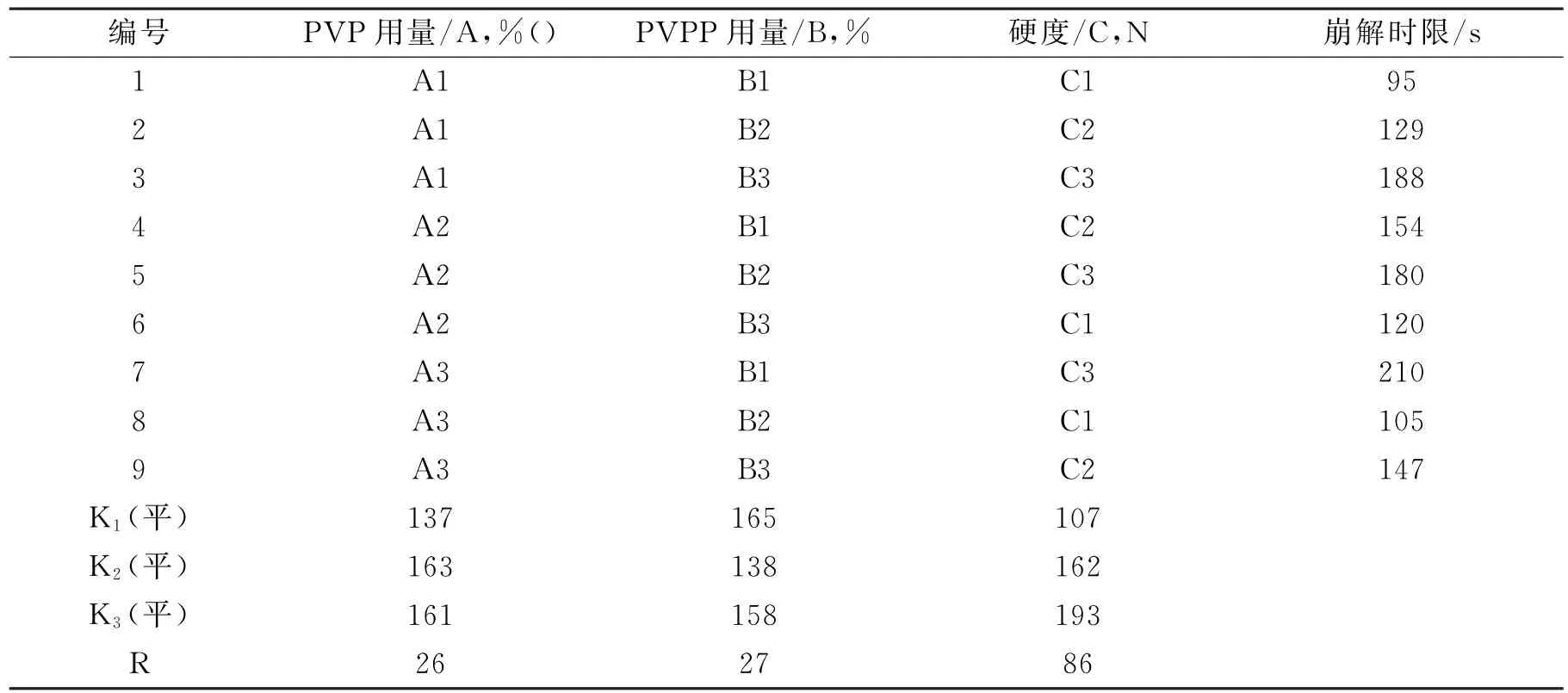
表3 正交实验设计及结果的直观分析

表4 正交试验结果的方差分析结果
由表4直观分析结果显示,各因素对黄芩苷崩解时限影响程度主次为C>B>A;表4方差分析结果表明,C(硬度)具有显著性意义,而因素A(PVP用量),C(PVPP用量)在选择的水平内无显著性差异,由直观分析可以看出,随着口崩片硬度的增加,崩解时间减慢。在硬度为2 kg时虽然崩解速度变得很快,但是口崩片的表面也变得粗糙无光泽;在硬度为6 kg时,口崩片的崩解时间明显减慢,在180 s以上;而硬度为4 kg时,口崩片的崩解时间在150 s以内,且表面光滑有光泽,所以,确定硬度为4 kg时为口腔崩解片的硬度。最佳的处方工艺为PVP用量在1%,PVPP用量在6%,硬度为4 kg。
对正交设计实验中不同处方工艺制备得到口崩片进行体外溶出度测定,结果见图2。

图2 正交设计试验片剂的溶出曲线
由图2溶出曲线比较发现,硬度是影响口崩片体外溶出特性的主要因素,九个处方工艺制得口崩片的溶出曲线分布在3个区域,尤其15 min前的溶出情况为随硬度减小,口崩片的溶出速度加快,溶出量增高,15 min以后硬度为4 kg和2 kg的累积溶出量相差不大,均达到85%以上,但硬度6 kg的溶出度明显下降,仅有55%左右,说明,硬度大小对溶出影响显著;崩解剂用量和黏合剂用量两个因素对溶出影响不显著。
2.1.5 矫味剂比例的筛选 黄芩苷包合物5.0 g; PVPP 0.9 g;体积分数5%PVP乙醇溶液3.0 m L;可压性淀粉8.35 g;硬脂酸镁0.15 g;甘露醇适量;阿司巴甜适量;按着上述处方制备片重0.3,制成50片,其中甘露醇,阿司巴甜总量是0.45 g,甘露醇和阿司巴甜不同配比制得的口崩片,进行品尝。
表5结果发现,口崩片中添加甘露醇,阿司巴甜可进一步掩盖黄芩苷的苦味,不同甘露醇与阿司巴甜配比的影响不同,其中1∶2甜度太高,2∶1稍有甜味,但崩解后有苦味,而1∶1口味甜,片剂崩散后苦味小,口感较好,因此确定甘露醇/阿司巴甜的比例为1∶1。
2.1.6 最终口崩片处方和工艺 通过以上试验,最终优化得到的黄芩苷口崩片的处方为:黄芩苷包合物5.0 g;PVPP0.9 g;体积分数5%PVP乙醇溶液3 m L;可压性淀粉8.35 g;硬脂酸镁0.15 g;甘露醇0.225 g;阿司巴甜0.225 g;制成50片。
制备工艺为:采用湿法制粒压片工艺。将研碎的主药、与稀释剂、崩解剂(加入一半),矫味剂混匀,混入粘合剂(加入崩解剂另一半)制成软材后过20目尼龙筛。于50~60℃干燥约60 min后整粒后于硬脂酸镁混合均匀,压片。控制片重0.3 g,硬度控制4 kg。
2.1.7 工艺重现性实验
按处方制备3批口崩片测定崩解时限并对其外观,口感,硬度及体外崩解时限和体外溶出度进行测定,结果见表5。

表5 连续3批质量检测结果
从表5数据和曲线发现,制备得到的口崩片的口感和体内外崩解时限与处方筛选时的数据是相当的,重复性良好,说明口崩片的处方工艺重现性好。
3 讨论
3.1 矫味剂的选择
黄芩提取物的味道比较苦,对于口腔黏膜具有一定刺激性。我们采用甘露醇和阿司巴甜调节口味。当甘露醇/阿司巴甜的配比为1∶1时,制取的黄芩提取物的粉末口感好,无沙砾感,对口腔黏膜没有刺激性,比较适合口腔崩解片的质量要求。
3.2 辅料种类及比例的筛选
通过对黄芩提取分离工艺的研究,制订了合理可行的生产工艺路线,得到质量稳定可控的黄芩苷口崩片,采用出现频率较高的崩解剂CMS-Na,PVPP,LHPC做崩解剂分别制片,将其与可压性淀粉以相同比例配比,以崩解时间为指标,确定PVPP为崩解剂,通过正交试验对其含量研究,结果PVPP含量为6%时,崩解时间较优。
3.3 辅料的选择
由于本类制剂不需要用水送服,为了达到良好的崩解效果,主药含量要小,总片重也较小。在制备过程中,需要加入大量辅料,否则会影响其速崩,速效的效果。所以本实验所用辅料为主药的2倍,有待于对辅料进一步研究。制备出辅料用量少,崩解时间较好的口崩片。本制剂的崩解时间在150 s左右,溶出度为85%以上。
3.4 片剂硬度
片剂硬度对口腔崩解片的崩解时间影响很大,随着硬度的增加,崩解时间减慢当片硬度在4 kg时,口腔崩解片的崩解时间在150 s以内,同时口腔崩解片的外观光滑有光泽。
4 结论
通过单因素实验确定PVPP作为最佳崩解剂,崩解剂采用内外加法;通过正交实验筛选得到最优处方和制备工艺为崩解剂用量6%,黏合剂用量1%,硬度为4 kg;通过矫味剂筛选确定在口崩片处方中添加甘露醇/阿司巴甜比例为1∶1的甜味剂;最终制备得到的口崩片质量检查项目均符合相关标准要求。
[1]Seager H.Drug delivery products and the Zydis fast-dissolving dosage form[J].Journal of Pharmacy and Pharmacology,1998,50(4):375.
[2]高申.现代药物新剂型新技术[M].北京:人民军医出版社,2002:42.
[责任编辑 李武营]
The Preparation and quality standard of orally disintegrating tablets of balcalin
SONG Weizhong,YANG Lei,LIU Wei,ZHANG Yu
(The Institute of TCM of He Nan University,Kai Feng,Henan 475001,China)
Objective We screen the optimal proportion of baicalin andβ-cyclodextrin inclusion complexes proportion,in order to solve the problem of low dissolution and improve the clinical application of baicalin.Methods
In this paper,we use the spray drying method to prepare the baicalinβ-cyclodextrin with a ratio of 1∶1,1∶2,1∶3,2∶1,inclusion complex,its content was determined by ultraviolet spectrophotometry,its dissolution was determined by smart dissolution test,load factors as an indicator of cumulative dissolution rate of inclusion complex package,filter the proportion inclusion.Using disintegration time as indicators and Lg(34)Orthogonal Design to choose orally disintegrating tablets prescription;through counterpart collapse film the main active ingredient of baicalin content determination,through the appearance,content,disintegration time and dissolution parameters as examining index for quality check.Results 1.Baicalin-βentrapped cyclodextrin complex possess higher dissolution in the dissolution medium,compared with baicalin bulk pharmaceutical chemicals,the proportion of clathrate dissolved in 15 min has a percentage of more than 90%,the dissolution rate is fast and dissolution is more completely.2.The dissolution rate of Baicalin cyclodextrin orally disintegrating tablets within 45 min is more than 85%,the dissolution of baicalin is higher than baicalin.3.The optimal disintegrant is cross-linked povidone(PVPP)with amount of 6%,using internal and external adder;adhesives is PVP with the amount of 1%;hardness control in the proportion of 4.0 kg,the ratio of mannitol and taste masking agent aspartame is 1∶1.ConclusionBaicalin orally disintegrating tablets has a good operability prepared through this method,the preparation process is stable and the releasing rate of baicalin is good,it also tastes good,and may have a good application prospects.
Baicalin;Orally disintegrating tablets;βentrapped cyclodextrin complex;Formulation and process;Quality evaluation
R944.9
A
1672-7606(2014)03-0175-04
2014-02-15
河南省科技厅科技攻关项目(132102310366)。
宋卫中(1970—),男,河南开封人,副教授,从事中药的教学与科研工作。

