托珠单抗治疗系统性硬化症10例
高 飞,吴燕芳,林 禾
(福建省立医院风湿免疫科, 福州 350001)
ChinJAllergyClinImmunol,2016,10(4):371- 376
系统性硬化症(systemic sclerosis,SSc)是一种相对少见的自身免疫性疾病,表现为皮肤及多系统器官进行性的纤维化,目前治疗方法包括一般免疫抑制剂(如糖皮质激素)和并发症的特异性治疗,临床疗效有限。应用托珠单抗(tocilizumab)治疗SSc国外有少量个案报道,国内尚未见报道。现总结本院2015年5月至2016年4月应用托珠单抗治疗10例SSc患者的临床资料。
资料和方法
临床资料
用药情况
在治疗起点0周及用药后每个月给予托珠单抗注射液 8 mg/kg,溶液为0.9%氯化钠注射液 100 ml,每次静滴时间>1 h。5例病程≥3年的患者均坚持应用托珠单抗治疗24周;5例病程<1年的患者3例用托珠单抗治疗12周,2例用托珠单抗治疗24周。
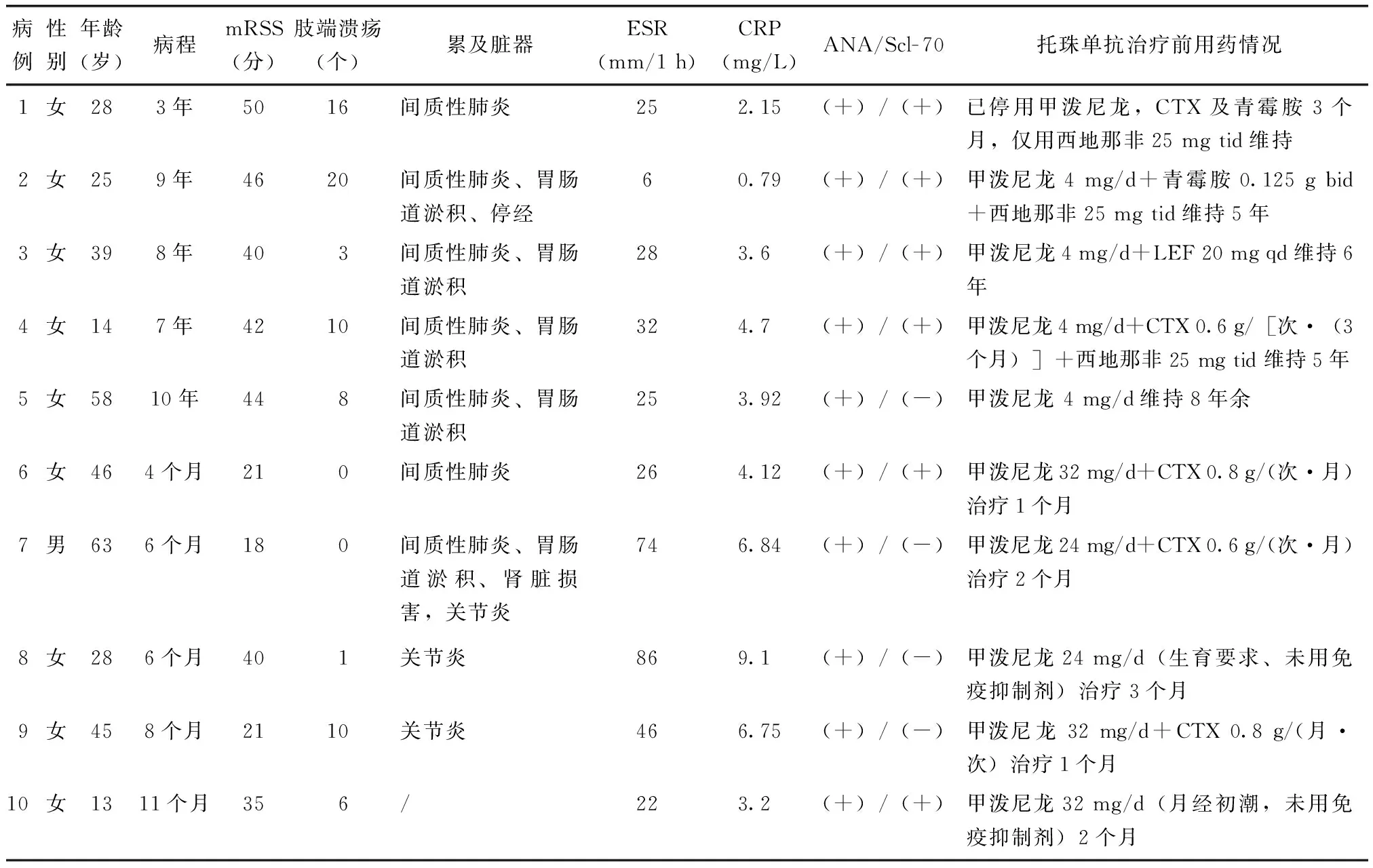
表1 患者一般资料Table 1 Clinical characteristics of 10 patients with systemic sclerosis
mRSS:改良Rodnon皮肤评分;ESR:红细胞沉降率;CRP:C反应蛋白;ANA:抗核抗体;CTX:环磷酰胺;LET:来氟米特;tid:每日3次;bid:每日2次;qd:每日1次
临床指标
由风湿科专科医师在给药前(基线水平)、第12周、第24周进行评估,观察指标判定点:血常规,尿常规,肝功能,肾功能;红细胞沉降率(erythrocyte sedimentation rate,ESR),C反应蛋白(C reactive protein,CRP);患者改良Rodnon皮肤评分(modified Rodnan skin score,mRSS),肢端溃疡数目,患者对疾病总体评估(0~100分),有肺间质病变患者进行肺部CT评估。mRSS是用改良的Rodnan皮肤厚度积分法[2]计算,具体方法:将患者体表划分为面部,前胸,腹部,左、右上臂,左、右前臂,左、右手,左、右手指,左、右大腿,左、右小腿,左、右足共17个区域;对每个区域按评分标准进行评分,厚度正常0分,轻度增厚1分,明显增厚2分,极度增厚3分,然后将17个区域积分累加,最高分51分。
统计学处理
采用SPSS 13.0软件进行统计学处理,将病程≥3年的患者及病程<1年患者分成两组分别进行分析。每次随访结果与基线数据采用Mann-Whitney检验进行比较,以P<0.05为差异有统计学意义。
结 果
mRSS、肢端溃疡数目及患者自我评分
实验每个位置各取了70组图像用于离线训练。准备阶段完成后,打开在线检测程序,任意顺序铆接4个位置,结果如图7所示。4个位置均准确识别,铆接状态均为合格。当4个位置全部铆接完成后,在线检测程序自动生成报表并保存,记录每个位置的铆接状态。
5例病程≥3年患者应用托珠单抗治疗24周后患者mRSS、肢端溃疡数目及患者自我评分均显著改善(P<0.05)。5例病程<1年患者治疗12周评估(表2),患者总体自我评估较基线水平差异有统计学意义(P<0.05);而治疗前后mRSS及肢端溃疡数目临床观察虽有减少,但差异无统计学意义。
皮肤分部位评估
托珠单抗治疗12周前后对患者面部、胸部、腹部、大腿、小腿、足部、手部7个不同区域皮肤变化程度进行组间差异分析,分部位比较后,仅胸部和腹部皮肤在治疗前后差异具有统计学意义,胸部及腹部皮肤改善程度较其他5个部位更为明显(图1)。
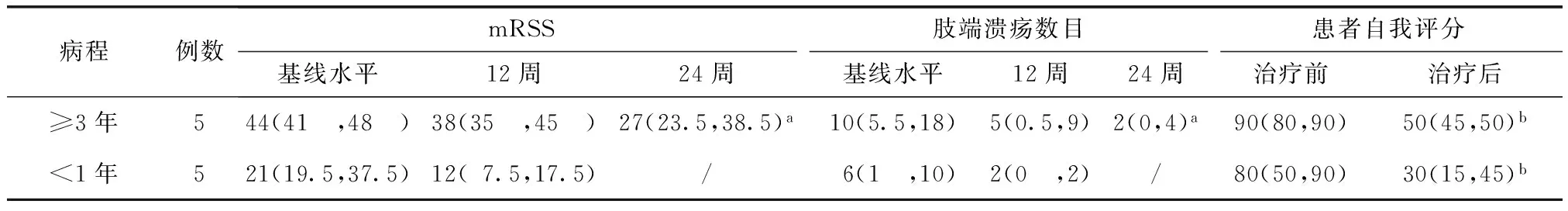
表2 患者治疗前后各项指标评估Table 2 Disease evaluation before and after tocilizumab [中位数(P25, P75)]
与本组基线水平比较,aP<0.05;与本组治疗前比较,bP<0.05
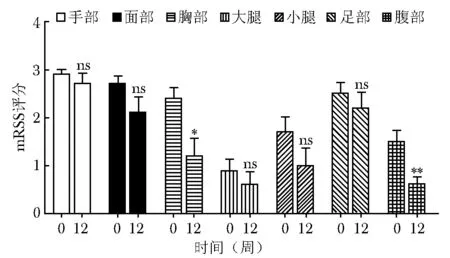
图1 托珠单抗治疗前后7个不同区域皮肤变化程度Fig 1 Comparison of mRss in different parts of skin in patients with tocilizumabns:差异无统计学意义;*P<0.05; **P<0.01
其他临床指标观察
5例病程<1年患者,3例并发关节炎,ESR及CRP升高,托珠单抗治疗后关节炎控制,ESR及CRP明显下降;2例有肺间质性炎症,1例治疗有改善,1例治疗无变化。病程≥3年的5例患者中均存在间质性肺炎,24周治疗后复查肺部CT,2例肺部病变改善,3例肺部病变无变化。10例患者中5例胃肠受累,表现进食后平卧有食物反流,胃肠钡影提示反流性食管炎、淤积性胃肠炎,治疗后症状无改变。病例7男性患者有肾脏受累,治疗前血尿素氮(blood urea nitrogen,BUN) 24.0 mmol/L、肌酐(creatinine,Cr) 186 mmol/L,双肾肾小球滤过率(glomerular filtration rate,GFR):39 ml/min;治疗12周,BUN及Cr恢复正常(BUN 6.6 mmol/L,Cr 111 mmol/L),但复查双肾GFR:35 ml/min无变化。病程长达9年的患者,病程中出现停经1年,托珠单抗治疗前监测性激素水平正常,但超声提示无排卵,托珠单抗12周后,月经来潮,治疗持续至24周,月经始终正常。
安全性观察
托珠单抗注射液治疗前及治疗后12和24周监测患者的血常规、肝功能、肾功能无异常变化,治疗期间均无明显不良反应。
典型病例
病例2,女,25岁,以进行性皮肤增厚、双手雷诺现象9年为主诉于2015年7月28日入院。9年前,出现双手皮肤增厚、变硬,伴指端皮肤遇冷相继变紫、变白。外院诊断:SSc。间断给予激素及青霉胺治疗,皮肤硬化加重,逐渐累及四肢、躯干、颜面部,影响关节活动。2010年9月给予甲泼尼龙40 mg/d并规律减量、CTX 0.6 g/(次·月)及青霉胺、西地那非治疗。入院前甲泼尼龙4 mg/d及青霉胺0.125 g bid、西地那非25 mg tid维持,CTX已停用。查体:生命征平稳,面具脸,口周皮肤放射性皱缩,张口受限(图2A),四肢、肢端、躯干皮肤皮革样增厚,不能捏起,双腕、双手、双肩关节活动受限(图3A、4A),四肢肢端破溃,部分远端指骨缩短,双下肺可闻及裂帛音,心腹体检无异常。肝肾功能:ESR 6 mm/1 h,CRP 0.79 mg/L;血气分析(未吸氧):pH 7.394、PCO240.5 mm Hg、PO296.7 mm Hg、SO297%;自身抗体:ANA 1∶3 200 (+)、Scl- 70(+),补体C3、C4正常,ANCA(-);肺部CT提示:肺间质病变(图5A)。入院诊断:SSc,继发性间质性肺病。治疗12个月mRSS 46分,肢端溃疡反复,肺间质病变无改善。2015- 08- 10给予托珠单抗(雅美罗)8 mg/(kg·月)。治疗6个月,患者自觉皮肤变软,张口距及上肢活动范围明显改善(图2B、3B、4B),mRSS由46分降至27分,肢端溃烂数目由20个减少为3个,患者自我评分由90分降至50分。复查肺部CT提示肺间质病变明显减轻(图5B)。治疗24周,监测血常规、肝肾功能均正常。
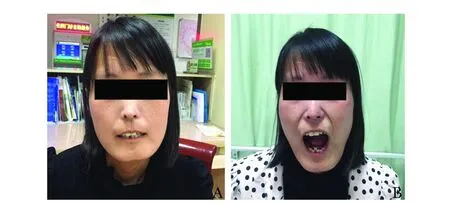
图2 托珠单抗治疗前后张口距Fig 2 Gape distance before and after tocilizumabA:治疗前;B:托珠单抗治疗24周张口距明显增宽
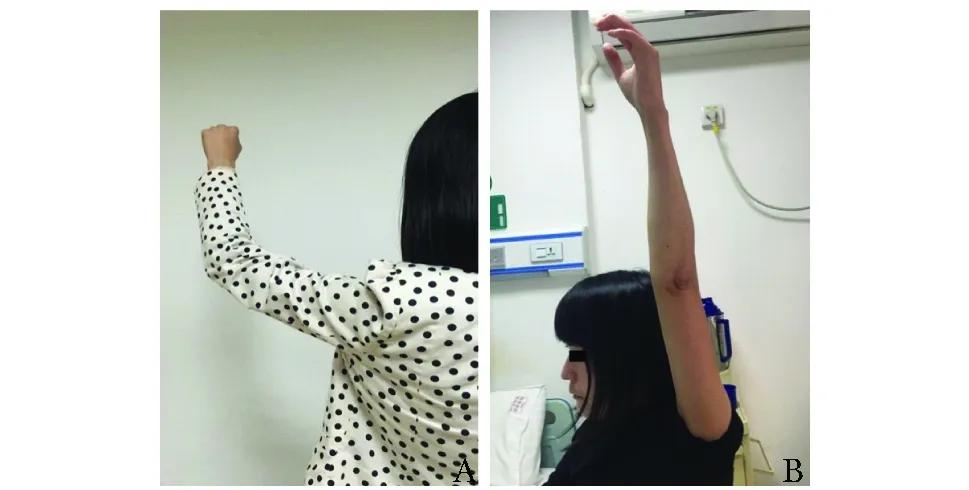
图3 托珠单抗治疗前后肩关节活动度Fig 3 Shoulder range of motion before and after tocilizumabA:治疗前;B:托珠单抗治疗后24周肩关节活动度明显增加
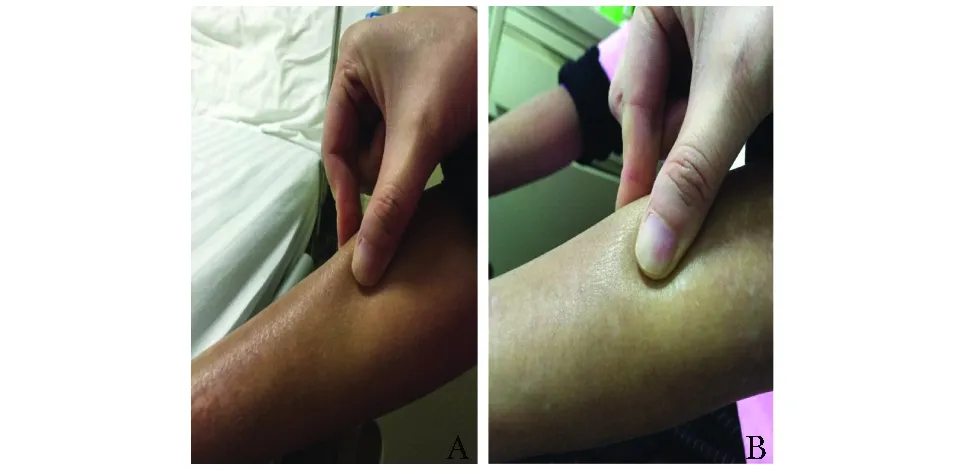
图4 托珠单抗治疗前后前臂皮肤Fig 4 The skin of forearm before and after tocilizumabA:治疗前;B:托珠单抗治疗24周,前臂皮肤肤色变白,变软
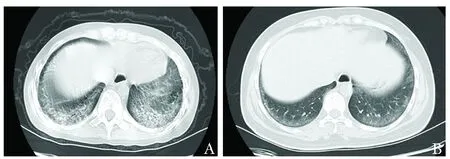
图5 托珠单抗治疗前后肺部CT表现Fig 5 CT manifestations of lung before and after tocilizumabA:治疗前肺部CT,提示下肺间质性病变;B:托珠单抗治疗24周复查肺部CT,双下肺间质性病变明显吸收
讨 论
SSc是一类复杂的病因不明的结缔组织病,目前单一药物治疗仍然无法有效阻止SSc疾病的进程。SSc一旦累及重要的脏器,生存率会明显的降低。研究发现皮肤硬化的范围与患者的生存率相关,患者预后与基线皮肤评分相关,皮肤评分改变与内脏并发症和预后相关[3- 4]。
白细胞介素(interleukin,IL)- 6是一种炎症细胞因子,由单核/巨噬细胞,内皮细胞,间充质细胞如成纤维细胞及滑膜细胞等多种细胞产生,参与多种自身免疫性疾病尤其是类风湿关节炎的发病过程。基础研究中发现IL- 6可能参与SSc的发病,博莱霉素诱导的硬皮病小鼠模型中,可在其血清及皮肤中监测到IL- 6水平的升高,抗IL- 6治疗后,可阻止及延缓小鼠皮肤纤维化[5]。
托珠单抗是一种IgG亚类的重组人源化抗IL- 6受体单克隆抗体,已批准用于治疗类风湿性关节炎,有报道美国正在进行随机的托珠单抗治疗SSc患者的随机临床研究(NCT 01532869)。有关托珠单抗治疗SSc的观察国外仅有个案报道[6- 7],均提示托珠单抗治疗过程中,可观察到SSc患者皮肤硬化程度的改善,2010年Shima等[6]首次报道了托珠单抗治疗2例硬皮病患者,治疗6个月后复查患者的皮肤病理发现治疗前后患者皮肤真皮胶原纤维束的厚度出现明显变薄及血管壁外α-平滑肌肌动蛋白(α-smooth muscle actin,α-SMA)阳性细胞减少,而α-SMA阳性的成纤维细胞的数目据既往文献报道与皮肤的纤维化正相关[8]。
本组例1~5患者临床表现类似:病程长(≥3年),发病初均经过甲泼尼龙[1 mg/(kg·d)]及规则的CTX[0.6~0.8 mg/(月·次)]治疗,疗效差,多次肢端破溃入院治疗,平均mRSS高达44.4分。5例患者,托珠单抗治疗12周时,mRSS分值及肢端溃疡数目较基线下降,但差异无统计学意义,继续治疗至24周,此两项指标改善情况较基线差异有统计学意义(P<0.05)。提示对于病程较长,硬化程度严重的SSc患者,3个月的托珠单抗疗程不足,最少需要6个月以上的疗程方能有明显疗效。另5例患者均为初治,平均病程7个月,应用托珠单抗治疗前,予甲泼尼龙≥24 mg/d同时3例联合予CTX治疗4周以上,患者平均mRSS为27分,托珠单抗治疗12周后,即发现患者自我评价明显改善(P<0.05),推断与病程短、患者皮肤改变尚处于较早时期、对治疗反应好有关,也不能排除患者应用较大激素及CTX治疗增加托珠单抗的疗效;12周评估患者mRSS及肢端溃疡数目,观察有改善趋势,但差异无统计学意义,可能随着治疗的继续或者患者数量的增多或选择更准确的高频超声评估SSc患者皮肤的厚度[9]会出现更有意义的结果。
本组病例,将体表皮肤分为面部、胸部、腹部、大腿、小腿、足部、手部这7个区域,托珠单抗治疗前后,对不同区域皮肤进行组间差异分析,提示胸部、腹部的皮肤硬化的改善程度较面部、手足部更显著,此现象机制不明,可能与SSc患者皮肤硬化的改变多首先出现在手指、面部,此处皮肤病程长、硬化程度重有关。
本组3例SSc患者并发关节炎,ESR及CRP明显增高,应用托珠单抗后,关节症状明显改善,炎症指标迅速下降,说明托珠单抗对SSc并发关节炎的患者疗效显著。10例患者中7例并发肺间质病变,3例复查肺部CT有改善,但样本小,临床上缺乏前后肺功能资料对比,是否能真的改善SSc患者重要靶器官损害还需进一步证实,期望美国随机对照试验最终完成能提供进一步的证据。10例SSc患者托珠单抗治疗中,未发现严重的不良反应发生,患者耐受性及安全性良好。
本组观察结果提示,托珠单抗治疗SSc过程中,可观察到患者皮肤硬化程度及肢端溃疡的改善;托珠单抗可能为常规治疗无效或皮肤硬化进展迅速的硬皮病患者提供一种新的治疗选择;此后还需要更多的样本量做进一步深入研究。
[1]Preliminary criteria for the classification of systemic sclerosis (scleroderma). Subcommittee for scleroderma criteria of the American Rheumatism Association Diagnostic and Therapeutic Criteria Committee[J]. Arthritis Rheum, 1980, 23: 581- 590.
[2]Furst DE, Clements PJ, Steen VD, et al. The modified Rodnan skin score is an accurate reflection of skin biopsy thickness in systemic sclerosis[J]. J Rheumatol, 1998, 25: 84- 88.
[3]Maurer B, Graf N, Michel BA, et al. Prediction of worsening of skin fibrosis in patients with diffuse cutaneous systemic sclerosis using the EUSTAR database[J]. Ann Rheum Dis, 2015, 74: 1124- 1131.
[4]徐东, 李梦涛, 赵久良,等. 系统性硬化症的诊治现状[J]. 中华临床免疫和变态反应杂志, 2012, 6:38- 42.
[5]Desallais L, Avouac J, Fréchet M, et al. Targeting IL- 6 by both passive or active immunization strategies prevents bleomycin-induced skin fibrosis[J]. Arthritis Res Ther, 2014, 16: R157.
[6]Shima Y, Kuwahara Y, Murota H, et al. The skin of patients with systemic sclerosis softened during the treatment with anti-IL- 6 receptor antibody tocilizumab[J]. Rheumatology (Oxford), 2010, 49: 2408- 2412.
[7]Shima Y, Hosen N, Hirano T, et al. Expansion of range of joint motion following treatment of systemic sclerosis with tocilizumab[J]. Mod Rheumatol, 2015, 25: 134- 137.
[8]Kissin EY, Merkel PA, Lafyatis R.Myofibroblasts and hyalinized collagen as markers of skin disease in systemic sclerosis[J]. Arthritis Rheum, 2006, 54: 3655- 3660.
[9]刘赫, 朱庆莉, 侯勇,等. 高频超声测量皮肤厚度在弥漫性系统性硬化症中的应用价值[J]. 中华临床免疫和变态反应杂志, 2015,9:91- 95.