电化学法制备高铁酸盐条件优化的研究
孙旭辉,李 强,李秀萍
(1.东北电力大学 化学工程学院,吉林 吉林 132012;2.中国石油吉林石化公司 研究院,吉林 吉林 132001)
电化学法制备高铁酸盐条件优化的研究
孙旭辉1,李 强1,李秀萍2
(1.东北电力大学 化学工程学院,吉林 吉林 132012;2.中国石油吉林石化公司 研究院,吉林 吉林 132001)
研究了电流密度、电解液浓度、电解液添加剂、电解时间等因素对电化学法制备高铁酸盐产品浓度和电流效率的影响,并从实用性出发,通过对比单位质量高铁酸盐所引入碱量的多少,来确定最佳电解液浓度。研究结果表明,电解时间控制在3 h内,电流密度为17.2 mA/cm2,NaOH电解液浓度为14 mol/L时,高铁酸钠浓度最大,电流效率最高。而从实用性角度,采用8 mol/L的NaOH电解液生产高铁酸钠时,等量高铁酸钠引入碱量最小,即对受纳水体pH值影响最小。在电解液里添加0.01%~0.1% NaCl,对电流效率有一定的提高作用,生成的高铁酸盐浓度提升了14.90%;而当添加0.01%~0.1% Na2SiO3时,电流效率显著提高,高铁酸钠产品浓度提升了40.70%。研究中发现,在低浓度电解液中,添加NaCl或Na2SiO3效果更为显著。
高铁酸盐;电流密度;电流效率;添加剂
高铁酸盐是一种六价铁盐,具有良好的氧化、消毒、灭藻、脱色和除臭等作用,反应后还原产物氢氧化铁具有吸附、絮凝作用,是公认的环境友好型水处理药剂[1,2]。在酸性和碱性条件下,常用的高锰酸盐与重铬酸盐氧化性比高铁酸盐弱,并且还原产物不具备高铁酸盐还原产物所具有的絮凝作用[3]。高铁酸盐与含氯消毒剂相比,不会产生诸如氯代烷烃、氯酚之类的有害物质,安全性更高[4]。随着社会不断发展,人类迫切需要各种效果佳而不引起二次污染的水处理方法[5]。高铁酸盐兼具氧化和絮凝效能,具有重要的研发价值和广阔应用前景。
目前制备高铁酸盐的方法主要分为三种,高温氧化法、次氯酸盐氧化法和电解法[6]。高温氧化法是通过过氧化物与含铁化合物或铁单质,在苛性碱存在下发生高温熔融反应来制备高铁酸盐;次氯酸盐氧化法是在含有铁盐的强碱性溶液中通入氯气,使生成的次氯酸盐氧化Fe (Ⅲ)盐制得Fe (VI)盐;电解法是以铁或惰性电极为阳极,在浓碱溶液中氧化低价铁得到Fe(VI)的工艺方法[7]。高温氧化法制备高铁酸盐,回收率和转化率较高,但化学试剂消耗大,所需反应温度高,容器腐蚀严重,危险性大,目前很少采用该方法[8、9]。次氯酸盐法生产成本较低,设备投资少,可制得较高纯度的高铁酸钾晶体,但需要反复提纯,操作复杂且设备腐蚀严重,环境污染较大[10]。电化学氧化法工艺简单、产品杂质少、环境污染小,使其成为近年来研究热点[11]。
在同一电解槽中,影响电解制备高铁酸盐产量的主要因素有:电解液中苛性碱的种类与浓度、电解液温度、阳极表观电流密度、金属铁电极的化学组成及结构等。在较短的反应时间内,和较低电流密度下可以得到较高的电流效率,但一般高铁酸盐的合成速率都不超过0.07 mol·L-1·h-1,这是由长时间电解后,铁电极钝化和高铁酸盐分解造成的[12]。本文研究了电流密度、电解液浓度、电解液添加剂、电解时间等因素,对电化学法制备高铁酸盐产品浓度和电流效率的影响,以获得一种高效率低能耗快速电解合成高铁酸钠的方法。并从实用性出发,通过对比单位质量高铁酸盐所引入碱量的多少,来确定最佳电解液浓度。
1 实验部分
制备高铁酸盐的电解装置如图1,包括:电解槽、阴极、阳极、离子交换膜和直流电源。将阴、阳极通过导线分别与直流电源负极、正极相连,用阳离子交换膜将两极室分开。向电解槽中注入苛性碱电解液,经过一定的电解时间后,在阳极制得高铁酸盐。阳极采用HT150型灰口铸铁,电极定做成尺寸为10 cm×1 cm×0.5 cm(长×宽×厚)的长方体。阴极采用和阳极尺寸大小相同的石墨电极或其它金属电极。电极使用前需用1:1的盐酸溶液浸泡以除去表面的氧化物膜。用去离子水配制浓度分别为2 mol/L、4 mol/L、6 mol/L、8 mol/L、10 mol/L、12 mol/L、14mol/L、16 mol/L和18mol/L的NaOH溶液作为电解液,待用。

图1 电解制备高铁酸盐的实验装置图
采用亚铬酸盐法标定阳极产生的高铁酸盐浓度,通过消耗已知浓度(NH4)2Fe(SO4)2溶液体积确定高铁酸盐浓度,滴定终点溶液由紫色变为亮绿色,根据公式(1)计算出高铁酸盐的浓度[13]。
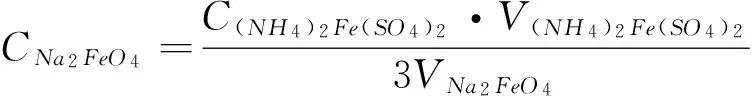
(1)
式中:C(NH4)2Fe(SO4)2为硫酸亚铁铵的浓度,单位mol/L;V(NH4)2Fe(SO4)2为消耗的硫酸亚铁铵体积,单位mL;VNa2FeO4为高铁酸钠的体积,单位mL。
电流效率的计算基于法拉第定律,公式如下[14]:

(2)
式中:Z为转移的电子数(6);F为法拉第常数(96 485.3 C/mol);V为高铁酸盐的体积,单位mL;C为高铁酸盐的浓度,单位mol/L;j为电流密度,单位mA/cm2;S为电极的有效面积,单位cm2;t为电解时间,单位s。
碱引入量,即投加单位质量的高铁酸盐所引入碱的量。实际水处理中引入的碱量过高会使受纳水体的pH值升高,达不到出水指标要求,这制约着高铁酸盐溶液的直接应用。碱引入量计算公式如下:
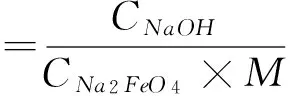
(3)
式中:C碱为每克高铁酸钠引入碱的量,单位mol/g;CNaOH为电解液NaOH溶液的浓度,单位mol/L;CNa2FeO4为投加高铁酸盐的浓度,单位mol/L;M为高铁酸钠的相对分子质量,单位g/mol。
2 结果与讨论
通过大量实验,我们对影响电解法合成高铁酸钠溶液浓度和电流效率较大的因素,如电流密度、电解液浓度、电解时间和电解液添加剂进行了对比研究。
2.1 电流密度的影响
在相同电极、直流电源,不同电解液浓度和电流密度条件下,电解2.5h,考察电流(电流密度)对高铁酸钠浓度和电流效率的影响。电流值分别设为0.1A、0.2A、0.3A、0.4A、0.5A,0.6A和0.7A(相应的电流密度为4.3mA/cm2、8.6mA/cm2、13.04mA/cm2、17.2mA/cm2、21.5mA/cm2、25mA/cm2,29.1mA/cm2)时,高铁酸盐产品浓度和电流效率如图2和图3所示。

图2 电流/电流密度和电解液浓度对合成高铁酸盐浓度的影响图3 电流/电流密度和电解液浓度对电流效率的影响
从图2可见,相同电流/电流密度下,电解液浓度越高,合成的高铁酸钠浓度越大。这是因为,在高浓度碱中,高铁酸根自身的电极电位更低,因而零价铁更容易被合成高铁酸根。相同浓度电解液中,高铁酸盐浓度起初随着电流/电流密度(0.1A/4.3mA/cm2~0.2A/8.6mA/cm2)增加而增加,继续加大电流,高铁酸盐浓度增加缓慢,当电流增至0.6A时,高铁酸盐浓度还有下降趋势。这是因为,电流过大时,二价或三价铁迅速生成,而转化为高铁酸根的速度相比之下较慢,因而造成两种影响,一是表面生成氧化物膜,增大了电阻,抑制了高铁酸盐的进一步生产;二是新生态的低价铁还原分解了高铁酸盐。这两种影响都导致合成的高铁酸盐浓度增长缓慢,或开始降低。另外,电流/电流密度增加之后,析出氧气的速度比析出高铁酸盐的速度更快,即副反应比例增加了,因而总体电流效率也随之下降,如图3。综合图2和图3,在电流/电流密度为0.3A/13.04mA/cm2~0.4A/17.2mA/cm2这个范围内,高铁酸盐产品浓度较高,电流效率下降缓慢,有利于节约电力成本并保证高铁酸盐产品品质。
2.2 电解液NaOH浓度的影响
本实验研究电解液NaOH浓度对制备高铁酸钠浓度、电流效率和应用时碱引入量的影响。

图4 NaOH浓度对高铁酸盐浓度的影响图5 NaOH浓度对电解效率的影响
实验选取了三个典型电流值0.2A,0.4A和0.7A进行电解如图4所示,当电解液浓度小于8M时,高铁酸盐浓度随着NaOH浓度的升高而增大,在8M附近产物浓度达到一个极大值;随着NaOH浓度增大产物浓度先减小后增大,最终在14M附近得到另一个极大值点,当电解液碱度继续增大产物浓度下降。蒋家强等人在电解制备高铁酸钠时也得出14M的氢氧化钠溶液适合作电解液[15]。
电流效率的变化如图5所示,电解效率的曲线与高铁酸盐浓度的曲线类似,均在NaOH浓度为8mol/L和14mol/L除出现了极大值点,当设置电流值为0.2A时曲线尤为明显。碱液浓度高于14mol/L时电流效率降低,原因是碱浓度过高,高铁酸盐溶解度降低,析出后附着在铁电极上,阻碍了铁的进一步溶出,减弱了电子的传递;另外碱浓度过高使得粘度过大,生成的气体难以排出,造成导电效率降低进而降低电流效率。
高铁酸钠溶液应用于在线水处理时出水pH值是一个重要指标,因此需要对碱引入量进行核算与分析。不同浓度电解液的碱引入量如图6所示,2MNaOH溶液碱引入量最大;随着碱浓度增加碱引入量减小,NaOH浓度为6M~8M时碱量最小,仅为0.411mol/g左右;当NaOH浓度升高到10mol/L时,碱引入量增加到0.8mol/g;在12M~14M范围内单位质量高铁酸盐引入的碱量减小到0.6mol/g左右。

图6 NaOH浓度对电解效率对碱引入量的影响
通过研究不同NaOH浓度对电解制备高铁酸钠浓度、电流效率和碱引入量影响和分析,8mol/LNaOH溶液比较适合在线电解制备应用高铁酸钠。
2.3 电解时间的影响
在35 ℃的条件下选择8mol/LNaOH溶液为电解液,每组实验使用同一直流电源控制不同的电解时间(具体为1h、2h、3h、4h、5h和6h)电解。

图7 电解时间对高铁酸钠浓度的影响图8 电解时间对电流效率的影响
高铁酸盐浓度随时间变化如图7所示,在其它电解条件一致的情况下,随着电解时间的增加,高铁酸盐的浓度呈递增趋势。2h末的高铁酸盐浓度几乎是1h末浓度的两倍,电解3h浓度比2h有较大的提高但没有前1h提高的明显,3h后高铁增加速率趋缓。
电解效率随时间变化如图8所示,电解4h和3h电流效率改变值较前3h的改变的平均值较大,即电解3h后电流效率减小速度加快,高铁酸盐生成速率明显减慢,这是由于电解3h后铁电极表面钝化严重导致电流效率下降加速。
综合不同时间对电解制备高铁酸盐的浓度和电流效率的影响,在8mol/L的NaOH电解液中电解HT150型铸铁3h最好,如果电解时间超过3h需要更换电极来减弱铁电级表面钝化从而减小电流效率降低速度。
2.4 添加剂对电解的影响
高铁酸钠在溶液中的稳定性不仅受高铁酸钠浓度、温度、碱液浓度影响,还与溶液中其它离子种类和含量有关,可以在电解液中投加不同试剂来提高电解反应的电流效率[16]。
2.4.1 添加剂NaCl对电解的影响
控制其它条件相同,在阳极电解液中加入不同剂量的助剂NaCl,具体量为:0.05%、0.1%、0.2%,0.5%和1%(均为质量分数,下同)电解制备高铁酸钠。
8mol/L的NaOH电解液中添加不同量的NaCl获得高铁酸钠浓度如图9(a)所示,当投加量为0.5%时对电解的促进作用最大,此时高铁酸钠的浓度为0.081 2mol/L,而空白组高铁酸钠浓度为0.071mol/L,浓度提升了14.37%。14mol/L的NaOH溶液中投加不同质量分数的NaCl获得高铁酸盐浓度如图9(b)所示,总体趋势与8mol/L的NaOH溶液产物浓度变化相似,在整个投加量范围内NaCl的投加都可以提高高铁酸钠的浓度。随着投加量的增多,高铁酸盐浓度也有所升高,当NaCl的投加量为0.2%时达到最大值,高铁酸钠的最大浓度为0.112 6mol/L,较空白组的0.098mol/L增加14.90%。NaCl提高高铁酸钠的浓度可能是由于Cl-是活化离子,能消除阳极钝化,加速铁溶解[17]。

图9 电解液中投加不同质量分数的NaCl对高铁酸盐浓度的影响
2.4.2 添加剂Na2SiO3对电解的影响
其它条件不变,在阳极电解液中加入不同剂量的助剂Na2SiO3,具体量为:0.05%、0.1%、0.2%,0.5%和1%,电解制备高铁酸钠。
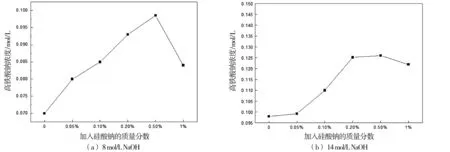
图10 电解液中投加不同质量分数的Na2SiO3对高铁酸盐浓度的影响
在8mol/L的NaOH电解液中添加不同剂量硅酸钠获得高铁酸钠如图10(a)所示,在0~0.5%投加范围内随着投加量的增加高铁酸钠浓度升高,当硅酸钠的质量分数超过0.5%时高铁酸钠浓度开始下降但仍然高于空白组。在整个Na2SiO3投加量范围内都可以提高高铁酸钠的浓度,当投加量为0.5%时高铁酸钠浓度达到极大值为0.098 5mol/L,与空白组的0.07mol/L相比提升了40.70%。硅酸钠提升高铁酸钠浓度的原因,可能是硅酸钠起到了稳定剂的作用,因为电解液中高铁酸盐的浓度=(合成的高铁酸钠-分解的高铁酸钠)/电解液体积,虽然稳定剂无法提高高铁酸钠的合成速率,但可以减少产物分解从而起到提升高铁酸钠浓度的作用[18]。
14mol/LNaOH中投加不同质量分数的Na2SiO3高铁酸盐浓度变化如图10(b)所示,随着硅酸钠加入量的增多高铁酸钠浓度逐渐提高,当投加量为0.5%时高铁酸钠浓度达到一个极大值,此时高铁酸钠浓度为0.126mol/L;随着投加剂量继续增加,高铁酸钠浓度略微下降,但在整个投加范围都可以提升高铁酸钠的浓度,最大值较空白组的0.098mol/L提升了26.55%。
3 结 论
浓度为8mol/L、14mol/L的NaOH溶液更适合电解制备高铁酸钠,最佳电流密度分别为17.2mA/cm2和21.5mA/cm2;最佳电解时间为3h;在线制备高铁酸盐应选用NaOH浓度为8mol/L的电解液,生产单位质量的高铁酸钠碱引入最低,对水体酸碱度影响最小;适量添加剂NaCl、Na2SiO3对制备高铁酸钠的浓度和电流效率有一定提高作用。
[1]E.L.Yang,J.J.Shi,H.C.Liang.On-lineelectrochemicalproductionofferrate(VI)forodorcontrol[J].ElectrochimicaActa,2012,63:369-374.
[2]SharmaVK.Potassiumferrate(VI):anenvironmentallyfriendlyoxidant[J].AdvancesinEnvironmentalResearch,2002,6(2):143-156.
[3]J.Q.Jiang,L.B.loyd.Progressinthedevelopmentanduseofferrate(VI)saltasanoxidantandcoagulantforwaterandwastewatertreatment[J].WaterRes,2002,36(6):1397-1408.
[4] 孙旭辉,李迎,常星岚,等.低强度交变磁场对盐水中紫铜的缓蚀作用[J].东北电力大学学报,2015,35(5) :27-32.
[5]V.K.Sharma.Ferrate(VI)andferrate(V)oxidationoforganiccompounds:kineticsandmechanism[J].CoordinationChemistryReviews,2013,257(2):495-510.
[6]Z.Macova,K.Bouzek,H.Jan,etal.Researchprogressintheelectrochemicalsynthesisofferrate(VI) [J].ElectrochimicaActa,2009,54(10):2673-2683.
[7] 张雪盈,杨长春,石秋芝.高铁酸盐研究进展[J].合成化学,2006,14(2):113-117.
[8] 孙旭辉,郑文平,庹万权,等.电化学合成法制备高铁酸盐的研究进展[J].化工进展,2014,33(6):1380-1386.
[9]V.K.Sharma.Oxidationofnitrogen-containingpollutantsbynovelferrate(VI)technology:areview.[J].JournalofEnvironmentalScience&HealthPartAToxic/hazardousSubstances&EnvironmentalEngineering,2010,45(6):645-667.
[10] 韩琦,董文艺.新型高效水处理剂高铁酸钾的研究进展[J].环境科学与技术,2012,35(12):200-205.
[11]N.Ljiljana,C.Milan,V.Mirjana,etal.Acomparativestudyofiron-containinganodesandtheirinfluenceonelectrochemicalsynthesisofferrate(VI) [J].JournalofIndustrialandEngineeringChemistry,2012,18(6):1931-1936.
[12]Z.Ding,C.Yang,Q.Wu.Theelectrochemicalgenerationofferrateatporousmagnetiteelectrode[J].ElectrochimicaActa,2004,49(19):3155-3159.
[13] 贾汉东,杨新玲,杨勇.高铁酸盐的直接分光光度法测定[J].分析化学,1999,27(5):617-620.
[14] 罗志勇,张胜涛,郑泽根.高容量绿色电池材料高铁酸盐的研究进展[J].材料导报,2014,28(12):123-127.
[15]J.Q.Jiang,C.Stanford,M.Alsheyab.Theonlinegenerationandapplicationofferrate(VI)forsewagetreatment—Apilotscaletrial[J].Separation&PurificationTechnology,2009,68(2):227-231.
[16] 何伟春,关春龙,左宏森.高铁酸盐制备方法研究进展[J].无机盐工业,2009,41(12):1-4.
[17]J.Q.Jiang,M.Alsheyab.Engineeringaspectsofelectrochemicalgenerationofferrate:asteptowardsitsfullscaleapplicationforwaterandwastewatertreatment[J].WaterAirSoilPollut.2010,210(1):203-210.
[18] 孙旭辉,李文超,李冰,等.高铁酸盐的制备、性质及在水处理中的应用[J].东北电力大学学报,2015,35(4):33-39.
Optimization on the Process of Electrochemical Ferrate(VI) Synthesis
Sun Xuhui1,Li Qiang1,Li Xiuping2
(1.School of Chemical Engineering,Northeast Electric Power University,Jilin Jilin 132012;2.Research Institute of Jilin Petrochemical Company,Jilin Jilin 132001)
Ferrate(VI) was synthesized by electrochemical method.Factors like electrolysis duration,current density,and electrolyte concentration that influence the ferrate concentration and current efficiency were studied.By comparing the different amount of alkali that was introduced into the received water body per unit mass of ferrate,practicality was evaluated.The results show that if the electrolysis time is controlled within 3h,the anode surface can avoid to be oxidized,and higher ferrate concentration could be gained.The highest current efficiency was obtained at 14mol/L of NaOH electrolyte.However,in water treatment,when 8mol/L of NaOH was used to produce ferrate,with the application of the same amount of ferrate,the alkali had the least effect on the pH of the receiving water.NaCl (0.01%~0.1%) as an additive of electrolyte can enhance the current efficiency,which made the ferrate concentration improved by 14.90%.While Na2SiO3(0.01%~0.1%) as an additive has a significant positive effect on the current efficiency,which made the concentration of the product improved by 40.7%.In the lower concentration of electrolyte,the additive has more remarkable effect on current efficiency.
Ferrate;Current density;Current efficiency;Additives
2017-03-12
吉林省科技厅科研项目基金(20170204016GX);吉林市科技局科研项目基金(2015334006)
孙旭辉(1966-),女,博士,副教授,主要研究方向:水处理技术.
1005-2992(2017)02-0052-07
O646;TQ138.1
A
电子邮箱: sunxh@neepu.edu.com(孙旭辉);757874175@qq.com(李强);xpl2003@126.com(李秀萍)

