维拉帕米联合卡托普利对家兔心肌缺血再灌注损伤的保护作用
心肌缺血再灌注损伤(myocardial ischemia reperfusion injury, MIRI)是指心肌局部缺血一段时间后由于血液中缺乏氧气和营养物质,在开放循环(恢复血液再灌注)后引起的心肌缺血性损伤。随着体外循环以及各种血管外科技术广泛应用于各类心脏手术、外科手术中,MIRI己成为影响各种心脏手术最终疗效的重要因素。研究表明,氧自由基(oxygen free radical, OFR)产生[1]、钙超载[2]及炎症反应[3]是MIRI发生的重要原因,而钙通道拮抗剂与血管紧张素抑制剂对心肌保护作用的研究也受到临床医师的广泛关注。本研究就维拉帕米联合卡托普利对家兔MIRI的保护作用进行分析,现报道如下。
1 材料与方法
1.1 实验动物与药品试剂
1.1.1 实验动物 选取健康家兔24只,雌雄各半,清洁级,体重 2.4~2.6 kg,由内江市第二人民医院动物实验中心提供。
1.1.2 药品试剂 盐酸维拉帕米注射液(江苏宜兴前进制药厂生产,批号:20170108)、卡托普利(常州制药厂有限公司生产,批号:20170404)、0.9%氯化钠注射液、1%戊巴比妥钠、无水乙醇(国产分析纯)、超氧歧化酶(SOD)试剂盒、丙二醛(MDA)试剂盒。
1.2 MIRI模型建立及分组
1.2.1 MIRI模型建立 于家兔耳缘静脉注射 1%戊巴比妥钠,麻醉药物起效后,将家兔仰卧位固定于手术台上,胸部备皮,将八导联电生理记录仪电极端刺入家兔四肢皮下,接通电源,测定家兔正常标Ⅱ导联心电图,于距家兔胸骨左缘约0.5 cm 处做一纵型切口,依次切开皮肤及皮下组织,暴露肋骨,采用止血钳剥离肋间肌肉,沿胸骨3~5肋间开胸,暴露心脏,剥离心包膜,探查冠状动脉左前降支,用持针器将心外科U型7-0带线圆针于家兔左心耳下缘约2 mm处进针,于肺动脉圆锥左侧缘出针,进针深度1.0~1.5 mm,宽度2.0~2.5 mm。将一小段硅胶管置于结扎线与冠状动脉之间,拧紧结扎,采用硅胶管压迫左冠状动脉前降支,使其闭塞。将心脏放回胸腔,迅速挤出胸腔内气体,关闭胸腔,整个开胸时间不超过30 s,假手术组只放置手术线而不结扎。以Ⅱ导联心电图QRS波幅度增高、增宽,ST段弓背向上抬高≥0.2 mv为结扎成功标志。调节室内温度使动物体温维持正常。于结扎成功后 30 min松开肠嵌,再次暴露心脏,剪断结扎线,去掉硅胶管,再灌注180 min(此操作过程不超过30 s)。以放松结扎线后,QRS波幅降低,抬高的ST段开始回落为再灌注成功标志。
1.2.2 动物分组 将所有家兔随机分为 6组,假手术组、对照组、缺血再灌注组、卡托普利组、维拉帕米组及卡托普利+维拉帕米组,每组4只。①假手术组(左前降支穿线不结扎,穿线后给予0.9%氯化钠注射液10 ml/kg);②对照组(左前降支结扎30 min,未灌注,建立急性心肌缺血模型,并给与0.9%氯化钠注射液10 ml/kg,不用药物干预);③模型组(左前降支结扎 30 min,再灌注180 min,建立 MIRI模型,于再灌注前10 min给予0.9%氯化钠注射液10 ml/kg);④卡托普利组(左前降支结扎30 min,再灌注180 min,于再灌注前10 min给予卡托普利2.1 ml/kg);⑤维拉帕米组(左前降支结扎30 min,再灌注180 min,于再灌注前10 min给予维拉帕米0.2 ml/kg);⑥联合给药组(左前降支结扎30 min,再灌注180 min,于再灌注前10 min给予卡托普利2.1 ml/kg+维拉帕米0.2 ml/kg)。
1.3 观察指标 实验结束后,测定家兔心肌组织中MDA和SOD水平,采用比色法测定MDA含量,通过亚硝酸盐法测定SOD含量。
1.4 统计学分析 采用SPSS 17.0统计软件对实验数据进行分析,符合正态检验的计量资料以±s表示,多组间比较采用单因素方差分析,方差齐者组间数据比较采用LSD检验,方差不齐者组间数据比较采用Games-Howell检验,P<0.05表示差异有统计学意义。
2 结果
模型组家兔心肌组织中的 MDA水平明显高于假手术组,但低于对照组,SOD水平明显低于假手术组,但高于对照组,差异均有统计学意义(均P<0.05);维拉帕米组、卡托普利组与模型组比较,MDA水平显著降低,SOD水平明显升高,差异均有统计学意义(均P<0.05);联合用药组与卡托普利组、维拉帕米组比较,MDA含量进一步降低,SOD活性进一步升高,差异均有统计学意义(均P<0.05)。见表 1。
3 讨论
随着外科手术发展,心脏手术、介入手术的普及,临床中MIRI患者也逐渐增加。MIRI发生与氧自由基增多、钙超载、炎症和心肌细胞凋亡等有关。在缺血再灌注过程中,由于缺血缺氧,自由基生成增多,可导致心肌组织发生脂质过氧化损伤,从而引起心肌细胞结构损伤和功能障碍,最终造成MIRI发生。MIRI引起的主要结构、功能和代谢变化包括再灌注性心律失常、心肌顿抑和微血管顿抑、心肌结构改变[4]。MIRI可严重影响缺血后心脏功能的恢复,甚至危及患者生命。因此,如何防治MIRI已成为当前医学热点之一。目前治疗MIRI最重要的途径为缺血预处理和缺血后处理,但这两种途径在临床实施中因操作难度高、风险大而受到限制。此后,相关学者相继发现积极使用药物预处理可以有效保护心肌细胞,其中包括钙通道拮抗剂与血管紧张素转换酶抑制剂[5-6]。
表1 5组家兔心肌组织中MDA和SOD水平比较(±s)
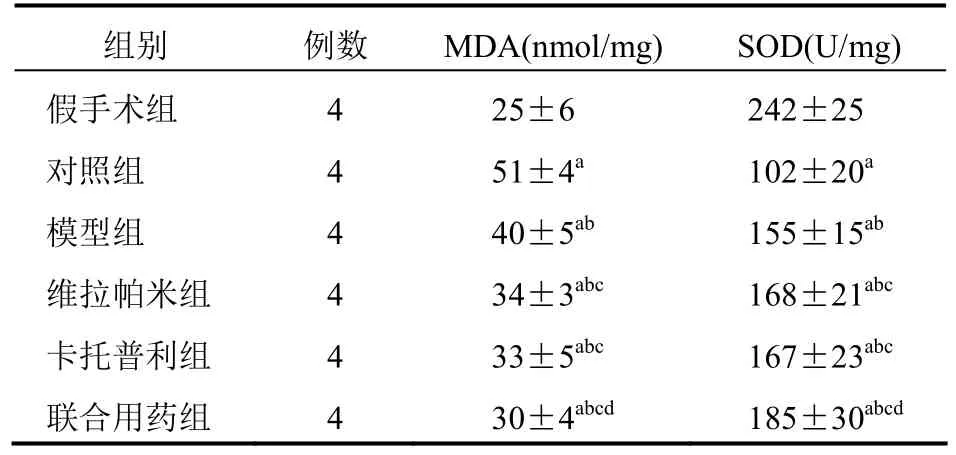
表1 5组家兔心肌组织中MDA和SOD水平比较(±s)
注:与假手术组比较,aP<0.05;与对照组比较,bP<0.05;与模型组比较,cP<0.05;与维拉帕米组比较,dP<0.05
组别 例数 MDA(nmol/mg) SOD(U/mg)假手术组 4 25±6 242±25对照组 4 51±4a 102±20a模型组 4 40±5ab 155±15ab维拉帕米组 4 34±3abc 168±21abc卡托普利组 4 33±5abc 167±23abc联合用药组 4 30±4abcd 185±30abcd
肾素-血管紧张素系统过度激活、血管紧张素Ⅱ异常升高是MIRI进一步发展的重要机制之一[6]。因此治疗MIRI的关键为抑制血管紧张素Ⅱ过度生成。卡托普利(captopril, Cap)作为第一代血管紧张素转换酶抑制剂(ACEI),常用于治疗高血压和充血性心力衰竭等疾病。最近研究表明,Cap除可扩张冠状血管外,具有抑制心肌细胞内钙离子超负荷[7]、抗氧自由基[8]、抑制缓激肤降解、减轻无复流现象、改善缺血心肌能量代谢[9]、改善微循环、抗心律失常等作用。但也有研究发现,单纯使用卡托普利并不能模拟经典的缺血预处理作用[10]。而维拉帕米是一种钙通道拮抗剂,其预防MIRI机制是通过抑制细胞胞膜钙离子通道,阻断钙超载的始动环节,抑制再灌注期钙离子内流。维拉帕米治疗MIRI的效果已被基础研究与临床试验所证实[11]。维拉帕米能降低缺血心肌组织中 MDA水平和保护 SOD活性,促进前列环素(PGI2)合成。心肌组织中的MDA水平直接反映机体受自由基攻击的严重程度与体内脂质过氧化程度,SOD是一种清除体内自由基必要的酶,SOD活性降低可减少自由基清除,因此维拉帕米对家兔MIRI具有保护作用[12]。
本研究结果显示,维拉帕米和卡托普利联合使用可明显提高MIRI家兔心肌组织中SOD的活性,降低MDA水平。提示联合使用后可明显改善MIRI家兔心脏功能。
本研究从药理学的角度揭示了维拉帕米与卡托普利治疗 MIRI的机制,为临床用药提供了理论依据。但本研究仅从MDA与SOD入手,未对其他可能的机制进行研究,后续应从血液流变学指标、心功能指标、基因蛋白表达的角度进行进一步研究。

