阪崎肠杆菌在不同品牌显色培养基上的对比分析
李 翠,周志云,杨 静,杨晓莉
(陕西省食品药品监督检验研究院,西安 710065)
本文按照国家标准[1-7]根据阪崎肠杆菌在分离平板的菌落形态,选择不同生产单位的分离培养基进行分离培养,对市售的不同生产单位的阪崎显色培养基(DFI)进行对比,评判不同生产单位培养基的选择性强弱,为生产企业及相关检验机构对培养基供应商的选择提供依据,为食品标准中阪崎肠杆菌检验培养基的选用提供参考。
1 材料与方法
1.1 试验材料
1.1.1试验用菌株 阪崎肠杆菌(ATCC 29544-3),批号:20160613,购自青岛高科技工业园海博生物技术有限公司。
1.1.2仪器材料 LRH-250F生化培养箱,重庆万达实验仪器厂生产;WP-600恒水式电热恒温培养箱,重庆万达实验仪器厂生产;LRH-250F生化培养箱,广东省医疗器械厂生产;CC型BagSystem样品均质器系统,法国interscience生产;全自动微生物生化鉴定系统VITEK2 Compact 30,法国梅里埃有限公司生产;革兰氏阴性细菌鉴定卡 (VITEK 2 GN Test Kit ),美国Biomer teux inc生产。
1.1.3培养基 试验中使用的培养基信息见表1。
1.1.4样品 奶粉,2017年国家食药总局盲样考核,规格100g/袋,样品编号CODE1~CODE10;菌株,国家食药总局盲样考核,规格1株/支,样品编号CODE1~CODE10。

表1 试验中使用的培养基信息
注:编号A、B、C、D、E分别为不同生产单位的不同品牌的阪崎肠杆菌显色培养基
1.2 方法
1.2.1前增菌和增菌 取奶粉100g和菌株1支从CODE1~CODE10分别加入已预热至44℃装有900mL缓冲蛋白胨水的均质袋中,用均质器均质1min,使样品充分溶解,置36℃培养18h。分别移取上述增菌液1mL转种于10mL mLST-Vm肉汤,置44℃培养24h。
1.2.2分离 轻轻混匀mLST-Vm肉汤培养物,各取增菌培养物1环,分别划线接种于5个生产单位各2个阪崎肠杆菌显色培养基平板,36℃培养24h。从每个阪崎显色培养基平板上分别挑取5个可疑菌落,不足5个的全部挑取,划线接种于TSA平板,25℃培养48h。 自TSA平板上直接挑取黄色可疑菌落,进行生化鉴定,并用VITEK 2全自动微生物生化鉴定系统进行确认。
2 结果与分析
与其他肠杆菌不同,阪崎肠杆菌独有a-葡萄糖苷酸酶。阪崎肠杆菌显色琼脂含有a-葡萄糖苷酸酶底物,当被阪崎肠杆菌水解时形成蓝绿色的阳性菌落。阳性菌株在所有生产单位生产的DFI上均显示为蓝绿色菌落。上述10个样本在A单位的DFI平板上,CODE2、CODE7有蓝绿色菌落生长,其余8个样本在DFI平板上均为褐色菌落;在B单位的DFI平板上除CODE5无菌落生长外,其余9个样本在DFI平板上均有蓝绿色菌落生长;在C单位的DFI平板上CODE2、CODE6、CODE7有蓝绿色菌落生长,CODE5无菌落生长,其余样本为白色菌落、白色中心黑色菌落;在D单位的DFI平板上,CODE2、CODE3、CODE4、CODE6、CODE7、CODE8、CODE10有蓝绿色菌落生长,CODE5和CODE9均为浅紫色菌落;在E单位的DFI平板上,CODE2、CODE7有蓝绿色菌落生长,其余8个样本在DFI平板上均为褐色菌落(表2)。
表3显示,对A单位DFI平板上的蓝绿色菌落进行鉴定,从CODE2平板上挑取的5个菌落和从CODE7平板上挑取的5个菌落均确认为阪崎肠杆菌。对B单位DFI平板上的蓝绿色菌落进行鉴定,CODE2平板上挑取的5个菌落中有3个确认为阪崎肠杆菌,其余2个菌落确认为奇异变形杆菌;CODE7平板上挑取的5个菌落中有3个确认有阪崎肠杆菌,其余2个菌落确认为奇异变形杆菌,CODE1、CODE3、CODE4、CODE8、CODE9、CODE10上分别挑取的5个菌落均确认为奇异变形杆菌,CODE6上挑取的5个菌落均确认为弗劳地柠檬酸杆菌。对C单位DFI平板上的蓝绿色菌落进行鉴定,CODE2和CODE7平板上挑取的5个菌落均确认为阪崎肠杆菌,CODE6上挑取的5个菌落均确认为弗劳地柠檬酸杆菌。对D单位DFI平板上的蓝绿色菌落进行鉴定,CODE2上挑取的5个菌落均确认为阪崎肠杆菌;CODE7上挑取的5个菌落中有2个菌落确认为阪崎肠杆菌,其余3个确认为奇异变形杆菌;CODE1、CODE3、CODE4、CODE8、CODE10上分别挑取的5个菌落均确认为奇异变形杆菌,CODE6上挑取的5个菌落均确认为弗劳地柠檬酸杆菌。对E单位DFI平板上的蓝绿色菌落进行鉴定,从CODE2平板上挑取的5个菌落和从CODE7平板上挑取的5个菌落均确认为阪崎肠杆菌。

表2 样品在DFI平板上的菌落形态

(续)

表3 各疑似菌落VITEK 2鉴定结果
备注:“/”表示显色平板未见疑似,未进行确认试验;“+”表示检出阪崎肠杆菌;“-”表示未检出阪崎肠杆菌
表4显示,A和E单位的DFI选择性明显优于其他3个单位的显色培养基,10份样本中有2个样本在显色培养基上有疑似菌落生长,从2个样本中挑取10个疑似菌落经纯化、鉴定确证为阪崎肠杆菌,阳性准确率达到100%,假阳性菌落数为0;C单位的DFI选择性次之,10个样本中有3个样本在显色培养基上有疑似菌落生长,从3个样本中挑取15个疑似菌落经纯化、鉴定确证10个疑似菌落为阪崎肠杆菌,阳性准确率为66.67%,假阳性菌落数为5;D单位的DFI和B单位的DFI选择性最低,10份样本中分别有7个样本和9个样本在显色培养基上有疑似菌落生长,分别挑取35个疑似菌落和45个疑似菌落经纯化、鉴定确证为阪崎肠杆菌的菌落数分别为7和6,假阳性菌落数分别为22和39,准确率仅为20.00%和13.33%。
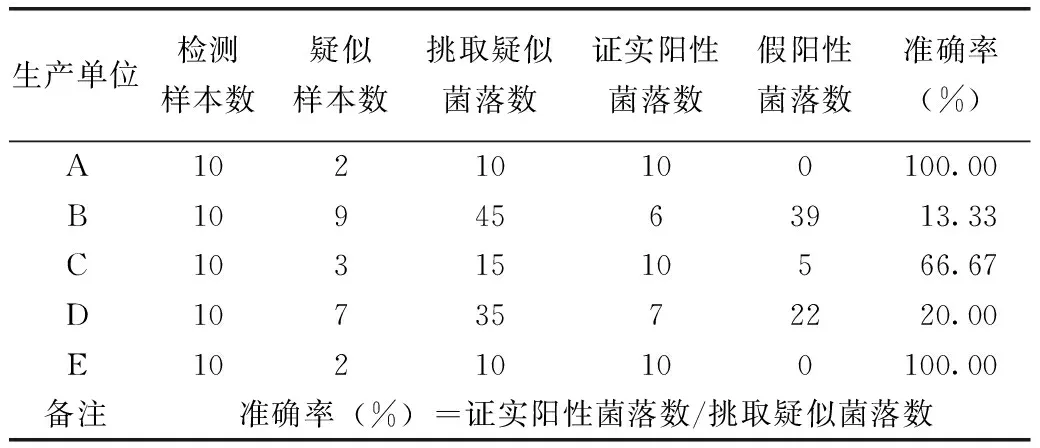
表4 各生产单位显色培养基选择性对比结果
3 讨论
本实验中E单位和A单位生产的DFI培养基具有较好的选择性,准确率均达到100%,且在平板上生长的菌落形态比较典型,在阪崎肠杆菌检查时,可首选此2个生产单位的显色培养基进行实验。显色培养基也存在一定的缺陷,由于某些肠道细菌也会含有与阪崎肠杆菌相同的α-D-葡萄糖苷酶,或奶粉在生产加工的过程中添加的有机或无机成分种类多且复杂,影响了酶与底物的反应,在没有高效的前增菌条件下,会出现假阳性和假阴性现象,从而干扰目标菌的检测。这些缺陷可以通过改变增菌培养条件等方法弥补而取得良好的分离、鉴定效果[8]。进行阪崎肠杆菌的检查时,在样品的前增菌和增菌培养中要严格按照标准操作,样品要加入到预热至44℃的缓冲蛋白胨水充分溶解,转种的mLST-Vm肉汤要临用新制,保证在24h内使用,使样品中可能污染的微生物充分复苏,以得到更加科学、准确地实验结果,确保食品的安全、可靠。B单位和D单位生产的DFI培养基选择性低,假阳性样本数分别为5和7,准确率分别为13.33%、20.00%,假阳性样本数较多,在显色培养基分离中不能快速、有效、准确的筛选出目标菌,使整个实验变得复杂,增加工作量。对于没有生化鉴定系统,需要通过显色培养基筛选结果判定的单位,可能会造成误判。建议必须通过API、VITEK、PCR等鉴定后才可以下结论。对同种培养基不同生产单位的对比较少[9-13],而不同生产单位的同种培养基的选择性、准确率差异较大,因此,建议各单位在参加盲样考核、能力验证、比对试验时尽量选择不同生产单位的增菌培养基或选择性分离培养基,避免因培养基的质量差异而出现检验结果的错判。同时,严格按照国标[14]进行培养基的验收检查。◇

