安罗替尼联合多西他赛对比单药多西他赛在驱动基因阴性晚期非小细胞肺癌二线治疗的临床研究
肖集文
怀化市第一人民医院,湖南 怀化 418000
肺癌为临床常见恶性肿瘤,其发病率居全球恶性肿瘤前列,其中非小细胞肺癌(non-small cell lung cancer,NSCLC)占80%左右,约60%NSCLC患者就诊时已处于晚期阶段,主要通过化疗缓解患者临床症状,延长其生存周期[1-2]。多数驱动基因阴性晚期NSCLC患者初次化疗后病情进展,常采用以多西他赛为主的二线化疗方案,但远期疗效难以达到理想效果[3]。如何优化二线化疗方案,提高远期疗效为临床研究热点之一。安罗替尼为多靶点酪氨酸激酶抑制剂,可抑制成纤维母细胞生长因子(fibroblast growth factor,FGF)、血小板衍生生长因子(plateletderived growth factor,PDGF)等,阻碍肿瘤进展。本研究选取我院驱动基因阴性晚期NSCLC患者78例,旨在探讨安罗替尼联合多西他赛治疗的远期疗效及安全性,现报道如下。
1 资料与方法
1.1 一般资料选取至我院驱动基因阴性晚期NSCLC患者78例(2018年6月至2019年1月),采用随机数字表法分为联合组(n=39)、单一组(n=39)。单一组男22例,女17例,年龄45~78岁,平均(61.52±7.11)岁;病理分型:鳞癌17例、腺癌14例、大细胞癌8例;TNM分期:ⅢB期27例、Ⅳ期12例。联合组男21例,女18例,年龄44~79岁,平均(60.03±7.52)岁;病理分型:鳞癌18例、腺癌11例、大细胞癌10例;TNM分期:ⅢB期26例、Ⅳ期13例。两组基线资料(性别、年龄、病理分型、TNM分期)均衡可比(P>0.05)。
1.2 选取标准①纳入标准:经细胞学或组织病理学确诊;预计生存时间≥3个月;临床分期为ⅢB~Ⅳ期;知情本研究并签署同意书。②排除标准:精神障碍性疾病;合并其他恶性肿瘤;近1个月内接受放疗者;合并免疫功能缺陷;合并严重肝、肾功能损伤;合并严重感染;对本研究药物过敏者。
1.3 方法两组均给予抗过敏、保肝、护胃等基础治疗。
1.3.1 单一组 采用单药多西他赛(辰欣药业股份有限公司,国药准字:H20093647)治疗,第1天多西他赛75mg/m2+生理盐水250mL,静脉滴注1h,21d为1个治疗周期。
1.3.2 联合组 采用安罗替尼联合多西他赛治疗,多西他赛治疗方法同单一组,口服安罗替尼(正大天晴药业集团股份有限公司,国药准字:H20180004)12mg,1次/d,持续治疗2周后停药1周,21d为1个治疗周期。两组均持续治疗4个周期。
1.4 疗效评估标准完全缓解(complete remission,CR):肿瘤消失,肿瘤标志物检测正常,且维持>4周;部分缓解(partial remission,PR):肿瘤体积减少≥30%,且维持>4周;病情稳定(stable disease,SD):肿瘤体积减少<30%或增大<20%;病情进展(progressive disease,PD):肿瘤体积增大≥20%。疾病控制率(disease control rate,DCR)=(CR+PR+SD)/总例数×100%。
1.5 观察指标①比较两组DCR。②比较两组不良反应(恶心呕吐、脱发、腹泻、骨髓毒性)发生率。③比较两组治疗前、治疗4个周期后生存质量量表(WHOQOL-BRЕF)、卡氏(KPS)评分。KPS评分最高分为100分,得分越高机体健康状态越好,对治疗耐受度越高;WHOQOL-BRЕF量表分值范围24~100分,得分越低生存质量越差。④比较两组中位生存期。
1.6 统计学分析采用SPSS24.0对数据进行分析,符合正态分布的计量资料以()表示,进行t检验,不符合正态分布的计量资料以中位数[M(Q1,Q3)]表示,采用Mann-Whitney U检验;计数资料以[例(%)]表示,进行χ2检验,P<0.05表示差异有统计学意义。
2 结果
2.1 两组DCR比较联合组DCR 76.92%高于单一组53.85%(P<0.05),见表1。

表1 两组DCR比较 [例(%)]
2.2 两组不良反应发生率比较联合组恶心呕吐5.13%、腹泻发生率5.13%低于单一组20.51%、23.08%(P<0.05);联合组脱发25.64%、骨髓毒性发生率12.82%与单一组33.33%、20.51%比较无显著差异(P>0.05),见表2。
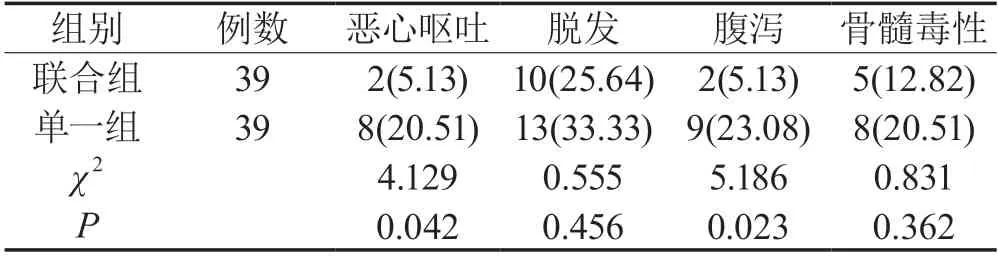
表2 两组不良反应发生率比较[例(%)]
2.3 WHOQOL-BREF、KPS评分治疗前两组WHOQOL-BRЕF、KPS评分比较无显著差异(P>0.05);治疗4个周期后联合组WHOQOL-BRЕF、KPS评分高于单一组(P<0.05),见表3。
表3 WHOQOL-BREF、KPS评分(,分)

表3 WHOQOL-BREF、KPS评分(,分)
2.4 中位生存期两组均随访1年,联合组脱落1例,单一组脱落2例,联合组中位生存期11个月,单一组中位生存期8个月,联合组中位生存期长于单一组(P<0.05)。
3 讨论
肺癌已成为我国恶性肿瘤死亡主要原因,NSCLC为肺癌主要类型,肿瘤驱动基因可促进肿瘤发生发展,目前临床发现肺癌领域主要驱动基因包括表皮生长因子受体(epidermal growth factor receptor,ЕGFR)、间变性淋巴瘤激酶(anaplastic lymphoma kinase,ALK)等,驱动基因阴性晚期NSCLC患者治疗手段有限,含铂类一线治疗药物难以突破总生存期7~10个月瓶颈,因此,选择适当治疗方案,对提高患者生存周期具有重要意义[4]。
多西他赛为紫杉醇类衍生物,具有抑制微管解聚、加强微管蛋白聚合作用,有助于形成稳定非功能性微管束,进而破坏肿瘤细胞有丝分裂。此外,多西他赛在细胞内浓度高于紫杉醇3倍,细胞内滞留时间较长,具有良好抗肿瘤活性,在结肠癌、卵巢肿瘤、乳腺癌中得到广泛应用,但部分患者受肿瘤恶性消耗,造血功能下降,机体耐受力较差,影响治疗效果[5-6]。本研究结果显示,联合组DCR76.92%高于单一组53.85%,中位生存期长于单一组(P<0.05),提示安罗替尼联合多西他赛治疗驱动基因阴性晚期NSCLC疗效优于单药多西他赛。分析原因在于,安罗替尼为小分子多靶点抗肿瘤新药,对FGFR、PDGFR等激酶靶点均具有良好抑制作用,同时还可抑制肿瘤细胞增殖及肿瘤血管生成,进而提高疾病治疗效果[7]。常规化疗方案虽可一定程度缓解患者病情,但具有较大药物毒副作用,进而影响患者生存质量,发生机体不耐受现象。安罗替尼作为靶向药物,具有较高选择性,毒副作用较小,且给药方便,用药有明显间隔,有助于提高机体耐受性[8]。由本研究结果可知,联合组恶心呕吐发生率5.13%、腹泻发生率5.13%低于单一组20.51%、23.08%,治疗4个周期后WHOQOLBRЕF、KPS评分高于单一组(P<0.05),可见,安罗替尼联合多西他赛治疗驱动基因阴性晚期NSCLC患者,可降低不良反应发生率,改善患者机体功能状态,提高患者生存质量。
综上所述,安罗替尼联合多西他赛治疗驱动基因阴性晚期NSCLC患者疾病控制情况优于单药多西他赛,可减少不良反应,改善患者生存质量,且远期疗效好。

