复配缓释凝胶吸附处理剂的制备及其除磷释氧性能
夏德春,郑 翔,吕树光,郑立新
(1.中国水利水电第十二工程局有限公司施工科学研究院,浙江 杭州 330103;2.华东理工大学资源与环境工程学院,上海 200237)
随着我国社会经济的快速发展以及城市化和工业化进程的急速推进,各种污染物的产生和排放量日益增加。特别是化工原料的过度使用、废物的任意排放以及有毒有害物质的不合理处置等,使得水生态环境问题层出不穷。其中,由于排水管网的渗漏和不完善的雨污水截流系统,大量的工业废水和生活污水以及农田径流中的植物营养物质向自然水体的排放更使得水体的富营养化程度日趋严重,破坏了原有自然水体的生态平衡,导致黑臭河道的发生[1]。
富营养化是一种氮、磷等营养物质含量过多所引起的水质污染现象。在自然条件下,随着河流夹带冲击物和水生生物残骸在河流、湖底的不断沉降淤积,水体会从贫营养型过渡为富营养型。这是一种极为缓慢的过程。人类的活动加速了这一过程的演变,导致水体中水生生物的结构组成发生巨大改变:藻类的大量繁殖将水中的溶解氧消耗殆尽,引起水中其他动植物及微生物大量死亡,水体发黑发臭,并产生大量的毒素,而这些毒素则通过食物链的富集最终会影响到人类的健康。由于污染源的复杂性及水体营养物质难以去除,富营养化的防治十分棘手且代价高昂。对于外源性营养物质一般通过制定排放标准、水质标准、实施截污工程等行政性管理手段来限制,而内源性营养物质的去除则由于输入到河流、湖泊中的营养物质在时间和空间上的分布非常复杂而变得十分困难[2-3]。针对上述含有大量内源有机物和氮磷营养物质的富营养化水体,开发低耗、高效的水处理技术成为现阶段水体环境治理研究的重点和难点。相较于氧化处理、生物处理等技术,吸附法具有高效、持久、经济等优势,因而被广泛应用于水处理中[4-6]。对于富营养化水体的治理,一方面需要控制并消除水体中含有的大量有机物及氮磷等内源污染物,另一方面亟需恢复水体生态系统的机制,提升水体的自净能力。因此,提高水体底部溶解氧水平,改善水体微生物生存环境,恢复水体自净能力成了治理并预防水体富营养化的一个关键因素[7-9]。
天然或工农业废弃物等吸附材料具有易得、量大、价廉等优势,对材料进行改性可以显著提高其除磷效果,但也存在着一些缺陷。耿雅妮等[10]利用改性铝污泥吸附除磷,较普通铝污泥取得了更好的应用效果,但热改性及其他改性方法也使得成本大幅上升。孙霄等[11]利用负载纳米铁花生壳吸附除磷,达到了良好的材料再生效果,但铁离子的大量释放导致水体逐渐酸化,不利于水生生物的生存。本文所选用材料为海藻酸钠(SA),是一种天然的多糖碳水高分子化合物,结构中含有大量的羧基,因此可以与水中的阳离子发生静电吸附,同时具备较强的螯合能力[12]。壳聚糖(chitosan)也是一种天然的高分子物质,分子结构中含有大量的氨基和羟基,容易形成阳离子聚电解质,能够吸附水中的有机质[13-15]。王凌匀等[16]通过质子化强化壳聚糖的除磷效果,结果表明在中性条件下壳聚糖的质子化程度不高,对总磷的去除也仅有40%左右。海藻酸钠与壳聚糖均具有生物可降解、相容、绿色无毒且环境友好等特点,因此对水体环境不会产生二次污染。孙少晨[17]研究了海藻酸钠-金属盐凝胶小球对水中无机磷的吸附去除效果,但在模拟废水中总磷的去除率仅接近50%。另外,徐慧等[18]利用市售过氧化钙除磷,在35℃下取得了50.25 mg/g的吸附容量,但市售过氧化钙一旦与水接触,会与水发生迅速的化学反应,并伴有过氧化氢和氧气的释放,在短时间内大量氧气的释放远远超过微生物的实际需求,且无法长期保持水体的溶解氧水平,进而导致在实际应用中过氧化钙利用率降低,且水体的pH值迅速升高至碱性,反而对水生生物造成一定的危害[19]。本文先利用海藻酸钠的凝胶性和壳聚糖的强吸附性能,制备了海藻酸钠包埋壳聚糖凝胶小球(SA-Chitosan);然后利用海藻酸钠的凝胶性和聚乙二醇4000的黏性及成膜性,制备了海藻酸钠/聚乙二醇4000复合包埋纳米过氧化钙缓释凝胶小球(PEG4000-SA@nCP);将二者进行复配,制备了一种可有效吸附水体中的磷并预防水体富营养化水华暴发的处理剂,为富营养化水体提供了一种长期有效的固体供氧、吸磷和有机物,并适于微生物生长环境的微胶粒水处理剂。
1 试验方法
1.1 原料和试剂
所用原料与试剂主要有:海藻酸钠((C6H7O6Na)n,化学纯,阿拉丁试剂有限公司)、壳聚糖(C6nH11nNO4n,99.0%,阿拉丁试剂有限公司)、六水合氯化铝(AlCl3·6H2O,分析纯,国药集团化学试剂有限公司)、无水氯化钙(CaCl2,分析纯,国药集团化学试剂有限公司)、聚乙二醇4000(PEG-4000,99.0%,阿拉丁试剂有限公司)、氨水(NH3·H2O,分析纯,上海凌峰化学试剂有限公司)、过氧化氢(H2O2,30%,优级纯,国药集团化学试剂有限公司)、磷酸氢二钠(NaHPO4·2H2O,分析纯,国药集团化学试剂有限公司),甲基橙(C14H14N3O3SNa,99.0%,阿拉丁试剂有限公司)。
1.2 测试与表征
实验仪器主要有:机械搅拌器(JB90-S,上海梅颖浦仪器仪表制造有限公司)、空气恒温摇床(HZQ-F160,上海晶坛仪器制造有限公司)、紫外分光光度计(DR-6000,哈希水质分析仪器有限公司)、电子分析天平(AL204,瑞士Metter-Toledo 集团)、超纯水机(CLASSIC UV MK2,英国ELGA公司)。
材料表征:使用X射线衍射仪(XRD)表征材料的晶格类型(RigakuUltima IV,日本),辐射光源为Cu的Kα射线,波长为0.154 nm, 管电压和管电流分别为40 kV和100 mA;使用扫描电子显微镜(SEM)和透射电子显微镜(TEM)表征材料的形貌特征(S-3400N,JEM-1400,日本),运行电压为80 kV;使用元素能谱仪(EDS)表征材料的元素含量及组成比例(Falion 60S,日本);使用傅里叶转换红外光谱仪(FTIR)表征材料的官能团(Thermo Nicolet Corp 6700,美国)。
1.3 试验步骤
1.3.1复配处理剂的合成
复配处理剂的制备包括SA-Chitosan凝胶小球的制备、PEG4000-SA@nCP缓释凝胶小球的制备以及两者的复配,具体步骤如下:
a. SA-Chitosan凝胶小球的制备方法。在室温20℃下,向50 mL超纯水中加入2 g海藻酸钠粉末,磁力搅拌2 h至均质透明;向上述均质海藻酸钠透明溶液中投加0.5 g壳聚糖粉末,磁力搅拌2 h至均质胶状,用5 mL注射针管以颗粒状滴入交联溶液(50 mmol/L CaCl2、AlCl3)中进行交联,交联时间为24 h,用超纯水充分洗涤,得到SA-Chitosan凝胶小球。
b. PEG4000-SA@nCP缓释凝胶小球的制备方法。准确称取3 g CaCl2放于30 mL超纯水中,准确称取2 g PEG-4000放于上述溶液中,磁力搅拌2 h至均质透明,加入15 mL浓度为1 mol/L的氨水溶液搅拌均匀,将混合溶液放置于磁力搅拌器上,以600 r/min恒定转速进行搅拌,用分液漏斗以0.125 mL/min的速率加入15 mL质量分数为30%的H2O2水溶液到上述溶液中;向50 mL超纯水中加入2 g海藻酸钠粉末,在室温20℃下,磁力搅拌2 h至均质透明,向上述均质海藻酸钠透明溶液中投加已制备好的PEG-4000包埋的nCaO2浆液,磁力搅拌24 h至均质胶状溶液,再用5 mL注射针管以颗粒状滴入交联溶液(50 mmol/L CaCl2)中进行交联,磁力搅拌0.5 h后,静置24 h,用超纯水充分洗涤,得到PEG4000-SA@nCP缓释凝胶小球。
c. 称取等质量的SA-Chitosan和PEG4000-SA@nCP凝胶小球,加入至50 mmol/L CaCl2溶液中,继续搅拌12 h,用超纯水充分洗涤,得到复配处理剂。
1.3.2目标污染物去除试验
为充分考察复配处理剂对水体中低、中和高浓度磷的去除效果,在250 mL棕色瓶中分别预配制不同初始浓度的含磷和甲基橙(MO)溶液。其中,设定预配制溶液中磷的初始质量浓度为1 mg/L、3 mg/L和6 mg/L时,实测值分别为0.81 mg/L、2.63 mg/L和5.42 mg/L(见第2.2.1节);磷初始质量浓度设置为16 mg/L时,实测值为15.59 mg/L(见2.2.2节);磷初始质量浓度设置为6 mg/L、10 mg/L和15 mg/L时,实测值分别为5.51 mg/L、10.12 mg/L和15.01 mg/L(见2.3.2节)。溶液中MO的初始质量浓度为32 mg/L。
试验时将反应器置于空气恒温摇床中,摇床转速为120 r/min,反应温度设定为20 ℃± 0.5℃,向反应器中投加预先设定剂量的复配处理剂后开始计时反应,并在规定的时间点取样分析。采用紫外分光光度计测定水中MO质量浓度(特征波长为464 nm)[20]。采用哈希内置USEPA PhosVer 3消解-抗坏血酸法测定磷质量浓度[21]。
实际河道水采集于上海华东理工大学校内青春河河道起始端。该河东通张家塘港、西接梅陇港,总长1.388 km,河口宽8~14 m,呈东西走向。采取水样测得pH为7.8,溶解氧(DO)质量浓度为1.2 mg/L,总磷质量浓度为2.1 mg/L,化学需氧量(COD)质量浓度为52 mg/L。
2 结果与讨论
2.1 材料表征
2.1.1SEM与TEM表征
图1(a)(b)为PEG4000-SA@nCP缓释凝胶小球的表面形貌。PEG-4000和SA对nCP颗粒进行包埋修饰后呈现出光滑的表面,其规则而光滑的表面有效减缓了材料中CP的快速释放,减缓了与水的快速反应,具备缓释功效,同时也减慢了处理剂中Ca2+及Al3+等的释放,能够达到更为高效持久的释氧和除磷效果。经表面修饰后,PEG4000-SA@nCP缓释凝胶小球具有相对均匀的粒径,平均粒径为50~200 nm。图1(c)(d)为SA-Chitosan凝胶小球的表面形貌,呈现出不规则的孔状表面,其多孔的表面增大了材料的比表面积,提高了吸附水中磷和有机物的活性位点。PEG4000-SA@nCP缓释凝胶小球的TEM图(图2)进一步表明制备的缓释小球呈纳米级球形颗粒,且外层被PEG-4000及SA有效包埋成膜。

图1 复配处理剂SEM
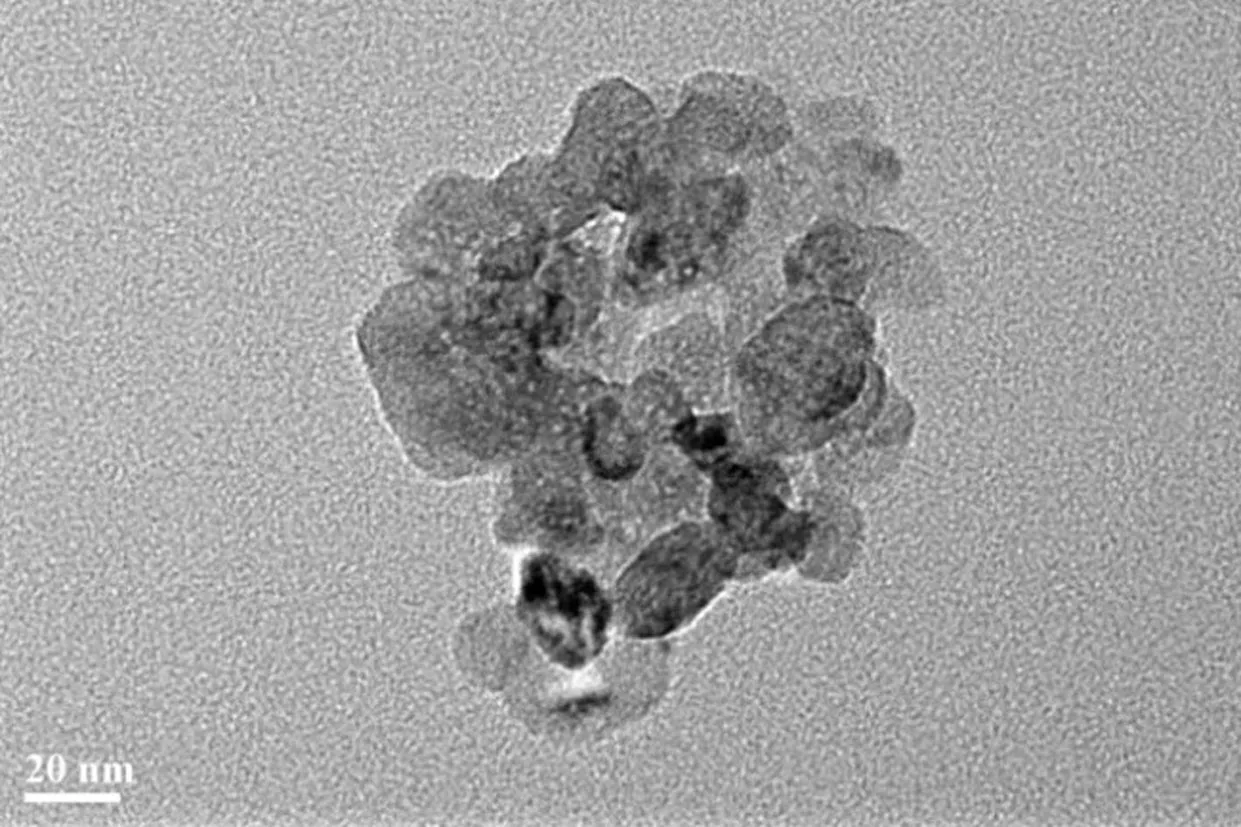
图2 PEG4000-SA@nCP缓释凝胶小球的TEM图
2.1.2XRD与EDS表征
如图3所示,在衍射角2θ值为30.72°、35.59°、47.30°和53.21°处的峰表明PEG4000-SA@nCP缓释凝胶小球中nCP的存在[22]。在2θ值为28.10°处的宽峰表明凝胶小球中壳聚糖的特征峰值由于受到SA的影响相较于原料壳聚糖而发生了偏移和宽化[23]。SA-Chitosan凝胶小球的EDS图表明材料中有多元素共存,其中Al和Ca元素的质量分别占4.15%和4.03%(图4(a))。图4(b)为PEG4000-SA@nCP缓释凝胶小球EDS图,其中23.87%的O元素和68.85%的Ca元素表明该小球中存在着大量的过氧化钙。

图3 复配处理剂的XRD表征

图4 SA-Chitosan凝胶小球和PEG4000-SA@nCP缓释凝胶小球的EDS表征
2.1.3FTIR表征
如图5所示,1 095 cm-1波数处的尖峰为壳聚糖中C—H官能团的振动吸收峰[24]。在波数为3 426 cm-1处的尖峰表明PEG4000-SA@nCP缓释凝胶小球及SA-Chitosan凝胶小球中的—OH官能团或者水分子的存在[25],在875 cm-1波数处的尖峰显示PEG4000-SA@nCP缓释凝胶小球的O—O键[26],在1 423 cm-1处的尖峰表明PEG4000-SA@nCP缓释凝胶小球的O—Ca—O键[27]。在2 863 cm-1至2 935 cm-1波数间的特征峰表明PEG4000-SA@nCP缓释凝胶小球中来源于PEG-4000和SA的长碳链结构基团[25]。上述特征结合2.1.1节中的SEM和TEM图,以及2.1.2节中XRD和EDS图谱的元素分析,表明nCP被PEG-4000和SA成功包埋。

图5 复配处理剂的FTIR表征

图6 复配处理剂对不同磷质量浓度的去除效果
2.2 污染物去除效果
2.2.1除磷试验
考察复配处理剂对水体中不同浓度磷的去除效果(图6)。当磷的初始质量浓度为0.81 mg/L时,向水中投加5.0 mg/L、10 mg/L和15 mg/L复配处理剂后,水中磷的质量浓度在1 h内快速下降至0.6 mg/L、0.52 mg/L和0.45 mg/L。随着处理剂投加剂量的增加,磷去除率从23.8%上升至44.4%(图6(a))。当磷的初始质量浓度为2.63 mg/L时,投加15 mg/L、25 mg/L和50 mg/L复配处理剂后,水中磷的质量浓度在1 h内快速下降至2.39 mg/L、1.23 mg/L和0.56 mg/L,最大去除率为78.7%(图6(b))。在吸附磷的初始阶段,复配处理剂表面存在着较多未饱和的活性吸附位点,能够将水中的磷快速吸附到其表面,但随着表面活性位点的逐渐饱和,吸附速率逐渐减慢,磷的去除速率也随之下降直至达到平衡。考察复配处理剂对高含磷水体中的磷的去除效果时(图6(c)),向含磷5.42 mg/L的水中分别投加了0.5 g/L、1.0 g/L和1.5 g/L复配处理剂,1 h后水体中磷的质量浓度分别下降至3.19 mg/L、1.54 mg/L和0.64 mg/L,相应地磷去除率分别为41.4%、71.6%和88.2%,表明复配处理剂投加量的增加能够持续提高高含磷水体中磷的去除率,这是因为用于吸附磷的复配处理剂表面的活性位点会随着处理剂投加量的增加而增加,水中处理剂的吸附容量也随之提高。上述结果表明复配处理剂对受低、中浓度磷污染的水体具有很好的处理效果,能够快速、高效地去除水中的磷;同时在处理剂投加量充足时,对高含磷水体中的磷也具有较好的去除效果。

图7 复配处理剂对水中磷及MO复合污染物的去除效果
2.2.2磷及MO复合污染去除效果
考察复配处理剂对水中磷及甲基橙(MO)复合污染物的去除效果(图7)。配制水中磷的初始质量浓度为15.59 mg/L,MO的初始质量浓度为32 mg/L。考虑到有机物MO对氧化剂的消耗,向水中投加5 g/L复配处理剂。在反应1 h后,水中磷质量浓度迅速降低至7.64 mg/L,且反应7 h后磷质量浓度持续降低到2.92 mg/L,随后磷去除速率减缓。水中MO的去除也分为两个阶段,在反应开始前7 h内,属于快速吸附阶段,水中大量的MO被去除,去除率达45.7%,而后转入慢速阶段,复配处理剂表面吸附位点逐渐饱和,磷及MO开始向复配处理剂的内部孔穴转移。经过45 h后,反应体系中磷和MO的最终质量浓度分别降低为0.85 mg/L和10.98 mg/L,去除率分别达到94.5%和65.7%。该结果与王凌匀等[16]和孙少晨[17]的研究中单独除磷的效果相比较,本文制备的复配处理剂不仅可以大大提高水中磷的去除率,同时也能去除磷和MO复合污染物。
2.2.3处理剂释氧效果
考察复配处理剂缓慢释氧的效果(图8),向超纯水(无氧)、含磷和MO水溶液(无氧)中投加4 g/L复配处理剂,释氧10 h后,水中溶解氧(DO)质量浓度分别上升至4.5和5.1 mg/L,表明该复配处理剂具有在水中缓慢释氧效果,显著提高了水中DO水平,且水质条件对其释氧效果无明显影响,这也为水泥交界处的好氧微生物提供了良好的好氧条件,进而可提高水体自净能力,有效避免厌氧环境的发生。

图8 复配处理剂释氧效果

图9 复配处理剂用量对实际河道水中除磷效果的影响
2.3 实际河道水体中污染物去除效果
2.3.1复配处理剂用量对除磷效果的影响
实际河道水体中复配处理剂用量对除磷效果的影响见图9,在不投加复配处理剂时,实际河道水中磷的质量浓度在2.1 mg/L左右。向水中分别投加1.0 g/L、1.5 g/L和2.0 g/L复配处理剂后,1 h内水中磷质量浓度大幅度下降,分别降至1.41 mg/L、1.02 mg/L和0.75 mg/L。随后磷的去除逐渐减缓,2.5 h后水中磷质量浓度最终分别降至1.25 mg/L、0.91 mg/L和0.68 mg/L。随着复配处理剂用量的增加,处理剂中可用的活性位点相应增加,水中除磷速率也随之加快。上述结果表明,该复配处理剂能够在较低用量下有效去除实际河道水中的磷。
2.3.2初始磷质量浓度对除磷效果的影响
在实际河道水中考察高质量浓度磷条件下复配处理剂除磷的效果(图10)。试验预先在实际河道水中投加磷以配制成5.51 mg/L、10.12 mg/L和15.01 mg/L的不同水体。向水中投加5 g/L复配处理剂反应1 h后,水中磷质量浓度分别降至2.32 mg/L、2.49 mg/L和2.61 mg/L。在复配处理剂用量一定时,高质量浓度水体中的磷能够更为快速有效地与处理剂活性位点接触并结合,因此在反应开始的前1 h内除磷效果更为高效。此外,由于向水中投加了足量的复配处理剂,因此处理剂提供的活性位点相较于磷处于充足状态,最终磷去除率均较高。这也表明在投加足量复配处理剂时,实际河道水中的高磷质量浓度对复配处理剂的除磷效果无明显影响,均可达到理想的效果。

图10 不同高磷质量浓度对复配处理剂处理实际河道水体中磷的效果
2.3.3实际水体中复配处理剂释氧效果
考察复配处理剂在实际水体中的释氧效果(图11)。向实际河道水体中投加4 g/L复配处理剂,实际河道水体中DO初始质量浓度为1.2 mg/L。在复配处理剂释氧10 h过程中,水中DO持续上升,最终DO水平达到4.8 mg/L,表明该复配处理剂在实际河道水中也具备良好的释氧效果,可为好氧微生物提供良好的生存环境。

图11 4 g/L复配处理剂在实际河道水体中的缓慢释氧效果
2.4 吸附机理探讨
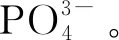
(1)
(2)
3 结 语
海藻酸钠包埋壳聚糖凝胶小球(SA-Chitosan)和海藻酸钠/聚乙二醇4000复合包埋纳米过氧化钙缓释凝胶小球(PEG4000-SA@nCP)为复配处理剂,具备高吸附和缓慢释氧等性能。试验结果表明该复配处理剂能够通过物理化学吸附作用高效去除水中的磷和有机物污染,对两者的复合污染也具有较高的去除效果。在实际河道复杂水体中对高质量浓度的磷也具有高效的除磷作用,处理剂的缓慢持久释氧功能可为河道水泥交界处的好氧微生物提供良好的好氧环境,提高水体自净能力,因此,该复配处理剂对防止河道黑臭及避免富营养化具有重要的实际应用价值,可为实际河道水体的治理提供一种新的处理剂选择。

