162例病毒性肠炎患儿肠外损伤及临床特征分析
鲁智英,王美芬,彭俊超,张建英,孙载鑫,杜丽江,罗云娇,甘 泉,刘春莉
(昆明市儿童医院感染性疾病科,云南 昆明 650028)
小儿腹泻是我国婴幼儿最常见的疾病之一,以6个月~2岁婴幼儿发病率最高,是造成儿童营养不良、生长发育障碍、甚至死亡的主要原因之一。引起小儿腹泻的病因复杂,病原种类繁多,有病毒、细菌、真菌和寄生虫感染等,其中最常见和最主要的病原是病毒。不论是在发达国家还是在发展中国家,轮状病毒感染是小儿急性腹泻病最常见的病因,其次为诺如病毒感染导致的急性胃肠炎[1-3]。临床上经常有一些病毒性肠炎引起的肠外器官功能损害,而轮状病毒和诺如病毒是引起小儿病毒性肠炎常见的病原。本研究对轮状病毒和诺如病毒感染导致的病毒性肠炎患儿的肝功能及心肌酶的变化及临床特征进行了研究,现报告如下。
1研究对象与方法
1.1研究对象
选取2019年1月至12月在昆明市儿童医院感染性疾病科就诊且病程小于14天水样腹泻并对粪便标本进行轮状病毒和诺如病毒检测阳性的住院患儿为研究对象,年龄为5个月~6岁,其中诺如病毒阳性79例(诺如病毒组),轮状病毒阳性83例(轮状病毒组);同时选取以水样腹泻且病毒学检测阴性的患儿81例为对照组。纳入标准:①符合儿童急性感染性腹泻的诊断标准[4];②均经过明确的患儿粪便病毒学检测阳性;③病程小于14天;④排外其他类型的感染性腹泻及其他基础疾病的患儿。本研究经昆明市儿童医院医学伦理委员会批准,患儿家属知情同意。
1.2研究方法
1.2.1粪便病毒学的检测
①轮状病毒的检测:取100mg粪便样本,采用A群轮状病毒检测试剂盒(胶体金法)检测卡;②诺如病毒的检测:吸取0.4mL粪便标本于1.5mL离心管中,以12 000r/min速度离心3min,吸取200μL标本上清液,添加5μL内标,进行核酸提取,采用诺如病毒核酸检测试剂盒。由我院专业人员完成粪便病毒学的检测。
1.2.2肝功能和心肌酶的测定
采集纳入研究对象患儿的空腹静脉血2mL,以3 500r/min速度离心10min后分离血清;采用奥林帕斯AU2700生化分析仪检测患儿谷草转氨酶(alanine transaminase,AST)、谷丙转氨酶(alanine transaminase,ALT)、肌酸激酶(creatine kinase CK)、肌酸激酶同工酶(creatine kinase isoenzyme,CK-MB)、乳酸脱氢酶(lactate dehydrogenase,LDH)、α-羟丁酸脱氢酶(α-hydroxybutyrate dehydrogenase,α-HBDH)。选择中生北控生物科技股份有限公司的ALT、AST试剂,选择北京世纪沃德生物科技有限公司的CK、CK-MB、LDH、α-HBDH试剂,由我院专业人员完成肝功能和心肌酶的检测。
1.3统计学方法

2 结果
2.1各组患儿肝功能ALT和AST的比较
三组患儿肝功能的Lg-ALT、Lg-AST差异均有统计学意义(均P<0.05)。进一步两两比较,诺如病毒组与轮状病毒组的Lg-ALT、Lg-AST差异均无统计学意义(均P>0.05);诺如病毒组与对照组的Lg-ALT、Lg-AST,轮状病毒组与对照组的Lg-ALT、Lg-AST差异均有统计学意义(均P<0.05),见表1。

表1 各组患儿肝功能ALT和AST的比较结果
2.2各组患儿心肌酶的比较
三组患儿心肌酶的Lg-CK-MB、Lg-CK、Lg-LDH、Lg-α-HBDH差异均有统计学意义(均P<0.05)。进一步两两比较,诺如病毒组与轮状病毒组的Lg-CK-MB、Lg-LDH、Lg-α-HBDH差异均有统计学意义(均P<0.05),Lg-CK差异无统计学意义(P>0.05);诺如病毒组与对照组的Lg-CK-MB、Lg-CK、Lg-LDH、Lg-α-HBDH差异均有统计学意义(均P<0.05);轮状病毒组与对照组的Lg-α-HBDH、Lg-CK差异均有统计学意义(均P<0.05),Lg-LDH、Lg-α-HBDH差异均无统计学意义(均P>0.05),见表2。

表2 各组患儿心肌酶的比较结果
2.3各组患儿临床症状的比较
三组患儿的发热、呕吐、脱水、抽搐发生率差异均有统计学意义(均P<0.05)。进一步两两比较,诺如病毒组与轮状病毒组的发热、呕吐、抽搐发生率差异均有统计学意义(均P<0.05),脱水发生率差异无统计学意义(P>0.05);诺如病毒组与对照组的呕吐、脱水、抽搐发生率差异均有统计学意义(均P<0.05),发热发生率差异无统计学意义(P>0.05);轮状病毒组与对照组的呕吐、脱水发生率差异均有统计学意义(均P<0.05),发热、抽搐发生率差异均无统计学意义(均P>0.05),见表3。
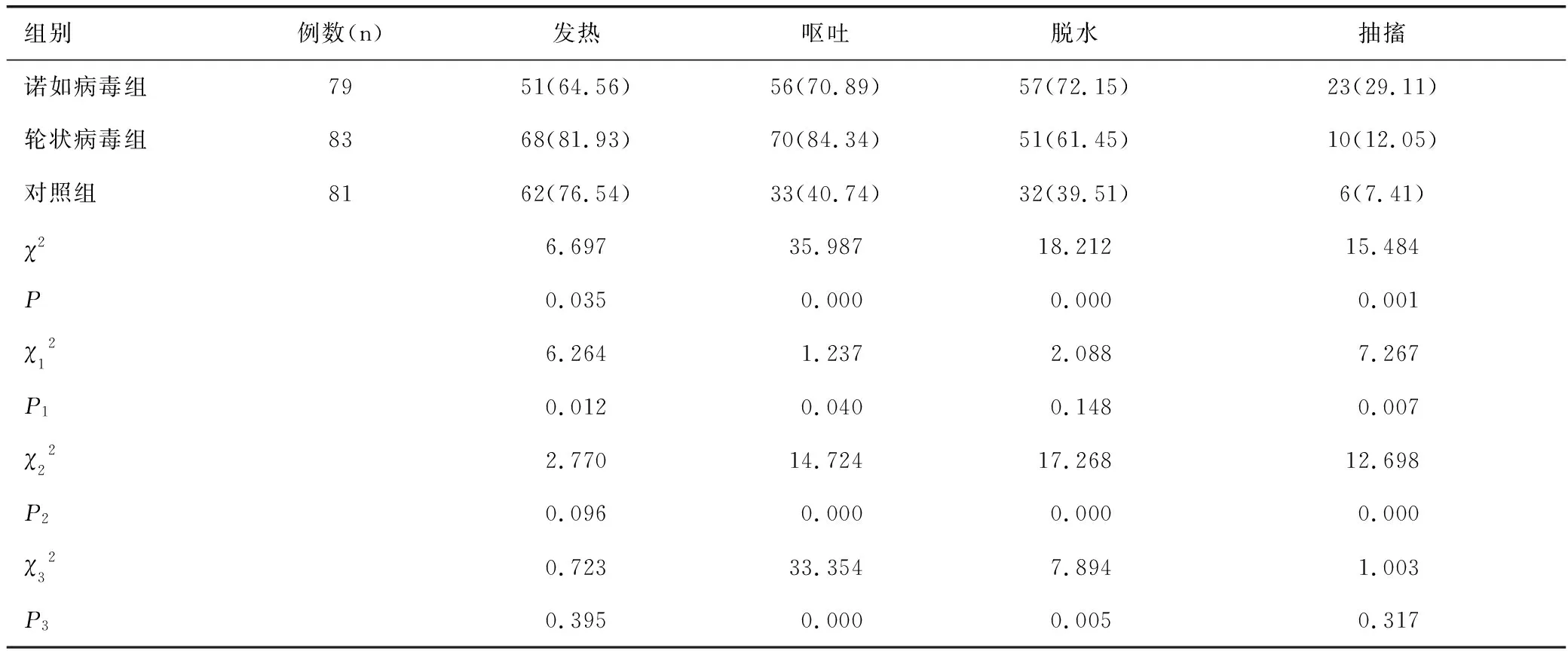
表3 各组患儿临床特征的比较结果[n(%)]
2.4两病毒组患儿年龄分布的比较
将162例患儿按年龄分为<1岁、1~岁、2~岁、≥3岁4个阶段;在<1岁阶段,诺如病毒组感染发生率明显高于轮状病毒组,在2~岁阶段,轮状病毒组感染发生率则明显高于诺如病毒组,差异均有统计学意义(均P<0.05);在1~岁和≥3岁阶段,诺如病毒组感染发生率与轮状病毒组差异均无统计学意义(均P>0.05),见表4。

表4 两病毒组患儿年龄分布的比较结果[n(%)]
3讨论
小儿腹泻病是我国儿童中常见疾病,由多病因所致,5岁以下儿童腹泻的主要病因是各种病原体的感染,其中最主要的是病毒感染[5]。诺如病毒、轮状病毒、肠道腺病毒、札如病毒和星状病毒等是病毒性腹泻的主要病原,其中最主要的是轮状病毒和诺如病毒。毕文俊等[6]对在上海市儿童医院内科门诊就诊并进行监测的1 041例腹泻病患儿进行病毒病原监测,病毒总检出率为26.0%,其中诺如病毒总检出率最高(11.0%),其次是轮状病毒(6.7%),其中1.83%为诺如病毒和轮状病毒混合感染,肠道腺病毒、札如病毒和星状病毒的总检出率分别为3.7%、3.7%和2.9%。商晓春等[7]对杭州地区≤5岁的婴幼儿病毒性腹泻进行研究,发现仍然以诺如病毒(23.41%)和轮状病毒(19.11%)为主。本研究对轮状病毒和诺如病毒感染引起的两种病毒性肠炎患儿的肝功能、心肌酶及临床特征进行了研究,发现轮状病毒感染的患儿发热比例更高,对心肌的损伤更严重;而诺如病毒感染的患儿抽搐发生率高于轮状病毒;<1岁的患儿更容易发生诺如病毒感染。
3.1诺如病毒的结构及其临床特征
诺如病毒是一个直径约28~35nm、单股正链RNA、基因组为7.4~7.7kb的病毒,包含3个阅读框(open reading frames,ORF)。ORF1在翻译后被切割成7种非结构成熟蛋白(NS1~NS7)作为病毒复制,ORF2和ORF3分别编码主要结构蛋白VP1和次要结构蛋白VP2,共同决定着病毒的结构[8]。病毒衣壳VP1是由壳结构域(S)和突出结构域(P)组成,具有90个二聚体。P结构域包括P1和P2子区域,P2子结构域含有中和抗体的结合位点,与组织血型组抗原(histoblood group antigen,HBGA)结合后大量附着在胃肠道黏膜上皮表面,促进了病毒浸润,推动了诺如病毒感染。目前诺如病毒被分为7个基因组(G),其中GⅠ、GⅡ和GⅣ可引起人类诺如病毒肠炎爆发[9-11]。粪-口传播是其主要传染途径,与感染者接触或通过接触受污染的食物和水或呕吐物产生的气溶胶都有可能发生传染。感染后潜伏期为12~48h,其临床表现是腹泻、呕吐、恶心和腹痛,以及低热、头痛、发冷、肌肉酸痛和疲劳。大部分患者在发病1或3天后自行好转[12-13]。诺如病毒感染后,肠道绒毛变钝,十二指肠管腔表面凋亡上皮细胞数量略有增加,上皮内淋巴细胞数量增加更多。诺如病毒感染可导致上皮屏障功能障碍,具有细胞毒性的上皮内淋巴细胞和凋亡上皮细胞数量增加,蛋白质紧密连接度下降。离子和水通过漏泵机制,从上皮下毛细血管扩散到肠腔,导致腹泻[14]。诺如病毒性肠炎可引起横纹肌溶解综合征,并在感染儿童的血清和脑炎患者的脑脊液中检测到诺如病毒RNA,表明诺如病毒发生肠外器官损伤的途径是通过病毒血症浸润到各个脏器,包括:肝脏、心肌及骨骼肌等,进一步引起肠外器官功能的损伤[15-16]。有研究显示,诺如病毒触发了神经系统抗原的免疫分子模拟,引起免疫失调或病毒直接触发神经系统而导致小儿抽搐[17-18]。
3.2轮状病毒的结构及其临床特征
轮状病毒是呼肠孤病毒科的一种未开发病毒,直径为70~100nm,基因组约为18.5kb,由11段双链RNA(dsRNA)组成。轮状病毒基因组编码6个结构蛋白(VP1~VP4,VP6和VP7)和6个非结构蛋白(NSP1~NSP6)。轮状病毒分为8个组(A~H),在人类和动物中都发现了轮状病毒A、B和C[19-21]。粪-口传播是其主要传播途径。潜伏期为2~3天,其临床表现有发热、少尿、口干、站起时头晕、腹痛,病初呕吐2~3天,后水样便腹泻3~8天。考虑其腹泻机制:①病毒感染胃肠道内膜,肠细胞空泡化和丢失,隐窝增生和绒毛变钝,导致肠道吸收不良。②轮状病毒非结构蛋白NSP4激活,诱导Ca2+依赖的Cl-分泌,抑制钠葡萄糖共转运载体(SGLT1-sodium glucose cotransporter,SGLT1),调节Na/K泵,改变细胞骨架紧密连接结构。肠道上皮细胞调节失调、消化酶降低、葡萄糖吸收不良、激活囊性纤维化非电导调节剂(cystic fibrosis transmembrane conductance regulator,CFTR)的Cl-分泌可能是腹泻的原因。③肠神经系统参与轮状病毒分泌性腹泻,引起肠动力增加。④病毒病原体影响的另一因素是轮状病毒感染肠嗜铬细胞(enterochromaffin cell capacity,EC)的能力。因此,血清素(5-羟色胺)从EC中释放出来并通过肠神经系统起作用,引起大脑结构迷走神经传入神经激活,发生恶心和呕吐。轮状病毒可存在于血清中,提示病毒血症可引起肠道内感染和肠外感染。小儿肝脏、心脏、肾脏等各脏器发育不成熟,肠道黏膜屏障功能差,分泌性IgA的缺乏可导致轮状病毒透过肠道屏障进入淋巴和血液循环,引起多器官损伤;轮状病毒可通过RNA逆转录酶(RT)定位到肠外组织(如心脏、肝脏和中枢神经系统),造成脏器多组织的损伤[22-23]。
3.3诺如病毒与轮状病毒性肠炎的特征分析
轮状病毒是导致婴幼儿发生腹泻的主要病原体。本研究显示,轮状病毒组的Lg-CK-MB高于诺如病毒组,而Lg-LDH、Lg-α-HBDH则相反。实验检查实际上是用α-HBDH代替乳酸或丙酮酸做底物测LDH总活性,因此检测α-HBDH与检测LDH及其同工酶的意义相似。LDH与α-HBDH并非心肌组织所特有,故通过LDH、α-HBDH单独判断心肌损伤的临床意义不大;而CK-MB主要分布在心肌内,可以作为心肌损伤的特异指标,提示轮状病毒更易引起心肌损伤[24]。本研究显示,诺如病毒组的Lg-ALT、Lg-AST及心肌酶谱中的Lg-CK与轮状病毒组比较均无明显差异,但均明显高于对照组,提示诺如病毒和轮状病毒易引起ALT、AST、CK升高,对肠外组织肝脏、心脏都有损伤,因此临床中应重视监测肝功能及心肌酶指标。本研究显示,诺如病毒组患儿抽搐发生率高于轮状病毒组,轮状病毒组发热发生率高于诺如病毒组,两者的临床表现有差异,提示轮状病毒相对诺如病毒致病力更强,而诺如病毒更易侵袭患儿神经系统而引起抽搐。本研究显示,在<1岁的患儿中,诺如病毒组感染发生率明显高于轮状病毒组,可能与婴儿期接种口服轮状病毒减毒活疫苗有关。接种该疫苗是预防轮状病毒胃肠炎的有效方法之一,可使婴儿轮状病毒发病率降低[25]。目前诺如病毒疫苗仍在研发中,目前未见上市。可能诺如病毒变异性特强,导致其发病率在婴儿期明显增高。本研究显示,在1~岁和≥3岁的患儿中,诺如病毒组感染发生率与轮状病毒组比较均无明显差异,但在2~岁患儿中,轮状病毒组感染发生率明显高于诺如病毒组,考虑轮状病毒致病力强,故在年长儿中更易感染。
综上所述,轮状病毒相对诺如病毒更易引起小儿心肌损伤,在诺如病毒和轮状病毒感染的病毒性肠炎患儿中,应重视肝功能和心肌酶的监测,进一步评估病情的进展。对临床出现发热、抽搐的水样腹泻患儿,应重视对诺如病毒及轮状病毒的检测。在口服轮状病毒疫苗接种普及后,诺如病毒感染更为明显,目前暂无有效疫苗及预防措施,其危害性不亚于轮状病毒,应引起临床医生的关注和重视。

