LED-254 nm紫外线对大鼠皮肤伤口愈合及血管生成的影响
张 钊,林希圣,高月明,王兴林
1 解放军医学院,北京 100853;2 解放军总医院第一医学中心 康复医学科,北京 100853;3 解放军总医院第二医学中心 康复医学科,北京 100853
皮肤伤口修复是一个由多种细胞、细胞因子、生长因子参与的复杂病理生理过程。当前,创面治疗技术研究热点包括细胞因子相关的基因工程技术、组织工程技术、干细胞技术等[1]。这些方法虽然在临床上取得了良好疗效,但其使用技术复杂,治疗成本较高,存在治疗短板。短波紫外线(ultraviolet C,UVC)照射可促进皮肤愈合。随着光生物学技术的发展,LED等冷光源在医用方面逐渐显示出其优势。LED-UVC的使用寿命是普通的荧光紫外线灯的3倍,不含有毒物质,较传统汞灯光源光谱范围更窄,光子能量更高,方向性好,输出稳定,便于量效关系评价[2]。当前基于冷光源的新型光学治疗设备不断产出,适应证也得到显著扩大。然而对于这种冷光源促进皮肤愈合及相关机制的研究较少。因此,本研究观察LED冷光源(峰值波长为254 nm)照射对SD大鼠背部皮肤创面愈合的影响,并对其影响皮肤创面愈合的机制进行初步探讨。
材料与方法
1 实验动物 32只SD雌性清洁级大鼠,体质量(200±20) g (解放军医学院实验动物中心提供)。饲养条件:每天光照12 h,相对湿度40%~60%,温度(22±3)℃。每只大鼠单独饲养,自由摄食。本实验经解放军总医院实验动物伦理委员会审批通过。
2 实验设备及材料 254 nm-LED灯由苏州生物医学工程技术研究所杨西斌研究员提供(专利号:ZL 2011 1 0387282.1),波长峰值为250~260 nm,使用电流300 mA,室温条件下(20℃ ~ 30℃) >90%波长为250~260 nm,输出功率为1.6 μW/cm2。血管内皮细胞标记CD31抗体(ab182981,ABCAM,美国);血管内皮生长因子(vascular endothelial growth factor,VEGF) ELISA试剂盒(ab100786,ABCAM,美国)。
3 造模与分组 32只大鼠术前1 d背部肩胛区备皮。手术当天,使用3%戊巴比妥钠3.5 mg/100 mL腹腔注射麻醉,75%乙醇消毒,使用皮肤活检钻孔器于大鼠肩胛区脊柱两侧分别做直径为8 mm的皮肤全层创面,根据Dunn等[3]描述的方法,使用自制硅胶夹板固定创面,防止大鼠皮肤创面回缩。建模后,每只大鼠单独饲养,自由摄食水。大鼠背部左侧创面作为对照组(Control),右侧创面作为实验组(Treated)。实验组于造模后即刻使用短波紫外LED灯(波长254 nm,功率220 μW/cm2)垂直照射大鼠背部皮肤1次(40 s),光源距创面5 mm,照射整个创面及创缘外3 mm皮肤,照射剂量为每创面33 mJ/cm2。对照组不做干预。
4 创面愈合率计算 造模当日计为0 d,在1 d、4 d、7 d、14 d分别取8只大鼠,观察大鼠背部伤口创面愈合情况,采集创面图片,用Image J软件计算创面面积,每张图片计算5次,并取平均值,并计算创面愈合率。创面愈合率(R)=(原始创面面积-未愈合创面面积)/原始创面面积×100%。
5 HE染色观察组织学变化 建模后,在1 d、4 d、7 d、14 d分别取8只大鼠,以创面中心为圆心,取直径15 mm的圆形皮肤样本,并将样本沿中线分为两份,一份用4%多聚甲醛固定,经脱水后石蜡包埋;另一份组织匀浆提取蛋白后,-80℃冻存待用。石蜡包埋的组织做厚度为4 μm的垂直创面的组织学切片,切片脱蜡至水后,经苏木精染色,盐酸乙醇分化,反蓝,伊红染色后,脱水封片,显微镜下对比观察大鼠皮肤创面组织学变化。
6 免疫组织化学染色观察血管再生情况 石蜡包埋的组织做厚度为4 μm的切片,切片脱蜡至水后,采用热修复法修复抗原,10%驴血清封闭抗原后,加一抗CD31(稀释比1∶2 000),4℃孵育过夜,加二抗,DAB显色,苏木素复染后脱水封片,光学显微镜下观察CD31(+)细胞生长情况,在同一标本中随机选取创面边缘及中心的5个视野,使用Image J软件进行平均光密度(optical density,OD)值分析。
7 酶联免疫吸附试验(ELISA)检测肉芽组织VEGF含量 取冻存对照组和实验组等量皮肤肉芽组织制备匀浆,离心机4℃,12 000 r/min离心5 min,收集上清。采用双抗体夹心ELISA法(Sandwich ELISA)对大鼠创面局部VEGF的表达进行定量分析。
8 统计学方法 采用SPSS21.0统计软件进行统计分析,计量资料以表示,组间比较采用配对t检验,P<0.05为差异有统计学意义。
结 果
1 皮肤创面愈合情况 建模后第1天伤口表面覆盖一层干燥的渗出层,实验组创面较对照组更为干燥,两组伤口均未见明显收缩。建模后第4天两组创面有痂形成,创面开始收缩,创面边缘皮肤发红,实验组创面表层结痂较厚,并有部分创面结痂边缘开始脱落。建模后第7天,两组创面愈合加快,出现肉眼可见的愈合,且实验组伤口愈合快于对照组。建模后14 d实验组皮肤创面均已愈合,痂脱落后可见小块粉红色裸露皮肤瘢痕。对照组部分皮肤创面仍可见小块痂未脱落。实验期间,所有大鼠创面均未见明显感染。见图1。
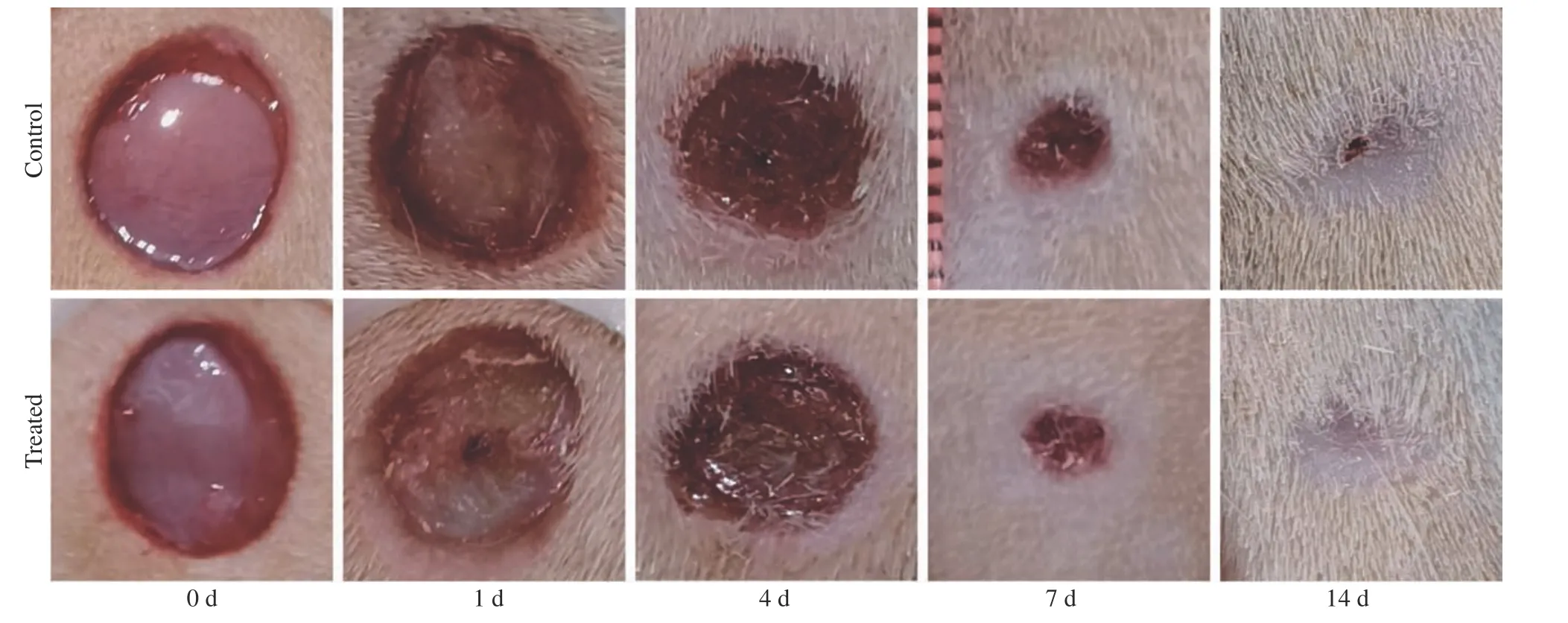
图1 大鼠皮肤创面愈合情况Fig.1 Appearance of wounds
2 皮肤创面愈合率 对照组和实验组在建模后第1天和第4天愈合率无明显差异。建模后第7天实验组创面愈合率为85.58% ± 5.37%,高于对照组的80.02% ± 7.38%,差异有统计学意义(P<0.01)。建模后第14天,实验组创面均已愈合,对照组虽然仍有部分创面未愈合,但由于创面过小,两组间愈合率无统计学差异。见表1。
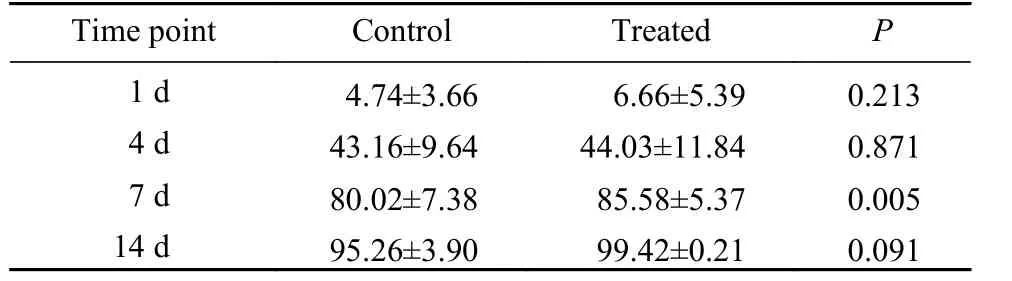
表1 两组不同时间点创面愈合率变化比较(%, n=8)Tab.1 Wound healing rates in two groups at different time points (%, n=8)
3 组织学观察 HE染色显示,建模后第1天对照组和实验组创面均可见大量的血管和炎细胞浸润。建模后第4天,实验组皮肤创面可见大量新生毛细血管,管腔较厚。肉芽组织增生明显,成纤维细胞数量多,可见较多红色的胶原纤维。对照组皮肤创面新生毛细血管增生,肉芽组织增生层较薄,成纤维细胞数量较少。建模后第7天,对照组创面仍可见大量血管,细胞外基质较少。实验组也可见大量血管,但管壁较对照组更成熟,细胞外基质较对照组多,可见成纤维细胞。建模后第14天,两组创面均已经被覆盖,皮下组织中仍可见毛细血管,成纤维细胞增多。见图2。
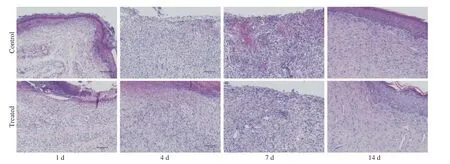
图2 两组不同时间点皮肤创面病理学观察(HE×100)Fig.2 Pathological changes of skin wounds in two groups at different time points (HE×100)
4 免疫组化CD31染色比较及平均光密度分析 免疫组织化学染色显示,建模后第7天对照组和实验组肉芽组织中均可见大量CD31(+)细胞,血管大量增生(图3A、图3C)。至建模后第14天,对照组CD31(+)细胞减少,实验组细胞仍可见较多CD31(+)细胞(图3B、图3D)。测量平均光密度显示,建模后第7天两组OD值无统计学差异;建模后第14天,实验组CD31(+)表达明显高于对照组(表2)。

图3 建模后7 d (A、C)、14 d (B、D)肉芽组织CD31表达情况 (免疫组化染色×100)Fig.3 New blood vessels in granulation tissue of control and treated group on day 7 (A, C) and 14 (B, D) after operation(IHC×100)
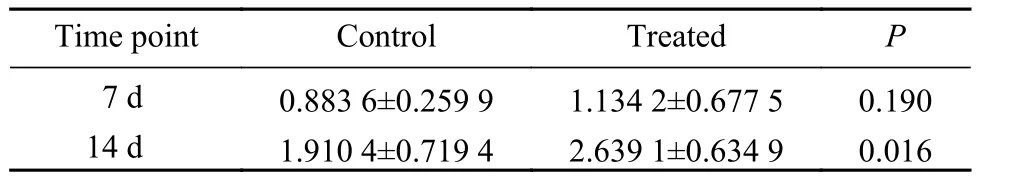
表2 建模后7 d、14 d免疫组织化学染色CD31(+)平均光密度值比较(n=8)Tab.2 Comparison of mean optical densities at 7 and 14 days after operation (n=8)
5 VEGF含量测定 ELISA实验分析,建模后1 d、4 d、7 d、14 d实验组VEGF的表达均明显高于对照组。见表3。

表3 两组不同时间点VEGF含量比较(pg/mL, n=8)Tab.3 VEGF levels in two groups at different time points(pg/mL, n=8)
讨 论
本实验结果显示,使用LED光源发射的254 nm UVC一次照射创面33 mJ/cm2可以促进大鼠皮肤创面的愈合,这一现象可能与照射后创面处VEGF含量增加,刺激了创面肉芽组织中血管生长有关。
UVC照射治疗是一种十分有效、方便且廉价的皮肤伤口治疗方法,对压疮、慢性伤口、感染伤口、糖尿病溃疡等均有良好的疗效[4-6]。目前临床上常用的紫外线治疗仪是低压汞灯紫外线治疗仪。这种低压汞灯存在着功率低、带宽大、光谱成分复杂、光输出不稳等问题,难以科学评价其量效关系,临床操作以经验为主,无法统一治疗标准。随着技术的发展,LED光源的出现使得光谱成分可控、波段专一的光源成为现实。且LED光源寿命长、光功率密度高、光量子能量高、输出功率可控,可以精确评价其输出功率,计算量效关系。因此,LED光源作为一种新型冷光源,在生物医学领域有着广阔的应用前景[7]。
不同波长的紫外线产生的光化学效应不同。一般认为紫外线治疗创面的有效波段为254 nm附近的短波紫外线。由于UVC可以被大气层完全吸收,自然界中并不存在UVC,因此目前对紫外线的研究主要集中在长波紫外线和中波紫外线[8]。已有的文献认为UVC促进伤口愈合 可能与下调炎症反应,提高血清生长因子水平等因素有关[9]。根据已有报道,低压汞灯UVC治疗大鼠皮肤新鲜创面采用15 mJ/cm2照射,连续照射3 d,具有显著的促进愈合作用[10],但UVC治疗皮肤创面的最适剂量未见明确报道。低压汞灯是利用汞在热作用下蒸发成蒸汽状态产生光,光谱中主要为180~390 nm紫外线及部分400~450 nm蓝紫光,光谱成分复杂。实验前,我们对已有低压汞灯输出功率进行测量,结果显示除UVC有效治疗波段外,还包含大量的长波紫外线和中波紫外线。而与已有报道使用的光源不同,本研究采用的LED光源产生的短波紫外线主要为250~260 nm,有效波长占比高,便于新式LED-UVC技术量效关系评价。但本实验使用的紫外线辐射剂量与文献报道的剂量存在差异[10]。已有的动物研究中需要使用UVC照射连续照射3次,总照射剂量为45 mJ/cm2,临床研究中需要使用12 mJ/cm2连续照射12 d[11]。而本实验采用LED-254 nm UVC照射1次,照射剂量仅为33 mJ/cm2,是文献中动物实验治疗剂量的2/3,临床研究剂量的1/6,也可以达到促进皮肤伤口愈合的效果。从理论上讲,更少剂量和次数的紫外线暴露可减少紫外线照射导致的不良事件[12]。
皮肤创伤愈合可以分3个阶段:炎症反应、细胞增殖、组织重塑,这3个阶段互有重合,并不完全分离[13]。我们观察到经LED-254 nm UVC照射的伤口创面更为干燥,结痂更厚且脱痂时间更早。HE染色显示,LED照射组胶原合成更早,且增生的血管也更为成熟。这些现象提示LED照射组的皮肤伤口可能更早进入增殖和重塑阶段,为下一步实验提供了方向。
血管再生对修复有很大的意义,是皮肤创面愈合的关键环节[14]。新生的血管为伤口提供营养、免疫细胞和氧气等修复必须物质[15]。本研究使用免疫组织化学染色检测CD31(+)血管内皮细胞,发现在建模后第7天和第14天,创伤部位血管均大量增生,第14天LED组血管增生明显多于空白组。VEGF是血管生成强有力的刺激因子,可促进内皮细胞增殖、迁移和新血管形成,并能促进胶原沉积和创面再上皮化[16-17]。本研究结果也表明LED组创伤部位的VEGF含量要高于对照组。这一结果提示UVC照射促进愈合的作用可能与血管再生相关。但VEGF的来源、VEGF增加与紫外线照射的剂量关系等问题仍待进一步探讨。
综上所述,LED 254 nm UVC照射可以加速大鼠皮肤创面愈合,这种促进创面愈合的效果可能与创面局部血管再生能力增强有关。这种治疗方法使用方便,照射剂量小,UVC波长控制好,较临床上使用的低压汞灯有一定的优势,有可能替代低压汞灯成为临床上进行UVC光疗的新型光源。紫外线的光化学效应不仅与紫外线的波长有关,也与辐射强度有着密切关系,如临床上一般使用大剂量照射处理感染伤口,使用小剂量照射处理新鲜伤口[10]。然而本研究由于受到光源输出功率的限制,仅对一种辐射剂量进行了研究,仍不能认为本实验中采用的剂量是促进创面愈合的最佳剂量。因此,我们将继续探索紫外线治疗的量效关系,并深入挖掘UVC治疗皮肤伤口的机制,以期找到更为合理的UVC光疗方案。

