全外显子测序技术在3例胎儿肠管增宽产前诊断中的应用*
边欣怡,杨 肖,石鑫玮,柳宛璐,曾万江,乔福元,冯 玲,陈素华,邓东锐,吴媛媛
(华中科技大学同济医学院附属同济医院妇产科,武汉 430030)
胎儿消化系统畸形是最为常见的胎儿先天性畸形之一,约占所有胎儿畸形的7.35%[1],在产前通常以胎儿肠管增宽为主要的胎儿腹部超声异常表现。胎儿消化系统疾病与遗传因素相关,通常需进行产前诊断,排除染色体异常可能。传统的染色体核型分析作为产前诊断染色体异常的金标准,存在耗时长、依赖细胞培养技术、难以检测染色体微缺失、微重复等微小变异的不足。目前,基于第二代测序(next-generation sequencing,NGS)技术的检测方法,如全外显子测序(whole exome sequencing,WES)得到了广泛认可,为临床医生对遗传性疾病的诊断提供了重要依据。本研究通过利用WES技术分析胎儿肠管增宽的致病性突变,为其产前诊断及遗传咨询提供帮助。
1 临床资料
病例1,女,26岁,孕33周,胎动消失伴不规律下腹痛13h。孕期颈项透明层(nuchal translucency,NT)超声检查未见明显异常。孕期胎儿彩超提示胎儿肠管进行性增宽,肠管最大内径2.51cm。孕23周于我院行羊膜腔穿刺,胎儿染色体核型分析46,XN;CNV检测未检出染色体非整倍体或100Kb以上已知的、明确的致病基因拷贝数变异(copy number variation,CNVs)。入院后行B超发现宫内死胎。病例2,女,29岁,孕30+4周,B超发现胎儿肠管扩张入院。孕期NT检查、无创产前DNA检测(non-invasive prenatal testing,NIPT)均未见明显异常。孕30+3周胎儿彩超提示下腹肠管扩张伴回声增强、胎儿头部偏大、双肾集合系统分离、羊水过多,羊水指数27.8cm。病例3,女,31岁,孕32+4周,B超发现胎儿肠管广泛扩张入院。孕期NT检查未见明显异常。孕18周于外院行羊膜腔穿刺,胎儿染色体核型分析46,XN;CNV检测未检出染色体非整倍体或100kb以上已知的、明确的致病基因拷贝数变异。孕32+1周胎儿彩超提示胎儿小肠均匀弥漫性扩张,羊水多,羊水指数30.0cm。
2 结 果
病例1,因“孕33周,宫内死胎”引产,经遗传咨询,患者夫妻双方知情同意后,采集胎儿组织进行WES检测,检出阳性突变后采集夫妻双方外周血进行Sanger测序验证突变位点。WES检测结果显示:在GDNF(NM_001190468.1)基因编码区检出1个错义变异c.329G>A(即第110位精氨酸变为谷氨酰胺),为杂合子。该变异使氨基酸发生改变,可能影响蛋白的正常功能,且在人群中的发生率极低。GDNF基因突变可引起先天性巨结肠症3型(OMIM#:613711),该病为常染色体显性遗传,主要临床表现为先天性巨结肠、肠神经节缺乏、急性新生儿梗阻等。推测GDNF基因c.329G>A杂合变异为该病例的临床意义未明突变。对该位点进行Sanger测序验证,结果显示:先证者和其父亲在GDNF基因上检出c.329G>A杂合变异,其母亲未检出上述变异。既往报道先天性巨结肠症涉及多个基因并伴有低外显率[2],追问患者病史,患者自诉两年前孕35+3周经阴分娩一男婴,孕期行B超发现胎儿肠管扩张,新生儿出生后未排胎便、呕吐黄绿色分泌物,出生后1月夭折,未行相关基因检测。结合既往病史推测,先证者在GDNF基因上的c.329G>A杂合变异导致了肠管增宽发生,该变异遗传自其父亲(图1)。

图1 病例1基因图谱(箭头所示为GNDF基因突变位点)
病例2,因“孕30+4周,胎儿多发畸形”引产,经遗传咨询,患者夫妻双方知情同意后,采集脐带血进行胎儿染色体核型分析,采集胎儿组织进行CNV、WES检测,检出阳性突变后采集夫妻双方外周血进行Sanger测序验证突变位点。染色体核型分析结果显示:46,XN。CNV结果显示:seq[hg19]dup(15)(q26.1q26.3)chr15:g.92600000_102400000dup,包含15q26 overgrowth syndrome的全部,该综合征患者主要的临床表征为肾异常(约45%,包括马蹄肾、肾发育不全、肾积水、多囊肾及膀胱输尿管返流、右肾盂重复),身材高大,特殊面容(长脸、下巴突出、大鼻子),学习困难,语言和运动能力发育迟缓等,与本例病例表型不符合。WES结果显示:根据美国医学遗传学与基因组学学会(ACMG)指南[3]及ClinGen序列变异解释(Sequence Variant Interpretation,SVI)专家组对指南标准的应用建议[4-6],提示基因NOTCH2的c.1310A>C突变为1个疑似致病突变位点,为杂合突变,与常染色体显性遗传疾病Alagille syndrome 2(Alagille综合征2型)、Hajdu-Cheney syndrome(Hajdu-Cheney综合征)相关,主要临床表现为肠旋转不良、肾发育不良等。对该致病位点进行Sanger 测序验证,该变异在其父母样本中均未发现,为家系样本中经双亲验证的新发变异。该变异发生于EGF-like calcium-binding domain;EGF-like domain;EGF-type aspartate/asparagine hydroxylation site;Notch功能结构域,错义变异是造成相关疾病表型的常见机制,且良性错义变异比例低,疾病特征与本例病例表型部分相符,因此判断,该变异为新发的疑似致病突变(图2)。

图2 病例2基因图谱(箭头所示为NOTCH2基因突变位点)
病例3,因“孕32+4周,胎儿肠管广泛扩张”引产,经遗传咨询,患者夫妻双方知情同意后,采集胎儿组织进行WES检测,检出阳性突变后采集夫妻双方外周血进行Sanger测序验证突变位点。WES检测结果显示:根据ACMG指南[3]及SVI专家组对指南标准的应用建议[4-6],提示基因SLC26A3的c.1427del突变和c.269_270dup突变为致病突变位点,均为杂合突变。该变异可引起基因开放阅读框发生改变,导致蛋白功能改变,与常染色体隐性遗传疾病先天性失氯性腹泻1型(Diarrhea 1,secretory chloride,congenital)相关,主要临床表现为肠扩张、羊水过多、腹泻、低氯血症等。Sanger验证结果显示:受检者在基因SLC26A3上发生c.1427del杂合突变,父亲发生杂合突变,母亲未突变,突变来自父亲;受检者在基因SLC26A3上发生c.269_270dup杂合突变,母亲发生杂合突变,父亲未突变,突变来自母亲,符合复合杂合突变(图3)。
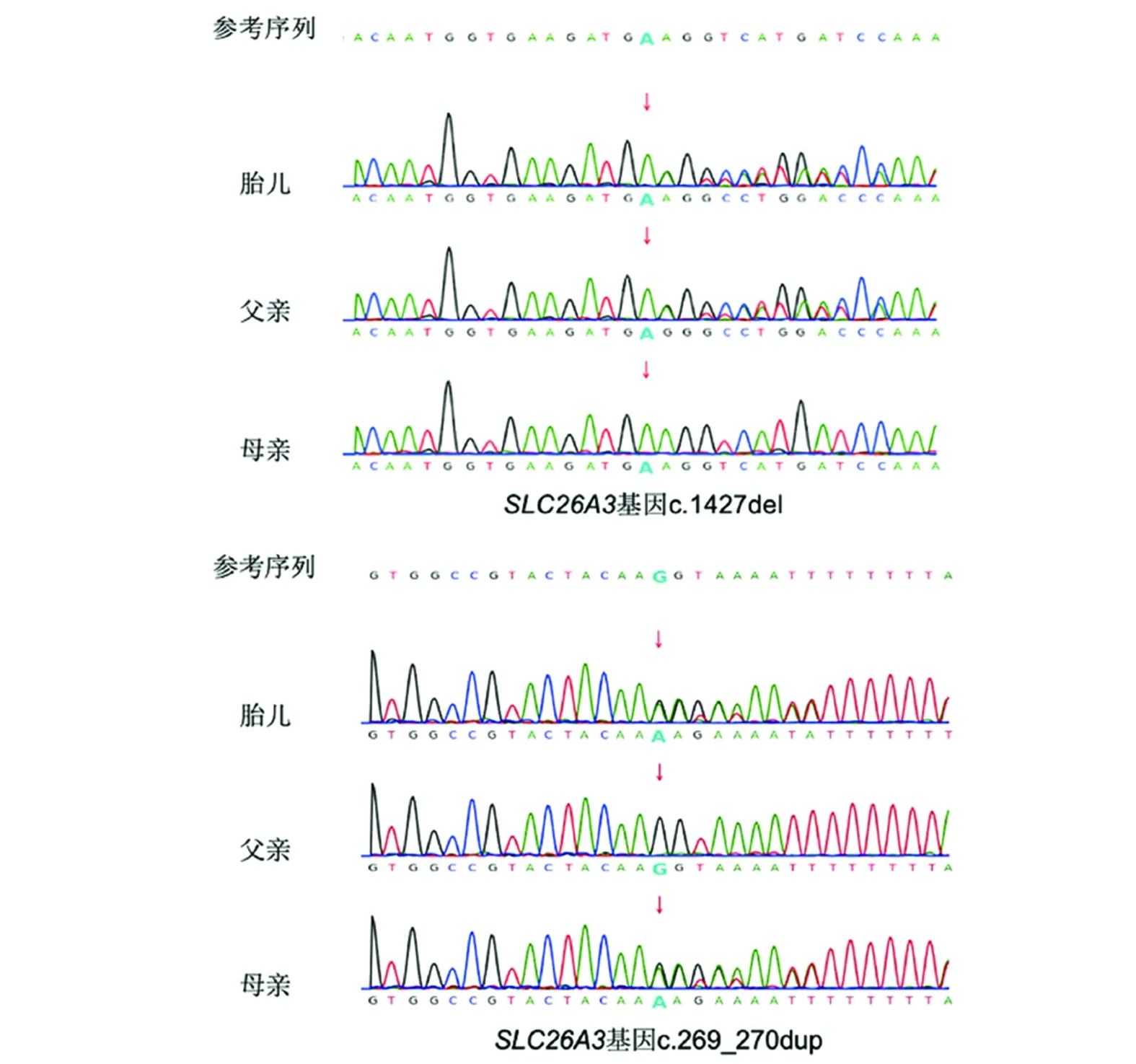
图3 病例3基因图谱(箭头所示为SLC26A3基因突变位点)
3 讨 论
导致人类遗传性疾病的病因复杂多样,主要包括染色体异常、单基因病、多基因病和线粒体病等。这些遗传性疾病可能导致患儿严重的智力障碍、生长发育异常、致残甚至死亡等不良结局且患儿通常预后不良。近年来,随着产前诊断和超声技术的不断进步,产前检查对于胎儿先天性畸形的检出率逐步升高,部分遗传性疾病可在孕期检查时发现。因此,尽早、准确地进行产前诊断,对于预测妊娠结局、及时终止妊娠生至关重要。
既往研究认为,胎儿肠管增宽可能与染色体异常有关,约50%的十二指肠增宽病例合并有染色体异常,其中合并21-三体综合征的病例约占十二指肠增宽病例的三分之一[7-9]。然而,空回肠增宽和结肠增宽与基因异常的相关性,目前尚不明确,可能与以往产前诊断技术,如染色体核型分析的分辨率较低,难以检测小于5~10Mb的染色体微缺失、微重复和单基因病、多基因病等有关。
过去几十年间,染色体核型分析一直是产前诊断染色体异常的金标准,然而其难以检测遗传物质的微小缺失、重复和变异,无法对单基因病和多基因病做出诊断,因此,第二代测序技术应运而生。第二代测序技术包括WES、全基因组测序(whole genome sequencing,WGS)、基因包(gene panel)测序等,其中WES的应用较为广泛。
外显子区是人类基因中具有重要功能的区域,约占人类整个基因组的3%。85%的人类遗传性疾病致病变异均发生在外显子区[10]。WES技术利用序列捕获技术,可选择性地捕获基因组中外显子区域的DNA序列,并对受检者基因组中功能基因编码序列的遗传变异进行检测,具有高效、覆盖率高、成本低等优点[11]。2009年,WES技术首次被应用于寻找单基因病的致病基因,并进行临床诊断[12]。此后,WES技术被逐渐应用于遗传性疾病的病因筛查及临床诊断。2016年的一项前瞻性研究显示,WES技术对于遗传性疾病的检测阳性率高达57.5%,显著高于传统方法13.75%的阳性率[13]。不同胎儿超声异常的产前WES阳性率也有不同,国外一项研究发现,胎儿淋巴水肿、骨骼系统发育异常、中枢神经系统异常和肾脏输尿管异常的WES阳性率明显高于胎儿先天性心脏病的阳性率[14]。
2020年1月ACMG发布的胎儿外显子组测序技术在产前诊断中的应用指南中建议,对于染色体核型分析和CMA检测结果正常的超声异常胎儿,可建议进行异常胎儿及父母的三人全外显子组检测(trio-WES)。本文中的3例胎儿肠管增宽孕妇均采集了羊水或脐静脉血对胎儿进行了染色体核型分析检测,结果均为正常;采集胎儿组织进一步进行CNV检测,病例2检测出胎儿15号染色体微重复,然而其疾病特征与本例病例不相符,其余2例CNV结果均为正常;对3例胎儿及父母双方进行trio-WES发现,3例胎儿均检测出导致肠管增宽的基因突变。因此,对于产前超声发现肠管增宽的胎儿,WES技术对于遗传变异的检出率可能高于CNV及传统的染色体核型分析技术。
综上所述,对于产前超声发现肠管增宽的胎儿,WES技术对于检测其遗传变异具有重要的诊断价值。应对孕妇及家属进行遗传咨询,并提供trio-WES技术进行基因诊断,降低遗传性疾病患儿的出生率。同时,若父母也携带有致病基因,应告知其再次妊娠时的疾病再发风险,并建议再次妊娠时对胎儿进行相关致病基因检测。

