新疆灰枣果核木脂素类化学成分研究
牟鹏云,麦合力帮古丽·尼牙孜,何秋映,万传星,周忠波,2*
(1塔里木大学生命科学与技术学院,新疆 阿拉尔 843300)
(2右江民族医学院药学院,广西 百色 533000)
木脂素是一类由苯丙素氧化聚合而成的天然酚类化合物[1-2],其作为药用植物中一类比较重要的活性成分,具有多样的结构和生物活性。木脂素类化合物的药理活性主要包括抗肿瘤、抗病毒、抗菌、保肝以及作用于心血管和中枢神经系统等[3]。
果核作为红枣加工产生的副产物,具有止渴生津、润肠通便的功效,可用于治疗走马疳、眼疾、内外腑疮等。前期研究表明,灰枣果核中含有酚类[4-6]、类黄酮[7]及皂苷[8]等化学成分。灰枣作为新疆重要的经济作物,产量大,果核利用率低,灰枣果核绝大多数以废弃物的形式丢弃或作为燃料,未能得到合理利用,造成资源的极大浪费。本文拟研究灰枣果核中木脂素类化学成分,为提高新疆灰枣果核利用率提供依据。
1 材料与仪器
1.1 试验材料及试剂
试验所用灰枣果核于2018年4月购于新疆生产建设兵团第一师十二团,经鉴定为鼠李科枣属植物灰枣(Ziziphus jujuba cv.Huizao)的果核。凭证标本(TLM-201803)存于新疆生产建设兵团塔里木盆地生物资源保护利用重点实验室天然产物研究室。将灰枣核洗净后自然风干备用。
柱层析硅胶(200~300目,青岛海洋化工厂),薄层层析硅胶板(青岛海洋化工有限公司),无水乙醇(天津市光复科技发展有限公司),乙酸乙酯(天津市光复科技发展有限公司),石油醚(天津市光复科技发展有限公司),甲醇(色谱纯,北京百灵威科技有限公司),乙腈(色谱纯,北京百灵威科技有限公司),其余试剂均为国产分析纯。
1.2 试验仪器
核磁共振谱仪(Bruker AV-500,德国Bruker公司),Agilent 1100-LC-MSD Trap/SL质谱仪(美国安捷伦公司),电子天平(CP224C,奥豪斯仪器(上海)有限公司),电热套(SZCL-A,博迅实业有限公司),电热恒温鼓风干燥箱(GZX-9420MBE,上海姚氏仪器设备厂),高效液相色谱仪(日本岛津公司),制备型高效液相色谱仪(日本岛津公司),Agilent HPLC色谱柱(4.6 mm×250 mm,5 μm,美国Agilent公司),旋转蒸发仪(N-1300V-WB,上海爱朗仪器有限公司)。
2 提取与分离
将1 kg去果肉洗净阴干的灰枣果核粉碎,用95%乙醇热回流提取3次(料液比1:10,m:v),每次2 h。将提取液合并浓缩得到的灰枣果核浸膏29 g。将浸膏用硅胶拌样,随后进行硅胶柱层析,依次用乙酸乙酯和95%乙醇进行洗脱,分别得到乙酸乙酯浸膏5.8 g、95%乙醇浸膏21.2 g。乙酸乙酯浸膏再次进行硅胶柱层析,依次用石油醚:乙酸乙酯为10:1、5:1、3:1、1:1、1:2(v:v)进行洗脱。经薄层色谱(TLC)检测后,石油醚:乙酸乙酯1:1组分合并得到3个组分(Fr.1~Fr.3),1:2组分合并得到4个组分(Fr.4~Fr.7)。组分Fr.2经制备型高效液相色谱(甲醇:水为30:70,流速:10 mL/min)等度洗脱得到4个化合物:化合物1(4.8 mg,tR=14.7 min)、化合物 2(4.4 mg,tR=18.0 min)、化合物 3(1.9 mg,tR=19.2 min)和化合物4(13.4 mg,tR=23.4 min)。组分Fr.7经制备型高效液相色谱(乙腈:水为25:75,流速:10 mL/min)等度洗脱得到2个化合物:化合物5(9.6 mg,tR=12.3 min)和化合物6(2.4 mg,tR=18.7 min)(图1)。
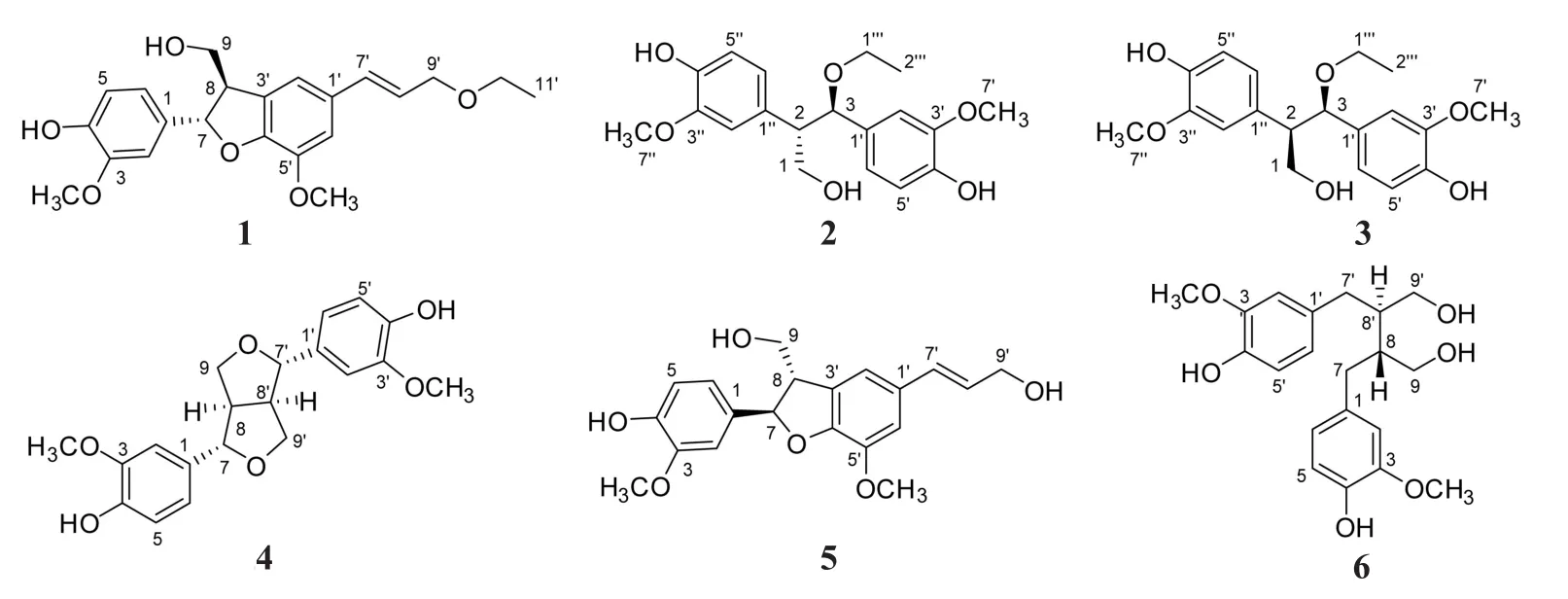
图1 化合物1~6结构图
3 结构鉴定
化合物1:淡黄色油状物,ESI-MS m/z 409[M+Na]+。1H NMR(500 MHz,CD3OD)δ:6.98(1H,s,H-2),6.95(2H,s,H-2′,6′),6.83(1H,d,J=8.5 Hz,H-6),6.77(1H,d,J=8.5 Hz,H-5),6.56(1H,d,J=16.0 Hz,H-7′),6.18(1H,dt,J=16.0,6.5 Hz,H-8′),5.53(1H,d,J=6.0 Hz,H-7),4.11(2H,dd,J=6.0 Hz,H-9′),3.88(3H,s,H-5′-OCH3),3.84(2H,m,H-9),3.82(3H,s,H-3-OCH3),3.55(2H,dd,J=14.0,7.0 Hz,H-8),3.49(1H,dd,J=12.0,6.0 Hz,H-10′),1.22(3H,t,J=7.0 Hz,H-11′);13C NMR(125 MHz,CD3OD) δ:149.6(C-4′),149.3(C-3),147.8(C-4),145.7(C-5′),134.7(C-1),134.2(C-7′),132.4(C-1′),130.5(C-3′),124.7(C-8′),119.9(C-6),116.8(C-2′),116.3(C-5),112.3(C-6′),110.7(C-2),89.5(C-7),72.6(C-9′),66.7(C-10′),65.0(C-9),57.0(C-5′-OCH3),56.5(C-3-OCH3),55.3(C-8),15.6(C-11′)。上述数据与文献报道一致[9],故鉴定为(+)-(7S,8R,7′E)-4-hydroxy-3,5′-dimethoxy-4′,7-epoxy-8,3′-neolign-7′-ene-9,9′-diol 9′-ethyl ether。
化合物2:无色油状物,ESI-MS m/z 349[M+H]+。1H NMR(500 MHz,CD3OD)δ:6.62(1H,d,J=8.0 Hz,H-5′′),6.61(1H,d,J=9.0 Hz,H-5′),6.56(1H,dd,J=8.0,1.5 Hz,H-6′),6.52(1H,d,J=1.5 Hz,H-2′),6.50(1H,dd,J=8.0,1.5 Hz,H-6′′),6.49(1H,d,J=1.5 Hz,H-2′′),4.40(1H,d,J=8.5 Hz,H-3),4.09(1H,dd,J=10.5,5.5 Hz,H-1),3.90(1H,dd,J=10.5,7.0 Hz,H-1),3.69(3H,s,H-7′),3.67(3H,s,H-7′′),3.40(1Ha,m,H-1′′′),3.34(1Hb,m,H-1′′′),2.98(1H,m,H-2),1.18(3H,t,J=7.0,H-2′′′);13C NMR(125 MHz,CD3OD) δ:148.5(C-3′),148.4(C-3′′),146.7(C-4′′),146.0(C-4′),133.4(C-1′′),132.8(C-1′),122.6(C-6′),121.3(C-6′′),115.7(C-5′′),115.5(C-5′),114.4(C-2′),112.3(C-2′′),85.8(C-3),65.1(C-1),65.1(C-1′′′),56.3(C-7′),56.3(C-7′′),56.1(C-2),15.6(C-2′′′)。上述波谱数据与文献报道一致[10],故鉴定为threo-2,3-bis(4-hydroxy-3-methoxypheyl)-3-ethoxypropan-1-ol。
化合物3:无色油状物,ESI-MS m/z 349[M+H]+。1H NMR(500 MHz,CD3OD)δ:6.69(1H,d,J=3.0 Hz,H-2"),6.68(1H,d,J=5.0 Hz,H-5′),6.66(1H,d,J=8.5,H-6′),6.60(1H,dd,J=8.0,1.5 Hz,H-6"),6.56(1H,dd,J=8.0,1.5 Hz,H-2′),6.47(1H,d,J=1.5 Hz,H-5"),4.60(1H,d,J=5.0 Hz,H-3),3.89(1H,dd,J=10.5,7.0 Hz,Ha-l),3.75(3H,s,C-7′),3.68(1H,dd,J=7.5,4.0 Hz,Hb-l),3.64(3H,s,C-7"),3.36(1H,dd,J=9.0,7.0 Hz,Ha-l′"),3.26(1H,dd,J=9.0,7.0 Hz,Hbl′"),2.84(1H,dd,J=12.0,6.5 Hz,H-2),1.11(3H,t,J=7.0 Hz,H-2′");13C NMR(125 MHz,CD3OD):δ:148.6(C-3"),148.2(C-3′),146.7(C-4′),146.2(C-4"),134.0(C-1′),132.3(C-1"),123.4(C-6"),121.1(C-6′),115.5(C-5′,5"),114.8(C-2"),111.9(C-2′),82.8(C-3),65.2(C-1′"),64.5(C-1),56.5(C-2),56.4(C-7′),56.2(C-7"),15.6(C-2′")。上述波谱数据与文献报道一致[11],故鉴定为erythro-2,3-bis(4-hydroxy-3-methoxyphenyl)-3-ethoxypropan-1-ol。
化合物 4:黄色固体,ESI-MS m/z 359[M+H]+。1H NMR(500 MHz,CD3OD)δ:6.95(2H,d,J=2.0,H-2,2′),6.81(2H,d,J=8.0,1.5,H-6,6′),6.77(2H,d,J=8.0,H-5,5′),4.70(2H,d,J=4.5,H-7,7′),4.22(2H,dd,J=9.0,7.0,Ha-9,9′),3.85(6H,s,H-3,3′-OCH3),3.82(2H,dd,J=8.0,5.5,Hb-9,9′),3.13(2H,dd,J=6.5,4.5,H-8,8′);13C NMR(125 MHz,CD3OD)δ:149.1(C-4,4′),147.3(C-3,3′),133.8(C-1,1′),120.0(C-6,6′),116.1(C-5,5′),111.0(C-2,2′),87.5(C-7,7′),72.6(C-9,9′),56.4(C-3,3′-OCH3),55.4(C-8,8′)。上述波谱数据与文献报道一致[12],故鉴定为pinoresinol。
化合物5:无色油状物,ESI-MS m/z 381[M+Na]+。1H NMR(500 MHz,CD3OD)δ:6.97(1H,s,H-6′),6.95(2H,s,H-2,2′),6.83(1H,dd,J=8.0,1.5 Hz,H-6),6.77(1H,d,J=8.0 Hz,H-5),6.54(1H,d,J=16.0 Hz,H-7′),6.23(1H,dt,J=16.0,6.0 Hz,H-8′),5.52(1H,d,J=6.0 Hz,H-7),4.20(2H,d,J=6.0 Hz,H-9′),3.87(3H,s,H-5′-OCH3),3.81(3H,s,H-3-OCH3),3.79(2H,overlapped,H-9),3.49(1H,dd,J=12.5,6.5 Hz,H-8);13C NMR(125 MHz,CD3OD)δ:149.4(C-4′),149.3(C-3),147.7(C-4),145.6(C-3′),134.7(C-1),132.7(C-1′),132.2(C-7′),130.5(C-5′),127.7(C-8′),119.9(C-6),116.7(C-6′),116.3(C-5),112.2(C-2′),110.7(C-2),89.5(C-7),65.0(C-9),64.0(C-9′),56.9(C-3′-OCH3),56.5(C-3-OCH3),55.3(C-8)。上述波谱数据与文献报道一致[13],故鉴定为(-)-dehydrodiconiferyl alcohol。
化合物6:淡黄色无定形固体,ESI-MS m/z 363[M+H]+。1H NMR(500 MHz,CD3OD)δ:6.66(2H,d,J=8.0 Hz,H-5,5′),6.59(2H,s,H-2,2′),6.54(2H,d,J=7.5 Hz,H-6,6′),3.74(6H,s,H-3,3′-OCH3),3.59(4H,m,H-9,9′),2.66(2H,dd,J=13.5,6.5 Hz,Ha-7,7′),2.55(2H,dd,J=13.5,7.5 Hz,Hb-7,7′),1.90(2H,m,H-8,8′);13C NMR(125 MHz,CD3OD) δ:149.0(C-3,3′),145.6(C-4,4′),134.0(C-1,1′),122.9(C-6,6′),115.9(C-5,5′),113.6(C-2,2′),62.3(C-9,9′),56.3(C-3,3′-OCH3),44.3(C-8,8′),36.2(C-7,7′)。上述波谱数据与文献报道一致[14],故鉴定为裂异落叶松脂醇。ethoxypropan-1-ol表现出醌还原酶诱导活性[11];pinoresinol具有改善记忆障碍,促进海马LTP的诱导活性,以及针对肿瘤坏死因子(TNF)-α诱导的MH7A细胞炎症模型的抗类风湿性关节炎(RA)活性[18-19];(-)-dehydrodiconiferyl alcohol能够通过灭活巨噬细胞NF-κB通路促进细胞愈合[20];裂异落叶松脂醇可以加速3T3-L1脂肪细胞中脂联素的产生[21]。鉴于木脂素类成分具有丰富多样的生物活性,加大对新疆灰枣果核木脂素类化学成分的开发力度,对提高新疆灰枣产品的附加值,推动新疆枣产业的健康发展具有重要意义。
4 结论与讨论
灰枣作为滋补保健的佳品,具有健脑安神,补气益血,保肝降脂,抗氧化等广泛的药理活性。目前对灰枣果肉中的有效成分研究较多,灰枣果核作为灰枣加工过程产生的副产品大多被丢弃,造成资源浪费。本研究通过对灰枣果核95%乙醇提取物乙酸乙酯部位化学成分的研究,共得到6个木脂素类化合物,分别为:(+)-(7S,8R,7′E)-4-hydroxy-3,5′-dimethoxy-4′,7-epoxy-8,3′-neolign-7′-ene-9,9′-diol 9′-ethyl ether(1)、threo-2,3-bis(4-hydroxy-3-methoxyphenyl)-3-ethoxypropan-1-ol(2)、erythro-2,3-bis(4-hydroxy-3-methoxyphenyl)-3-ethoxypropan-1-ol(3)、pinoresinol(4)、(-)-dehydrodiconiferyl alcohol(5)和裂异落叶松脂醇(6),化合物1~6皆为首次从鼠李科中分离得到。据文献报道,(+)-(7S,8R,7′E)-4-hydroxy-3,5′-dimethoxy-4′,7-epoxy-8,3′-neolign-7′-ene-9,9′-diol 9′-ethyl ether具有一定的保肝和抗炎活性[9],以及抑制芳香酶催化活性[15],在细胞毒、抗氧化、抗HIV-1复制以及神经毒性保护等方面未表现出明显活性[9,16];threo-2,3-bis(4-hydroxy-3-methoxyphenyl)-3-ethoxypropan-1-ol具有抑制RAW264.7巨噬细胞中LPS诱导NO产生的活性[17];erythro-2,3-bis(4-hydroxy-3-methoxyphenyl)-3-

