老年高血压伴糖耐量减低患者胰岛素抵抗指数对血压变异率及昼夜节律的影响
赵凤凤 钮恩静 陈亮
(1 潍坊医学院临床医学院,山东 潍坊 261053; 2 青岛大学附属妇女儿童医院综合内科)
高血压作为老年群体中最常见的慢性非传染性疾病之一,也是心血管疾病的主要死亡危险因素之一[1]。现有研究表明,血压变异率(BPV)短期或长期升高及血压昼夜节律的改变,与靶器官损伤的进展和严重程度、心血管疾病死亡率之间均有较强相关性,并且有可能是药物治疗的疗效指标[2-5]。研究表明,与单纯高血压患者相比,老年高血压伴糖尿病患者血压昼夜节律紊乱及靶器官损害严重程度进一步增加[6-7]。糖耐量减低(IGT)作为糖尿病前期的糖代谢异常状态,胰岛素抵抗(IR)是其主要发生机制之一,IR可通过多种生化机制促进靶器官的损害,加速心血管疾病进程[8]。老年高血压伴IGT导致BPV及血压昼夜节律改变的危险因素尚不可知。目前,国内外对于IR与血压昼夜节律相关性的研究较少,关于IR与BPV的相关性研究尚未见报道。本研究通过对老年高血压伴IGT患者进行动态血压监测,分析胰岛素抵抗指数(HOMA-IR)与BPV、血压昼夜节律的相关性,为此类患者的治疗及其靶器官损害的预防提供新思路。
1 资料与方法
1.1 一般资料
回顾性分析2020年10月—2021年9月青岛市妇女儿童医院综合内科门诊及住院的老年高血压伴IGT患者106例,其中男59例,女47例,平均年龄(67.78±4.44)岁,以HOMA-IR的第50百分位数(P50)为分界线,将受试者分为高IR组(53例)和低IR组(53例)。
患者纳入标准:①高血压符合《中国高血压防治指南2018年修订版》的诊断标准[9];②IGT符合《中国2型糖尿病防治指南(2020年版)》诊断标准[10];③年龄在60岁以上。排除标准:①继发性高血压;②糖尿病病史及服用降糖药物;③严重心脑血管疾病;④多器官功能衰竭;⑤恶性肿瘤病史;⑥甲状腺功能亢进;⑦从事夜班工作。
1.2 研究方法
收集患者年龄、性别、BMI、吸烟史、饮酒史、高血压病程、降压药物使用情况等临床资料。所有患者均于清晨采集空腹静脉血,测空腹血糖(FPG)、空腹胰岛素(FINS)、糖化血红蛋白(HbA1c)、总胆固醇、三酰甘油、低密度脂蛋白、高密度脂蛋白、血肌酐,口服75 g葡萄糖后,测餐后2 h血糖(2 h PG)。选取HOMA-IR作为评价IR程度的指标。
以德国IEM动态血压仪对患者行24 h血压监测。设置昼间血压时间为7:00~22:00,每30 min测量一次血压,设置夜间血压时间为22:00~7:00,每1 h测量一次血压,有效血压读数≥95%为有效。记录昼间、夜间平均收缩压,昼间、夜间、24 h收缩压标准差,昼间、夜间、24 h舒张压标准差,昼间、夜间、24 h收缩压变异系数,昼间、夜间、24 h舒张压变异系数,计算夜间收缩压下降百分率。选取血压标准差和血压变异系数作为评价BPV的指标,夜间收缩压下降百分率作为评价血压昼夜节律的指标。血压变异系数=血压标准差/平均血压,夜间收缩压下降百分率=(昼间平均收缩压-夜间平均收缩压)/昼间平均收缩压×100%。夜间收缩压下降百分率10%~20%者为勺型血压,即正常血压昼夜节律;夜间收缩压下降百分率0~10%者为非勺型血压,>20%者为超勺型血压,<0者为反勺型血压,后三者为异常血压昼夜节律。
1.3 统计学方法
2 结 果
2.1 两组患者一般资料比较
高IR组患者BMI、FINS、HOMA-IR均高于低IR组,差异有统计学意义(t=-2.412~-13.416,P<0.05)。两组患者间其他指标比较,差异均无统计学意义(P>0.05)。见表1。
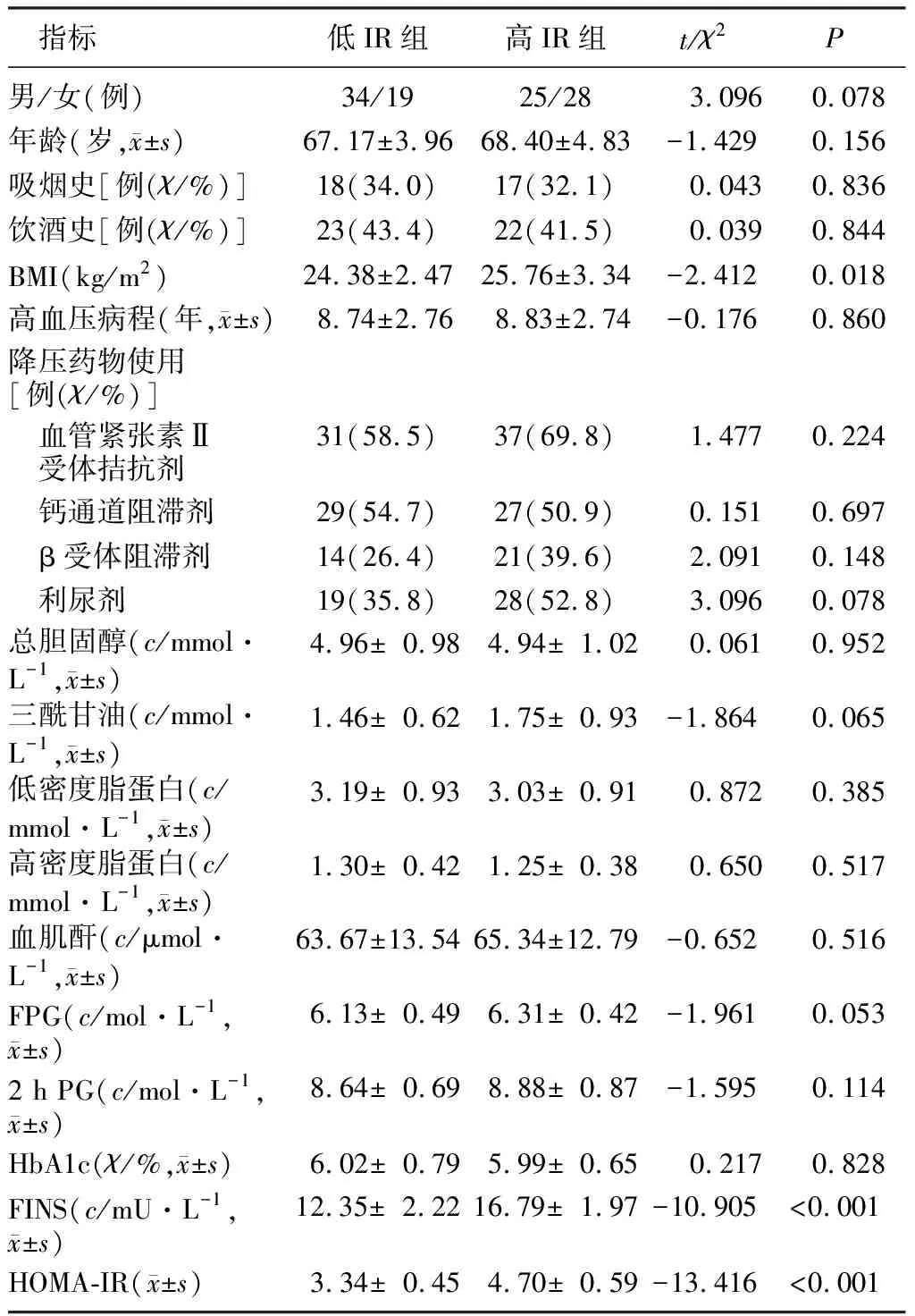
表1 两组患者一般资料比较(n=53)
2.2 两组患者BPV结果比较
高IR组患者的昼间、夜间、24 h收缩压标准差,以及昼间、夜间、24 h收缩压变异系数均高于低IR组,差异具有统计学意义(t=-4.180~-2.356,P<0.05)。见表2。

表2 两组患者BPV结果比较
2.3 两组患者血压昼夜节律结果比较
根据夜间收缩压下降百分率将所有患者的血压昼夜节律类型分为正常血压昼夜节律(勺型)和异常血压昼夜节律(非勺型、超勺型、反勺型)。低IR组检出勺型血压22例,非勺型血压18例,超勺型血压2例,反勺型血压11例;高IR组检出勺型血压12例,非勺型血压25例,超勺型血压3例,反勺型血压13例,高IR组患者异常血压昼夜节律构成比显著高于低IR组(χ2=4.330,P<0.05)。
2.4 所有患者HOMA-IR与BPV的相关性分析
所有老年高血压伴IGT患者的HOMA-IR与昼间、夜间、24 h收缩压标准差,以及昼间、夜间以及24 h收缩压变异系数均呈正相关(r=0.202~0.328,P<0.05)。
3 讨 论
自1958年第一次全国范围内高血压调查以来,我国高血压发病率呈逐年上升趋势,目前我国60岁以上老年人高血压患病率达到50%,80岁以上老年人高血压患病率达到90%[9]。高血压导致的心脑血管事件发生率居高不下,已经成为老年人致死和致残的重要因素之一[11]。多项研究结果表明,在轻中度高血压患者中,相对平均血压、BPV升高具有对心血管事件更强的风险预测价值[12-13]。2017年美国心脏病学会发布的《高血压预防、评估和管理指南》中已经将BPV作为预测患者心血管事件的独立危险因素[14]。
BPV指在一定时间内血压动态波动的程度,其是由外在环境、行为因素和心血管调节机制等因素相互作用形成[15]。在正常情况下,血压的昼夜节律呈现为“两峰一谷”的勺型曲线,故正常人的血压昼夜节律为勺型血压。老年高血压患者由于动脉管壁硬度增加、大血管容量负荷和外周血管阻力负荷增加、压力感受器反射障碍以及肾脏维持电解质平衡的能力下降等原因,易导致BPV发生不同程度的改变,同时血压昼夜节律曲线的形态多表现为非勺型、超勺型,甚至表现为夜间血压异常升高的反勺型血压[15-16]。国内外多项研究表明,当高血压患者BPV增高及夜间血压下降不足时,可增加机体左心室肥厚、早期肾脏损伤,同时可增加心肌梗死、脑梗死及脑出血等血管疾病的发病风险[17-19]。近年来,高血压的降压目的不再局限于降低平均血压,在血压控制较好的人群中,控制BPV及恢复血压昼夜节律逐渐成为药物降压的目标。
当高血压伴随血糖、血脂异常等代谢状态时,其患心血管疾病的危险系数明显增高[20]。GUL等[21]研究表明,高血压患者中IGT的发生率为42.6%,这种现象在老年人群中更为多见。IGT作为糖尿病前期病变状态,IR是导致IGT的关键所在,能否改善IR现象,是IGT是否进展为糖尿病的关键因素[22]。研究发现IR普遍存在于多种慢性疾病中,YAMAZOE等[23]对日本1 006例男性非糖尿病患者进行随访发现,IR是其冠状动脉钙化的独立预测因子。多项对高血压伴IR患者的研究结果显示,HOMA-IR与早期肾损伤、颈动脉厚度及硬化程度、心力衰竭等因素显著相关,并且IR较重的患者,靶器官病变危险性增加[24-25]。
本研究回顾性分析106例老年高血压伴IGT患者临床资料,初步证实IR对高血压伴IGT患者BPV及血压昼夜节律有明显影响,主要表现为高IR组的昼间、夜间、24 h收缩压标准差,以及昼间、夜间、24 h收缩压变异系数显著高于低IR组;同时,高IR组非勺型、反勺型、超勺型血压现象较低IR组更为普遍,这与欧阳征鹏等[26]研究结果较为一致,其认为IR可能通过动脉硬化导致高血压伴糖尿病患者异常血压昼夜节律的发生。另外本研究进一步对HOMA-IR与BPV的相关性进行分析,结果表明HOMA-IR与患者昼间、夜间、24 h收缩压标准差,以及昼间、夜间、24 h收缩压变异系数呈正相关。目前,IR与血压BPV和血压昼夜节律之间关系的机制尚不明确,可能为以下几点:①IR状态下,胰岛素可作用于肾单位的近端小管和远端小管的胰岛素受体底物2通路,增加肾单位对钠离子的吸收,导致水钠潴留[27-28];②IR状态下,胰岛素介导的血管内皮细胞和平滑肌细胞中的磷酯酰肌醇3激酶信号通路途径受损,内皮细胞产生的一氧化氮释放量下降,导致血管内皮舒张功能受损[29]。③高浓度的胰岛素可以通过丝裂原活化蛋白激酶信号通路诱导血管平滑肌细胞的增生、肥大,致使血管内皮增厚、管壁硬度增加[30]。④高浓度胰岛素可以使交感神经系统和肾素-血管紧张素-醛固酮系统活性增加,表现为交感神经的持续性兴奋,夜间迷走神经功能受损,同时影响心率变异性,导致循环系统外周阻力增加,血压增高,打乱正常的血压昼夜节律[31]。
综上所述,老年高血压伴IGT患者的HOMA-IR与BPV升高呈正相关,IR是老年高血压伴IGT患者BPV增高及血压昼夜节律的危险因素。IR现象在IGT患者治疗中未引起过多重视,未形成以IR为靶向治疗的综合治疗对策,因此在老年高血压伴IGT患者的治疗中,应关注改善IR现象。

