碱催化丁酮和甲醛羟醛缩合反应研究
汪 波,蒋泽晨,张胜红
(北京石油化工学院新材料与化工学院,恩泽生物质精细化工北京市重点实验室,北京 102617)
甲基异丙基酮(3-甲基-2-丁酮)作为一种重要的精细化工中间体和有机溶剂,广泛用于染料、医药、农药和其他高值精细化学品的合成,是我国长期依赖进口的重要精细化工品种之一[1]。甲基异丙基酮的合成按照起始原料可以分为异丁酸法、异丁醛法、异戊二烯和丁酮(MEK)法[2-4]。其中,以丁酮和甲醛为原料采用多级串联反应釜能够实现70%的甲基异丙基酮收率[5],是一条极具市场应用前景的技术路线。该工艺涉及丁酮和甲醛发生羟醛缩合(Aldol)生成α,β-不饱和酮及其催化加氢两个过程,且Aldol反应的效率是进一步提升产品收率的关键。
Aldol反应是指有α氢的醛(酮)在碱或酸的催化作用下缩合形成β-羟基醛(酮)的反应。Morgan和Holmes早在1932年就报道了氢氧化钠催化丁酮和甲醛间的缩合反应,但产物较为复杂,除4-羟基-3-甲基-2-丁酮(HMBO)及其脱水产物甲基异丙烯酮(MIPK)外,还含有1-羟基-3-戊酮(HPO)、次级Aldol反应以及丁酮自身缩合的产物[6-7]。与碱催化不同,酸催化丁酮和甲醛缩合难以得到HMBO,产物主要是5-乙酰基-5-甲基-1,3-二氧六环;其中,甲醛和丁酮烯醇式异构体的加成为反应的决速步骤[8]。相比之下,碱催化丁酮和甲醛Aldol反应的产物HMBO能够进一步脱水加氢得到甲基异丙基酮,但如何实现丁酮和甲醛的定向Aldol缩合并高收率地制备HMBO至今尚未有完美的解决方案。
最近,大量的实验报道显示[9-11],有机胺及其盐能够高选择性地催化甲醛和其他醛(酮)间的交叉Aldol缩合,α,β-不饱和醛(酮)产物的选择性超过90%,为丁酮和甲醛定向Aldol反应催化剂的筛选提供了借鉴。因此,笔者详细考察了不同有机碱催化丁酮和甲醛羟醛缩合反应的性能,优化反应参数并基于产物的时间分布曲线初步推导了可能的反应路径。
1 实验部分
1.1 试剂及仪器
丁酮、碳酸钾、乙胺、二环己基胺、乙二胺和三乙胺,分析纯,上海阿拉丁生化科技股份有限公司生产;甲基异丙烯酮和4-羟基-3-甲基-2-丁酮,分析纯,百灵威科技有限公司生产;25%氨水和37%甲醛溶液,国药集团化学试剂有限公司生产。
WP-TDC-020P加压平行反应仪,西安华太科思化学技术有限公司生产;Shimadzu GC-2014气相色谱仪和GCMS-QP 2010 Plus气相色谱-质谱联用仪,日本岛津公司生产;Nicolet 6700红外光谱仪,美国ThermoFisher公司生产;ME204/02电子天平,梅特勒-托利多国际贸易(上海)有限公司生产。
1.2 催化性能评价
采用间歇式平行反应仪对碱催化丁酮和甲醛羟醛缩合反应的性能进行评价。首先在硬质玻璃反应管中按照一定摩尔比加入丁酮和37%甲醛溶液,然后加入摩尔分数为5%(相对于丁酮)的碱催化剂,以5 ℃/min的速率升温到目标反应温度并开始计时。反应液采用电磁搅拌且磁子搅拌速率为300 r/min,反应温度为40 ℃,反应时间为4 h。
1.3 产物分析
反应液经冷却和滤膜(0.45 μm)分离后分别采用配置有Supelco WAX-10毛细管柱(30 m×0.32 mm×0.5 μm)的气质联用仪和气相色谱仪进行定性和定量分析,同时辅以红外图谱进行佐证。产物主要有MIPK、HMBO、甲醛缩一(4-羟基-3-甲基-2-丁酮)(FHMBO)和其他少许副产物。丁酮的转化率[(X(MEK)]和产物Pi选择性[(S(Pi)]的计算式分别为:

(1)

(2)
式中:n(Pi)和n(MEK)分别为反应液中产物Pi和残留原料MEK的物质的量。
2 结果与讨论
2.1 丁酮和甲醛Aldol缩合产物的定性分析
丁酮和甲醛Aldol缩合反应主要产物的EI质谱图如图1所示。由图1中可以看出,产物依次对应于MIPK、HMBO和FHMBO。其中,m/z84为MIPK的分子离子峰,其发生α断裂失去甲基后得到m/z69的碎片离子;与MIPK不同,HMBO的分子离子峰m/z102较弱,其失水得到m/z 84的碎片离子或失去C3H5得到m/z61碎片离子。相比之下,FHMBO未观察到分子离子峰,其质谱中丰度最高的为CH2=C(CH3)-O碎片。

图1 主要产物的质谱数据图Fig.1 Mass spectra of the main products
丁酮和甲醛Aldol缩合反应产物(未分离)与HMBO标准品的红外光谱图如图2所示。由图2中可以看出,HMBO在3 200~3 650 cm-1处宽吸收带为羟基的吸收,1 702 cm-1和1 360 cm-1处的尖锐吸收峰分别对应于羰基和甲基的吸收。反应液具有和HMBO相似的红外吸收图谱,佐证了HMBO是丁酮和甲醛Aldol缩合反应的主要产物,与质谱分析结果一致。此外,MIPK和HMBO也分别通过比照其与相应标准品的气相色谱保留时间进行了验证。
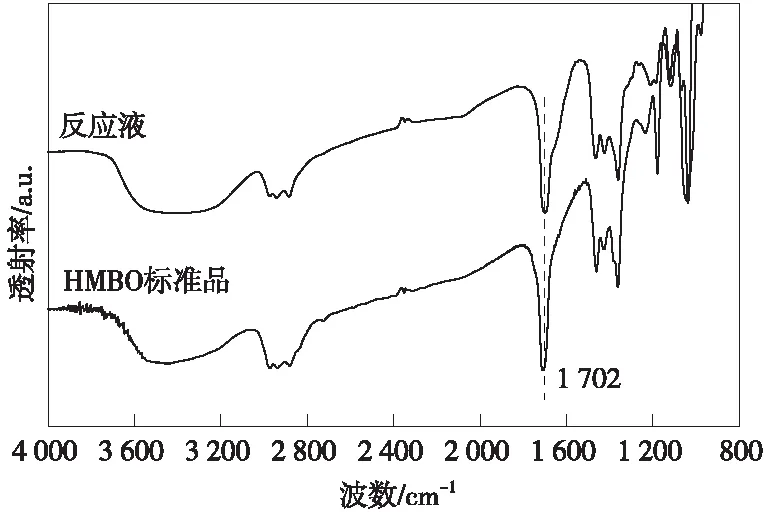
图2 反应产物和HMBO标准品的红外光谱的对比图Fig.2 FT-IR spectra of HMBO and the mixed reaction products
2.2 不同碱催化丁酮和甲醛羟醛缩合反应的性能
不同碱催化丁酮和甲醛Aldol缩合反应的性能如表1所示。由表1中可以看出,在n(HCHO)/n(MEK)为1.1、温度为60 ℃的条件下反应4 h,空白反应中MEK的转化率仅为6.5%,表明未加入碱时丁酮和甲醛间难以发生有效的羟醛缩合。在上述反应体系引入摩尔分数5%(相对于丁酮)的氨水,丁酮的转化率提高到31.1%,羟醛缩合反应产物及其衍生物(HMBO、FHMBO和MIPK)的总选择性为69.1%,但深度聚合导致的副产物的选择性仍然高达30.9%。采用碱性更强的碳酸钾作为催化剂能够进一步提高丁酮的转化率到83.4%,并促进产物HMBO分子内脱水形成MIPK,但同时也增加了聚合副产物的含量。与无机碱不同,有机胺催化丁酮和甲醛缩合反应的活性较为温和且与催化剂的结构无明显关联,但目标产物的选择性却显著提高,尤其是三乙胺 (TEA) 为催化剂时高达88.1%,表明三乙胺是催化丁酮和甲醛羟醛缩合反应的理想催化剂。
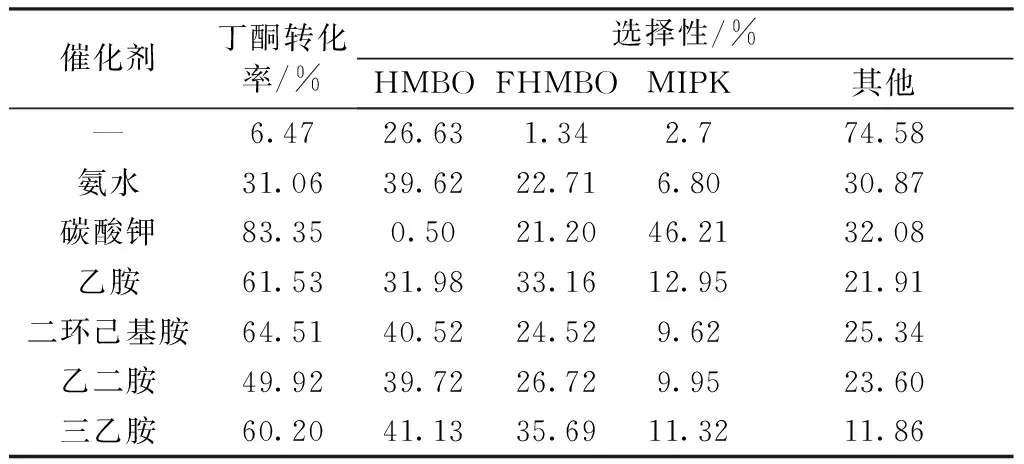
表1 不同碱催化丁酮和甲醛羟醛缩合反应的性能
2.3 三乙胺催化丁酮和甲醛羟醛缩合反应条件的优化
为优化三乙胺催化丁酮和甲醛羟醛缩合反应的工艺条件,采用单一变量法依次考察了温度、醛酮摩尔比、催化剂用量和反应时间对羟醛缩合反应的影响。温度对丁酮和甲醛羟醛缩合反应的转化率和选择性的影响如图3所示。由图3可以看出,低温时丁酮的转化率随着温度的升高而增加;一旦温度超过60 ℃丁酮的转化率受温度的影响不大,基本维持在62%。尽管如此,随着温度从40 ℃提高到90 ℃,副产物的选择性却从10.1%增加到20.0%,表明高温有利于聚合副产物的形成。因此,丁酮和甲醛的羟醛缩合应该维持在相对低的反应温度以获得高的目标产物(MIPK、HMBO及其衍生物FHMBO)选择性。

注:TEA的摩尔分数为5%,n(HCHO)/n(MEK)=1.1,t=4 h。图3 温度对丁酮和甲醛羟醛缩合反应的影响Fig.3 Effect of temperature on the Aldol reaction between MEK and formaldehyde
在催化剂三乙胺摩尔分数为5%、反应温度为40 ℃、反应时间为4 h的条件下,甲醛和丁酮摩尔比对缩合反应的影响如图4所示。由图4中可以看出,随着醛酮摩尔比从1.0提高到2.0,丁酮的转化率逐步增大,但在醛酮摩尔比大于1.5时增长趋势明显放缓;另外,HMBO的选择性随醛酮摩尔比的增加持续降低,同时伴随着FHMBO选择性的提高并且二者选择性的加和几乎保持不变,表明HMBO和过量的甲醛继续发生亲核加成反应生成半缩醛FHMBO。此外,一旦醛酮摩尔比超过1.5,副产物的选择性随醛酮摩尔比的增加而缓慢升高,而MIPK的选择性对醛酮摩尔比不太敏感。因此,丁酮和甲醛Aldol缩合反应的理想醛酮摩尔比为1.5。
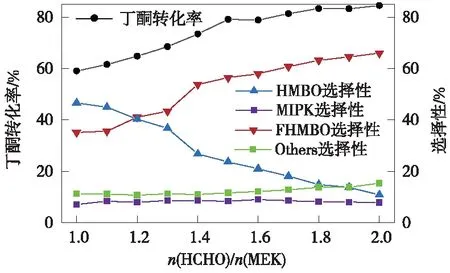
注:TEA摩尔分数为5%,T=40 ℃,t=4 h。图4 甲醛和丁酮摩尔比对二者羟醛缩合反应性能的影响Fig.4 Effect of the molar ratios of formaldehyde to MEK on their Aldol reaction
三乙胺用量对丁酮和甲醛羟醛缩合反应的影响如图5所示。由图5中可以看出,不存在催化剂时,40 ℃反应4 h后丁酮的转化率仅为4.9%,与表1中的结果吻合;0.5%三乙胺的引入能够将丁酮的转化率大幅提高到50.5%并且其数值随三乙胺摩尔分数的提高持续增加,直至三乙胺摩尔分数超过10%后稳定在70%左右。与此同时,HMBO的选择性随催化剂摩尔分数的提高持续降低并趋于稳定,FHMBO表现出相反的趋势,而MIPK和聚合副产物的选择性几乎与三乙胺的摩尔分数无关。结果表明,少量的三乙胺即能有效催化丁酮和甲醛间的羟醛缩合反应,过量三乙胺的存在则促进HMBO和甲醛发生亲核加成生成半缩醛FHMBO。
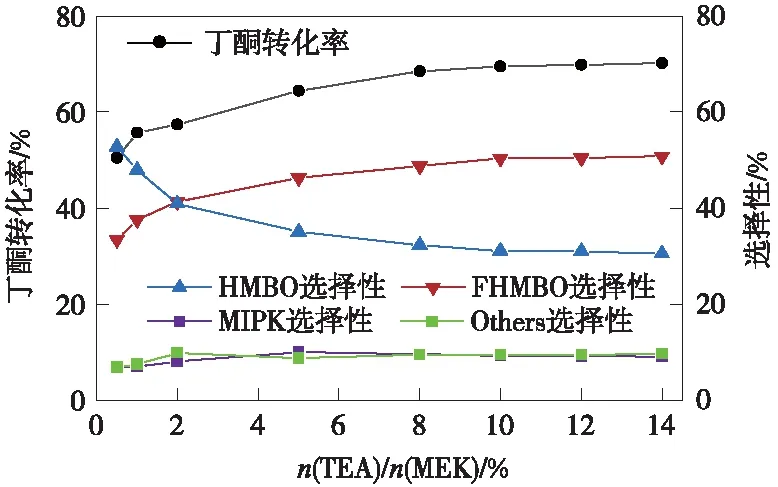
注:n(HCHO)/n(MEK)=1.1,T=40 ℃,t=4 h。图5 三乙胺用量对丁酮和甲醛羟醛缩合反应性能的影响Fig.5 Effect of the TEA doses on the Aldol reaction between MEK and formaldehyde
三乙胺催化丁酮和甲醛羟醛缩合反应中产物的时间分布曲线如图6所示。从图6中可以看出,丁酮的转化率在升温过程中已经达到了31.1%且随反应时间的延长持续增大;反应6 h后丁酮的转化率趋于稳定,约为64%。产物选择性方面,随着反应时间延长至8 h,HMBO的选择性从65.5%降低为38.0%,FHMBO的选择性则从21.9%增加到44.7%,二者的总选择性基本维持在83%左右;与此不同,MIPK的选择性几乎不随反应时间而改变,维持在7%左右。结果表明,延长反应时间不能促进HMBO脱水生成MIPK,而是有利于HMBO和甲醛间的缩合,进而拉动丁酮和甲醛羟醛缩合反应平衡的右移并提高丁酮的转化率。
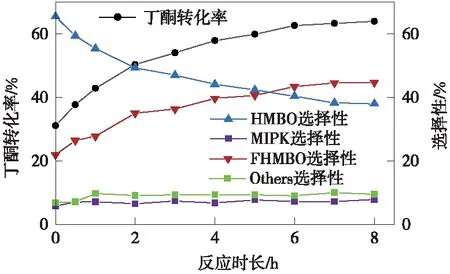
注:TEA摩尔分数为5%,T=40 ℃,n(HCHO)/n(MEK)=1.1。图6 反应时间对甲醛和丁酮羟醛缩合反应性能的影响Fig.6 Effect of reaction time on the Aldol reaction between MEK and formaldehyde
2.4 三乙胺催化丁酮和甲醛羟醛缩合反应的路径
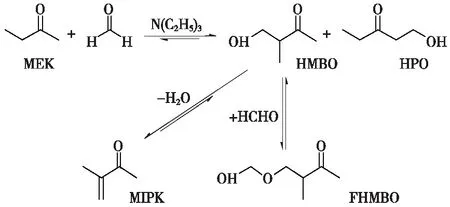
图7 三乙胺催化丁酮和甲醛Aldol缩合反应路径Fig.7 The proposed reaction network for the Aldol condensation between MEK and formaldehyde
基于图6中的转化率-选择性曲线以及醛酮摩尔比对产物分布的影响,可以推测丁酮和甲醛缩合反应的反应路径如图7所示。三乙胺为催化剂时,丁酮中羰基邻位的亚甲基碳和端甲基碳均可以失去1个质子,形成碳负离子并进攻甲醛分子,分别生成HMBO和HPO;其中,前者为主要产物。HMBO进一步脱水生成MIPK或与多余的甲醛分子发生亲核加成反应生成FHMBO,与Mahajani等[12]报道的丁酮和乙醛交叉Aldol反应的路径类似。尽管HMBO和甲醛的加成反应为典型的可逆过程,但其却提供了一个有效提升丁酮转化率的反应策略,即通过增大原料中的醛酮摩尔比促进HMBO向FHMBO的转化,进而拉动丁酮和甲醛羟醛缩合反应的不断右移。
3 结论
考察了碱催化剂类别和反应参数对丁酮和甲醛羟醛缩合反应性能的影响,得出以下结论:
(1)三乙胺是催化丁酮和甲醛羟醛缩合反应的高效催化剂;
(2)低温相对有利于丁酮和甲醛间的羟醛缩合,在反应温度为40 ℃、醛酮摩尔比为1.1的条件下,三乙胺催化丁酮和甲醛羟醛缩合产物的总选择性超过92%;
(3)三乙胺催化丁酮和甲醛羟醛缩合遵从平行-序列的反应路径,4-羟基-3-甲基-2-丁酮为反应的中间产物,其与甲醛形成相对稳定的半缩醛或脱水生成稳定的甲基异丙烯酮。

