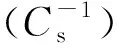油酸包覆的Fe3O4纳米颗粒与DPPG单层膜的相互作用*
王益祎,朱华泽,刘鑫鑫
(西安科技大学 理学院,西安 710054)
0 引 言
磁性Fe3O4纳米颗粒(MNPs)具有优异的生物相容性、化学亲和性和超顺磁性,在靶向给药、催化剂、生物传感器、分离和纯化生物分子以及癌症治疗等方面具有广阔的应用前景[1-6]。纳米技术迅速发展的同时增加了纳米材料与人类和环境接触的可能[7]。有研究表明纳米颗粒通过呼吸道吸入肺泡后,会直接进入肺表面活性单层膜[8,9],可能会引起膜的相变、重组和溶解,从而导致人体疾病。因此,探索纳米颗粒与生物膜分子之间的相互作用及其对人体产生的影响是一个亟需解决的课题[7]。
研究中常用Langmuir技术模拟单层生物膜,分析纳米颗粒的掺入对处于空气-液体界面的模拟膜的影响。近年来,纳米颗粒对脂质单层膜结构和物理化学性质的影响受到广泛关注[9-13]。Guzman分别研究了二氧化钛(TiO2)[12]和二氧化硅(SiO2)[13]纳米颗粒对DPPC单层膜界面性质的影响,发现TiO2纳米颗粒影响了单层膜的动态响应,改变了准平衡扩张弹性和粘弹性模量的高频极限值;而SiO2纳米颗粒使界面分子的平均分子面积减小,改变了DPPC单层膜的横向堆积和界面上脂质分子之间的内聚力,降低了脂单层膜的力学性能。Chakraborty[9]分别研究了工程碳纳米颗粒(ECN)对4种(DPPC/POPC、DPPC/DPPG、DPPC/DOPG和DPPC/DPPE)肺表面活性单层模拟膜在空气-液体界面的崩溃机制的影响,结果表明,ECN并不影响单层膜的崩溃机制,但是在膜崩溃过程中将肺表面活性物质保留在界面上的能力,以及在压缩-扩张循环后活性物质重新吸附到界面的能力会不同程度地被ECN改变。Xu[11]研究发现疏水性Fe3O4MNPs与POPC/DPPC混合脂分子尾链的排斥作用会导致脂-MNPs复合体溶入亚相;而亲水性Fe3O4MNPs与脂质亲水头基的相互作用会增强脂分子间的相互吸引作用。Piosik[1]研究了氨化壳聚糖修饰的MNPs吸附/掺入模拟膜的过程,发现在生理膜压下(35mN/m),MNPs可以吸附/掺入DPPC模拟膜中,而且吸附/掺入的MNPs数量可以通过MNPs浓度来调节。上述研究表明,纳米颗粒的组成、修饰、亲/疏水等性质会对单层膜产生较大影响。MNPs的出现可能会降低磷脂分子在界面上的可用面积,改变单层膜的结构和内聚性,同时影响单层膜的压缩性和稳定性。
Fe3O4纳米颗粒的化学活性高,在空气中容易被氧化成Fe2O3,且Fe3O4纳米颗粒容易聚集,从而失去磁性纳米结构的相关特性。因此,在Fe3O4纳米颗粒的应用中,常利用有机分子、聚合物、表面活性剂或生物分子对其进行表面改性。油酸分子(OA)的尾链中存在一个顺式双键,使用OA包覆Fe3O4纳米颗粒,可以形成致密的保护层,增强Fe3O4纳米颗粒的稳定性和分散性,得到高度均匀和单分散的纳米颗粒[10]。本文针对油酸包覆的Fe3O4纳米颗粒展开研究。
卵磷脂(PC,电中性)、磷脂酰甘油(PG,带负电)、磷脂酰乙醇胺(PE,带正电)是生物膜中常见的几种磷脂[14]。生物膜中含量最丰富的磷脂DPPC与纳米颗粒的相互作用已得到高度关注[1,7,12-15],但纳米颗粒与带电磷脂分子之间的相互作用尚未得到充分的了解。因此,本文结合Langmuir等温线实验、压缩-扩张实验、振荡实验以及布鲁斯特角显微镜(BAM)实验[15],从表面压、平均分子面积、压缩-扩张特性和流变性等方面分析了OA-Fe3O4MNPs与带负电的DPPG单层膜在空气-水界面的相互作用,为Fe3O4MNPs的安全应用提供实验支持[16,17]。
1 实 验
1.1 实验材料
二棕榈酰磷脂酰甘油(DPPG)购自Corden Pharma公司(德国),纯度99%;油酸包覆的磁性纳米颗粒(OA-Fe3O4MNPs)购自西安瑞禧生物有限公司。无水乙醇、甲醇、氯仿等有机溶剂均购自天津富宇精细化工有限公司。实验用水均采用超纯水。
Langmuir-Blodgett(LB)膜分析仪为芬兰KSV公司的Medium型,槽面积为243 cm2。用Wilhelm板测量表面张力(γ),精度0.01mN/m. 表面压(π)定义为π=γw-γ,其中γw为纯水的表面张力[9,15]。
DPPG溶解在氯仿/甲醇(3∶1,v/v)溶液中,浓度为0.5mg/mL[15]。OA-Fe3O4MNPs分散在氯仿中形成浓度0.5mg/mL的储备液[15],使用前超声处理5min,避免因MNPs团聚而对实验造成不利影响[12]。采用恒温循环水槽控制亚相温度为(28.0±0.1)℃(HX-105型,长流科学仪器有限公司)。
1.2 实验方法
1.2.1 测绘π-A等温线[1,11,16]
保持DPPG质量不变,改变OA-Fe3O4MNPs的质量,配置按一定质量比混合的实验样品(DPPG:OA-Fe3O4MNPs =m∶m′),用微量进样器将混合液滴加至纯水表面,使其自动铺展20分钟,以确保有机溶剂完全挥发。以10 mm/min的速率压缩单层膜,测绘表面压-平均分子面积(π-A)等温线。
1.2.2 测绘Δπ-t曲线[1,11]
将单层膜压缩至固定表面压π0=25 mN/m,停止移动滑障,记录表面压π(t)随时间t的变化曲线,计算得到Δπ-t曲线(Δπ=π(t)-π0)。
1.2.3 压缩-扩张实验[9,17]
以10 mm/min的速率将单层膜压缩至50 mN/m,然后以相同的速率扩张单层膜至最大面积,循环3次,记录表面压的变化。
1.2.4 振荡实验[15]
压缩单层膜至目标表面压π0=25 mN/m,停止移动滑障,静置10 min使单层膜达到平衡状态。然后滑障以固定振幅按正弦规律振荡,振荡频率5,20,50,80,100,200mHz,记录表面压随时间的变化曲线。
2 结果与讨论
2.1 DPPG与OA-Fe3O4 MNPs混合单层膜的热力学分析
图1(a)给出了掺入不同浓度的OA-Fe3O4MNPs后,DPPG单层膜的π-A/A1等温线(A1是DPPG分子在空气-水界面充分扩散后的平均占有面积[15])。纯DPPG单层膜的起始平均分子面积为0.98 nm2,膜由气相(G)进入液态扩张相(LE)的压缩比(A/A1)为0.57,单层膜的崩溃压约56 mN/m。掺入OA-Fe3O4MNPs后,等温线向平均分子面积增大的方向移动,且起始平均分子面积(图1(a)Δ标记)也随之增大,这表明OA-Fe3O4MNPs吸附到空气-水界面,占据了DPPG分子在界面上的部分可用面积,产生了具有显著纳米颗粒浓度依赖性的排除面积效应(excluded area effects)[15,18]。掺入OA-Fe3O4MNPs后,单层膜的表面压明显升高,当A/A1=0.4时,表面压升高幅度(Δπ0.4)达最大;当DPPG∶OA-Fe3O4MNPs(m∶m′)=2∶1时,Δπ0.4高达25 mN/m。表面压如此大幅度的升高可能对生物膜系统(如肺表面活性膜)的功能(如呼吸作用)产生明显的不利影响。表面压大幅升高与磷脂带电头部基团和OA-Fe3O4MNPs的相互作用有关,这可能导致DPPG的凝聚,也可能形成DPPG-OA-Fe3O4MNPs复合体。将OA-Fe3O4MNPs掺入DPPG单层膜后,未观察到单层膜崩溃压(πc)的明显变化,πc值均集中在56 mN/m左右,纳米颗粒的加入并未改变DPPG单层膜的崩溃机制。Piosik[1]研究发现氨基壳聚糖修饰的Fe3O4MNPs对DPPC单层膜的崩溃压亦无明显影响。Chakraborty[9]研究了工程碳纳米颗粒与二元磷脂混合单层膜的相互作用,发现二元混合膜的崩溃机制也没有受到明显影响。随着OA-Fe3O4MNPs浓度的增加,DPPG单层膜的极限分子面积(Aext)随之增大,该现象也出现在由氨基壳聚糖修饰的Fe3O4MNPs与DPPC组成的单层膜体系中[1]。由此可见,纳米颗粒可对磷脂单层膜的极限分子面积产生显著影响,而且这种影响与纳米颗粒的浓度相关联。
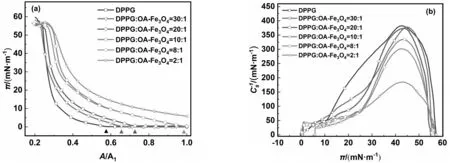
图1 DPPG与OA-Fe3O4 MNPs混合单层膜的π-A/A1等温线(a)及CS-1-π曲线(b)Fig.1 π-A/A1 isotherms and CS-1-π curves of mixed monolayers of DPPG and OA-Fe3O4 MNPs
利用BAM实时监测了单层膜的成膜过程,观察单层膜的表面结构特征。图2(a)-(e)为π=10 mN/m时纯DPPG及DPPG:OA-Fe3O4MNPs(m∶m′)=20∶1、10∶1、8∶1和2∶1的单层膜的BAM图像。结果发现,温度为28 ℃时,纯DPPG单层膜结构均匀,BAM图呈现整齐排列的圆形微区结构(图2(a)),DPPG单层膜在10 mN/m的压力下可能处于并不显著的LE-LC相变共存区。这与D.Vollhardt[21]发现温度处于26~37 ℃之间时,DPPG仅在LE-LC相变共存区呈现规则形状的微区结构一致。当DPPG:OA-Fe3O4MNPs (m∶m′) =20∶1时,混合单层膜中可见明显的OA-Fe3O4MNPs颗粒状结构(图2(b)),颗粒之间存在黑色间隙,而在图2(a)中出现过的圆形微区消失。BAM图像中还存在面积较大的明亮区域(见红色圈标记)。根据BAM成像原理可知上述标记区域中膜的厚度显著增加,推测这是由于DPPG与OA-Fe3O4MNPs形成了复合体。随着OA-Fe3O4MNPs浓度的增加(10∶1和8∶1),BAM图像呈现出大量的颗粒结构(图2(c),(d))。但当DPPG:OA-Fe3O4MNPs(m∶m′)=2∶1时,膜中颗粒状结构消失(图2(e))。当π=25 mN/m时,单层膜的BAM图像如图2(a′)-(e′)所示。纯DPPG单层膜在该表面压下处于LC相(图1(b)),界面上整齐排列的圆形微区结构消失,形成均匀的单层膜(图2(a′)),其界面分子的可能排列如图3(a)所示。当DPPG:OA-Fe3O4MNPs (m∶m′)=20∶1和10∶1时,单层膜中的颗粒状结构排列得更加紧密(图2(b′),(c′)),且质量比10∶1单层膜的BAM图像中明亮区域的数量更多、面积增大,这说明随着MNPs浓度的增加,单层膜中形成的复合体增多,单层膜部分区域的厚度增加。当质量比为8∶1时,单层膜的BAM图像右上角区域的亮度明显高于左下角(图2(d′)),说明在复合体持续增多的过程中,复合体与DPPG分子出现相分离现象,导致单层膜的厚度不均。在质量比为2∶1的BAM图像中没有出现明显的相分离现象,界面上形成了均匀、致密的单层膜(图2(e′)),但与图2(a′)中的DPPG单层膜相比,混合单层膜的亮度增大,这表明大量的DPPG-OA-Fe3O4MNPs复合体与DPPG在界面形成了混合膜,界面上可能的分子组成如图3(d)所示。
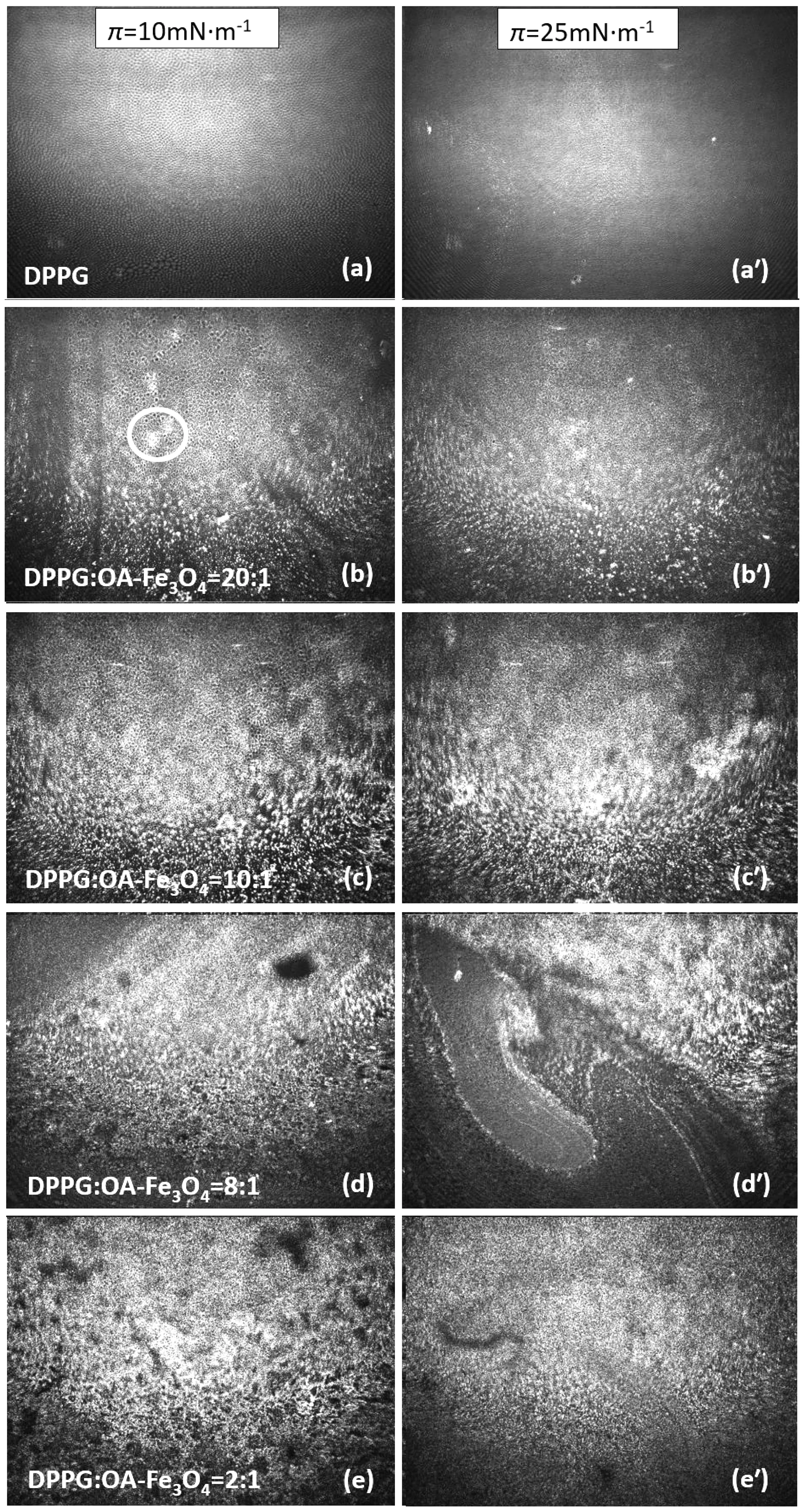
图2 DPPG与OA-Fe3O4 MNPs混合单层膜的BAM图像Fig.2 BAM images of mixed monolayers of DPPG and OA-Fe3O4 MNPs: (a),(a′)DPPG,(b),(b′)DPPG:OA-Fe3O4 MNPs(m:m′)=20∶1,(c),(c′)10∶1, (d),(d′)8∶1,(e),(e′)2∶1
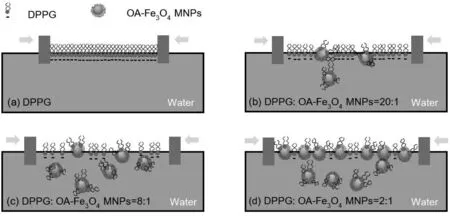
图3 混合单层膜的界面行为示意图Fig.3 The schematic diagram of mixed monolayers at the interface: (a)DPPG,(b)DPPG:OA-Fe3O4 MNPs(m∶m′)=20∶1,(c)8∶1,(d)2∶1
2.2 DPPG与OA-Fe3O4 MNPs混合单层膜的动力学研究
为了研究磁性OA-Fe3O4MNPs对DPPG单层膜结构稳定性的影响,测量了OA-Fe3O4MNPs掺入DPPG单层膜的动力学信息。图4(a)给出了π=25 mN/m时,OA-Fe3O4MNPs与DPPG单层膜分子间相互作用过程的表面压-时间曲线(Δπ-t)。随着时间增加,表面压均呈现逐渐减小的趋势。经历1 h,Δπ随OA-Fe3O4MNPs浓度的变化情况如图4(b)所示。纯DPPG单层膜的表面压在1h内变化很小,约减小了3.5 mN/m,这主要归因于界面有微量的磷脂分子损失进亚相中。而在DPPG单层膜中掺入OA-Fe3O4MNPs后,随着MNPs浓度增加,Δπ变大。当DPPG: OA-Fe3O4MNPs(m∶m′)=8∶1时,Δπ达最大,约7.8 mN/m,这是由于界面上的DPPG分子与OA-Fe3O4MNPs形成复合体[22],减小了DPPG分子在界面的占有面积,表面压随之降低,如图3(b),(c)所示。另有部分复合体从界面损失到亚相,导致表面压持续减小[19,22-23]。当DPPG:OA-Fe3O4MNPs(m∶m′)=2∶1时,表面压减小约5 mN/m,这是由于DPPG与高浓度的OA-Fe3O4MNPs形成大量复合体,在部分复合体损失到亚相后,界面上仍吸附有大量复合体,因此与质量比8∶1的单层膜相比,表面压下降幅度有所减小(图3(d))。
在研究DPPG单层膜的压缩-扩张动态过程时,首先将DPPG单层膜压缩至50 mN/m(避免单层膜完全崩溃),随即扩张循环。在压缩过程中,部分DPPG从界面挤出,但扩张后又会缓慢地重新吸附到界面上,这导致DPPG单层膜的压缩和扩张曲线中出现滞回现象(图5(a)),这一现象也出现在循环压缩DPPC单层膜的实验中[17]。利用压缩-扩张循环实验进一步研究了OA-Fe3O4MNPs在DPPG单层膜中的挤出和再吸附过程(图5(b)-(d))。在DPPG:OA-Fe3O4MNPs(m∶m′)=10∶1和8∶1的单层膜中,扩张曲线存在明显滞后现象(图5(b),(c)),说明界面上有分子被挤出到亚相,这与动力学研究结果一致(图4(a));3次压缩-扩张曲线基本重合,特别是在高表面压区(π>20 mN/m)完全重合,这表明从界面挤出的分子依然会缓慢地重新吸附到界面上,空气-水界面上的膜组分具有动态稳定性[19,24]。值得注意的是,当DPPG∶OA-Fe3O4MNPs (m∶m′)=2∶1,表面压π>28 mN/m时,第2、3次压缩-扩张曲线向平均分子面积更大的方向移动。增加循环次数,发现第4、5次压缩-扩张曲线亦有相同的移动现象(图5(d))。这可能与DPPG-OA-Fe3O4MNPs复合体的形成有关,形成复合体的DPPG分子和MNPs在扩张过程中并不能重新分开,而再次压缩时又有新的复合体形成,最终导致曲线在高表面压区间向右移动。实验中,DPPG-OA-Fe3O4MNPs复合体的形成可能受表面压和OA-Fe3O4MNP浓度的共同影响,为此我们考察了DPPG:OA-Fe3O4MNPs(m∶m′)=5∶1的体系,发现压缩-扩张曲线在第2、3次的压缩-扩张仍然向右移(图5(c)插图)。

图4 混合单层膜在固定表面积下的Δπ-t曲线(a)及弛豫1h后Δπ随MNPs浓度的变化情况(b)Fig.4 Δπ-t curves of mixed monolayer at constant A and the variation of Δπ with the concentration of MNPs after relaxation for 1 h

图5 混合单层膜的压缩-扩张曲线Fig.5 Compression-expansion curves of mixed monolayers: (a)DPPG,(b)DPPG:OA-Fe3O4 MNPs (m∶m′)=10∶1,(c)8∶1,(d)2∶1
2.3 DPPG与OA-Fe3O4 MNPs混合单层膜的流变响应
为了分析OA-Fe3O4MNPs对空气-水界面上DPPG单层膜粘弹性的影响,测量了在固定应变(u0=ΔA/A=5%)、固定表面压(25 mN/m)和恒定频率(f=20,50,100 mHz)下单层膜的振荡曲线。控制滑障以恒定频率f振荡,平均分子面积的应变为[25-26]:
ut=A0[1+u0sin(2πft+φu)]
(1)
则单层膜的应力为[26]:
πt=π0+π1sin(2πft+φπ)
(2)
式中:A0为π0=25 mN/m时的平均分子面积,π1为应力幅值,φu、φπ分别为ut、πt的相位。振荡过程中单层膜的扩张弹性模量E′和粘性模量E″有如下关系[26]:
(3)
式中:E*是单层膜的扩张粘弹性,φ=φu-φπ是应力与应变的相位差。
实验发现,应力与应变曲线的相位差均为φ=0,代入公式(3)可知扩张粘弹性中的虚部为零,这表明该混合单层膜的粘弹性以弹性为主[26]。图6给出了DPPG: OA-Fe3O4MNPs(m∶m′)=20∶1,振荡频率为20mHz时单层膜的应变、应力实验曲线(虚线),利用公式(2)对应力曲线进行拟合(图6(b)实线),结果显示实验曲线与拟合曲线基本吻合,但值得注意的是实验曲线在峰值处出现畸变,这表明单层膜在振荡过程中的应力可能存在非线性响应[27]。利用快速傅里叶变换(FFT)对应力曲线进行频谱分析,发现频谱中存在2次谐波、3次谐波和5次谐波(图6(c)),这证实了单层膜应力对应变的非线性响应[12]。上述现象也存在于其它几种质量比和振荡频率的实验体系中。综上,DPPG单层膜中掺入OA-Fe3O4MNPs后,单层膜的应力对应变存在非线性响应。

图6 振荡实验中的应变曲线(a);表面压的应力曲线(b);应力曲线的FFT频谱(c)Fig.6 (a) Strain curve in oscillation experiment; (b) stress curve of surface pressure; (c)FFT spectrum of stress cure
为了进一步研究OA-Fe3O4MNPs浓度与单层膜应变响应的关系,测绘了3个振荡周期的应力与应变关系曲线,得到应力-应变李萨如图(图7)[27-28]。图7显示,各单层膜3个周期的李萨如图均相互重合。对于纯DPPG单层膜,各频率的李萨如图均表现为正滞回曲线(图7(a)-(a″)),说明在振荡过程中,压缩使单层膜中的DPPG分子排列更加有序,表面压增大[25];振荡频率越高,李萨如图的滞回面积越大,这说明单层膜的粘性有所增加[29];虽然DPPG单层膜是弹性膜,但当振荡频率较高时(100 mHz),振荡压缩首先使单层膜的有序性增加,表面压增大,然而界面快速扩张时表面压降低的速度比压缩时表面压增大的速度慢,导致李萨如图的滞回面积增加,反应了单层膜存在微弱的粘性特征。
图7(b)-(e),(b′)-(e′),(b″)-(e″)显示,4种不同质量比例混合的单层膜在各振荡频率下的李萨如图均出现交叉现象,说明单层膜应力对应变的响应均是非线性的,这是由于OA-Fe3O4MNPs破坏了DPPG单层膜的均匀性(如图2(d′)),引起了应力的非线性响应,这与a-PMMA单层膜体系相似[25]。当DPPG:OA-Fe3O4MNPs(m∶m′)=2∶1时,混合单层膜的李萨如图均呈现负滞回曲线(图7(f)-(f″)),这是由于在振荡过程中,压缩使单层膜的部分分子从界面挤出,表面压降低[25]。负滞回曲线中没有出现交叉现象,且压缩和扩张曲线的对称性优于其他比例的混合单层膜,说明该条件下单层膜的应力对应变响应的非线性成分减少,两种组分在空气-水界面形成了均匀致密的单层膜,这与BAM图像一致(图2(e′))。

图7 DPPG与OA-Fe3O4 MNPs混合单层膜的李萨如图,箭头表示李萨如图的前进方向Fig.7 Lissajous plots of mixed monolayer of DPPG and OA-Fe3O4 MNPs. An arrow in the figure indicates the forward direction of the Lissajous plots: (a)-(a″)DPPG,(b)-(b″)DPPG:OA-Fe3O4 MNPs(m∶m′)=30∶1,(c)-(c″)20∶1,(d)-(d″)10∶1,(e)-(e″)5∶1,(f)-(f″)2∶1
即使实验考虑的条件与典型的呼吸周期(更高的频率和变形幅度)还有很大区别,但是探索纳米颗粒对DPPG单层膜的影响有助于评估纳米颗粒对生物膜,特别是肺表面活性膜功能的影响。通过分析粘弹性模量的频率依赖性来探索单层膜的流变响应,能够获得纳米颗粒对磷脂单层膜平衡过程中所涉及的弛豫机制的影响信息[30]。
利用式(4)由应力-应变曲线可得单层膜的粘弹性模量[26],根据公式(5)对粘弹性模量的实验值进行理论拟合[12,15,30]:
(4)
(5)
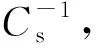


图8 DPPG与OA-Fe3O4 MNPs混合单层膜在不同频率下的粘弹性模量,图中实线为根据(5)式拟合的理论曲线Fig.8 Viscoelastic modulus of DPPG and OA-Fe3O4 MNPs mixed monolayers at different frequencies. The solid lines in the figure are the theoretical curves fitted according to formula(5)∶ (a)DPPG,(b)DPPG∶OA-Fe3O4 MNPs(m∶m′) =20∶1,(c)10∶1,(d)2∶1

图9 特征频率与OA-Fe3O4 MNPs浓度的关系Fig.9 Relaxation frequency dependences of concentration of OA-Fe3O4 MNPs
为了探明OA-Fe3O4MNPs浓度对单层膜弛豫过程的影响,图9给出了特征频率f1随OA-Fe3O4MNPs浓度的变化关系[15]。在实验频率范围内,随着单层膜中OA-Fe3O4MNPs浓度的增加,f1在10-3Hz上下波动。由此可知,当π=25 mN/m、振荡频率在10-3~10-1Hz之间时,DPPG与OA-Fe3O4MNPs混合单层膜弛豫过程的时间尺度受OA-Fe3O4MNPs浓度的影响并不显著。
3 结 论