吉非替尼联合新辅助化疗对ⅢA 期EGFR突变型非小细胞肺癌患者血清肿瘤标志物和远期预后的影响
刘方方,吴勇奇,吴文耀,李荟苹
河南大学第一附属医院呼吸与危重症医学科一病区,开封 475000
肺癌是全球发病率排名第2 位的恶性肿瘤,其具有发病率高、疗效差、5 年生存率低的临床特点[1]。目前,我国肺癌发病率为57.3/10 万,死亡率为45.9/10 万,位居恶性肿瘤死亡原因的首位[2]。肺癌主要包括非小细胞肺癌(non-small cell lung cancer,NSCLC)和小细胞肺癌,其中NSCLC占80%以上[2-3]。目前,针对肿瘤负荷大、淋巴结转移、血管侵犯能力强以及手术风险高的ⅢA 期NSCLC 患者,新辅助化疗联合根治性手术治疗仍是其最佳的治疗方式。新辅助化疗可降低肿瘤负荷以及临床分期,提高手术切除率,但治疗效果仍不理想[4-5]。因此,如何降低中晚期NSCLC 患者的手术风险、提高患者临床疗效、降低术后复发转移率已成为临床亟待解决的热点问题。表皮生长因子受体(epidermal growth factor receptor,EGFR)突变是常见的肺腺癌驱动突变之一,已成为其分子治疗的重要靶点。研究显示,亚洲NSCLC 患者的EGFR突变率约30%~50%,而EGFR酪氨酸激酶抑制剂可显著延长EGFR突变型中晚期 NSCLC 患者的生存期[6]。吉非替尼作为EGFR酪氨酸激酶抑制剂和NSCLC 的靶向治疗药物,相较于铂类化疗药物具有高效、毒性较低的特点,多用于EGFR突变型中晚期非NSCLC 的二、三线治疗[7-9]。基于此,本研究选取吉非替尼术前辅助化疗ⅢA 期EGFR突变型NSCLC 患者,探讨其对手术切除的NSCLC患者远期疗效以及血清肿瘤标志物表达水平的影响,现报道如下。
1 资料与方法
1.1 一般资料
选取2016 年1 月~2017 年1 月期间于该院行手术切除治疗的104 例ⅢA 期EGFR突变型NSCLC 患者作为研究对象,按照随机数字表法分为对照组和研究组,每组52 例。对照组:男性32 例,女性20 例,年龄34~67 岁,平均年龄(54.3±6.8)岁,体重指数19.1~24.8kg/m2,平均体重指数(22.7±2.1)kg/m2。研究组:男性34 例,女性18 例,年龄35~68 岁,平均年龄(55.9±7.2)岁,体重指数18.7~25.0kg/m2,平均体重指数(23.5±2.5)kg/m2。两组患者性别、年龄、体重指数等一般资料比较无统计学差异(P>0.05),具有可比性(表1)。本研究经本院伦理委员会批准,所有患者及家属均知情同意。
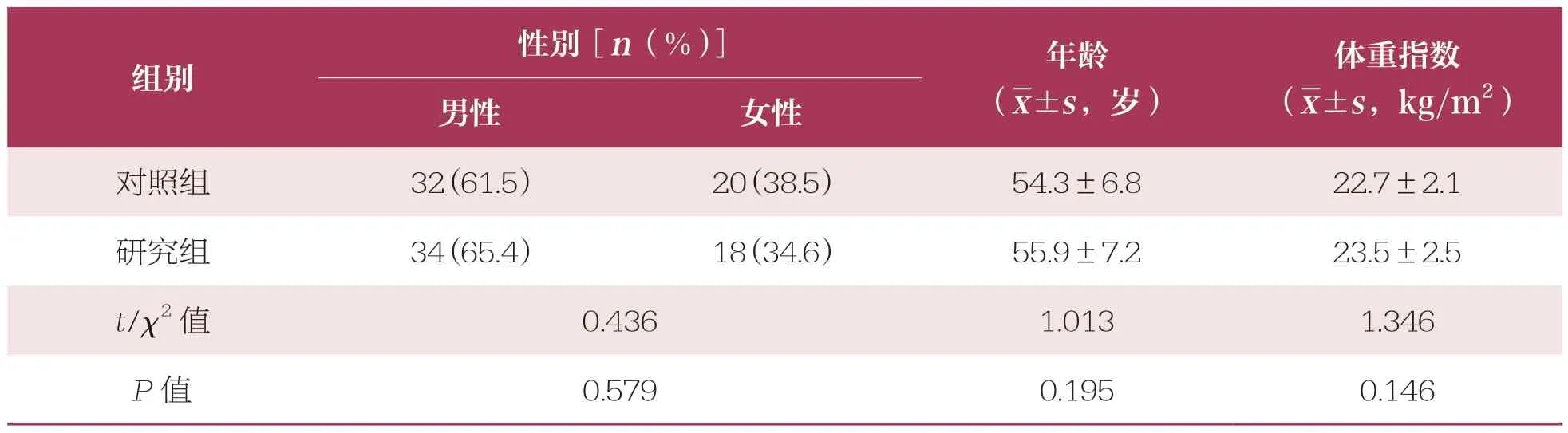
表1 两组一般资料比较 n=52
纳入标准:①术前经支气管镜活检初次确诊为NSCLC 者。②病灶局限于一侧,胸腔无远处转移者。③术前综合评估临床分期为ⅢA 期者。④术前检测为EGFR突变型者。⑤卡诺夫斯凯计分(Kanofsky performance score,KPS)> 80 分者。
排除标准:①合并严重心、肝、肾、血液、免疫系统疾病者。②术前经临床和影像学检查确诊存在广泛淋巴结转移、胸膜转移或远处脏器转移者。③术前检测为EGFR野生型者。④一般情况差,无法耐受手术治疗者。⑤术后不能配合随访者。
1.2 研究方法
对照组术前给予紫杉醇+奈达铂新辅助化疗并联合手术切除治疗,紫杉醇注射液(广东星昊药业有限公司,国药准字H20084439,规格5ml ∶30mg)135mg/m2,于第1 天静脉滴注;注射用奈达铂(吉林恒金药业股份有限公司,国药准字H20051482, 规格100mg)80mg/m2, 于第1天~第5 天静脉滴注,21 天为1 个周期,术前化疗 2 个周期。化疗结束1 个月后复查血常规、肝肾功能、胸腹部计算机断层扫描术(computer tomo-graphy,CT),确定无手术禁忌症后给予根治性手术治疗。研究组在对照组基础上术前加用吉非替尼片[齐鲁制药(海南)有限公司,国药准字H20163465,规格0.25g]辅助化疗,口服,每次250mg,qd, 28 天为1 个周期,术前给予1 个周期,其他治疗同对照组。两组患者术后2 周均给予紫杉醇+奈达铂辅助化疗+普通外照射放疗+吉非替尼辅助靶向治疗:给予紫杉醇+奈达铂辅助化疗2 个周期;给予普通外照射,剂量 45~50Gy,5~6 周;给予吉非替尼辅助靶向治疗,每次 250mg,qd,持续24 个月。
1.3 观察指标
(1)临床资料。记录患者一般临床资料,如年龄、性别、体重指数、吸烟情况等;记录患者肿瘤相关资料,如病理类型、TNM/T 分期、淋巴结转移、微血管侵犯;记录患者手术相关信息,如手术时间、术中出血量。
(2)血清肿瘤标志物及血管内皮生长因子。分别于治疗前(新辅助化疗前)和治疗后(新辅助化疗完成后2 周)采集患者清晨空腹肘静脉血 5ml,置于抗凝管中,采用KH19A 离心机(湖南凯达科学仪器有限公司,r=10cm),3500r/min、4℃离心20min,取上清液,低温储存。采用BDTeCLXP 电化学发光仪(日本日立公司)检测两组患者血清肿瘤标志物癌胚抗原(carcinoembryonic antigen,CEA)、血清铁蛋白(serum ferritin,SF)、糖类抗原125(carbohydrate antigen 125,CA125)表达水平,试剂盒由德国罗氏公司提供。采用BK-EL10A 酶联免疫分析仪(济南欧莱宝生物技术有限公司)检测两组患者血管内皮生长因子(vascular endothelial growth factor,VEGF)表达水平,试剂盒购自上海酶联生物科技有限公司。
(3)随访。所有患者术后均随访5 年,记录术后5 年内肿瘤复发转移时间和患者死亡时间,并记录相应的无病生存时间和总生存时间。
1.4 统计学方法
应用SPSS 25.0 软件对数据进行分析处理。计量资料以±s 表示,行t检验;计数资料以n(%)表示,行χ2检验;Kaplan-Meier 生存分析两组患者术后5 年无病生存率和总生存率。P<0.05 为具有统计学差异。
2 结果
2.1 基线资料
两组患者吸烟、病理类型、TNM/T 分期、TNM/N 分期、微血管侵犯、手术时间以及术中出血量比较均无统计学差异(P>0.05)(表2)。

表2 两组基线资料比较 n=52
2.2 血清肿瘤标志物及VEGF
治疗前,两组血清CEA、CA125、SF 以及VEGF 水平比较均无统计学差异(P>0.05);治疗后,对照组血清SF 水平较治疗前降低(P<0.05),研究组血清CEA、CA125、SF 以及VEGF 水平较治疗前均降低(P<0.05)(表3)。
表3 两组血清肿瘤标志物水平比较 n=52,±s
CEA:癌胚抗原;CA125:糖类抗原125;SF:血清铁蛋白;VEGF:血管内皮生长因子;与同组治疗前比较,a:P<0.05
CEA(μg/L)CA125(U/ml)SF(μg/L)VEGF(ng/L)治疗前治疗后治疗前治疗后治疗前治疗后治疗前治疗后对照组 21.4±3.7 20.3±3.5 33.6±4.1 32.7±3.3 234.5±32.5 212.7±30.9a 145.6±32.7 141.8±30.2研究组 22.6±3.5 17.2±2.9a 32.7±3.9 28.5±3.2a 229.4±34.6 195.7±28.6a 148.5±31.6 108.6±25.3a t 值0.6752.3450.6632.1780.9872.0160.7346.789 P 值0.4890.0170.5120.0230.2780.0320.3480.000组别
2.3 术后并发症
两组患者术后主要并发症肺部感染、肺不张、支气管胸膜瘘、出血、切口感染以及吻合口狭窄发生率比较均无统计学差异(P>0.05)(表4)。

表4 两组术后主要并发症比较 n=52,n(%)
2.4 术后5 年无病生存率
两组患者术后5 年无病生存率比较具有统计学差异(P<0.05),且研究组患者术后1 年、3 年及5年累积无病生存率均高于对照组(P<0.05)(图1)。
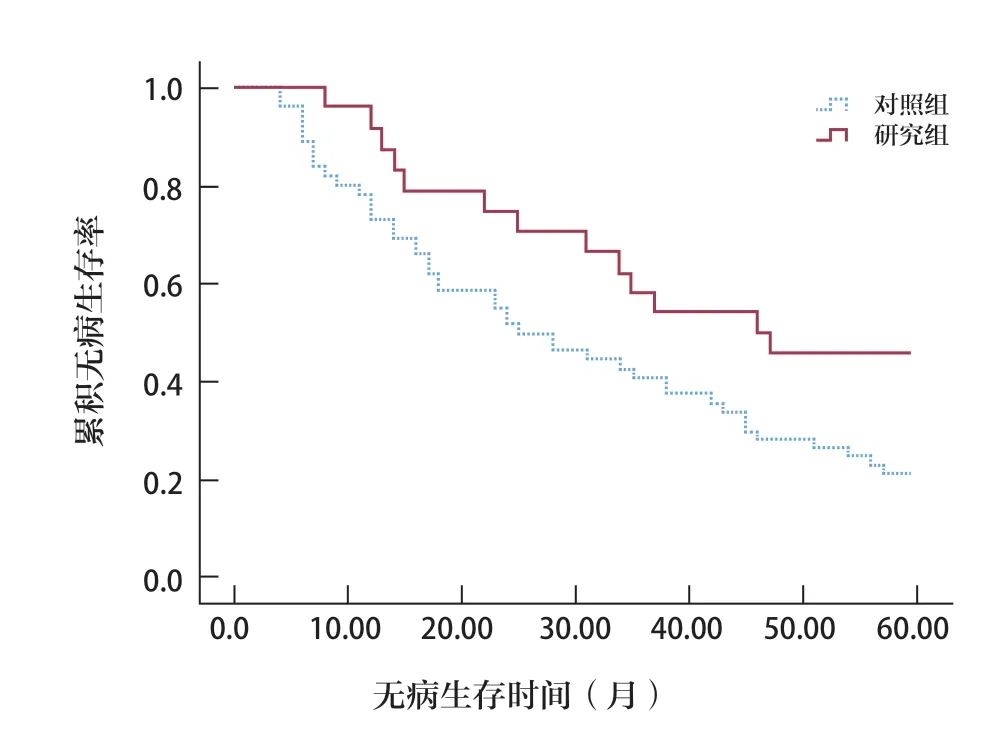
图1 两组术后5 年无病生存率比较
2.5 术后5 年总生存率
两组患者术后5 年无病生存率比较具有统计学差异(P<0.05),且研究组患者术后1 年、3 年及5年累积总生存率均高于对照组(P<0.05)(图2)。

图2 两组术后5 年总生存率比较
3 讨论
近年来,随着医疗技术的发展和分子靶向药物的不断开发使用,ⅢA 期NSCLC 患者的预后较10年前明显改善,但总体生存率仍不理想。即使患者接受了新辅助化疗联合手术治疗,但术后较高的复发转移率仍制约着患者生活质量和远期生存率的提高[9-11]。因此,对于ⅢA 期NSCLC 患者,选择安全有效的治疗方法以提高手术疗效及降低术后复发转移率尤为重要。有研究报道[2],ⅢA 期NSCLC患者的EGFR突变率约为30%~50%,其推荐的治疗方法为新辅助化疗+根治性手术切除+术后辅助性放化疗+分子靶向治疗。研究显示[12-16],吉非替尼治疗伴有EGFR突变型NSCLC 患者取得了较好的疗效,可显著提高EGFR突变型NSCLC 患者的生存期。相关研究证实[17-19]对于具有肿瘤负荷较大、多发性病灶、淋巴结转移、肿瘤侵袭较强等情况的NSCLC 患者,于术前加用吉非替尼辅助化疗可显著降低手术风险,提高手术疗效。Zhao 等[20]的研究结果显示,吉非替尼联合放化疗治疗中晚期NSCLC 可明显缩小患者病灶体积,减少放化疗治疗的不良反应,提高患者的耐受性。但关于术前加用吉非替尼辅助化疗对ⅢA 期EGFR突变型NSCLC患者的术后远期生存情况以及血清肿瘤标志物表达水平的影响未见报道。
CEA、CA125、SF 以及VEGF 为公认的NSCLC 血清肿瘤标志物[21-23]。相关研究[21-23]显示,与健康人群相比, NSCLC 患者血清CEA、CA125、SF 以及VEGF 表达水平明显升高,提示NSCLC 患者肿瘤负荷较大和肿瘤侵袭转移能力较强。本研究结果显示,加用吉非替尼术前辅助化疗的患者治疗后血清CEA、CA125、SF 以及VEGF表达水平较治疗前均降低(P<0.05),且以上各指标水平均低于对照组(P<0.05),提示加用吉非替尼术前辅助化疗可降低血清肿瘤标志物表达水平,早期消除和控制NSCLC 亚临床型转移灶,降低肿瘤负荷和TNM 分期,提高手术切除率和肿瘤局部控制率,从而降低手术风险和提高手术疗效。
此外,本研究对纳入的所有NSCLC 患者进行了术后5 年的随访发现,术前加用吉非替尼辅助化疗的NSCLC 患者术后1 年、3 年及5 年累积无病生存率和总生存率均高于对照组(P<0.05),提示术前加用吉非替尼辅助化疗可明显降低患者术后复发转移风险,提高患者术后生存期。其原因可能为:吉非替尼可特异性地作用于EGFR突变阳性靶点,抑制和杀灭肿瘤细胞,降低肿瘤负荷和TNM 分期,从而提高手术切除率;同时吉非替尼可使肿瘤血管闭塞,阻断肿瘤供血,抑制肿瘤细胞增殖,减少肿瘤微转移,从而降低术后复发转移风险[13,24]。本研究结果显示,术前加用吉非替尼辅助化疗治疗对ⅢA 期EGFR突变型NSCLC 患者疗效确切。但本研究也存在一定局限性,如研究选取的样本量较小,后续仍需大样本前瞻性的随机对照研究进一步证实。
综上所述,吉非替尼联合新辅助化疗可降低ⅢA 型EGFR突变型NSCLC 患者血清肿瘤标志物表达水平,提高患者术后无病生存率和总生存率,值得临床推广应用。

