血清HBsAg、HBV RNA水平对慢性乙型肝炎患者核苷(酸)类药物治疗停药预测的价值
吴宝灵,徐 龙,余海滨,徐贞秋,吴 敏,张 伟,范声春,李艳艳,李金明
(南昌市第九医院肝二科,南昌 330002)
在我国,慢性乙型肝炎(CHB)患者主要使用核苷(酸)类似物(NAs)药物治疗,而临床上多以血清乙型肝炎表面抗原(HBsAg)消失作为评价CHB“临床治愈”和停药的标准,但现有的NAs药物治疗很少能使血清HBsAg阴转,为减少停药带来的病毒学反弹和疾病复发,各国CHB防治指南多强调患者需要长期甚至终身用药,而实际上有部分患者停药后并不会反弹。将血清HBsAg持续消失作为功能性治愈或临床治愈的判定标准,可能会使一些患者继续接受不必要的抗病毒治疗[1]。目前,临床上仍缺乏甄别和确定CHB患者安全停药的可靠指标。本研究拟探讨NAs停药时血清HBsAg和乙型肝炎病毒核糖核酸(HBV RNA)水平与停药复发的关系,为CHB患者安全停药提供参考。
1 资料与方法
1.1 一般资料
回顾性分析2019年6月至2020年6月南昌市第九医院肝病科治疗的80例接受NAs治疗并符合停药标准、已停药并配合随访的CHB患者临床资料。纳入标准:1)CHB治疗、停药均符合2019版《慢性乙型肝炎防治指南》[2]标准,达到乙型肝炎e抗原(HBeAg)阴性或乙型肝炎e抗体(HBeAb)阳性后,丙氨酸氨基转氨酶(ALT)正常、乙型肝炎病毒脱氧核糖核酸(HBV DNA)<20 U·mL-1、巩固治疗至少3年,总疗程不少于4年的患者;2)为初次接受单一NAs治疗,无变异耐药。排除标准:1)妊娠期及哺乳期女性;2)治疗前无肝硬化或疑似肝硬化、肝衰竭的患者;3)合并恶性肿瘤或自身免疫缺陷疾病;4)合并其他病毒感染、自身免疫性肝病、药物性肝损伤及长期吸毒、酗酒的患者。
1.2 研究方法
收集患者停药时的性别、年龄、体重指数(BMI)、病程、HBV感染家族史、饮酒史、HBV基因型、基线ALT、基线HBV DNA、基线HBV RNA、总疗程等。
选择停药时HBV DNA<20 U·mL-1,HBsAg定量<200 U·mL-1和HBsAg定量200~1000 U·mL-1的患者各40例进行随访,同时进行HBV RNA检测。停药后3个月内每月检测1次血生化、HBsAg定量、HBV DNA、HBV RNA,此后每3个月检测1次,停药1年后,每半年检测1次,同时每半年复查甲胎蛋白(AFP)及腹部彩超,共随访3年或病毒反弹(复发)时研究终止。比较HBV RNA阴性与HBV RNA阳性,HBsAg定量<200 U·mL-1和HBsAg定量200~1000 U·mL-1的患者停药后复发情况。
本研究在充分告知停药后风险的情况下开展,一旦确定出现病毒反弹,根据情况及时再次给予抗病毒治疗并停止随访。病毒反弹的标准:若检测到HBV DNA>100 U·mL-1,伴或不伴ALT升高,定义为病毒学反弹。
1.3 检测方法
1)生化检测:选择日本日立7600型全自动生化分析仪进行诊断。
2)HBsAg定量:使用罗氏试剂进行化学发光法检测,HBsAg检测下限为0.05 U·mL-1。
3)HBV DNA定量:使用罗氏COBAS TaqMan病毒载量检测系统进行荧光定量PCR的检测,检测下限为20 U·mL-1。
4)HBV RNA定量:使用湖南圣湘生物科技有限公司HBVpgRNA试剂盒进行检测,检测下限为100 U·mL-1。
1.4 统计学方法

2 结果
1)以随访期间是否出现病毒反弹分为复发组和无复发组,2组患者年龄、性别、BMI、病程、HBV感染家族史、饮酒史、HBV基因型、基线ALT、基线HBV DNA、基线HBV RNA以及总疗程对比,差异均无统计学意义(P>0.05)。见表1。
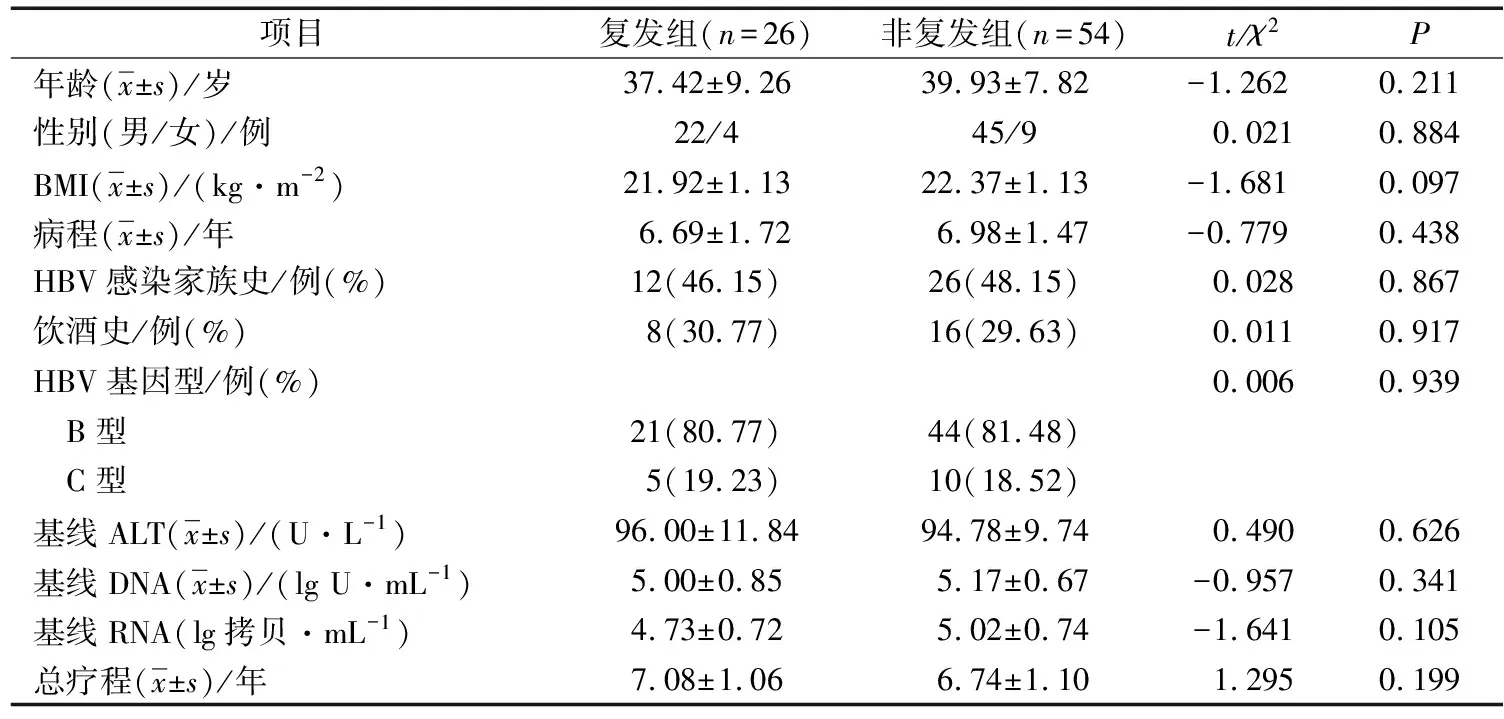
表1 2组患者一般资料以及实验室指标比较
2)依据HBsAg定量<200 U·mL-1和HBsAg定量200~1000 U·mL-1分组,2组患者停药3年时的复发情况比较差异有统计学意义(P<0.05)。见表2。
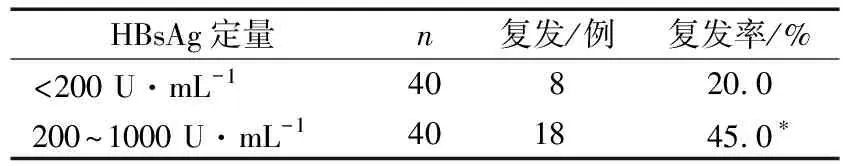
表2 停药时HBsAg定量分组的复发情况比较
3)依据停药时HNV RNA载量<100 U·mL-1和>100 U·mL-1分组,2组患者停药3年时的复发情况比较差异有统计学意义(P<0.05)。见表3。
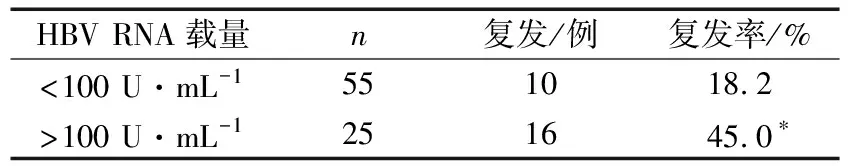
表3 停药时HBV RNA载量分组的复发情况比较
4)依据停药时HBsAg定量及HBV RNA载量分组,同时具备HBsAg<200 U·mL-1、HBV RNA<100 U·mL-1为A组,其余均为B组,A、B 2组停药3年的复发情况比较差异有统计学意义(P<0.05)。见表4。
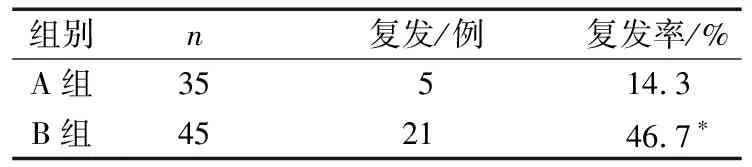
表4 停药时HBsAg定量以及HBV RNA载量分组的复发情况比较
3 讨论
随着扩大CHB抗病毒治疗逐渐推广,越来越多的患者需要抗病毒治疗,其中大多数使用NAs抗病毒治疗。由于NAs治疗没有明确的停药标准,降低了患者的依从性。近年来,很多学者围绕NAs治疗CHB患者停药后的复发、预测因素以及安全性等问题进行研究,但有关其复发率报道存在很大差异(15%~97%)[3]。如何实现安全停药、减少复发,需要更多的研究来优化现有的停药标准。血清中HBsAg定量检测,不仅反映病毒与肝细胞的免疫应答的平衡关系,也能反映共价闭合环状DNA(cccDNA)的复制水平,NAs治疗只是抑制了HBV DNA的复制,但对于肝细胞内的cccDNA没有清除作用,停药后会出现病毒学反弹。王昌生等[4]报道,应用HBsAg定量检测预测恩替卡韦停药后CHB患者复发具有较高的诊断效能。CHEN等[5]研究HBsAg水平与复发之间的关系,治疗末HBsAg水平(<150 U·mL-1)与较低的病毒学复发率有关,患者HBsAg水平可用于指导治疗的停药时机。曹佳伟[6]报道,停药时HBsAg≤200 U·mL-1的患者发生临床复发的可能性更小。本研究显示,停药时血清高敏HBV DNA<20 U·mL-1,HBsAg定量<200 U·mL-1和HBsAg定量200~1000 U·mL-1的患者,停药3年时的复发率分别为20%和45%,差异有统计学意义(P<0.05),可能是安全停药的预测指标,指导停药有一定的作用,但还是有局限性。
NAs的作用机制是竞争性抑制HBV DNA聚合酶的活性,从而抑制HBV复制,但不能清除肝内cccDNA,由于HBV cccDNA检测需要进行肝组织活检,限制了其在临床上的应用。有研究[7]证实,血清中的HBV RNA来自感染细胞内cccDNA的活性转录,特别是在接受NAs治疗的CHB患者,DNA合成被阻断后,其血清中的HBV RNA能反映肝细胞内cccDNA的状态。当血清中检测不到HBV RNA时,提示患者肝细胞内cccDNA的消失或者转录静默,预示着可以安全停药[8-9]。张琪等[10]报道,血清HBV RNA对于预测CHB患者停药后复发有重要意义。相比于HBsAg、HBV DNA等传统的血清学指标,血清HBV RNA水平可以更好地反映肝内病毒复制水平,可作为CHB患者管理的新型标志物[11]。WANG等[12]报道,在治疗停止后24周,21例HBV RNA阳性患者均发生病毒学反弹,然而在HBV RNA低于检测下限的12例CHB患者中,有3例发生病毒学反弹。本研究显示,根据HBV DNA<20 U·mL-1、HBV RNA<100 U·mL-1停药时,停药3年时的复发率仍有18.2%,提示可能需要多个病毒学标志物联合指导停药。
目前,多数学者证实NAs治疗后停药复发与多种因素有关。有研究[13]表明,监测血清HBV RNA水平也可预测经抗病毒治疗后实现HBsAg消失即“临床治愈”的CHB患者出现病毒反弹的风险。最新研究[14]提出以HBV cccDNA消失或静默为基础,以HBV RNA持续阴性和低HBsAg水平为标准的“准临床治愈”,可作为抗病毒治疗的新阶段终点,对指导CHB患者安全用药、停药及疗效预测等方面可能有重要意义。本研究在停药时血清HBV DNA<20 U·mL-1的前提下,根据停药时HBsAg定量及HBVRNA载量分组,同时具备HBsAg<200 U·mL-1、HBV RNA<100 U·mL-1为A组,其余均为B组,结果显示停药3年时A组有14.3%(5/35)复发,B组复发率为46.7%(21/45),2组比较差异有统计学意义(P<0.05)。提示HBV DNA<20 U·mL-1的同时,HBsAg<200 U·mL-1、HBV RNA<100 U·mL-1作为NAs治疗停药指标比较安全,HBsAg、HBV RNA水平对CHB患者停药时机的判断具有一定的参考意义。当然,由于本研究的样本量较少,相关结论还有待于扩大样本量进一步研究论证。

