植物乳杆菌固体发酵对复方中药中有效成分含量的影响
侯楠楠,谢全喜*,王俊贤,王 倩,王 梅,谷 巍
(山东宝来利来生物工程股份有限公司 山东省动物微生态制剂重点实验室,山东 泰安 271000)
近年来我国畜牧业得到快速发展,广大农牧科技人员在开发利用中草药资源、促进农牧业发展方面,取得了一定成果[1]。2013年,农业部修订的《饲料原料目录》将115种中草药列入饲用植物原料目录。2020年我国规定,退出除中药外的所有促生长类药物饲料添加剂品种。因此,开发中草药饲料添加剂替代抗生素成为行业研究的热点。
我国是中药生产大国,但随着中药材在人体及动物体上的广泛应用,中药也出现供不应求现象[2]。发酵是中药传统炮制工艺之一,工艺简单,发酵中药性质稳定,不易产生抗药性,避免了原料的浪费,提高了中药的利用率,可作为药食同源的饲料添加剂,是防治动物疾病、替代抗生素的理想选择[3-4]。王福刚[5]研究发现,日粮中添加5%复合益生菌培养物可以显著提高肉羊生长性能、血液中免疫球蛋白含量以及抗氧化活性。史洪涛等[6]研究发现,口服0.2%液体发酵中药蛋鸡的过氧化氢酶(catalase,CAT)、超氧化物歧化酶(superoxide dismutase,SOD)、总抗氧化能力(total antioxidant capacity,T-AOC)活性均显著高于对照组(P<0.05)。益生菌发酵中药可以使益生菌和中药协同增效,如李继开等[7]研究发现,利用植物乳杆菌(Lactobacillus plantarum)与枯草芽孢杆菌(Bacillus subtilis)对黄芪、绞股蓝、马齿苋3种中药构成的组方进行液体发酵,可显著提高中药粗多糖的含量。耿江苏[8]研究发现,使用益生菌发酵鱼腥草等中药,可提高中药益生菌数量至5.68×108CFU/mL。但中药成分错综复杂,目前研究比较多的主要是液体发酵,关于固体发酵中药作为饲料添加剂的报道比较少。
本研究使用3种植物乳杆菌对黄芪、甘草和益母草等复方中药进行固体发酵,研究其对复方中药微生物和有效成分的影响,以期为中药原料作为饲料添加剂提供数据支撑。
1 材料与方法
1.1 材料与试剂
1.1.1 材料与菌株
植物乳杆菌(Lactobacillus plantarum)BLCC2-0015、BLCC2-0126和BLCC2-0410:山东宝来利来生物工程股份有限公司菌种保藏中心;黄芪、茯苓、益母草、甘草和当归:泰安永春堂药店。
1.1.2 试剂
乳酸、阿魏酸、芦丁等标准品(纯度均>98%):上海源叶生物科技有限公司。其他试剂均为国产分析纯。
1.1.3 培养基MRS肉汤培养基、LBS培养基、伊红美蓝培养基、孟加拉红培养基:青岛海博生物技术有限公司。
1.2 仪器与设备
LC-20A高效液相色谱(high performance liquid chromatography,HPLC)仪、InertSustain AQ-C18色谱柱(5 μm,4.6 mm×250 mm):日本岛津公司;AL204电子分析天平:瑞士梅特勒托利多有限公司;GL21M高速冷冻离心机:湖南凯达科学仪器有限公司;CLDC271509超纯水净化系统(超纯水仪):重庆潺林热能设备有限公司;PHS-3C雷磁精密酸碱度计:上海精密科学仪器有限公司;SB120D超声波清洗机:宁波新芝生物科技股份有限公司。
1.3 方法
1.3.1 植物乳杆菌发酵液的制备
将4 ℃保存的植物乳杆菌(Lactobacillus plantarum)BLCC2-0015、BLCC2-0126和BLCC2-0410斜面活化,转接至装有100 mL MRS液体培养基的盐水瓶中,37 ℃静置培养24 h,活菌数均≥109CFU/mL,备用。
1.3.2 植物乳杆菌固体发酵复方中药
选择甘草、黄芪、茯苓、益母草和当归五味中药,按质量比4∶2∶2∶2∶1进行充分混合。按复方中药、麸皮和豆粕质量比为7∶2∶1配制基料。称取一定质量的基料,按照基料与水比为1.0∶0.5(g∶mL)配制好发酵底物,按100 g/袋进行装袋,每个处理设3个平行。分别按2.0%的接种量接入培养好的植物乳杆菌发酵液,以不接种任何菌株的空白料为对照组,压实后于37 ℃培养箱进行生料厌氧发酵,分别于发酵24 h、48 h和72 h取样,测定pH值、微生物含量、总酸含量、有机酸含量、甘草酸、粗多糖、总黄酮、阿魏酸和甘草次酸含量。
1.3.3 检测方法
pH值:准确称取10.00 g样品加入90 mL灭菌后的生理盐水中,搅拌均匀后静置10 min用玻璃电极pHS-3C型pH计测定。
微生物含量:准确称取10.00 g样品加入90 mL带有玻璃珠的无菌生理盐水中,振荡均匀,采用10倍梯度稀释法稀释,取适当稀释度的样品分别涂布于LBS培养基、孟加拉红培养基和伊红美兰培养基中,分别于37 ℃、30 ℃和37 ℃培养48 h、48 h和24 h。乳杆菌参照GB 4789.35—2016《食品安全国家标准食品微生物学检验乳酸菌检验》进行菌落计数;霉菌参照GB 4789.15—2016《食品安全国家标准食品微生物学检验霉菌和酵母计数》进行菌落计数;大肠杆菌(Escherichia coli)参照GB 4789.38—2012《食品安全国家标准食品微生物学检验大肠埃希氏菌计数》进行菌落计数。根据菌落数计算发酵中药中乳杆菌、霉菌和大肠杆菌的活菌数,结果用CFU/g表示。
总酸含量:参照国标GB/T 12456—2021《食品中总酸的测定》,采用酸碱滴定法测定。
有机酸含量:参照国标GB 5009.157—2016《食品安全国家标准食品中有机酸的测定》,采用高效液相色谱法测定。
粗多糖含量:参照牛晓方等[9]的方法,以葡萄糖质量浓度(x)为横坐标,吸光度值(y)为纵坐标,绘制葡萄糖标准工作曲线,得到葡萄糖标准曲线回归方程为y=0.010 3x-0.002 3(相关系数R2=0.999),根据标准曲线回归方程计算粗多糖含量。
总黄酮含量:参照GB/T 20574—2006《蜂胶中总黄酮含量的测定方法分光光度比色法》检测,以芦丁对照品的质量浓度(x)为横坐标,吸光度值(y)为纵坐标,绘制芦丁标准曲线,得到芦丁标准曲线回归方程为y=13x-0.000 6(相关系数R2=0.996 7),根据标准曲线回归方程计算总黄酮含量。
甘草酸、甘草次酸含量:参照SN/T3854—2014《出口食品中天然甜味剂甜菊糖苷、甜菊双糖苷、甘草酸、甘草次酸的测定高效液相色谱法》测定。阿魏酸含量:参照团体标准T/SHRH025—2019《化妆品中阿魏酸含量的测定》测定。
1.3.4 数据处理
试验数据用Excel 2016软件进行初步处理后,采用SPSS 22.0软件进行统计分析,采用One-way ANOVA进行方差分析,最小显著差别(least significant difference,LSD)法进行组间多重比较,结果以“平均值±标准差”表示,P<0.05表示差异显著。
2 结果与分析
2.1 植物乳杆菌发酵对复方中药pH值和微生物数量的影响
植物乳杆菌发酵对复方中药pH值和微生物数量的影响见表1。由表1可知,与对照组相比,实验组均可显著降低发酵复方中药pH值(P<0.05),发酵72 h时均降至4.50以下,实验组间差异不显著(P>0.05)。实验组均可显著提高发酵复方中药的乳杆菌数量(P<0.05),发酵24h、48h和72h时,实验组的乳杆菌数量均可达到109CFU/g。发酵过程中,对照组大肠杆菌活菌数呈增加趋势,发酵72 h时达到(1.13±0.20)×103CFU/g,而实验组均未检出大肠杆菌;对照组霉菌活菌数呈增加趋势,发酵72 h时达到(5.61±0.23)×103CFU/g,而植物乳杆菌BLCC2-0015发酵复方中药的霉菌活菌数呈下降趋势,发酵72 h时低于100 CFU/g,植物乳杆菌BLCC2-0126和BLCC2-0410发酵复方中药均未检出霉菌。结果表明,植物乳杆菌发酵可提高复方中药的乳杆菌活菌数,降低大肠杆菌及霉菌活菌数,且植物乳杆菌BLCC2-0126效果最好,其次为植物乳杆菌BLCC2-0410。耿江苏[8]研究证实,使用益生菌发酵鱼腥草等中药,可提高中药益生菌数量至5.68×108CFU/mL,4 ℃保存一个月后活菌数为4.80×108CFU/mL,显微镜检查无杂菌污染,与本试验结果一致。
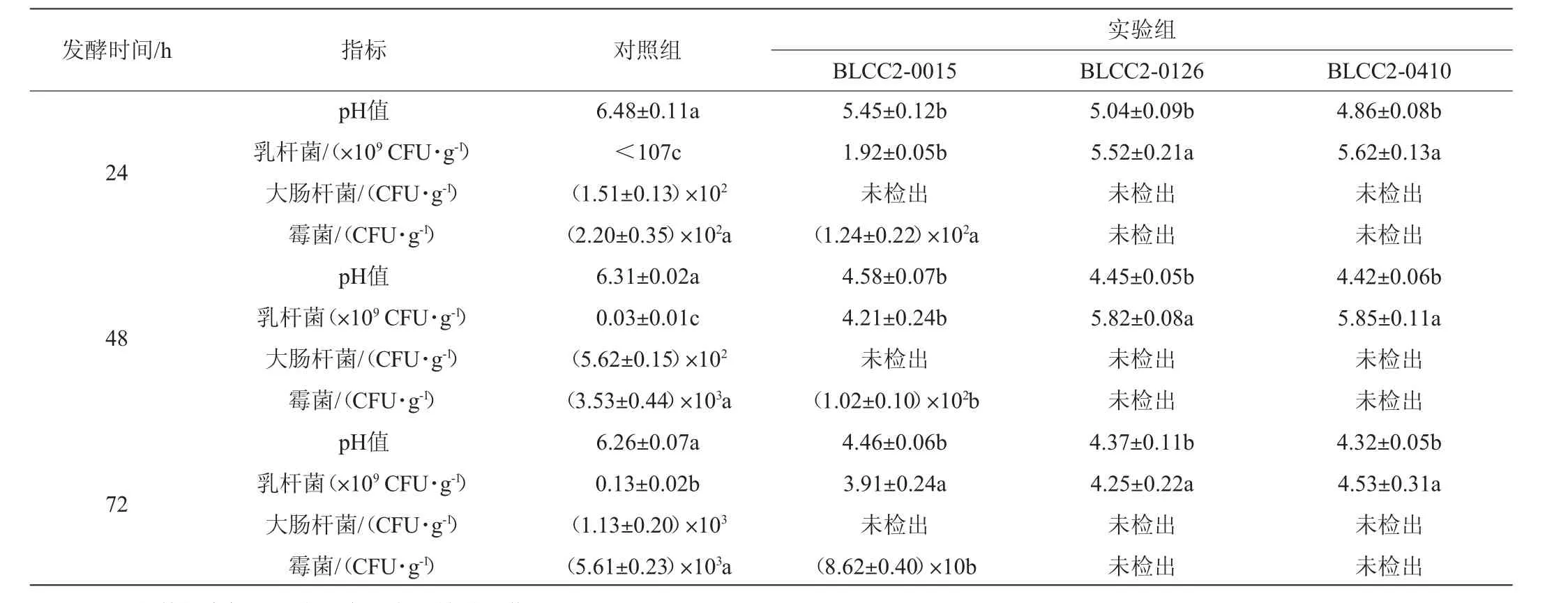
表1 植物乳杆菌发酵对复方中药pH值和微生物数量的影响Table 1 Effects of Lactobacillus plantarum fermentation on pH and microbial number of compound Chinese medicine
2.2 植物乳杆菌发酵对复方中药总酸和机酸含量的影响
植物乳杆菌发酵对复方中药总酸及有机酸含量的影响分别见表2和表3。
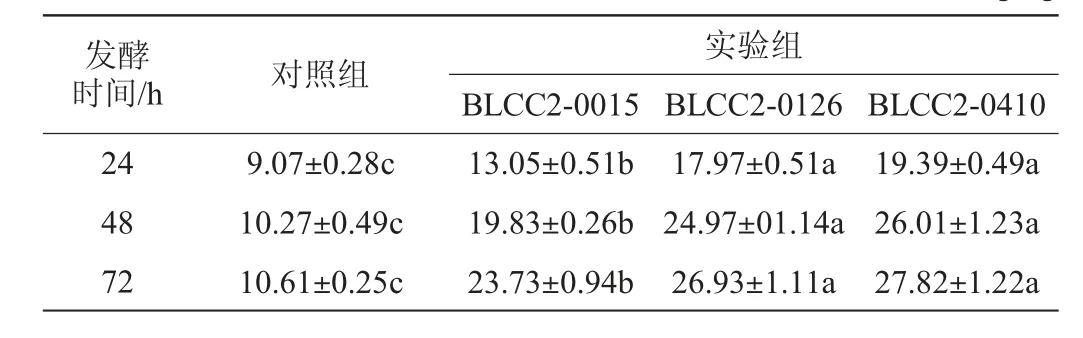
表2 植物乳杆菌发酵对复方中药总酸含量的影响Table 2 Effects of Lactobacillus plantarum fermentation on total acid contents of compound Chinese medicine g/kg

表3 植物乳杆菌发酵对复方中药有机酸含量的影响Table 3 Effect of Lactobacillus plantarum fermentation on organic acid contents of compound Chinese medicine g/kg
由表2可知,与对照组相比,实验组均可显著提高总酸含量(P<0.05),其中,植物乳杆菌BLCC2-0410发酵复方中药中总酸含量最高,其次为植物乳杆菌BLCC2-0126发酵复方中药,且均显著高于植物乳杆菌BLCC2-0015发酵复方中药(P<0.05)。植物乳杆菌BLCC2-0410发酵复方中药72 h时总酸含量达到(27.82±1.22)g/kg。结果表明,植物乳杆菌发酵可以显著提高复方中药中的总酸含量,且植物乳杆菌BLCC2-0410提高效果最好,其次为BLCC2-0126。亓秀晔等[10]研究发现,植物乳杆菌发酵猪全价料,总酸含量可达到20.68 g/kg,与本试验结果一致。
有机酸是乳酸菌发酵饲料提高饲料风味的重要指标,能够改善中药气味和口感辛辣刺鼻等动物适口性的问题,其含量的多少与发酵程度密切相关[11]。吴锦兰等[12]研究发现,在乳酸菌LB-1-23接种量2.6%、pH值5.5、发酵温度32 ℃条件下发酵30 h,乳酸产量达到12.74 g/L。由表3可知,与对照组相比,实验组可显著提高乳酸和苹果酸含量(P<0.05),降低乙酸、草酸和琥珀酸含量,对酒石酸和柠檬酸影响不显著(P>0.05)。这与王芮东等[13]的研究结果一致,发酵过程中乳杆菌繁殖利用乙酸、草酸等产生更多的乳酸、苹果酸,导致乳酸、苹果酸含量升高。乳酸、苹果酸的增加可以提高中药的酸香味,乙酸、草酸的降低可以减少中药的刺鼻味[11]。其中,植物乳杆菌BLCC2-0410发酵效果最好,发酵复方中药72 h时,乳酸、苹果酸含量分别达到(19.25±0.15)g/kg、(4.06±0.18)g/kg,乙酸、草酸分别降低至(3.70±0.13)g/kg、(1.28±0.07)g/kg。
2.3 植物乳杆菌发酵对复方中药粗多糖和总黄酮含量的影响
植物乳杆菌发酵对复方中药粗多糖及总黄酮含量的影响分别见表4和表5。
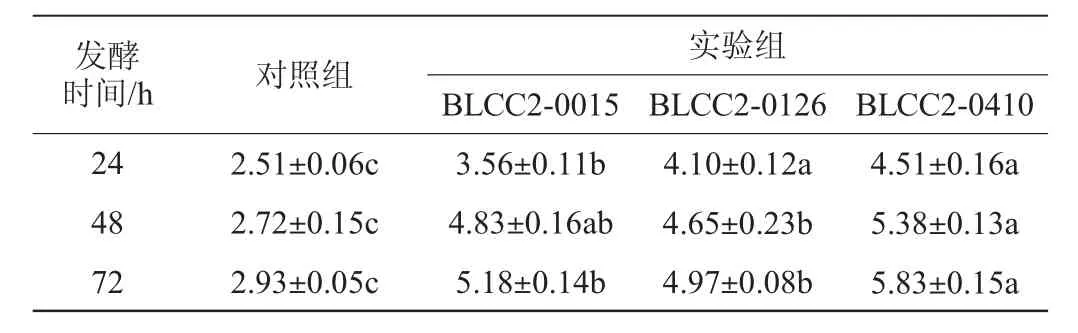
表4 植物乳杆菌发酵对复方中药粗多糖含量的影响Table 4 Effect of Lactobacillus plantarum fermentation on crude polysaccharide contents of compound Chinese medicine%
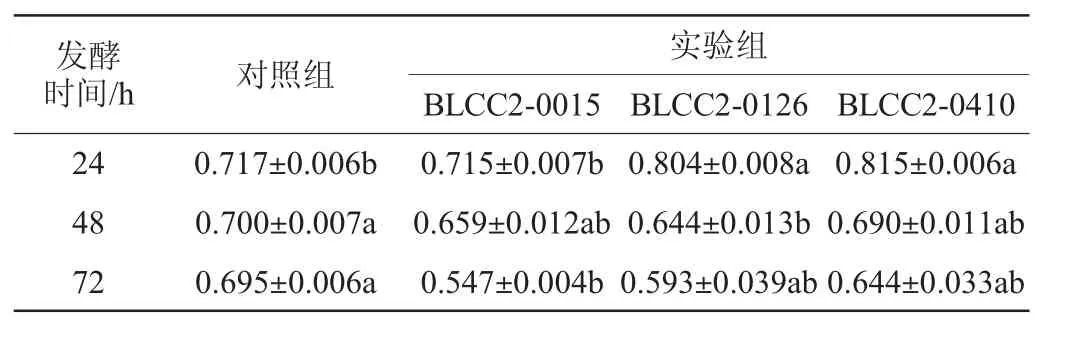
表5 植物乳杆菌发酵对复方中药总黄酮含量的影响Table 5 Effect of Lactobacillus plantarum fermentation on total flavonoid contents of compound Chinese medicine%
粗多糖对氧自由基和羟自由基都有很好的清除作用,是一种天然抗氧化剂[14]。由表4可知,与对照组相比,实验组均可显著提高粗多糖含量(P<0.05),且以植物乳杆菌BLCC2-0410发酵复方中药的粗多糖含量最高,发酵72 h时达到(5.83±0.15)%。分析原因主要是微生物代谢过程中会分泌大量纤维素酶、蛋白酶、果胶酶、淀粉酶等胞外酶,可以使细胞间隙增大,细胞破裂,中药成分溶出,提高中药有效成分得率,随着处理时间的延长,溶出的多糖不断积累[15]。唐鑫等[16]研究发现,植物乳杆菌CCFM8661发酵天山雪莲粗多糖可达1.29 g/L。
有研究表明,总黄酮具有非常强的抗氧化以及消除自由基的作用[17]。由表5可知,与对照组相比,发酵24 h时,植物乳杆菌BLCC2-0126和BLCC2-0410发酵复方中药总黄酮含量显著升高(P<0.05),分别提高12.13%和13.67%。总黄酮含量的增加,从结构上增加了活性OH基团,减少空间位阻,可以提高中药的抗氧化活性[17]。随发酵时间延长,植物乳杆菌发酵复方中药总黄酮含量均呈下降趋势,发酵48 h时,植物乳杆菌BLCC2-0126发酵复方中药中总黄酮含量显著低于对照组(P<0.05),这可能是因为营养物质消耗殆尽,植物乳杆菌分泌多种糖苷酶分解黄酮糖苷类物质作为能源物质消耗[2]。
2.4 植物乳杆菌发酵对复方中药阿魏酸、甘草酸及甘草次酸含量的影响
2.4.1 植物乳杆菌发酵对复方中药阿魏酸含量的影响
阿魏酸是一种安全环保的天然抗菌剂,能够有效抑制大肠杆菌、金黄色葡萄球菌和志贺氏菌[18]。植物乳杆菌发酵复方中药对阿魏酸含量的影响见表6。
由表6可知,与对照组相比,实验组均可显著提高阿魏酸含量(P<0.05),且植物乳杆菌BLCC2-0126和BLCC2-0410发酵复方中药的阿魏酸含量显著高于植物乳杆菌BLCC2-0015(P<0.05)。发酵24 h、48 h和72 h时均以植物乳杆菌BLCC2-0410发酵复方中药时阿魏酸含量最高,分别比对照组高211%、212%和289%,且随发酵时间的延长呈增加趋势。分析原因可能是,在植物细胞中阿魏酸通过苷键或酯键与纤维素等相连接,益生菌发酵可以产阿魏酸酯酶,水解阿魏酸与纤维素、半纤维素、木质素等相互作用的酯键,破坏细胞壁的致密网状结构释放出阿魏酸,使得阿魏酸含量升高[19-20]。结果表明,植物乳杆菌发酵可以提高复方中药中阿魏酸的含量,这与尹志娜等[21-22]的研究结果一致。
2.4.2 植物乳杆菌发酵对复方中药甘草酸及甘草次酸含量的影响
植物乳杆菌发酵对复方中药甘草酸和甘草次酸含量的影响见表7。甘草次酸具有抗炎、抗病毒和提高机体免疫力等作用[23]。由表7可知,与对照组相比,实验组甘草酸含量显著降低(P<0.05),甘草次酸含量显著升高(P<0.05),其中,植物乳杆菌BLCC2-0410发酵复方中药72 h时甘草次酸含量最高为517.9 mg/kg,比对照组高135.09%。分析原因可能是植物乳杆菌发酵复方中药产生甘草酸水解酶,水解甘草酸产生甘草次酸[24]。吕丽静等[25]研究发现,酿酒酵母(Saccharomyces cerevisiae)与植物乳杆菌发酵甘草药渣,甘草苷和甘草酸含量有所下降;樊梅娜等[26]研究发现,植物乳杆菌NBL-B3003发酵甘草24 h,甘草酸含量较未发酵降低90.44%。本研究中植物乳杆菌发酵甘草后甘草酸含量下降,推测亦可能是由于植物乳杆菌促进了甘草酸的生物转化引起的。同时已有研究表明,在体内甘草酸转化成甘草次酸后才发挥药理作用,包括解毒、抑制肝纤维化、抗炎和抗肿瘤等[27]。
3 结论
采用植物乳杆菌(Lactobacillus plantarum)BLCC2-0015、BLCC2-0126和BLCC2-0410固体发酵复方中药(黄芪、甘草和益母草等)后,可降低复方中药的pH值;提高乳杆菌活菌数,抑制大肠杆菌(Escherichia coli)及霉菌的生长;提高总酸、乳酸、苹果酸、粗多糖、阿魏酸及甘草次酸的含量。其中,植物乳杆菌BLCC2-0410发酵效果最好,发酵72 h时,复方中药的pH为4.32,乳杆菌活菌数为4.53×109CFU/g,大肠杆菌及霉菌未检出;总酸、乳酸、苹果酸、粗多糖、阿魏酸和甘草次酸含量均显著升高(P<0.05),分别为27.82 g/kg、19.25 g/kg、4.06 g/kg、5.83%、42.00 mg/kg和517.9 mg/kg。

