Rades 评分和 Tomita 评分在预测脊柱转移瘤患者预后的应用比较
王雅玲 张睿 彭国霖 蒋欣廷 张玉容
恶性肿瘤死亡患者中有 30%~70% 存在脊柱转移,脊柱转移会增加患者痛苦,降低生存质量[1]。近年来,脊柱转移瘤发生率明显上升[2]。肿瘤发生脊柱转移时已是终末期,姑息手术、放化疗等对症治疗是脊柱转移瘤的重要治疗手段[3]。脊柱转移瘤可能因压迫神经导致疼痛和脊柱稳定性下降,患者生存质量明显降低,有效预测患者生存期有助于选择更合理的治疗方式,避免治疗不及时或过度治疗[4]。生存期预测模型广泛用于各类恶性肿瘤患者临床预后预测中,国内外学者已建立脊柱转移瘤的预后预测评分系统,如原始 / 修订 Tokuhashi 评分[5]、Tomita 评分[6]、Rades 评分[7]等,这些预测工具各有优缺点,但结论还不统一[8],其有效性如何还有待进一步验证。本研究通过随访 2010 至 2020年,我院收治的 127 例脊柱转移瘤患者的临床结局,比较 Rades 评分和 Tomita 评分在脊柱转移瘤患者临床结局预测中的应用。
对象与方法
一、纳入标准与排除标准
1. 纳入标准:( 1 ) 2010 年 1 月至 2020 年12 月,我院骨科收治的脊柱转移瘤患者;( 2 ) 病理明确诊断为脊柱转移瘤者;( 3 ) 原发病灶明确者;( 4 ) 临床和随访资料完整者。
2. 排除标准:( 1 ) 诊断不明者;( 2 ) 确诊后在院外接受过其它治疗者;( 3 ) 伴有自身免疫疾病者。
二、研究对象
本研究共纳入 127 例,男 83 例,女 44 例;年龄 24~75 岁,平均 ( 48.8±11.4 ) 岁;95 例伴有内脏转移。脊柱转移位置:颈椎 30 例,胸椎 66 例,腰椎 31 例;原发肿瘤类型:肺、胃肠、食道、膀胱或胰腺共 28 例,肝、胆囊或来源不明 24 例,淋巴、结肠、卵巢或尿道 22 例,肾脏或子宫 19 例,直肠 20 例,甲状腺、乳腺或前列腺 19 例;病理类型:腺癌 91 例,鳞癌 29 例,其它 7 例。
本研究经宜宾市第一人民医院伦理委员会审批通过 ( 批准号:2020-YBET-007 )。
三、研究方法
1. 资料收集:查阅病历资料,收集患者一般信息 ( 年龄、性别、确诊时间等 )、治疗方式 ( 手术、放疗或姑息治疗等 )、原发肿瘤类型、脊柱外骨转移情况、治疗前卡氏评分 ( KPS )、内脏转移情况、身体活动情况、脊髓损伤程度及血液学、影像学检查。所有数据均来自患者病历档案。
2. Rades 预后评分系统:Rades 预后评分系统于 2013 年提出,主要用于筛选以姑息治疗为主的患者,初始 Rades 评分纳入 7 项影响因素 ( ECOG 表现评分、原发肿瘤类型、脊柱外骨转移、内脏转移、癌症诊断至脊柱转移时间、治疗前行走状态及运动缺失发生时间 ),总分 11~25 分,若评分 ≥ 24 分则预期生存期 < 2 个月,应以姑息治疗和护理为主[9]。随后由于 ECOG 表现评分与治疗前行走状态某些维度重合,本研究中的 Rades 评分仅纳入 6 项预后影响因素,且得分赋值也做了修订,包括原发肿瘤类型 ( 乳腺癌 8 分、前列腺癌 7 分、骨髓瘤 / 淋巴癌9 分、肺癌 3 分、其它类型恶性肿瘤 4 分 )、是否存在脊柱外骨转移 ( 有 5 分,无 7 分 )、是否出现内脏转移 ( 是 2 分,否 8 分 )、肿瘤诊断至脊柱转移时间( ≤ 15 个月 4 分、> 15 个月 7 分 )、治疗前能否自由活动 ( 能 7 分、不能 3 分 ) 及治疗前出现不可自由活动时间 ( 1~7 天计 3 分、8~14 天计 6 分、> 14 天计 8 分 ),所有 6 项因素评分相加为 Rades 评分,评分越高说明患者状态越好,参照文献 [10] 将分值20~30 分定义为高危组,31~35 分定义为中危组,36~45 分定义为低危组。Rades 评分二分类 ( 以截断值分为高危和低危 ) 以 ROC 曲线计算。
3. Tomita 预后评分系统:Tomita 预后评分系统于 2001 年提出,共纳入原发肿瘤类型、内脏转移及骨转移数目等 3 项预后影响因素,该评分认为脊髓损伤程度仅与术后功能预后有关,与生存时间无关,因此并未将脊髓损伤程度指标纳入[11]。根据原发肿瘤恶性程度分别计 1、2、3 分,如乳腺、前列腺、甲状腺等生长缓慢的恶性肿瘤计 1 分,肾脏及子宫等生长速度中等的恶性肿瘤计 2 分,而将肺、肝、胃和结肠等生长速度快的恶性肿瘤计 3 分;无重要脏器转移计 0 分,有但可以行手术或栓塞治疗计 2 分,有且不可治疗计 4 分;单发或孤立脊柱转移灶计 1 分,多发骨转移计 2 分,3 项评分相加为Tomita 评分 ( 总分为 2~9 分 ),评分越高说明患者预后越差。Tomita 评分 2~3 分判定为预期生存时间 > 2 年,建议广泛手术治疗以获得长期局部控制;4~5 分判定为预期生存时间 1~2 年,建议边缘或病灶内手术以获得中期局部控制;6~7 分则判定为预期生存时间 6~12 个月,可采取姑息性手术;8~9 分则预期生存时间 < 3 个月,以姑息性治疗为主[12]。Tomita 评分二分类也以 ROC 曲线计算最佳截断值。
4. 随访与结局:患者出院后定期随访,出院6 个月内每 2 个月随访 1 次;6 个月后每个月随访1 次,门诊随访和电话随访相结合,记录患者生存及复发情况。随访截止日期为 2022 年 6 月 30 日,总体生存率 ( overall survival,OS ) 定义为确诊脊柱转移瘤至死亡或随访截止日期。
四、统计学处理
数据采用统计分析软件 SPSS 25.0 进行录入和分析,正态分布的数值资料用±s描述,组间比较用t检验;计数资料用频数或 % 描述,组间比较用χ2检验。采用 Kaplan-Meier 法绘制生存曲线,Log-Rankχ2检验进行生存率的单因素分析,Cox 回归进行多因素分析,以P< 0.05 为差异有统计学意义。
结 果
一、127 例患者生存情况
本组 127 例,平均随访 11.7 个月,中位生存时间 10 个月,随访期内死亡占比 76.38% ( 97 / 127 );3 个月、6 个月和 12 个月生存率分别为 97.64%、69.29% 和 27.56%。
二、不同 Rades 评分和 Tomita 评分患者的生存时间比较
以 Rades 标准评分分类:20~30 分、31~35 分和 ≥ 36 分的患者生存时间分别为 ( 7.0±2.6 )、( 11.7±2.3 ) 和 ( 17.7±4.7 ) 个月,以 ROC 曲线截断值分类:≤ 36 分和 ≥ 37 分的患者生存时间分别为 ( 8.2±3.2 ) 和 ( 18.1±4.6 ) 个月 (P均 < 0.001 )。以 Tomita 标准评分分类:2~3 分、4~5 分、6~7 分和 8~9 分的患者生存时间分别为 ( 18.5±4.7 )、( 11.9±2.2 )、( 8.4±3.0 ) 和 ( 5.5±1.5 ) 个月,以ROC 曲线截断值分类,≤ 4 分和 ≥ 5 分的患者生存时间分别为 ( 16.9±5.2 ) 和 ( 8.2±3.3 ) 个月 (P均 <0.001 ) ( 表1 )。
三、Rades 评分和 Tomita 评分预测患者生存时间的 ROC 曲线
Rades 评分预测患者生存时间的 ROC 曲线下面积 ( AUC 及 95%CI) 为 0.931 ( 0.874~0.987 ),最佳截断值为 36.5,约登指数为 0.771 ( 图1a );Tomita评分预测生存时间的 ROC 曲线下面积为 0.928( 0.874~0.982 ),最佳截断值为 4.5,约登指数为0.733 ( 图1b )。

图1 Rades 评分 ( a ) 和 Tomita 评分 ( b ) 预测患者生存时间的 ROC 曲线Fig.1 ROC curve of Rades score ( a ) and Tomita score ( b ) in predicting patients’ survival time
四、Rades 评分及相关因素预测患者临床预后的单因素分析及多因素 Cox 回归分析
单因素分析发现:Rades 评分分级、治疗方式、原发肿瘤类型、治疗前能否自由活动、是否有脊柱外骨转移、是否内脏转移、肿瘤诊断至脊柱转移时间和治疗前不能自由活动时间等 8 个指标可能是患者预后的影响因素 (P< 0.05 ),Cox 回归显示:Rades 评分分级、原发肿瘤类型、治疗前能否自由活动、有无内脏转移和肿瘤诊断至脊柱转移时间是脊柱转移瘤预后的影响因素,Rades 评分 20~30 分和 31~35 分 ( 相比于 ≥ 36 分 ) 的HR( 95%CI) 分别为 41.871 ( 4.495~390.060 ) 和 4.728 ( 1.400~15.962 ),肺癌和其它癌症( 相比于骨髓瘤 / 淋巴瘤 ) 的HR( 95%CI) 分别为10.039 ( 2.320~43.443 ) 和 8.475 ( 2.112~34.013 ),治疗前能自由活动的HR( 95%CI) 为 0.703 ( 0.582~0.850 ),无内脏转移的HR( 95%CI) 为 0.606 ( 0.455~0.808 ),肿瘤诊断至发生脊柱转移时间 > 15 个月的HR( 95%CI) 为 0.496 ( 0.358~0.686 ) (P均 < 0.05 )( 表2 )。若按 Rades 评分 36.5 分转化为二分类变量,单因素分析 Rades 评分对预测患者预后有意义,但纳入 Cox 回归却发现其并无意义。
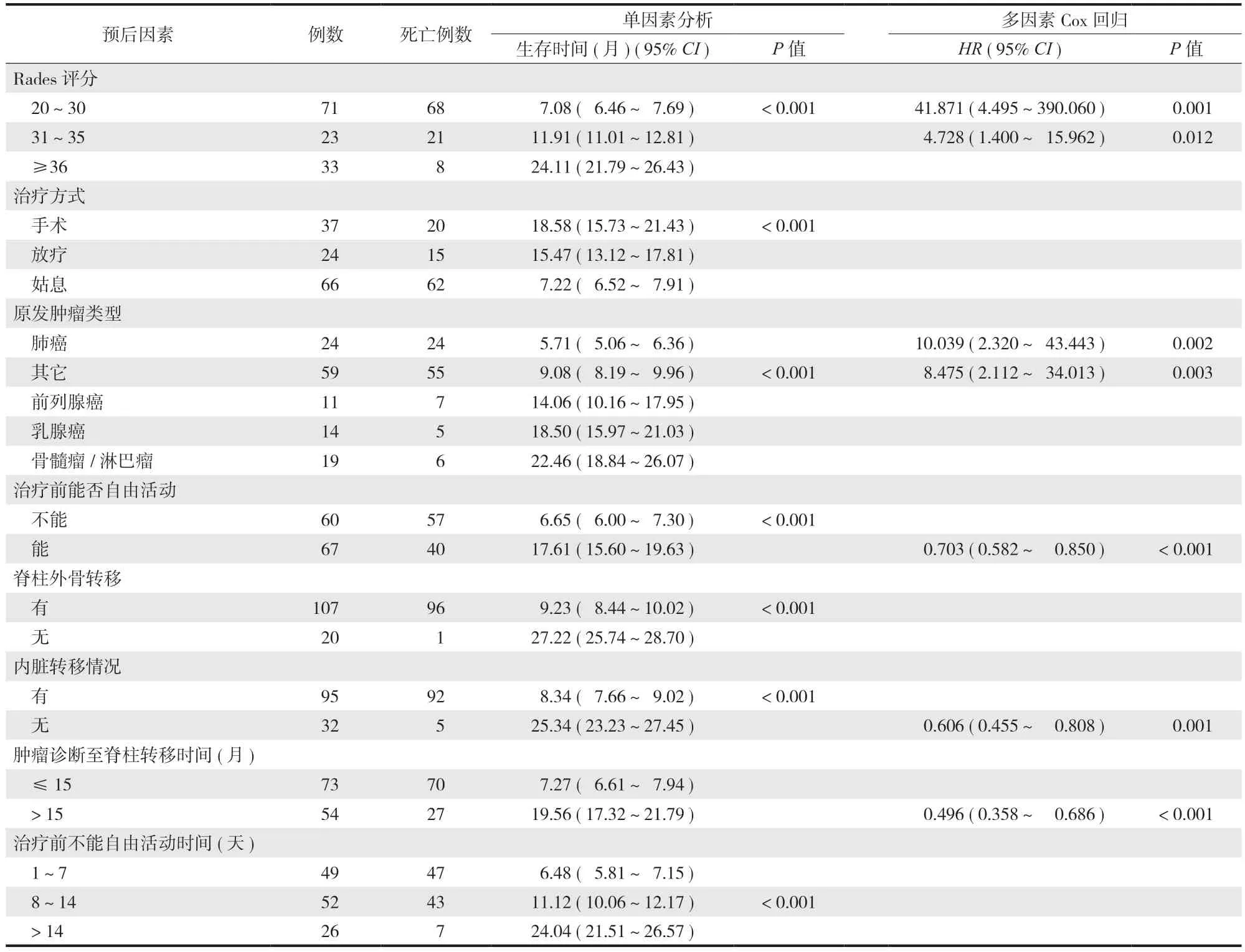
表2 Rades 评分及相关因素预测患者临床预后的单因素和 Cox 回归分析Tab.2 Univariate and Cox regression analysis of Rades score and related factors predicting clinical prognosis of patients
五、Tomita 评分及相关因素预测患者临床预后的单因素及 Cox 回归分析
单因素分析显示:Tomita 评分、原发肿瘤生长速度、骨转移数目、内脏转移、KPS 评分及 NRS 2002 评分等 6 项指标可能是影响脊柱转移瘤患者生存时间的因素 (P< 0.05 ),Cox 回归显示:Tomita 评分和 KPS 评分与患者生存时间有关,Tomita 评分4~5 分、6~7 分和 8~9 分 ( 相比于 2~3 分 ) 的HR( 95%CI) 分别为 8.506 ( 2.571~28.144 )、25.284( 7.879~81.142 ) 和 84.590 ( 24.078~297.184 ),KPS 评分 50~70 分和 ≥ 80 分 ( 相比于 ≤ 40 分 ) 的HR( 95%CI) 分别为 0.226 ( 0.122~0.418 ) 和 0.129( 0.048~0.349 ) ( 表3 )。
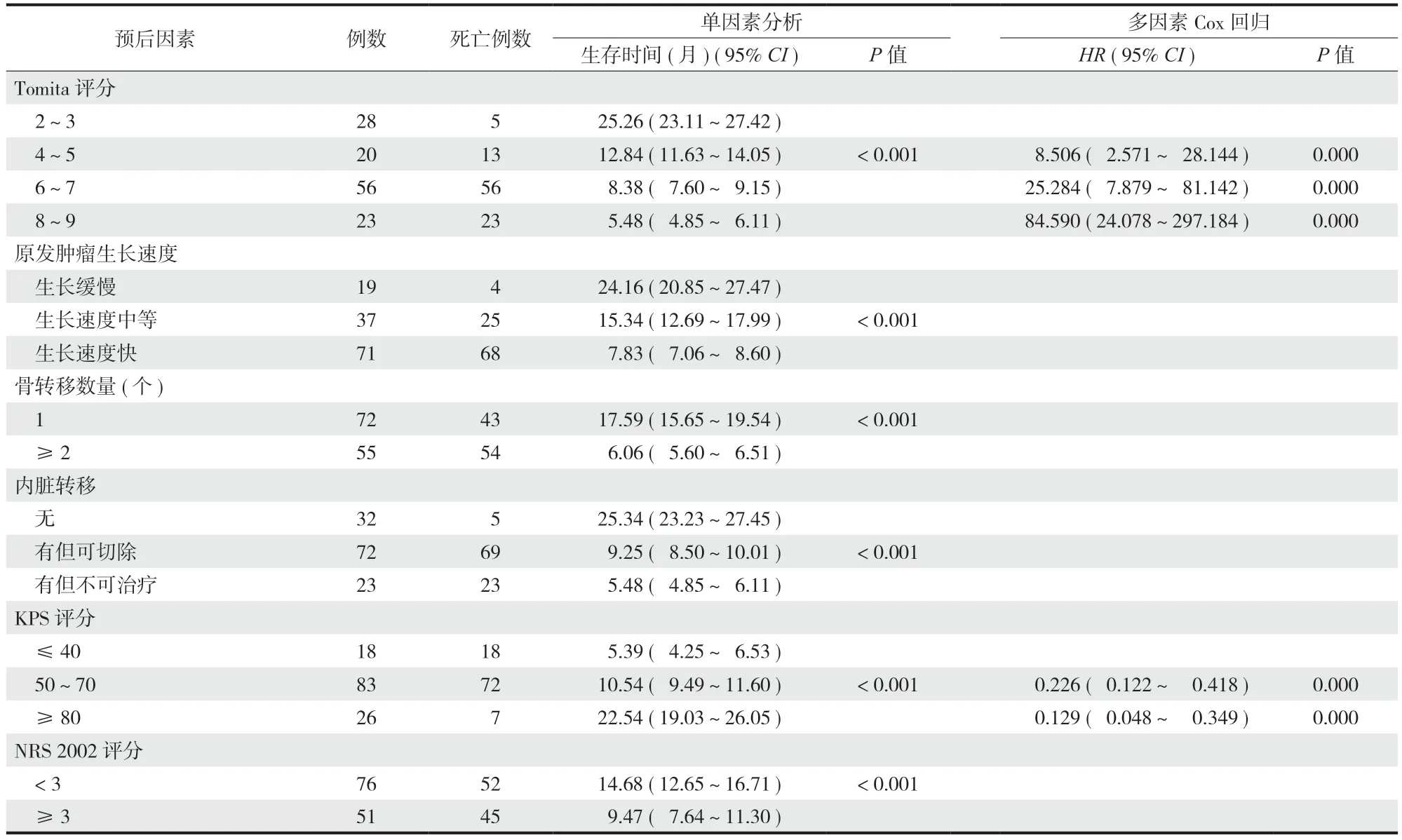
表3 Tomita 评分及相关因素预测患者临床预后的单因素和 Cox 回归分析Tab.3 Univariate and Cox regression analysis of Tomita score and related factors predicting clinical prognosis of patients
六、Rades 评分和 Tomita 评分等相关因素预测患者预后的生存曲线
Rades 评分 20~30 分、31~35 分和 ≥ 36 分的患者 6 个月生存率分别为 45.07%、100.00% 和100.00%,1 年生存率分别为 1.41%、26.09% 和84.85% ( 图2a );确诊肿瘤至脊柱转移时间 ≤ 15 个月和 > 15 个月的患者 6 个月生存率分别为 46.58%和 100.00%,1 年生存率分别为 2.74% 和 61.11%( 图2b );有无内脏转移的患者 6 个月生存率分别为 58.95% 和 100.00%,1 年生存率分别为 8.42% 和84.38% ( 图2c );治疗前能否自由活动的患者 6 个月生存率分别为 98.51% 和 36.67%,1 年生存率分别为50.75% 和 1.67% ( 图2d )。Tomita 评分 2~3 分、4~5 分、6~7 分和 8~9 分的患者 6 个月生存率分别为100.00%、100.00%、60.71% 和 26.09%,1 年生存率分别为 96.43%、50.00%、5.36% 和 0.00% ( 图3a );KPS 评分 ≤ 40 分、50~70 分和 ≥ 80 分的患者 6 个月生存率分别为 16.67%、74.70% 和 88.46%,1 年生存率分别为 5.56%、24.10% 和 73.08% ( 图3b )。

图2 Rades 评分及相关因素预测患者预后的 OS 曲线Fig.2 Overall survival curve of Rades score and related factors in predicting prognosis of patients

图3 Tomita 评分及相关因素预测患者预后的 OS 曲线Fig.3 Overall survival curve of Tomita score and related factors in predicting prognosis of patients
讨 论
骨转移已成为恶性肿瘤患者死亡的主要原因之一,其中脊柱转移引发的骨痛和病理性骨折会直接影响患者生活质量。对发生脊柱转移的终末期肿瘤患者而言,应充分考虑生存质量、生存时间、治疗花费等各方面因素,尽可能优化治疗手段,从而使患者得到最大获益。预测脊柱转移瘤患者的临床预后,不仅可以规避过度医疗风险,也能科学指导治疗措施的选择,对提高患者生活质量和延长生存时间有着重要的实践意义[13]。目前关于脊柱转移瘤预后预测的评分系统主要分为 2 类,传统评分模型提出较早,主要包括 Tokuhashi 评分、Linden 评分、Tomita 评分和 Bauer 评分等,而新式评分系统于近5 年提出,包括国内学者雷明星等建立的 Lei 模型、Rades 评分、Bollen 评分模型、Oswestry 脊柱风险指数等,但各评分系统预测的准确性不一致,尚无证据证实哪种模型可作为“金标准”[14]。各评分模型纳入的预测因素有类似也有不同,仅用肿瘤原发部位和内脏转移预测预后的准确率也高达 90%[15]。Rades 评分提出时间短,在国内应用较少,而 Tomita已提出 20 余年,在国内应用相对较多,本研究重点对比 Rades 评分和 Tomita 评分在脊柱转移瘤预后预测中的应用价值。
两种预后预测模型纳入预后因素不一,Rades评分和 Tokuhashi 评分类似,将原发肿瘤类型和是否内脏转移及脊柱外骨转移等 3 个因素作为影响患者预后的重要因素,评分时赋值均较高,而 Tomita评分重点强调内脏转移,赋值时分值较高。本研究中,Rades 评分采用标准分类时患者实际生存时间与前期研究结果接近[16],说明 Rades 评分对预测患者生存期有一定意义,能指导选择合理的治疗方式。本研究采用 ROC 曲线获得的 Rades 评分最佳截断值为 36.5,采用该分类进行单因素和多因素Cox 回归,得到单因素有意义而 Cox 回归无意义,说明 Rades 评分采用截断值进行二分类并不适用于预后预测,而传统 3 分类 ( 20~30 分、31~35 分和36 分及以上 ) 则能更好分级预测出患者的预期生存时间。治疗手段是决定患者生存时间的重要影响因素,尽管 Rades 评分纳入 6 个独立因素预测患者临床结局,仍有研究认为目前的预后评分系统预测患者生存时间不够准确[17]。Rades 评分系统预测预后的单因素分析共得到 8 个可能的影响因素,其中包括了 Rades 评分系统纳入的 6 个预测因子。有研究认为 ECOG 评分可预测患者预后,但由于 ECOG 评分与“治疗前能否自由活动”维度定义上类似,所以本研究中并未纳入 ECOG 评分。Cox 回归显示:Rades 评分分级、原发肿瘤类型、治疗前能否自由活动、有无内脏转移和肿瘤诊断至脊柱转移时间等5 个因素是脊柱转移瘤预后的影响因素,而 Tomita评分系统中,仅 Tomita 评分和 KPS 评分与患者生存时间有关。不管哪种评分系统,均重点关注原发肿瘤类型,认为原发肿瘤部位对患者临床结局影响最大,其中肺癌、食管、胰腺、胃肠、肝脏和胆囊等传统恶性程度高的肿瘤若发生脊柱转移,患者预后较差,该研究结果和 Tokuhashi 评分关于原发肿瘤类型的赋值类似[18],当然也有研究认为原发肿瘤类型在预测患者生存时间上无实际意义[19]。有学者比较了 Tokuhashi 评分和 Tomita 评分对 6 个月生存期预测的准确性,认为两者准确性均不高,且截断值还不能确定[20]。也有研究认为包括 Tomita 和 Tokuhashi在内的多种评分对原发部位为肺癌的脊柱转移瘤预后预测无效[21]。KPS 评分反应患者功能状况,也对患者生存期预测有一定意义。内脏转移和脊柱外骨转移也是影响患者预后的重要因素,原发肿瘤可控、脊柱外骨转移灶少且无内脏转移的患者生存期相对较长[22],而对已发生脊柱外转移和内脏转移的患者建议姑息治疗或姑息性手术为主,减轻患者痛苦,从而避免过度医疗[23]。
综上所述,脊柱转移瘤患者整体预后差,Rades评分和 Tomita 评分一定程度上能预测患者预后,对选择合适的治疗方式有一定指导意义,但 Rades 评分和 Tomita 评分的最佳界值目前尚有争论。由于本研究为单中心研究,且样本量不大,近 10 年来关于脊柱转移瘤的治疗手段也日新月异,尚须更多前瞻性临床研究进一步证实。

